Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (2): 294-302.doi: 10.3969/j.issn.2095-4344.0021
Previous Articles Next Articles
Hyaluronic acid scaffolds: application research and product prospects
- Bloomage Freda Biopharm Co., Ltd., Jinan 250101, Shandong Province, China
-
Received:2017-12-11Online:2018-01-18Published:2018-01-18 -
Contact:Guo Xue-ping, Researcher, Bloomage Freda Biopharm Co., Ltd., Jinan 250101, Shandong Province, China -
About author:Zhang Xiao-ou, Doctor, Bloomage Freda Biopharm Co., Ltd., Jinan 250101, Shandong Province, China
CLC Number:
Cite this article
Zhang Xiao-ou, Lv Yang, Mao Hua, Fan Xin-yi, Huang Si-ling, Guo Xue-ping.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
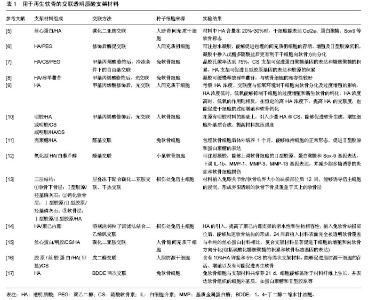
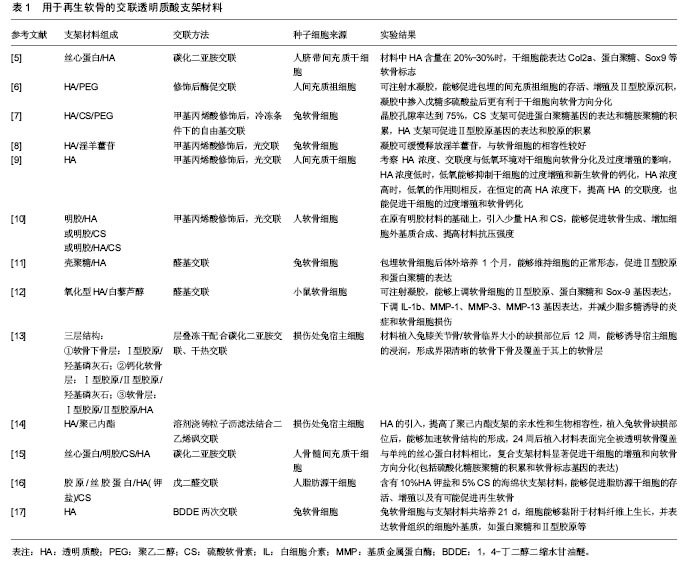
经过文献分析,以透明质酸为主要成分的组织工程支架材料,在软骨/骨、脂肪、心血管系统、神经系统的再生修复方面应用研究较多,在皮肤、角膜、视网膜、肝脏的再生修复方面也有少量应用研究。材料中的透明质酸有的以游离状态分散于其他材质的网络结构中,有的经过修饰(如酯化),但最多的是通过光交联、腙交联、碳化二亚胺交联等方式在透明质酸分子内、分子间或者透明质酸与其他聚合物分子之间形成共价交联。剂型以可注射凝胶居多,这主要是考虑临床应用的易操作性以及微创手术的患者依从性。透明质酸支架材料与细胞的组合方式主要有两种:包埋干细胞或诱导宿主细胞浸润,而有些材料在促进干细胞与宿主细胞的相互作用方面也能发挥一定作用。 2.1 在软骨/骨再生方面的应用 2.1.1 软骨再生 骨关节炎与关节软骨的磨损、退化相关,而软骨是一种很难再生的非血管化少细胞组织,为模拟细胞外基质的组成成分,多种基于透明质酸的支架材料通过修饰、交联或与其他生物材料复合,被用于软骨的修复。 HYAFF®是一类透明质酸的酯化衍生物,酯化后透明质酸材料的亲水程度减弱,降解时间延长,细胞的黏附作用增强。HYALOFAST®是Anika公司已商品化的基于HYAFF®技术的苄基酯化透明质酸骨/软骨修复材料,已取得医疗器械CE认证,配合间充质干细胞,通过微创手术植入膝关节或踝关节的缺损部位,可促进间充质干细胞的黏附、增殖与分化和细胞外基质的分泌。Cavallo等[4]将HYAFF-11与骨髓浓缩物共培养,可促进软骨生成,表达软骨相关标志分子,如Ⅱ型胶原、蛋白聚糖等,以替代间充质干细胞,避免体外培养过程引入的安全风险。 交联过程可以改善透明质酸凝胶的力学性质,延长其降解时间(表1)。一种由丝心蛋白与透明质酸通过碳化二亚胺交联得到的支架材料,包埋干细胞后,体外再生软骨,通过对细胞形态、增殖和基因表达的分析,证实复合材料中透明质酸所占比例在20%-30%时效果最 佳[5]。Frith等[6]将经过修饰的透明质酸和聚乙二醇(PEG)通过辣根过氧化酶催化交联获得聚乙二醇/透明质酸复合可注射凝胶,促进包埋的间充质祖细胞存活、增殖与Ⅱ型胶原的沉积,特别是当凝胶中加入戊糖多硫酸盐后,更有利于间充质祖细胞向软骨方向分化。甲基丙烯酸化透明质酸可通过自由基引发交联,冷冻致孔后,形成晶胶,孔径大,孔隙率高,能够促进Ⅱ型胶原合成,有利于再生软骨[7]。淫羊藿苷是一种能够促进软骨再生的化合物,四川大学的He等[8]通过光交联将甲基丙烯酸化的透明质酸与淫羊藿苷共价结合,合成了一种透明质酸/淫羊藿苷水凝胶,可缓慢释放淫羊藿苷,与软骨细胞的相容性较好,可用于软骨再生。香港中文大学的Zhu等[9]制备了包埋间充质干细胞的光交联透明质酸水凝胶,考察透明质酸浓度及缺氧环境对软骨再生的影响,结果表明,缺氧对正常的软骨生成没有影响,只对过度增生和钙化有影响,当透明质酸浓度低时,缺氧环境能够抑制间充质干细胞的过度增生与新生软骨的钙化,而当透明质酸浓度高时,缺氧环境反而促进间充质干细胞的过度增生和钙化,在恒定的高透明质酸浓度下,提高透明质酸的交联密度,也会促进过度增生和钙化。在原有明胶材料的基础上,引入少量透明质酸和硫酸软骨素,制备出一种光交联明胶/透明质酸/硫酸软骨素(chondroitin sulfate,CS)支架材料,可以促进软骨生成、增加细胞外基质合成、提高材料压缩模量[10]。Remya等[11]采用醛基交联的透明质酸/壳聚糖凝胶,包埋软骨细胞后体外培养1个月,能够维持细胞的正常形态,促进Ⅱ型胶原和蛋白聚糖的表达。Sheu等[12]也采用醛基交联的方法将透明质酸氧化后与白藜芦醇交联,研制了一种可注射凝胶,可上调软骨细胞的Ⅱ型胶原、蛋白聚糖和Sox-9基因表达,减少脂多糖诱导的炎症和软骨细胞损伤。与需要在成胶前预先包埋细胞的支架材料不同,一种用于骨/软骨缺损修复的多层支架材料,其底层含有Ⅰ型胶原和羟基磷灰石,用于修复软骨下骨,中间层含有Ⅰ型胶原、Ⅱ型胶原和羟基磷灰石,用于修复钙化软骨,表层含有Ⅰ型胶原、Ⅱ型胶原和透明质酸,用于修复关节软骨,这种材料在植入兔膝关节骨/软骨缺损部位后,能够诱导宿主细胞的浸润,形成界限清晰的多层 骨/软骨结构,这种材料是通过层叠冻干配合碳化二亚胺交联、干热交联的方法制备的[13]。一种无细胞的透明质酸/聚己内酯(PCL)支架通过溶剂浇铸粒子沥滤法(solvent casting and particulate leaching (SC/PL) techniques)结合二乙烯砜交联制备而成,与单纯的聚己内酯支架相比,透明质酸的引入提高了材料的亲水性和生物相容性,植入兔软骨缺损部位后,能够加速软骨结构的形成,24周后植入材料表面完全被透明软骨覆 盖[14]。Sawatjui等[15]通过冻干结合碳化二亚胺交联制备的丝心蛋白/明胶/硫酸软骨素/透明质酸支架材料,能显著促进骨髓间充质干细胞的增殖和向软骨方向分化。戊二醛交联获得的含有胶原、丝胶蛋白、10%透明质酸(钾盐)和5%硫酸软骨素的海绵状支架材料,能够促进脂肪源干细胞的存活、增殖以及再生软骨[16]。刘少英等[17]采用1,4-丁二醇二缩水甘油醚两次交联的方法制备了透明质酸支架材料,并进行了兔软骨细胞与透明质酸支架的共培养研究,细胞能够黏附于材料上生长,并表达软骨组织细胞外基质,如蛋白聚糖和Ⅱ型胶原等。 含有透明质酸的复合材料,则充分利用了透明质酸的生物学活性,促进软骨细胞的增殖。Tavakoli等[18]也采用SC/PL法合成了一种聚乳酸乙醇酸(PLGA)/透明质酸/纤维蛋白/生物活性玻璃纳米复合物,与纯聚乳酸乙醇酸材料相比,改善了压缩模量和抗压强度,可用于软骨组织工程。Skaalure等[19]开发了一种透明质酸与聚乙二醇半互穿水凝胶,光交联的可降解聚乙二醇中穿插了透明质酸分子,并缓释透明质酸(4周释放90%),促进了包埋的软骨细胞增殖以及胶原和硫酸化糖胺聚糖的合成,高分子透明质酸比低分子透明质酸更有利于延迟凝胶的降解。甲基丙烯酸化乙二醇壳聚糖通过光交联形成凝胶,透明质酸分子穿插于凝胶网络中,这样的凝胶通过调整交联度,可以使包埋的软骨细胞存活率达到80%以上,与不含透明质酸的凝胶相比,加入透明质酸可有效促进软骨细胞的增殖和细胞外基质的分泌[20]。李音 等[21]以魔芋葡甘聚糖和透明质酸为原料,丙三醇为增塑剂,乳酸为改性剂,结合微波处理与湿法纺丝技术,制备纤维膜,能够支持间充质干细胞的生长。 2.1.2 髓核再生 髓核为椎间盘结构的一部分,位于两软骨板与纤维环之间,是由软骨细胞和基质纤维组成的具有弹性的胶冻状物质,随着年龄增长,基质纤维降解、老化,水分减少,髓核损伤,易出现椎间盘病。含有透明质酸的组织工程材料也被应用于髓核的再生修复。 Li等[22]采用碳化二亚胺共价交联纤维蛋白原和透明质酸,与非交联纤维蛋白原/透明质酸复合材料和单纯的纤维蛋白相比,具有更好的稳定性和机械性能,促进髓核细胞的增殖和标志基因的表达,在髓核全切术后恢复抗压刚度及椎间盘高度。Mercuri等[23]通过碳化二亚胺结合五没食子酰葡萄糖交联,制备的弹性蛋白/硫酸软骨素/透明质酸/胶原支架材料,在体外能够诱导脂肪源干细胞向髓核细胞分化,植入体内后能够诱导宿主髓核细胞浸润,这种材料具有一定抗酶解能力。Kim等[24]采用光交联的透明质酸凝胶提高包埋的髓核细胞的特异性基因表达和细胞外基质合成,改善材料的机械性能。Jeong等[25]通过二乙烯基砜修饰的聚乙二醇与巯基化透明质酸交联制备凝胶材料,并采用人工神经网络的方法考察了材料对髓核细胞和纤维环细胞生长的影响,含有低相对分子质量透明质酸的材料能够促进2种细胞的增殖和细胞外基质中硫酸化糖胺聚糖的合成。 2.1.3 骨再生 骨组织再生对支架材料力学性能提出了更高的要求,因此多为交联材料,而仿生支架材料能否支持自体或异体成骨细胞在骨缺损部位形成有效的增殖与基质矿化,是评价支架材料生物性能的关键。 Cui等[26-27]制备了2种透明质酸凝胶支架,均表现出较高的孔隙率和平衡溶胀比,一种是通过腙键交联结合光交联形成的聚丙烯酰赖氨酸/透明质酸支架,形状恢复能力强,比单纯的透明质酸凝胶压缩模量高5倍以上,谷胱甘肽响应性降解,另外一种是通过腙键交联制备的透明质酸/聚乙二醇凝胶支架,可被透明质酸酶、还原物质或酸性环境降解,2种支架都能够支持前成骨细胞的存活与增殖,允许细胞与组织浸润。Zhu等[28]分别采用光交联和二硫苏糖醇(DTT)交联的方法,由甲基丙烯酸化透明质酸交联形成2D和3D凝胶,其中3D凝胶采用了聚甲基丙烯酸甲酯(PMMA)基础框架,并用精氨酸-甘氨酸-天冬氨酸肽(RGD肽)和N-钙黏着蛋白模拟肽共价修饰凝胶,RGD肽对间充质干细胞能黏附在材料上是不可缺少的,而N-钙黏着蛋白模拟肽则促进了间充质干细胞之间和间充质干细胞与已分化的成骨细胞之间的黏附与相互作用,体内体外实验表明,这种材料能够促进间充质干细胞表达成骨标志基因,提高碱性磷酸酶活性、Ⅰ型胶原的沉积和基质矿化作用,有利于骨再生。Bellini等[29]开发了基于透明质酸、结冷胶和氯化钙的离子敏感型原位凝胶,无化学交联剂,透明质酸的含量主要影响凝胶的降解时间和材料的稳定性,筛选最优配方能够显著促进材料在骨缺损部位的黏附、包埋的人成骨细胞的增殖与基质矿化。Kisiel等[30]将纤连蛋白序列中包含整合素结合域的部分片段共价结合到醛基交联的透明质酸凝胶上,促进了间充质干细胞在材料上的黏附与伸展,然后将这种修饰透明质酸凝胶作为重组人骨形成蛋白2(rhBMP-2)的载体,在体内体外均能有效促进间充质干细胞再生骨组织,与未经修饰的透明质酸凝胶相比,胶原纤维生成的量提高了1倍。Wu等[31]通过醛基化透明质酸与酰肼化透明质酸的腙键交联制备可注射原位透明质酸凝胶,同时对酰肼化透明质酸的一部分酰肼基团以多聚磷酸盐进行共价修饰,与添加了游离状态的多聚磷酸盐的凝胶相比,显著促进包埋的前成骨细胞的增殖、成骨分化,提高成骨标志基因的表达以及碱性磷酸酶活性。林永新等[32]以透明质酸、壳聚糖为基质,在微酸性环境中与氯化钙和磷酸二氢钠混合,冷冻干燥得到多孔复合支架,再在乙醇/水/尿素的环境中陈化,使生成的磷酸氢钙转变为羟基磷灰石,最终形成深度矿化的、适合骨形成的支架材料。 牙周炎的长期不愈会逐渐对牙周软组织和牙槽骨造成损伤,Subramaniam等[33]通过共沉淀的方法制备了羟基磷灰石/半水合硫酸钙/透明质酸复合材料,并装载了胶原酶,目的是植入牙槽骨缺损部位后,利用胶原酶降解损伤部位的纤维组织,释放更多的宿主成骨细胞,研究表明,这种复合材料的机械性能与小梁骨相近,胶原酶的释放在前30 min达到60%,有利于材料与宿主细胞的相互作用,材料生物相容性高,能有效促进宿主成骨细胞再生牙槽骨组织。 2.2 在脂肪及软组织再生方面的应用 成熟的脂肪细胞通过移植进入新的体内微环境后,存活时间很短,易发生液化,而脂肪干细胞也同样存在移植后存活率较低的问题,基于透明质酸的支架材料能够对脂肪干细胞提供保护,延长存活时间。 Lequeux等[34]采用由非交联透明质酸、氨基酸、维生素、矿物质组成Cytocare®,辅助脂肪干细胞移植重建软组织,能够显著提高干细胞的存活率、生物利用率和增殖率。Açil等[35]比较了2种商品化胶原膜(Bio-Gide®, Tutodent® )和一种透明质酸凝胶(Belotero®)作为脂肪干细胞移植载体的差异,体外研究表明,Bio-Gide和Belotero均有助于改善移植效果。Chang等[36]则采用碳化二亚胺结合冷冻的方法,制备了由明胶和透明质酸组成的晶胶,在体外和体内都能有效促进脂肪干细胞的增殖与脂肪方向分化,材料具有较高的延展性、韧性和从较大应变完全恢复的能力,还具有高孔隙率、大孔径、较高的溶胀比和较快的溶胀速率。南京理工大学的Jia等[37]通过Diels-Alder反应使分别经呋喃和马来酰亚胺基团修饰的透明质酸分子之间形成交联,同时用地塞米松肽段进行了共价修饰,包埋了超顺磁性氧化铁颗粒,做成了一种磁性透明质酸纳米微球,能够显著提高脂肪干细胞的存活率,并可在磁场引导下定点再生脂肪。 2.3 在心血管系统再生方面的应用 心血管组织工程主要包括心肌梗死区域的心肌组织再生、心脏瓣膜置换以及血管重建。 2.3.1 心肌再生 心肌梗死是造成心衰从而导致患者死亡的主要原因,心肌梗死会诱发大量心肌细胞丧失收缩功能,梗死区域逐渐被无功能性纤维组织替代。相对分子质量较低的透明质酸具有促血管生成的作用,含有透明质酸的支架材料用于心肌梗死坏死区域的修复治疗,伴随材料的降解和小分子透明质酸的释放,血管生成作用增强,从而改善损伤部位的营养供给,同时透明质酸还能促进心肌细胞的增殖,减少纤维化的发生。 一种可原位成胶的腙键交联海藻酸/透明质酸凝胶,交联过程中加入人源Ⅰ型胶原蛋白和新生大鼠心肌细胞,能够产生具有收缩能力的心肌组织,与单纯的胶原材料相比,含有透明质酸的材料再生的心肌组织收缩力更强[38]。Fiumana等[39]将大鼠间充质干细胞与酯化透明质酸(HYAFF-11)支架经体外培养后植入大鼠体内的心肌梗死损伤部位,体外培养过程中间充质干细胞紧密黏附于材料上并分泌大量细胞外基质,间充质干细胞在植入2周后向凝胶表面靠近冠状血管处迁移,促进了损伤区域的毛细血管形成,减少了纤维化的发生。Yong等[40]研究发现,一种巯基化透明质酸与聚乙二醇二丙烯酸酯(PEGDA)组成的复合凝胶,可通过缓慢交联模拟机体发育过程中细胞外基质随时间逐渐变硬的过程,从而促进心肌细胞的逐渐成熟,但巯基化透明质酸在心肌这种血管丰富的区域,由于游离巯基的存在而易使炎性细胞富集,也比普通透明质酸更容易降解,因此更适合血管化程度较低和需要一定硬度的部位的修复。Muscari等[41]采用酯化透明质酸(HYAFF-11)结合自体骨髓间充质干细胞,能够显著改善冠状动脉结扎模型小猪心肌梗死区域的血流灌注,使其恢复至正常动物的水平,并且几乎完全抑制了炎症反应的发生。Yoon等[42]将丙烯酸化透明质酸和巯基化聚乙二醇混合,通过迈克尔加成反应交联,生成的可注射凝胶用于心梗组织再生修复,效果与透明质酸分子质量(50,130,170 ku)以及心肌梗死病程有关,对于亚急性期模型,50 ku的透明质酸凝胶心肌再生与功能恢复效果最好,而在慢性期模型中效果显著下降,说明早期修复很重要,而在凝胶中装载血管内皮生长因子并没有形成协同增效作用。Gaetani等[43]通过3D打印技术制备了包含人心源祖细胞的透明质酸/明胶多层补片,应用于心肌梗死部位的修复,该补片能够维持祖细胞的存活、增殖与分化,植入小鼠心肌梗死模型后显著提高心脏功能。 2.3.2 瓣膜置换 含有透明质酸的支架材料,也被用于心脏瓣膜缺陷或损伤的修复。理想的人工瓣膜不仅要实现正常的机械性能和血液动力学性能,还应该能够与宿主组织整合,并伴随生长,作为细胞外基质主要成分的透明质酸,能够支持干祖细胞的存活、增殖、分化或材料与宿主细胞的相互作用。 Duan等[44]采用甲基丙烯酸化的透明质酸和明胶,结合光交联和3D打印技术制备凝胶,包埋人主动脉瓣间质细胞(HAVIC),用于重建三叶瓣膜导管,细胞能够维持活性和成纤维表型,并分泌细胞外基质分子(胶原和糖胺聚糖),适当提高材料中明胶的浓度,可促进细胞的黏附与扩散。Eslami等[45]将电纺制备的聚甘油癸二酸-聚己内酯纤维支架(PGS-PCL),与甲基丙烯酸化透明质酸和明胶光交联产生的凝胶结合,形成了纤维强化凝胶支架用于心脏瓣膜组织工程,包埋羊二尖瓣间质细胞后,透明质酸凝胶的存在能够促进细胞的迁移扩散,且不影响材料的机械性能。 2.3.3 血管重建 由于低相对分子质量透明质酸具有促血管生成的作用,因此透明质酸支架材料在血管再造方面也有很好的应用前景。 Zhu等[46]采用重组类人胶原和透明质酸(分子质量约10×104 u)通过戊二醛交联和冷冻干燥制成三维支架用于血管内膜再生,类人胶原与透明质酸的比例为10︰1时,材料具有合适的孔径和孔隙率,抗压和抗拉强度最强,降解较慢,生物相容性好。透明质酸的含量提高,能够促进血管内皮细胞的增殖,提高机械性能。Wang等[47]在透明质酸的羧基基团上通过酯化反应连接酪胺,并与带有两个酚羟基基团的Phenol2-PEG-RGD人工合成片段,通过辣根过氧化物酶与过氧化氢催化,在苯酚基团的羟基之间形成交联,从而形成了RGD肽共价修饰的可注射交联透明质酸凝胶,提高了透明质酸凝胶的细胞黏附性能,显著促进包埋的人脐静脉内皮细胞的增殖、迁移以及毛细血管网的形成,当人脐静脉内皮细胞与人成纤维细胞同时包埋入凝胶,并植于皮下后2周,可形成功能性血管组织。 2.4 在神经系统再生方面的应用 神经系统自我修复能力很弱,采用神经干/祖细胞(NPSCs)治疗外伤性脑损伤或脊髓损伤的临床前研究,取得了一些进展,但受限于干细胞的存活率和植入率太低(2%-4%)以及分化方向的失控。含有透明质酸的支架材料有助于延长干细胞的存活期、促进干细胞与宿主组织的整合以及诱导干细胞的定向分化。 Addington等[48]发现聚乙二醇-二乙烯砜交联的透明质酸/层粘连蛋白凝胶能够提高神经干细胞对损伤区域释放的趋化因子(如SDF-1α)浓度梯度的动态响应,促进神经干/祖细胞表达SDF-1α的受体(CXCR4)以适应损伤环境,同时促进神经干祖细胞根据SDF-1α浓度梯度的迁移。Schizas等[49]的研究表明,与胶原凝胶或聚酯膜相比,腙键交联透明质酸凝胶能够促进神经元、特别是运动神经元的存活、增殖,增加休眠的白质小胶质细胞数量,减少激活的灰质小胶质细胞数量,从而有利于组织保存。Mothe等[50]采用重组大鼠血小板源生长因子A修饰的甲基纤维素/透明质酸复合凝胶,与神经干/祖细胞混合移植入大鼠亚急性脊髓损伤模型,能够显著减少脊髓空洞,促进移植物存活和少突细胞分化,加快运动功能恢复。吴婷等[51]考察了鼠尾胶原、交联透明质酸和海藻酸钠3种凝胶,添加或不添加层粘连蛋白,共12种生物支架,应用于大鼠神经干细胞的体外培养,其中透明质酸凝胶以聚乙二醇二丙烯酸酯为交联剂交联巯基化透明质酸,研究表明胶原和透明质酸凝胶支架能够促进神经干细胞的黏附,胶原凝胶组细胞增殖能力最强,含15%交联剂的添加了层粘连蛋白的透明质酸凝胶支架有利于神经干细胞向神经元分化。Entekhabi等[52]通过电纺制备了由透明质酸和聚己内酯组成的高孔隙率纳米纤维,当透明质酸和聚己内酯的含量比为5︰95时,在体外显著促进人神经母细胞瘤细胞的增殖与迁移。Arulmoli等[53]的研究表明,鲑鱼纤维蛋白原经过凝血酶处理后形成的支架与哺乳动物来源的纤维蛋白原相比,更有利于人神经干/祖细胞的增殖,但材料降解速度过快,新开发的酶法交联的鲑鱼纤维蛋白原/透明质酸/层粘连蛋白(5︰1︰0.1)可注射原位凝胶支架,能够延长降解时间,促进神经干/祖细胞植入后存活、增殖与分化,并促进共培养的血管内皮细胞增殖,从而促血管生成,材料力学性质接近于脑组织,分子质量250 ku的巯基化透明质酸最有利于神经干/祖细胞的存活。Wang等[54]通过氧化聚合制备了电传导性聚乙烯二氧噻吩/透明质酸/聚乳酸复合膜,配合电刺激,显著促进神经突的生长,促进神经元样嗜铬细胞瘤细胞(PC12)的黏附与增殖,材料具有较好的电化学稳定性,较低的表面接触角,与聚乳酸比有更快的降解速率。Kuo等[55]采用甲基丙烯酸化透明质酸与甲基丙烯酸化明胶,通过光交联,诱导包埋的诱导性多能干细胞向神经元分化,提高凝胶总体浓度时,材料溶胀率降低,诱导性多能干细胞的包封率提高,而当提高凝胶中甲基丙烯酸化透明质酸的比例时,反而会提高溶胀率,降低诱导性多能干细胞包封率。 2.5 在皮肤组织再生方面的应用 烧烫伤及外伤造成的皮肤缺损,特别是全层皮缺损,目前依靠自体或异体皮片、微粒皮的移植来进行修补,来源有限,采用含透明质酸的支架材料,配合其他皮肤组织细胞外基质成分,可预接种人源皮肤细胞,也可刺激宿主细胞增殖,透明质酸在材料中主要发挥促进创伤愈合、减少瘢痕、促进皮肤细胞增殖和血管生成的作用。 一种喷雾辅助层叠组装技术制备的聚电解质多层膜用于重建皮肤[56],表皮层含有多层透明质酸和聚赖氨酸,真皮层是腙键交联多孔透明质酸支架,这种多层材料能够促进表皮角质细胞的黏附,重建表皮屏障功能,且表皮细胞不会向真皮支架迁移,为真皮支架接种成纤维细胞预留了空间,有望用于全层皮缺损的治疗。Yan等[57]通过碳化二亚胺交联结合冷冻干燥制备了丝心蛋白/硫酸软骨素/透明质酸(80︰5︰15)支架材料,用于真皮层再生修复,硫酸软骨素和透明质酸的加入提高了材料的亲水性,从而缩小了孔径,透明质酸提高了材料的溶胀比,从而有利于在生理条件下维持多孔结构的稳定,在体外这种复合材料显著促进小鼠成纤维细胞的黏附与增殖,植入真皮缺损部位后,复合材料炎性反应低,促进宿主细胞表达相关生长因子同时促进血管生成,真皮组织再生的速度与材料降解的速度相匹配。Monteiro等[58]开发了一种同时具有真皮层和表皮层的全层皮支架,真皮层含有纤维蛋白和腙键交联透明质酸,并以细胞黏附肽共价修饰,可原位成胶,包埋人真皮成纤维细胞后能促进细胞的黏附与增殖;表皮层通过腙键交联、静电沉积以及碳化二亚胺交联,将透明质酸和多聚赖氨酸交联形成薄膜,表面再包被层粘连蛋白,能够促进角质形成细胞的黏附并呈单层生长;两层支架的结合处存在胺醛缩合,因此结构稳定。 2.6 在眼科组织再生方面的应用 在眼科组织工程中,透明质酸出众的光学特性使其很适合应用于角膜、视网膜、玻璃体等组织的再生修复,同时可促进角膜干细胞、视网膜祖细胞等的增殖与迁移。 Xiang等[59]设计了一种T形人工角膜,主体成分是聚甲基丙烯酸羟乙酯凝胶,伞状裙边部分由透明质酸和阳离子明胶静电沉积形成的多层聚电解质海绵组成,以促进角膜干细胞的黏附,在人工角膜与宿主角膜组织间形成膜状衔接,底部还包被了聚乙二醇,防止细胞的浸润形成人工角膜后膜。华南理工大学的研究团队设计的通过碳化二亚胺交联的胶原/明胶/透质酸仿生膜(6︰3︰1) [60],具有最佳光学特性、亲水性、机械性能和扩散性能,能够支持人角膜上皮细胞的黏附与增殖,有望应用于角膜组织工程,代替角膜移植术。第三军医大学采用HyStem和Extralink巯基交联体系制备了一种透明质酸凝胶[61],用于包埋视网膜祖细胞,能够保持祖细胞的未分化状态,3周后降解,祖细胞分化、表达视觉恢复蛋白(成熟的光感受器标志)并迁移分布至整个视网膜,材料可注射,因此移植过程对视网膜结构损伤小。 2.7 在肝脏组织再生方面的应用 肝脏的再生修复由于其复杂的血液供给网络而变得十分困难,透明质酸添加到支架材料中能够有效促进血管生成,改善肝组织的营养供给。 Shang等[62]将半乳糖基化壳聚糖与透明质酸混合冻干,制备的复合海绵,能够支持原代肝细胞和内皮细胞的共培养,促进肝细胞的黏附、增殖、特异基因表达、尿素产生、睾酮代谢等,其中内皮细胞表达CD44,能够与透明质酸结合,从而促进内皮细胞的增殖,进而有利于肝脏血窦再生。 "
| [1]Hemshekhar M, Thushara RM, Chandranayaka S, et al. Emerging roles of hyaluronic acid bioscaffolds in tissue engineering and regenerative medicine. Int J Biol Macromol. 2016;86:917-928.[2]Lam J, Truong NF, Segura T. Design of cell-matrix interactions in hyaluronic acid hydrogel scaffolds. Acta Biomater. 2014;10(4): 1571-1580.[3]Collins MN, Birkinshaw C. Hyaluronic acid based scaffolds for tissue engineering--a review. Carbohydr Polym. 2013;92(2): 1262-1279.[4]Cavallo C, Desando G, Columbaro M, et al. Chondrogenic differentiation of bone marrow concentrate grown onto a hylauronan scaffold: rationale for its use in the treatment of cartilage lesions. J Biomed Mater Res A. 2013;101(6): 1559-1570.[5]Jaipaew J, Wangkulangkul P, Meesane J, et al. Mimicked cartilage scaffolds of silk fibroin/hyaluronic acid with stem cells for osteoarthritis surgery: Morphological, mechanical, and physical clues. Mater Sci Eng C Mater Biol Appl. 2016;64:173-182.[6]Frith JE, Cameron AR, Menzies DJ, et al. An injectable hydrogel incorporating mesenchymal precursor cells and pentosan polysulphate for intervertebral disc regeneration. Biomaterials. 2013;34(37):9430-9440.[7]Han ME, Kim SH, Kim HD, et al. Extracellular matrix-based cryogels for cartilage tissue engineering. Int J Biol Macromol. 2016;93(Pt B):1410-1419. [8]He L, Yang J, Lu J, et al. Preparation and characterization of a novel hyaluronic acid–icariin conjugate hydrogel. Mater Lett. 2014;136: 41-44.[9]Zhu M, Feng Q, Bian L. Differential effect of hypoxia on human mesenchymal stem cell chondrogenesis and hypertrophy in hyaluronic acid hydrogels. Acta Biomater. 2014;10(3):1333-1340.[10]Levett PA, Melchels FP, Schrobback K, et al. A biomimetic extracellular matrix for cartilage tissue engineering centered on photocurable gelatin, hyaluronic acid and chondroitin sulfate. Acta Biomater. 2014;10(1):214-223.[11]Remya NS, Nair PD. Engineering cartilage tissue interfaces using a natural glycosaminoglycan hydrogel matrix--an in vitro study. Mater Sci Eng C Mater Biol Appl. 2013;33(2):575-582.[12]Sheu SY, Chen WS, Sun JS, et al. Biological characterization of oxidized hyaluronic acid/resveratrol hydrogel for cartilage tissue engineering. J Biomed Mater Res A. 2013;101(12):3457-3466.[13]Levingstone TJ, Thompson E, Matsiko A, et al. Multi-layered collagen-based scaffolds for osteochondral defect repair in rabbits. Acta Biomater. 2016;32:149-160.[14]Lebourg M, Martínez-Díaz S, García-Giralt N, et al. Cell-free cartilage engineering approach using hyaluronic acid-polycaprolactone scaffolds: a study in vivo. J Biomater Appl. 2014;28(9):1304-1315.[15]Sawatjui N, Damrongrungruang T, Leeanansaksiri W, et al. Silk fibroin/gelatin-chondroitin sulfate-hyaluronic acid effectively enhances in vitro chondrogenesis of bone marrow mesenchymal stem cells. Mater Sci Eng C Mater Biol Appl. 2015;52:90-96.[16]Dinescu S, G?l??eanu B, Albu M, et al. Biocompatibility assessment of novel collagen-sericin scaffolds improved with hyaluronic Acid and chondroitin sulfate for cartilage regeneration. Biomed Res Int. 2013;2013:598056.[17]刘少英,陈建英,陈倩倩,等. 以交联透明质酸钠为支架体外构建组织工程软骨[J].中国组织工程研究,2014,18(8):1191-1197.[18]Tavakoli E, Mehdikhani-Nahrkhalaji M, Hashemi-Beni B, et al. Preparation, Characterization and Mechanical Assessment of Poly (Lactide-Co-Glycolide)/ Hyaluronic Acid/ Fibrin/ Bioactive Glass Nano-composite Scaffolds for Cartilage Tissue Engineering Applications. Procedia Materials Science. 2015; 11:124-130.[19]Skaalure SC, Dimson SO, Pennington AM, et al. Semi-interpenetrating networks of hyaluronic acid in degradable PEG hydrogels for cartilage tissue engineering. Acta Biomater. 2014;10(8):3409-3420.[20]Park H, Choi B, Hu J, et al. Injectable chitosan hyaluronic acid hydrogels for cartilage tissue engineering. Acta Biomater. 2013; 9(1):4779-4786.[21]李音,颜廷亭,朱伟波,等. 魔芋葡甘聚糖/透明质酸钠纤维膜生物性能的研究[J]. 材料导报B:研究篇, 2013,27(7):90-92,112.[22]Li Z, Kaplan KM, Wertzel A, et al. Biomimetic fibrin-hyaluronan hydrogels for nucleus pulposus regeneration. Regen Med. 2014; 9(3):309-326.[23]Mercuri J, Addington C, Pascal R 3rd, et al. Development and initial characterization of a chemically stabilized elastin-glycosaminoglycan-collagen composite shape-memory hydrogel for nucleus pulposus regeneration. J Biomed Mater Res A. 2014;102(12):4380-4393.[24]Kim DH, Martin JT, Elliott DM, et al. Phenotypic stability, matrix elaboration and functional maturation of nucleus pulposus cells encapsulated in photocrosslinkable hyaluronic acid hydrogels. Acta Biomater. 2015;12:21-29.[25]Jeong CG, Francisco AT, Niu Z, et al. Screening of hyaluronic acid-poly(ethylene glycol) composite hydrogels to support intervertebral disc cell biosynthesis using artificial neural network analysis. Acta Biomater. 2014;10(8):3421-3430.[26]Cui N, Qian J, Xu W, et al. Preparation, characterization, and biocompatibility evaluation of poly(N?-acryloyl-L-lysine)/hyaluronic acid interpenetrating network hydrogels. Carbohydr Polym. 2016; 136:1017-1026.[27]Cui N, Qian J, Liu T, et al. Hyaluronic acid hydrogel scaffolds with a triple degradation behavior for bone tissue engineering. Carbohydr Polym. 2015;126:192-198.[28]Zhu M, Lin S, Sun Y, et al. Hydrogels functionalized with N-cadherin mimetic peptide enhance osteogenesis of hMSCs by emulating the osteogenic niche. Biomaterials. 2016;77:44-52.[29]Bellini D, Cencetti C, Meraner J, et al. An in situ gelling system for bone regeneration of osteochondral defects. European Polymer Journal. 2015;72:642-650.[30]Kisiel M, Martino MM, Ventura M, et al. Improving the osteogenic potential of BMP-2 with hyaluronic acid hydrogel modified with integrin-specific fibronectin fragment. Biomaterials. 2013;34(3): 704-712.[31]Wu AT, Aoki T, Sakoda M, et al. Enhancing osteogenic differentiation of MC3T3-E1 cells by immobilizing inorganic polyphosphate onto hyaluronic acid hydrogel. Biomacromolecules. 2015;16(1):166-173.[32]林永新,丁志勇,周孝斌,等. 透明质酸/壳聚糖复合支架的制备及其力学性能评价[J].中国临床解剖学杂志, 2014,32(1):52-56.[33]Subramaniam S, Fang YH, Sivasubramanian S, et al. Hydroxyapatite-calcium sulfate-hyaluronic acid composite encapsulated with collagenase as bone substitute for alveolar bone regeneration. Biomaterials. 2016;74:99-108.[34]Lequeux C, Rodriguez J, Boucher F, et al. In vitro and in vivo biocompatibility, bioavailability and tolerance of an injectable vehicle for adipose-derived stem/stromal cells for plastic surgery indications. J Plast Reconstr Aesthet Surg. 2015;68(11):1491-1497.[35]Açil Y, Zhang X, Nitsche T, et al. Effects of different scaffolds on rat adipose tissue derived stroma cells. J Craniomaxillofac Surg. 2014;42(6):825-834.[36]Chang KH, Liao HT, Chen JP. Preparation and characterization of gelatin/hyaluronic acid cryogels for adipose tissue engineering: in vitro and in vivo studies. Acta Biomater. 2013;9(11):9012-9026.[37]Jia Y, Fan M, Chen H, et al. Magnetic hyaluronic acid nanospheres via aqueous Diels-Alder chemistry to deliver dexamethasone for adipose tissue engineering. J Colloid Interface Sci. 2015;458:293-299.[38]Dahlmann J, Krause A, Möller L, et al. Fully defined in situ cross-linkable alginate and hyaluronic acid hydrogels for myocardial tissue engineering. Biomaterials. 2013;34(4):940-951.[39]Fiumana E, Pasquinelli G, Foroni L, et al. Localization of mesenchymal stem cells grafted with a hyaluronan-based scaffold in the infarcted heart. J Surg Res. 2013;179(1):e21-29.[40]Young JL, Tuler J, Braden R, et al. In vivo response to dynamic hyaluronic acid hydrogels. Acta Biomater. 2013;9(7):7151-7157.[41]Muscari C, Bonafè F, Martin-Suarez S, et al. Restored perfusion and reduced inflammation in the infarcted heart after grafting stem cells with a hyaluronan-based scaffold. J Cell Mol Med. 2013; 17(4):518-530.[42]Yoon SJ, Hong S, Fang YH, et al. Differential regeneration of myocardial infarction depending on the progression of disease and the composition of biomimetic hydrogel. J Biosci Bioeng. 2014;118(4):461-468.[43]Gaetani R, Feyen DA, Verhage V, et al. Epicardial application of cardiac progenitor cells in a 3D-printed gelatin/hyaluronic acid patch preserves cardiac function after myocardial infarction. Biomaterials. 2015;61:339-348.[44]Duan B, Kapetanovic E, Hockaday LA, et al. Three-dimensional printed trileaflet valve conduits using biological hydrogels and human valve interstitial cells. Acta Biomater. 2014;10(5):1836-1846.[45]Eslami M, Vrana NE, Zorlutuna P, et al. Fiber-reinforced hydrogel scaffolds for heart valve tissue engineering. J Biomater Appl. 2014;29(3):399-410.[46]Zhu C, Fan D, Wang Y. Human-like collagen/hyaluronic acid 3D scaffolds for vascular tissue engineering. Mater Sci Eng C Mater Biol Appl. 2014;34:393-401.[47]Wang LS, Lee F, Lim J, et al. Enzymatic conjugation of a bioactive peptide into an injectable hyaluronic acid-tyramine hydrogel system to promote the formation of functional vasculature. Acta Biomater. 2014;10(6):2539-2550.[48]Addington CP, Heffernan JM, Millar-Haskell CS, et al. Enhancing neural stem cell response to SDF-1α gradients through hyaluronic acid-laminin hydrogels. Biomaterials. 2015;72:11-19.[49]Schizas N, Rojas R, Kootala S, et al. Hyaluronic acid-based hydrogel enhances neuronal survival in spinal cord slice cultures from postnatal mice. J Biomater Appl. 2014;28(6):825-836.[50]Mothe AJ, Tam RY, Zahir T, et al. Repair of the injured spinal cord by transplantation of neural stem cells in a hyaluronan-based hydrogel. Biomaterials. 2013;34(15):3775-3783.[51]吴婷,李朝晖,崔占峰,等. 应用多种水凝胶支架材料构建三维神经干细胞培养模型[J]. 中国细胞生物学学报,2015,37(1):66-73.[52]Entekhabi E, Haghbin Nazarpak M, Moztarzadeh F, et al. Design and manufacture of neural tissue engineering scaffolds using hyaluronic acid and polycaprolactone nanofibers with controlled porosity. Mater Sci Eng C Mater Biol Appl. 2016;69:380-387.[53]Arulmoli J, Wright HJ, Phan DTT, et al. Combination scaffolds of salmon fibrin, hyaluronic acid, and laminin for human neural stem cell and vascular tissue engineering. Acta Biomater. 2016;43:122-138. [54]Wang S, Guan S, Wang J, et al. Fabrication and characterization of conductive poly (3,4-ethylenedioxythiophene) doped with hyaluronic acid/poly (l-lactic acid) composite film for biomedical application. J Biosci Bioeng. 2017;123(1):116-125.[55]Kuo YC, Chen YC. Regeneration of neurite-like cells from induced pluripotent stem cells in self-assembled hyaluronic acid-gelatin microhydrogel. J Taiwan Inst Chem E. 2016;67:74-87.[56]Monteiro IP, Shukla A, Marques AP, et al. Spray-assisted layer-by-layer assembly on hyaluronic acid scaffolds for skin tissue engineering. J Biomed Mater Res A. 2015;103(1):330340.[57]Yan S, Zhang Q, Wang J, et al. Silk fibroin/chondroitin sulfate/hyaluronic acid ternary scaffolds for dermal tissue reconstruction. Acta Biomater. 2013;9(6):6771-6782.[58]Monteiro IP, Gabriel D, Timko BP, et al. A two-component pre-seeded dermal-epidermal scaffold. Acta Biomater. 2014; 10(12):4928-4938.[59]Xiang J, Sun J, Hong J, et al. T-style keratoprosthesis based on surface-modified poly (2-hydroxyethyl methacrylate) hydrogel for cornea repairs. Mater Sci Eng C Mater Biol Appl. 2015;50: 274-285.[60]Liu Y, Ren L, Wang Y. Crosslinked collagen-gelatin-hyaluronic acid biomimetic film for cornea tissue engineering applications. Mater Sci Eng C Mater Biol Appl. 2013;33(1):196-201.[61]Liu Y, Wang R, Zarembinski TI, et al. The application of hyaluronic acid hydrogels to retinal progenitor cell transplantation. Tissue Eng Part A. 2013;19(1-2):135-142.[62]Shang Y, Tamai M, Ishii R, et al. Hybrid sponge comprised of galactosylated chitosan and hyaluronic acid mediates the co-culture of hepatocytes and endothelial cells. J Biosci Bioeng. 2014;117(1):99-106. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [3] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [4] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [5] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [6] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [7] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [8] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [9] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [10] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [11] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [12] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [13] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [14] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [15] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||