Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (20): 3266-3272.doi: 10.12307/2023.444
Previous Articles Next Articles
hFOB1.19 application in bone tissue engineering
Wang Yanyang, Xu Pu
- Department of Oral Implantation, Affiliated Haikou Hospital, Xiangya Medical School, Central South University Hainan Provincial Stomatology Center, Haikou 570208, Hainan Province, China
-
Received:2022-05-20Accepted:2022-07-21Online:2023-07-18Published:2022-11-21 -
Contact:Xu Pu, MD, Chief physician, Department of Oral Implantation, Affiliated Haikou Hospital, Xiangya Medical School, Central South University Hainan Provincial Stomatology Center, Haikou 570208, Hainan Province, China -
About author:Wang Yanyang, Master candidate, Department of Oral Implantation, Affiliated Haikou Hospital, Xiangya Medical School, Central South University Hainan Provincial Stomatology Center, Haikou 570208, Hainan Province, China -
Supported by:the National Natural Science Foundation of China, No. 82060194 (to XP); 2022 Key R&D Project of Hainan Province, No. ZDYF2022SHFZ119 (to XP)
CLC Number:
Cite this article
Wang Yanyang, Xu Pu. hFOB1.19 application in bone tissue engineering[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(20): 3266-3272.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

2.1 hFOB1.19概述 永生化hFOB1.19是从自然流产的婴儿四肢组织中筛选出的一种可以分化为成熟成骨细胞的细胞系。具体方法是在G418环境下,利用编码猴空泡病毒40(Simian vacuolar virus,SV40)的大T抗原基因(T-Ag)的温度敏感突变体tsA58电穿孔转染人胎儿细胞建立永生,并通过碱性磷酸酶活性筛选出的一组细胞。hFOB1.19被认为是较早期的成骨祖细胞,被描述为一种永生化但未转化的细胞系,具有最小的染色体异常和正常的基质蛋白谱,能够迅速增殖并保持稳定的成骨细胞研究模型[7-8]。 永生化是指利用病毒永生化基因、原癌基因或编码永生化基因转染细胞,使细胞能够渡过分裂危险期,延长细胞生长增殖寿命的过程。SV40是一种最早发现于猴肾细胞的病毒,包含有显著延长细胞周期作用的T-Ag基因,是建立永生化细胞株的一种常见基因来源[9-10]。SV40转染后的细胞寿命显著延长,永生化率增加,机制可能涉及端粒的稳定、生长抑制因子的失活等。同时,转染后的细胞形态、表型、分化潜能和生物学特性没有明显变化,且没有明显成瘤性。编码条件温度依赖性T-Ag (如 tsA58)的序列转染后,细胞可在允许温度(约34 ℃ )下可以长时间保持“年轻状态”,增加细胞活力及寿命。高温(39 ℃)时细胞恢复自然状态,细胞增殖能力改变,寿命也恢复至未转染时的状态,生长逐渐停滞或死亡[11]。 2.1.1 细胞形态 hFOB1.19的形态类似于典型的成骨细胞,置于倒置显微镜观察,胞浆嗜碱性,呈梭形、立方形或者锥形,细胞核位于一端,核仁明显,有突起与邻近细胞连接[12]。在培养过程中,刚接种的hFOB1.19呈圆形,最佳黏附时间为30-60 min,细胞逐渐伸出细丝后延长[13]。这种细丝被认为是肌动蛋白组成直径7 nm骨架,对细胞的黏附及延长有影响。培养第3天细胞基本黏附完成,细胞形状变得大而扁平,呈多边形或三角形,逐渐矿化,直到第8-10天矿化结节清晰可见[14]。培养14 d后,使用电子显微镜观察,hFOB1.19的细胞核椭圆,细胞器发达,有由成束的纤维、不规则排列的细纤维和囊泡组成的细胞外基质,与人成骨细胞外基质相似[8],长期培养(20 d)后,细胞呈复层生长,并有矿化结节[14]。 2.1.2 细胞特异性蛋白表达 曾在建立细胞系时,HARRIS等[6]通过免疫组化发现hFOB1.19骨钙素、骨桥素、骨涎蛋白及Ⅰ型胶原蛋白高表达,成熟后还能表达骨形态发生蛋白等。研究者可以通过碱性磷酸酶及上述蛋白特异性表达鉴定hFOB1.19,鉴定方法与原代分离的成骨细胞极为相似[7,12,15-16]。 2.1.3 细胞核型分析 荧光原位杂交实验检测结果显示hFOB1.19的细胞核型与人原代细胞差距不大(除6号染色体上有1个断点),几乎没有恶性发展征兆,植入小鼠体内后核型也能保持稳定[8]。 2.1.4 细胞表型分析 hFOB1.19与骨髓间充质干细胞表达相同的表型CD44,CD73,CD90及CD105,而不表达CD34,CD45及HLA-DR等造血细胞标记物,这与原代人成骨细胞一致[12]。CD146是间充质干细胞的关键标记,赋予细胞克隆形成性和多能性,其在hFOB1.19中高表达,由此可以推断其实际上是胎儿干细胞样细胞而不仅是专门的成骨细胞[17]。hFOB1.19还含有甲状旁腺素受体,可参与内分泌调节过程[6]。同时,hFOB1.19可以参与免疫反应,表达T细胞特异性分子CD6等分子的配体,与T细胞有双向激活作用[18]。 2.1.5 细胞分化潜能 hFOB1.19在39 ℃条件下直接分化成熟,能够表达核结合因子α1和骨钙素的相关mRNA,成熟后开始逐步分泌碱性磷酸酶并矿化。hFOB1.19具有多向分化潜能,与骨髓间充质干细胞有相似性,能有相似的表面标记,如Oct-4和Rex-1等。体外诱导分化实验检测hFOB1.19具有集落形成、迁移能力和作为多细胞聚集体生长的倾向,由此推测其可能属于较早的间充质干细胞[19]。除了其预定途径成熟成骨细胞外,hFOB1.19能够被诱导分化为软骨细胞和脂肪细胞,还能被诱导表达造血细胞及神经样细胞表型[20]。与其他骨细胞一样,hFOB1.19可以被诱导转化为具有骨肉瘤性质的恶性肿瘤细胞[21]。 2.2 hFOB1.19的培养与传代 hFOB1.19需要于-130 ℃以下的液氮的气相中冻存,常规培养温度为34 ℃,CO2体积分数为5%,湿度为100%[7]。34℃适宜细胞迅速增殖,39.5℃时增殖明显降低,会直接分化为成熟的成骨细胞表型,且细胞凋亡未增加。部分研究在37 ℃环境下,此时细胞生长更快[22-25],但是研究表明37 ℃作为半允许温度对“细胞聚集体”形成产生负面影响,并且对细胞的潜在干性特征有影响[17]。与常氧条件(20% O2)相比与生理情况更加接近的缺氧条件(3% O2)可以在一定程度上刺激细胞增殖,但是细胞的迁移能力受阻[17]。并且,细胞常氧情况下参与糖酵解及脂质代谢过程,在缺氧条件下也可以参与糖原代谢[26]。 培养基选用基础培养基HAM’s F12培养基与DMEM培养基1∶1混合,再加质量浓度0.3 g/L遗传霉素418(Geneticin,G418)和体积分数10%的胎牛血清制备完全培养基。也有研究者直接向含有体积分数10%胎牛血清的DMEM培养基中,加入G418、丙酮酸钠和Na2CO3[14,27-29]。因细胞在39 ℃情况下更易分化,所以也有研究强调分化培养,即先常规培养10 d后,将细胞移入39 ℃环境,再在加入了维生素C,D及K的分化培养基中分化培养14 d[31]。 基本培养及传代流程与正常贴壁细胞相似,复苏过程中应避免培养基过碱性,建议将含有完整培养基的培养容器,置于培养箱中15 min,使培养基pH值达到7.0-7.6后再加入细胞,之后每隔两三天更换培养基。 通常细胞生长达到70%-80%后,以1∶3-1∶4比例进行传代。细胞可以传代至第32-34代(34 ℃)或18-20代(37 ℃)后[6, 17],增殖显著减慢。经过多次传代后,细胞大小增加并且迁移能力显著降低,细胞周期调节因子p16和p21的转录增强导致细胞自我更新潜能降低[17]。 2.3 hFOB1.19的应用 ISO及FDA等标准的原理及方法影响了新型骨替代材料的体外细胞实验设计,主要分为3个方面[2,31]:①细胞学研究较多,主要分为细胞形态、黏附、增殖、分化、凋亡和氧化应激等几个方面;②组学研究主要分为基因组、转录组和蛋白质组研究,通常研究生物材料应用后差异的基因和蛋白质;③生物信息学研究的手段有很多,从聚类分析、GO分析、信号通路分析及互相作用网络中挖掘和分析数据,以验证关键基因及蛋白质的影响。综合使用体外细胞实验方法、前期生物材料表征研究及后期体内实验,才能全面评价新型材料的生物性能。 2.3.1 hFOB1.19形态 在2D培养条件下,普遍认为细胞的形态与材料表面粗糙度有关,在细胞相容性好的粗糙表面hFOB1.19呈圆形或扁平状覆盖材料表面,延伸出连接到材料的突触,连续共培养7 d后细胞连接形成细胞群;而在相容性不好的表面细胞生长缓慢且失去正常形态,比正常细胞形态更加细长[32-34]。在3D条件下,细胞容易黏附的培养板表面显示出典型的hFOB表型,细胞伸展并且形成细胞球状体,靠近细胞球内核的细胞不迁移并保持原位[17]。在支架上细胞可通过孔隙生长到支架内部[14,22-23]。在正常培养条件下,3D细胞培养活力小于30 d,生物反应器中3D培养的细胞寿命可以延长到4个月[35]。 部分研究者用染色方法,有研究分别用甲苯胺蓝染色、单宁酸染色观察支架上hFOB1.19,细胞先略缩小再沿纤维长轴方向伸长[36]。OLIVEIRA等[13]用结晶紫染色观察细胞形态呈梭型,细胞核深染,核仁明显,周围有清晰空泡化的细胞质,有单层汇合的迹象。细胞观察法可以横向对比不同粗糙度和相容性表面细胞状态,但实验结果较为主观,可以作为其他细胞研究的补充研究。 2.3.2 hFOB1.19黏附 细胞的黏附可以分为接触、附着、扩散和增殖几个阶段,主要发生在接种后72 h内。与细胞黏附关系密切的有3种蛋白 [35]:①纤连蛋白是细胞外基质的糖蛋白,与组织重塑和修复相关细胞黏附过程中起到重要作用;②整联蛋白,又称整合素,是细胞表面的一种跨膜蛋白,能够与纤连蛋白结合,由α族及β族的多种亚基组成;③纽蛋白,又称附着斑蛋白,是一种膜-细胞骨架蛋白,参与将整联蛋白与肌动蛋白细胞骨架连接。 对于贴壁细胞而言,从球状到盘状的过程是由附着斑和跨膜整合素组成的斑块的形成介导的,它们将细胞骨架锚定到由表面结合细胞分泌的细胞外基质上。所以,研究者可以选择通过形态学变化判断细胞黏附阶段。MENG等[23]将hFOB1.19接种于复合支架1 h后呈球形,有贴壁现象;6 h后伪足延长生长;24 h后细胞基本完全附着,附着的细胞形状不规则;3 d后,细胞呈梭形,表面有突起,通过微丝及伪足紧密黏附在支架上。TONG等[14]在接种1 h内观察到29%的细胞黏附率。在第1,3,7天,细胞从圆形向多边形及典型的成骨细胞形态转变,连接方式也从微丝到伪足,最终形成板状足和丝状足。细胞紧密黏附在支架表面或内部,周围有颗粒状和丝状基质,大量细胞聚集在一起形成“细胞聚集体”[22]。 研究者还通过特殊染色方法来确定细胞的黏附状态,例如鬼笔环肽染色及罗丹明-鬼笔环肽染色显示细胞有丝状伪足延伸和F-肌动蛋白的小斑点[37-38]。有研究使用vinculin-actin-nucleus(V-A-N)三染法分别对附着斑蛋白、肌动蛋白和细胞核染色[29],镜下见细胞骨架,附着斑蛋白分布在细胞的中心和周围区域,细胞面积也显著增加,表明细胞与涂层结合良好。有研究也用V-A-N三染法观察,结果显示细胞具有粗且有规律的丝状肌动蛋白束,附着斑在细胞内广泛分布,表明其伸展能力较好[39]。LIM等[40]整合了图像信息,用考马斯蓝染色并通过图像分析软件进行视觉评估,通过细胞覆盖率和占用面积评估细胞黏附状态结果较为敏感。并通过整联蛋白/肌动蛋白免疫荧光染色显示亲水性好的材料表面有明显的大斑块的整合素亚基,它们与肌动蛋白应力纤维末端的共定位。也有研究使用定量方法分析黏附过程,LOHBERGER等[41]采用实时荧光定量多聚核苷酸链式反应(real time-Quantitative polymerase chain reaction,RT-qPCR分析整合素亚基α1,α3,α5和β1表达及纤连蛋白、整联蛋白、纽蛋白印迹,证实钴铬钼合金钛涂层可以显着增强整联蛋白亚基的表达。LIM等[40]还通过蛋白质免疫印迹法(Western Blot)及RT-qPCR技术分析整合素亚基αv和β3的表达,研究其与骨桥素和Ⅰ型胶原蛋白表达情况的联系,结果表明材料表面润湿性调节整合素介导的骨细胞黏附,进一步影响骨细胞-细胞外基质复合物的表达。 上述常规及染色观察,定性及定量实验方法为研究者们观察hFOB1.19的细胞黏附过程提供许多选择。在研究黏附过程中发现了一个有趣的现象,研究者们常规认为hFOB1.19黏附很大程度取决于材料的表面粗糙度[32-33]。但是也有研究认为,其与样本表面化学没有太大关系,在细胞相容性差的疏水表面的细胞黏附过程只是稍有延迟和减弱,在后续培养过程(3 d)中能够很快恢复状态,实质上细胞重塑了材料表面[35,40]。 hFOB1.19在骨组织工程材料中的形态与黏附情况见图3。"

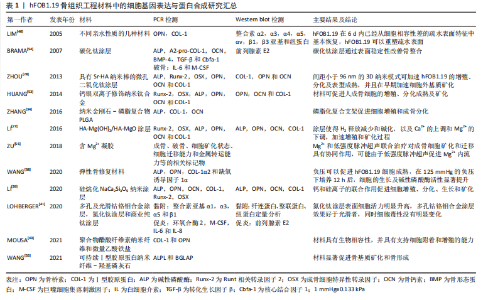
2.3.3 hFOB1.19的增殖、分化和凋亡 研究者通常通过体外细胞增殖状态评价材料生物相容性,hFOB1.19作为成骨细胞模型不仅可以研究材料的毒性作用,还可以研究成骨功能。活-死染色法是测定细胞毒性的常规手段[28,42],DAPI染料也可以穿透细胞膜与DNA强力结合鉴定活细胞[49],EthD-1染色信号可以染色死细胞[43]。有研究用alamar blue法测定硅烷化新型纳米涂层表面大部分细胞染色后呈绿色,表明这些细胞具有高活性,对照组表面有许多细胞死亡,呈红色[39]。 MTT法及在其基础上的WST法和CCK法等,是通过还原活细胞线粒体内的脱氢酶形成带有颜色的物质,再通过分光光度法检测酶含量来确认细胞黏附和增殖状态,是最常见的试验方法[29,33-34,42-48]。现也有更加成熟的成品试剂,原理也是检测线粒体内的乳酸脱氢酶衡量细胞的活力与毒性,在检测速度和结果稳定性上有提升,如CellTiter-Glo?细胞活力、CytoTox ONE?、CellTracker?Green 5和PrestoBlue等[41,45,49]。此外,还有生物发光法,其原理是萤光素酶催化碱性磷酸酶和萤光素形成光,根据光强度计算ATP浓度[50]。 碱性磷酸酶是一种成熟的成骨细胞的典型的标志酶,可以用来判定成骨细胞分化成熟,常与细胞增殖实验联合使用[14,22-23]。 有研究对比了hFOB1.19和Saos-2(人骨肉瘤细胞)2种细胞,分别接种于矿化前后的2种聚己内酯支架,观察细胞黏附并使用MST法、定量碱性磷酸酶分析[36],14 d后,羟基磷灰石层能够在不仅能改善hFOB1.19的黏附,也能够促进增殖、分化过程;但对Saos-2的影响只发生在黏附阶段。 检测细胞凋亡是一种直观反应材料生物相容性的方法,通过观察方法判断形态变化及凋亡小体,或通过上述染色方法鉴定凋亡细胞。Caspase-1是一种与真核细胞凋亡密切相关的水解酶,通过检测其活性可材料细胞毒性[33]。膜联蛋白V-PI染色法,流式细胞术可以帮助判断细胞凋亡的发生时期。有研究使得羟基磷灰石纳米颗粒有效地包覆了3D打印合金支架,通过CCK-8和膜联蛋白V-PI凋亡测定,发现矿化后的支架能够明显增加细胞增殖且对细胞凋亡没有明显促进作用[51]。 当前检测增殖、分化最常用的细胞是小鼠成骨细胞,细胞毒性常用的是小鼠成纤维细胞,成骨材料要求的特殊性是既要无细胞毒性,还需要能够促进成骨过程,此时使用成骨细胞系会更加恰当。生物因子的使用产生附加效果也需要成骨细胞系的检验。然而,当下使用小鼠成纤维细胞L929细胞有相关的毒性有相关检测标准,而成骨细胞系尚且没有。 2.3.4 hFOB1.19的细胞外基质 细胞外基质是成骨实际发生的微环境,成熟的成骨细胞可以分泌Ⅰ型胶原及碱性磷酸酶促进钙离子沉积完成矿化[49,52]。hFOB1.19通常在培养第7天开始矿化,约14 d达到高峰,用茜素红染色观察矿化结节,可以借助图像处理软件分析[28,44,53]。天狼星红可以将胶原蛋白染成深红色,马森三色是一种能够区分细胞的染料组合,它可以使染成蓝绿色的胶原纤维可视化,二者可以配合使用[13,23,53]。 有研究在培养7,14 d发现每个实验组表面的胶原分泌和细胞外基质矿化均增加[39],培养21 d时,使用茜素红染色细胞,可见大小不等的棕红色矿化结节,中央为不透光的黑色颗粒[44]。还有研究证实了晶体表面拓扑结构变化可以影响细胞内Ca2+浓度,从而加速hFOB1.19细胞的增殖、分化及表型成熟,并且在早期加速细胞外基质矿化[28]。此外,可采用X射线能谱分析细胞钾、钙元素的沉积量[54]。免疫细胞化学也可以帮助鉴定细胞外基质中的蛋白质种类,脱矿骨基质培养细胞48 h后,细胞外基质中颗粒物沉积鉴定为纤连蛋白,核周为层黏连蛋白[13]。 成骨细胞矿化位于是分化的最后阶段,矿化情况也是衡量材料能否形成骨质的直观标志。眼下对于细胞外基质中胶原合成及矿化的研究方法多采用染色观察并辅助计算机对图片处理分析,然而众多细胞外基质有关的实验中,定量分析较少且观察时间不连续,缺少对完整矿化过程的研究。 2.3.5 hFOB1.19的组学研究——基因表达及蛋白合成 骨组织工程实验中常通过RT-qPCR技术检测基因表达,通过Western Blot检测蛋白合成情况。检测成骨细胞分化标记物有很多种类,最常见的衡量成骨性的有成骨细胞特异性转录因子(osterix,OSX)、Runt相关转录因子2(Runx2)、骨桥素、骨钙素、Ⅰ型胶原蛋白和骨形态发生蛋白等[27,43,53]。研究者发现碱性磷酸酶是细胞分化早期标志物,在细胞外基质开始矿化后降低,而由BGLAP基因编码的骨钙素是一种重要的非胶原分泌因子,参与骨基质矿化和骨形成的晚期标志物,将随着碱性磷酸酶降低而升高[34,39,55]。 hFOB1.19在骨组织工程材料中的细胞基因表达与蛋白合成研究进展见表1。"
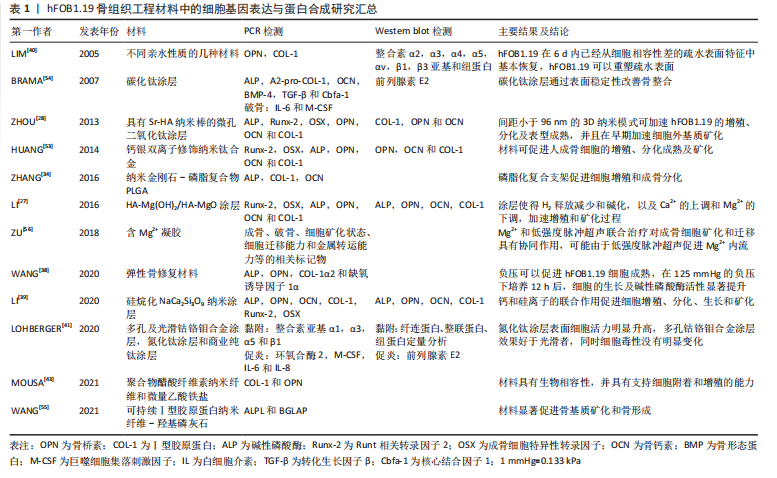
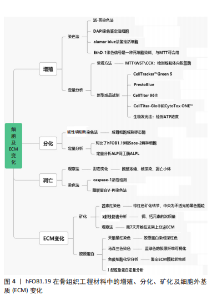
除了成骨标志以外,还可以测量其他因子:转化生长因子β和核结合因子α1(core binding factorα1,Cbfa-1)也可以用来衡量hFOB1.19的成骨分泌合成状态,白细胞介素6和巨噬细胞集落刺激因子衡量细胞破骨状态[28,54];还有细胞矿化状态、细胞迁移能力和金属转运能力等的相关标记物[56]。LOHBERGER等[41]研究新型钛涂层的促炎作用,检测了环氧合酶2、巨噬细胞集落刺激因子、白细胞介素6和白细胞介素8的相对mRNA表达和相应的前列腺素E2水平,发现光滑和多孔的锡涂层具有刺激骨细胞产生抗炎作用。 hFOB1.19的基因表达及蛋白合成情况与其他成骨细胞系既有相似也有不同。ZHANG等[34]发现材料表面生长hFOB1.19与人骨肉瘤细胞MG-63、人骨膜衍生细胞和小鼠成骨细胞等细胞系成骨相关基因表达量具有相同的变化趋势。通常认为,骨肉瘤细胞蛋白质合成较为旺盛,hFOB1.19可能需要更长的作用时间才能达到与MG63相似的蛋白表达水平[25,30]。也有实验发现原代人成骨细胞与hFOB1.19的转化生长因子β1及骨钙素基因表达趋势相同但表达量略有差距,这可能由于细胞活性及培养条件不同[54]。 骨增量材料组学分析主要集中于成骨方面的研究,对于材料潜在的细胞毒性及破骨作用研究尚且较少,完善此方面的研究可以为下一步动物实验及临床试验提供引导,节省实验中间阶段的损耗。组学分析可以对比同一修复材料对不同细胞系的影响,但尚且没有这方面的深入研究。因研究不同特性的标记分子选择多,筛选标记物及建立引物模型可能耗费研究者大量时间,可以利用生物信息学研究提供指导,初步筛选差异明显的特性及标记物。 hFOB1.19在骨组织工程材料中的增殖、分化、矿化及细胞外基质变化情况见图4。"
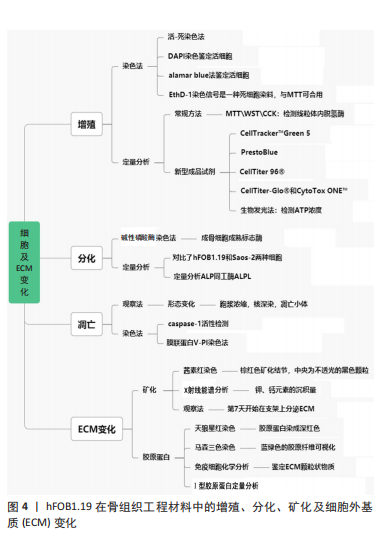

2.3.6 hFOB1.19的生物信息学研究 生物信息学研究通过多种手段从作用网络中挖掘和分析数据,来验证关键基因及蛋白的作用。LU等[57]通过3种不同的酶水解明胶,发现木瓜蛋白酶水解物激活Wnt/β-连环蛋白途径介导细胞增殖和分化效率较高。ZHANG等[58]使用划痕和Transwell检测转化生长因子β1促进细胞迁移,并通过PI3K/AKT信号通路影响下游基因mTOR/S6K1促进hFOB1.19的成骨和矿化。使用3D生物反应器中分别加入HA珠及β-TCP珠循环培养hFOB1.19,DNA微阵列分析表明,HA珠组细胞成骨过程进展迅速,β-TCP珠组只有部分细胞的分化显著[30]。镁基合金作为可吸收金属,降解中产生的Mg2+可能对细胞产生不利影响,而ZHANG等[59]发现Mg2+通过TRPM7/PI3K信号通路上调Runx2和碱性磷酸酶的表达显著增强hFOB1.19细胞成骨活性,为镁基金属作骨修复材料提供理论基础。ZU等[56]通过转录组测序分析低强度脉冲超声和Mg2+联合治疗的效果,微阵列分析表明联合组hFOB1.19细胞中转化生长因子β,MAPK和肿瘤坏死因子信号通路优先过表达,3者具有协同作用。 生物信息学可以使得研究者了解成骨机制,但骨组织工程材料更新迭代速度快,探讨自然成骨状态及骨肉瘤、骨质疏松等病理状态机制结果更加稳定,研究者间数据可以相互交流验证。在骨组织工程材料研究方面,生物信息学可帮助高效调整材料配比及了解研究材料潜在影响。 2.3.7 hFOB1.19的体内实验研究 hFOB1.19常被作为体外实验的良好模型,但现存体内实验记录较少,郭乾臣[15]曾将hFOB1.19接种于小鼠皮下发现细胞没有成瘤性。SUBRAMANIAM等[8]曾将hFOB1.19植入小鼠背部骨缺损处,结果显示没有明显的炎症反应及骨吸收。 目前暂且没有关于hFOB1.19作为骨组织工程材料的种子细胞的相关研究。ATCC建议hFOB1.19仅供实验室研究使用,不用于治疗、食用或诊断[7]。虽然其核型与正常细胞差距很小,但后续研究者可能要进一步验证其遗传安全性。 2.3.8 hFOB1.19的其他实验研究 hFOB1.19在骨组织工程领域除了作为评价生物材料安全性的模型,也被用于研究细胞间相互作用,KAZIMIERCZAK等[60]证实巨噬细胞发生M2极化,可以促进hFOB1.19的分化。KHALIFEHZADEH等[61]使用金属-无机物材料作为转染的载体,研究hFOB1.19的基因转移效率。 2.4 hFOB1.19的优缺点 使用hFOB1.19作为体外实验模型可以弥补一些常用细胞模型的不足。常规选用的动物细胞模型种属来源的差异会使得实验结果与人原代成骨细胞不同[62]。骨肉瘤细胞核型与人原代细胞差距较大,尽管在细胞黏附、骨钙素表达和整合素亚单位表达等方面与正常成骨细胞相似,但它们在3D培养条件下可能恢复恶性状态,同时细胞增殖、碱性磷酸酶表达和基质缺乏矿化方面也表现出异常反应[63]。对比常见的原代人间充质干细胞和成骨细胞模型,hFOB1.19具有更高的可塑性,能够产生连续的一系列细胞[17]。同时,原代人间充质干细胞还存在诱导分化效率低,种子细胞纯化困难的问题[64]。对比其他转基因人成骨细胞,如SV40转染从成年人成骨细胞得到的人成骨细胞系及转染了人端粒酶逆转录基因的永生化成骨细胞系clone5,接近于成熟成骨细胞,干细胞性不如hFOB1.19[63,65]。 当前,hFOB1.19在骨组织工程实验中没有广泛应用,因其存在一些不足,特殊的培养温度(34 ℃)会造成部分实验资源的浪费,允许温度内升高温度培养(37 ℃)又可能影响细胞活性。SV40转染细胞虽然可以具备永生性质,但其能力没有人工编码基因转染建立永生稳定,细胞寿命仅延长到40群体倍增次数。此外,一个位点的核型的不同是否影响了正常细胞的生理功能,由此带来的生物安全性的考虑还需要进一步研究。"

| [1] KOONS GL, DIBA M, MIKOS AG. Materials design for bone-tissue engineering. Nat Rev Mater. 2020;5(8):584-603. [2] 倪卓,杨莎,王应,等.骨替代材料的研究方法及进展[J].深圳大学学报(理工版),2015,32(4):331-342. [3] 徐杨俊,赵建宁.体外培养成骨细胞的研究进展[J].中国骨伤,2010, 23(7):562-565. [4] BRUN P. Culture of human primary bone cells and phenotype assessment. Methods Mol Biol. 2018;1727:413-421. [5] 李楠,王和鸣.体外培养成骨细胞研究新进展[J].中国骨伤,2003, 16(3):63-65. [6] HARRIS SA, ENGER RJ, RIGGS BL, et al. Development and characterization of a conditionally immortalized human fetal osteoblastic cell line. J Bone Miner Res. 1995;10(2):178-186. [7] MAYO FOUNDATION FOR MEDICAL EDUCATION AND RESEARCH. Immortalized human fetal osteoblastic cells: US19960697906[P].1997-12-02. [8] SUBRAMANIAM M, JALAL SM, RICKARD DJ, et al. Further characterization of human fetal osteoblastic hFOB 1.19 and hFOB/ER alpha cells: bone formation in vivo and karyotype analysis using multicolor fluorescent in situ hybridization. J Cell Biochem. 2002; 87(1):9-15. [9] 程斌,程海燕.永生化骨髓间充质干细胞模型的构建[J].现代医院,2015,15(1):13-15. [10] 张露文,戴鹏秀,张翊华,等.猴空泡病毒40大T抗原基因诱导人骨髓间充质干细胞的永生化[J].中国组织工程研究,2022,26(13): 1969-1973. [11] 解慧琪,杨志明,屈艺.SV40与细胞永生化[J].中国修复重建外科杂志,2000,14(3):170-174. [12] 陈文明,陈子兴,岑建农,等.人成骨细胞系hFOB1.19生物学特性的研究[J].中国实验血液学杂志,2008,16(2):339-344. [13] OLIVEIRA PF, PINTO JP, SANTOS AR, et al. Evaluation of the growth and differentiation of human fetal osteoblasts (hFOB) cells on demineralized bone matrix (DBM). Organogenesis. 2021;17(3-4):136-149. [14] TONG S, XU DP, LIU ZM, et al. Construction and in vitro characterization of three-dimensional silk fibroinchitosan scaffolds. Dent Mater J. 2015: 34(4):475-484. [15] 郭乾臣.人骨肉瘤细胞株和成骨细胞株差异蛋白的比较蛋白质组学研究[D].广州:中山大学,2007. [16] JO S, LEE JK, HAN J, et al. Identification and characterization of human bone-derived cells. Biochem Biophys Res Commun. 2018;495(1):1257-1263. [17] MAROZIN S, SIMON-NOBBE B, IRAUSEK S, et al. Kinship of conditionally immortalized cells derived from fetal bone to human bone-derived mesenchymal stroma cells. Sci Rep. 2021;11(1):10933. [18] STANLEY KT, VANDORT C, MOTYL C, et al. Immunocompetent properties of human osteoblasts: interactions with T lymphocytes. J Bone Miner Res. 2006;21(1):29-36. [19] DOMINICI M, LE BLANC K, MUELLER I, et al. Minimal criteria for defining multipotent mesenchymal stromal cells. The International Society for Cellular Therapy position statement. Cytotherapy. 2006;8(4):315-317. [20] YEN ML, CHIEN CC, CHIU IM, et al. Multilineage differentiation and characterization of the human fetal osteoblastic 1.19 cell line: a possible in vitro model of human mesenchymal progenitors. Stem Cells. 2007;25(1):125-131. [21] 孟刚,李懿,辛榕,等.人永生化成骨细胞hFOB1.19恶性转化的研究[J].第三军医大学学报,2007,29(5):380-383. [22] TONG S, XUE L, XU DP, et al. In vitro culture of hFOB1.19 osteoblast cells on TGF-beta1-SF-CS three-dimensional scaffolds. Mol Med Rep. 2016;13(1):181-187. [23] MENG X, GONG K, SUN C, et al. Nonmineralized and mineralized silk fibroin/gelatin hybrid scaffolds: chacterization and cytocompatibility in vitro for bone-tissue engineering. J Craniofac Surg. 2020;31(2):416-419. [24] FERREIRA CF, CARRIEL GOMES MC, FILHO JS, et al. Platelet-rich plasma influence on human osteoblasts growth. Clin Oral Implants Res. 2005; 16(4):456-460. [25] TITORENCU I, ALBU MG, ANTONF, et al. Collagen-dexamethasone and collagen-d3scaffolds for bone tissue engineering. Mol Cryst Liq Cryst. 2012;555(1):208-217. [26] CUI YC, QIU YS, WU Q, et al. Metabolic utilization of human osteoblast cell line hFOB 1.19 under normoxic and hypoxic conditions: a phenotypic microarray analysis. Exp Biol Med (Maywood). 2021; 246(10):1177-1183. [27] LI B, HAN Y, LI M. Enhanced osteoblast differentiation and osseointegration of a bio-inspired HA nanorod patterned pore-sealed MgO bilayer coating on magnesium. J Mater Chem B. 2016;4(4):683-693. [28] ZHOU J, LI B, LU S, et al. Regulation of osteoblast proliferation and differentiation by interrod spacing of Sr-HA nanorods on microporous titania coatings. ACS Appl Mater Interfaces. 2013;5(11):5358-5365. [29] LI B, HAN Y, QI K. Formation mechanism, degradation behavior, and cytocompatibility of a nanorod-shaped HA and pore-sealed MgO bilayer coating on magnesium. ACS Appl Mater Interfaces. 2014;6(20): 18258-18274. [30] NOMOTO H, MAEHASHI H, SHIRAI M, et al. Bio-artificial bone formation model with a radial-flow bioreactor for implant therapy-comparison between two cell culture carriers: porous hydroxyapatite and beta-tricalcium phosphate beads. Hum Cell. 2019;32(1):1-11. [31] MASAELI R, ZANDSALIMI K, TAYEBI L. Biomaterials evaluation: conceptual refinements and practical reforms. Ther Innov Regul Sci. 2019;53(1):120-127. [32] HUAG HS, CHOU SH, DON TM, et al. Formation of microporous poly (hydroxybutyric acid) membranes for culture of osteoblast and fibroblast. Polym Adv Tech. 2009;20(12):1082-1090. [33] GYORGY E, TORICELLI P, SOCOL G, et al. Biocompatible Mn2+-doped carbonated hydroxyapatite thin films grown by pulsed laser deposition. J Biomed Mater Res A. 2004;71(2):353-358. [34] ZHANG F, SONG Q, HUANG X, et al. A novel high mechanical property PLGA composite matrix loaded with nanodiamond-phospholipid compound for bone tissue engineering. ACS Appl Mater Interfaces. 2016;8(2):1087-1097. [35] LIU X, LIM JY, DONAHUE HJ, et al. Influence of substratum surface chemistry/energy and topography on the human fetal osteoblastic cell line hFOB 1.19:Phenotypic and genotypic responses observed in vitro. Biomaterials. 2007;28(31):4535-4350. [36] TANG Y, ZHAO Y, WONG CS, et al. Apatite-coated three-dimensional fibrous scaffolds and their osteoblast response. J Biomed Mater Res A. 2013;101(3):674-683. [37] PANDEY A, MIDHA S, SHARMA RK, et al. Antioxidant and antibacterial hydroxyapatite-based biocomposite for orthopedic applications. Mater Sci Eng C Mater Biol Appl. 2018;88:13-24. [38] WANG R, THAYER P, GOLDSTEIN A, et al. Interaction of material stiffness and negative pressure to enhance differentiation of bone marrow-derived stem cells and osteoblast proliferation. J Tissue Eng Regen Med. 2020;14(2):295-305. [39] LI K, XUE Y, ZHOU J, et al. Silanized NaCa2HSi3O9 nanorods with a reduced pH increase on Ti for improving osteogenesis and angiogenesis in vitro. J Mater Chem B. 2020;8(4):691-702. [40] LIM JY, TAYLOR AF, LI ZY, et al. Integrin expression and osteopontin regulation in human fetal osteoblastic cells mediated by substratum surface characteristics. Tissue Eng. 2005;11(1-2):19-29. [41] LOHBERGER B, STUENDL N, GLAENZER D, et al. CoCrMo surface modifications affect biocompatibility, adhesion, and inflammation in human osteoblasts. Sci Rep. 2020;10(1):1682. [42] KUMAR A, HAN SS. Enhanced mechanical, biomineralization, and cellular response of nanocomposite hydrogels by bioactive glass and halloysite nanotubes for bone tissue regeneration. Mater Sci Eng C Mater Biol Appl. 2021;128:112236. [43] MOUSA HM, HUSSEIN KH, SAYED MM, et al. Development and characterization of cellulose/iron acetate nanofibers for bone tissue engineering applications. Polymers (Basel). 2021;13(8):1339-1356. [44] 刘晓峰,张郑瑶,田秀丽,等.纳米磷酸三钙/明胶/鹿茸多肽复合材料的制备及对人成骨细胞增殖、分化及矿化的影响[J].中国兽医学报,2013,33(6):898-904. [45] BABUSKA V, PALAN J, KOLAJA DOBRA J, et al. Proliferation of osteoblasts on laser-modified nanostructured titanium surfaces. Materials (Basel). 2018;11(10):1827-1840. [46] SMIGA-MATUSZOWICZ M, JANICKI B, JASZCZ K, et al. Novel bioactive polyester scaffolds prepared from unsaturated resins based on isosorbide and succinic acid. Mater Sci Eng C Mater Biol Appl. 2014;45:64-71. [47] HAMDAN ALKHRAISAT M, MOSEKE C, BLANCO L, et al. Strontium modified biocements with zero order release kinetics. Biomaterials. 2008;29(35):4691-4697. [48] TAI HY, CHOU SH, CHENG LP, et al. Asymmetric composite membranes from chitosan and tricalcium phosphate useful for guided bone regeneration. J Biomater Sci Polym Ed. 2012;23(9):1153-1170. [49] ZO S, CHOI S, KIM H, et al. Synthesis and characterization of carboxymethyl chitosan scaffolds grafted with waterborne polyurethane. J Nanosci Nanotechnol. 2020;20(8):5014-5018. [50] DONNADIO A, BINI M, CENTRACCHIO C, et al. Bioinspired reactive interfaces based on layered double hydroxides-zn rich hydroxyapatite with antibacterial activity. ACS Biomater Sci Eng. 2021;7(4):1361-1373. [51] YUAN W, HE X, ZHOU X, et al. Hydroxyapatite nanoparticle-coated 3d-printed porous ti6al4v and cocrmo alloy scaffolds and their biocompatibility to human osteoblasts. J Nanosci Nanotechnol. 2018; 18(6):4360-4365. [52] GU RL, LIU H, ZHU Y, et al. Is extracellular matrix (ECM) a promising scaffold biomaterial for bone repair? Histol Histopathol. 2021;36(12): 1219-1234. [53] HUANG R, HAN Y, LU S. Enhanced osteoblast functions and bactericidal effect of Ca and Ag dual-ion implanted surface layers on nanograined titanium alloys. J Mater Chem B. 2014;2(28):4531-4543. [54] BRAMA M, RHODES N, HUNT J, et al. Effect of titanium carbide coating on the osseointegration response in vitro and in vivo. Biomaterials. 2007;28(4):595-608. [55] WANG JK, CIMENOGLUC, CHEAM NMJ, et al. Sustainable aquaculture side-streams derived hybrid biocomposite for bone tissue engineering. Mater Sci Eng C Mater Biol Appl. 2021;126:112104. [56] ZU H, YI X, ZHAO D. Transcriptome sequencing analysis reveals the effect of combinative treatment with lowintensity pulsed ultrasound and magnesium ions on hFOB1.19 human osteoblast cells. Mol Med Rep. 2018;18(1):749-762. [57] LU M, ZHAO XH. The growth proliferation, apoptotic prevention, and differentiation induction of the gelatin hydrolysates from three sources to human fetal osteoblasts (hFOB 1.19 Cells). Molecules. 2018;23(6):1287-1304. [58] ZHANG Z, ZHANG X, ZHAO D, et al. TGFbeta1 promotes the osteoinduction of human osteoblasts via the PI3K/AKT/mTOR/S6K1 signalling pathway. Mol Med Rep. 2019;19(5):3505-3518. [59] ZHANG X, ZU H, ZHAO D, et al. Ion channel functional protein kinase TRPM7 regulates Mg ions to promote the osteoinduction of human osteoblast via PI3K pathway: in vitro simulation of the bone-repairing effect of Mg-based alloy implant. Acta Biomater. 2017;63:369-382. [60] KAZIMIERCZAK P, KOZIOL M, PRZEKORA A. The Chitosan/Agarose/NanoHA bone scaffold-induced M2 macrophage polarization and its effect on osteogenic differentiation in vitro. Int J Mol Sci. 2021;22(3): 1190-1204. [61] KHALIFEHZADEH R, ARAMI H. DNA-templated strontium-doped calcium phosphate nanoparticles for gene delivery in bone cells. ACS Biomater Sci Eng. 2019;5(7):3201-3211. [62] 孙中洋,李东韬,赵学武,等.成骨细胞体外培养模型的研究进展[J].中国骨质疏松杂志,2015,21(6):733-736,748. [63] JIANG T, XU G, CHEN X, et al. Impact of hydrogel elasticity and adherence on osteosarcoma cells and osteoblasts. Adv Healthc Mater. 2019;8(9):e1801587. [64] 孙亚东,张宏宇,华进联,等.胚胎干细胞体外分化为成骨细胞研究进展[J].中国修复重建外科杂志,2007,21(12):1381-1383. [65] 殷晓雪,陈仲强,郭昭庆,等.转导人端粒逆生长细胞生长发育成骨生长的研究[J].中华医学杂志,2003,83(14):1251-1254. [66] GHASEMI-MOBARAKEH L, KOLAHREEZ D, RAMAKRISHNA S, et al. Key terminology in biomaterials and biocompatibility. Curr Opin Biomed Eng. 2019;10:45-50. [67] KOSKI C, VU AA, BOSE S. Effects of chitosan-loaded hydroxyapatite on osteoblasts and osteosarcoma for chemopreventative applications. Mater Sci Eng C Mater Biol Appl. 2020;115:111041. [68] SARKAR N, BOSE S. Liposome-encapsulated curcumin-loaded 3d printed scaffold for bone tissue engineering. ACS Appl Mater Interfaces. 2019;11(19):17184-17192. [69] LIU Y, QIAO Z, GAO J, et al. Hydroxyapatite-bovine serum albumin-paclitaxel nanoparticles for locoregional treatment of osteosarcoma. Adv Healthc Mater. 2021;10(2):e2000573. [70] MAVER T, MASTNAK T, MIHELIC M, et al. Clindamycin-based 3d-printed and electrospun coatings for treatment of implant-related infections. Materials (Basel). 2021;14(6):1464-1481. [71] VIDAL-GUTIERREZ X, PRADO-PRONE G, RODIL SE, et al. Bismuth subsalicylate incorporated in polycaprolactone-gelatin membranes by electrospinning to prevent bacterial colonization. Biomed Mater. 2021. doi: 10.1088/1748-605X/ac058d. [72] HADRUP N, SHARMA A, LOESCHNER K. Toxicity of silver ions, metallic silver, and silver nanoparticle materials after in vivo dermal and mucosal surface exposure: a review. Regul Toxicol Pharmacol. 2018;98:257-267. [73] RADHAKRISHNAN S, NAGARAJAN S, BELAID H, et al. Fabrication of 3D printed antimicrobial polycaprolactone scaffolds for tissue engineering applications. Mater Sci Eng C Mater Biol Appl. 2021;118:111525. |
| [1] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| [2] | Qin Yuxing, Ren Qiangui, Li Zilong, Quan Jiaxing, Shen Peifeng, Sun Tao, Wang Haoyu. Action mechanism and prospect of bone microvascular endothelial cells for treating femoral head necrosis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 955-961. |
| [3] | Zhang Min, Zhang Xiaoming, Liu Tongbin. Application potential of naringin in bone tissue regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(5): 787-792. |
| [4] | Chen Feng, Ren Guowu, Zhang Xiaoyun, Chen Yueping, Shi Rusheng. Receptor activator of nuclear factor-kappa B ligand signal transduction mechanism and osteoclast activation [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(2): 293-299. |
| [5] | Xue Peng, Du Bin, Liu Xin, Sun Guangquan, Cheng Tongfei, Chen Hao, He Shuai. Characterization and osteogenic ability of Mg-F membrane/icariin membrane/beta-tricalcium phosphate scaffolds fabricated by coating process combined with 3D printing [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(16): 2480-2487. |
| [6] | Huang Yixuan, Du Bin, Liu Xin, Yuan Xinwei, Xi Hongzhong, Guo Mingbin, Mai Jianbin. Research progress and application prospect of polyethyleneimine in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(16): 2563-2570. |
| [7] | Jia Yuanyuan, Duan Mianmian, Tang Zhenglong. Research and application of local drug delivery system in promoting fracture healing [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(16): 2587-2594. |
| [8] | Huang Yanni, Yang Hua, Yang Dongmei, Hu Xulin, Gao Hong, Huang Yina. Rat bone defect repaired with polytrimethylene carbonate/beta-tricalcium phosphate microsphere scaffold [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(12): 1856-1862. |
| [9] | Zhang Zihan, Wang Wenli, Li Jinnuo, Li Yourui. Effects of carvacrol on osteoblasts and common oral pathogens [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(11): 1765-1771. |
| [10] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [11] | Kang Kunlong, Wang Xintao. Research hotspot of biological scaffold materials promoting osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 597-603. |
| [12] | Li Hui, Chen Lianglong. Application and characteristics of bone graft materials in the treatment of spinal tuberculosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 626-630. |
| [13] | He Yunying, Li Lingjie, Zhang Shuqi, Li Yuzhou, Yang Sheng, Ji Ping. Method of constructing cell spheroids based on agarose and polyacrylic molds [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 553-559. |
| [14] | Lin Zhiyu, Han Jie, Ren Guowu, Chai Yuan, Wen Shuaibo, Wu Yukun, Xie Xiaozhong, Jin Wanqing. Active components of flemingia in regulating the signaling pathways related to knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(36): 5889-5896. |
| [15] | Zhang Chang, Yu Zhengwen. Application of manganese in biomaterials: current situation and problems [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(34): 5504-5511. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||