Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (16): 2609-2615.doi: 10.12307/2023.109
Previous Articles Next Articles
Application of endovascular steerable catheter system in interventional surgery
Guo Tingting, Cui Chaoqiang, Liu Baokun, Gu Hao, Zhou Dong
- Department of Vascular Surgery, Second Hospital of Lanzhou University, Lanzhou 730030, Gansu Province, China
-
Received:2022-04-24Accepted:2022-05-19Online:2023-06-08Published:2022-11-11 -
Contact:Zhou Dong, Associate professor, Chief physician, Master’s supervisor, Department of Vascular Surgery, Second Hospital of Lanzhou University, Lanzhou 730030, Gansu Province, China -
About author:Guo Tingting, Master candidate, Department of Vascular Surgery, Second Hospital of Lanzhou University, Lanzhou 730030, Gansu Province, China -
Supported by:Natural Science Foundation of Gansu Province, No. 20JR10RA721 (to ZD)
CLC Number:
Cite this article
Guo Tingting, Cui Chaoqiang, Liu Baokun, Gu Hao, Zhou Dong. Application of endovascular steerable catheter system in interventional surgery[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(16): 2609-2615.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

2.1 手动操纵导管系统 目前,应用于临床微创介入治疗中的可调弯导管大部分为手动操纵导管系统,为了解决临床外科医生在一些复杂手术中难以精准地控制导管进入病变位置等问题,研究者对手动操纵导管系统进行不断地改进。早在1996年,LIM等[7]就利用硅-玻璃连接结构发明了一种用于微创诊断技术和经皮外科治疗的多关节多向导管,这在可操纵导管系统的发展历史上具有重要意义。DEBOER[8]于2007年设计了一种液压室驱动导管,在其轴壁上具有4个平行转向室,每个转向室都充满了可增压流体,导管的手柄中有一个4个按钮的控制系统,每个按钮都连接到一个转向室;通过按动一个或多个按钮使转向室内部流体压力发生变化,在特定方向产生弯曲力从而使导管尖端弯曲;另外,当同时按压所有按钮可暂时增加导管的刚度和可推性,但是由于这种液压驱动原理可能会对人体产生严重的危害而未投入到后续商业生产之中。 为了实现全向弯曲和多自由度,有研究提出可以使用多根平行电缆来对导管尖端进行变形控制,WATSON[9]就在专利中描述了一种具有2根平行排列电缆的不对称的双向导向导管,他在尖端加入镍钛诺或不锈钢等材料并利用它们不同的横向弯曲性能来获得2条不对称的曲线,其利用2根转向电缆,从近端手柄穿过轴来在2个方向上驱动柔性尖端,将这种理念运用于临床之中的就是Agilis NxT可调弯导管,可在不对称曲线下提供双向导向[10]。同样是设计一种多自由度导管,ALI等[11]则设计了一种通过一只手的拇指和食指操作2个独立操纵杆就可驱动导管尖端的四自由度的导管,称为西格玛导管,在多个平面中,通过使用2个可转向段可创建S形曲线并使导管尖端沿圆形路径移动;TANGEN等[12]对DEAM设计和生产的一系列具有相对较硬的导管主体和灵活可操纵尖端的可导向导管进行了测试,这种手动可操纵导管可通过手柄来推/拉和旋转机械手将导管尖端弯成大约90°并分别旋转360°并且操作者可完全控制导管远端尖端的方向,而无需旋转导管本身,因此避免了从近端控制手柄向远端尖端传递扭矩的挑战。 下文将目前已应用于临床介入治疗中的手动可操纵导管进行对比成表,见表2,具体分为以下几种:Fustar可调节弯曲导管通过在血管系统建立通道将器械或药物带入或带出病变位置,多用于经皮血管造影或治疗;日本生产的Terumo亲水涂层长导管,其管尖笔直弯曲,长度45-90 cm,适用于内脏腔内治疗动脉、颈动脉、椎动脉和锁骨下动脉等病变;Ansel 长导管具有专为肾动脉设计的弯曲尖端,长度为 45 cm,内径为6F,适用于肾动脉、肠系膜上动脉、脾动脉等内脏动脉的超选择性治疗;Balkin长导管,俗称交叉导管,长度为40 cm,内径6-8F,具有专门为下肢动脉交叉治疗而设计的弯曲尖端[13];CPS Venture导管,分为长度54 cm和61 cm,内径7F,可提供多种弯度,主要应用于冠状动脉以及外周动脉的介入治疗中的单向可操纵导管[11];SwiftNINJA是一种无需导线的可导向微导管,它具有180°的旋转尖端,可通过简单地转动导管中心的一个塑料刻度盘来操控从而进入一些复杂的血管,如其尖端不到3 min就可到达子宫左动脉,与平均手术时间为55 min的标准经桡动脉子宫动脉栓塞术相比,手术时间减少了60%,该导管还可应用于介入治疗中的更多更广泛的领域[14]。第二代螺旋测绘导管(Achieve Advance,Medtronic Inc,Minneapolis,MN,SMC2)将电线绕在芯线上并且不含一代螺旋测绘导管的钢护套,这种设计的改变使导管有一个更灵活的轴从而随意弯曲[15]。"
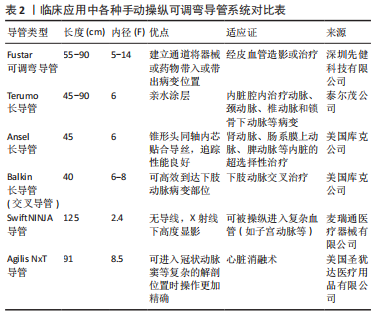
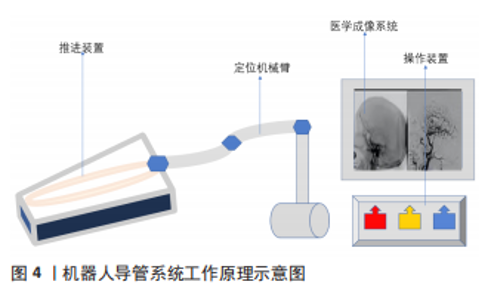
先前叙述的这些手动可操纵导管虽可进行各种曲线的弯曲变形,但临床医生不能在手术过程中对导管尖端进行精准的定位。因此有研究者提出可用超声引导导管来进行精准的定位。目前的超声引导导管是基于9F Unison鞘来设计的,它不需要将微创工具和超声机直接连接也不需要对扫描仪的硬件或软件进行修改,而是使用现有的多普勒超声机作为引导。KUMAR等[16]设计了一种可以通过脉冲波多普勒成像和多普勒谱图精确定位导管尖端的微型压电晶体,并开发了一种具有声活性尖端的导管,他所提出的新算法可通过脉冲波多普勒明确识别,并可通过独特的彩色覆盖实时可视化,这种实时识别导管尖端的能力有助于超声引导下的活检和微创手术[17]。KATAYAMA等[18]采用常规彩色多普勒成像技术对超声引导导管进行心内导航,通过脉冲波多普勒采样窗口交互式地识别和跟踪导管尖端并且通过彩色多普勒标记器瞬间识别导管尖端,这种颜色标记引导声学活性导管尖端到心内目标点较B型超声具有更高的空间精度。BELOHLAVEK等[19]证实了可以使用彩色多普勒超声心动图来引导静脉-静脉体外膜氧合套管,可通过单独的颜色标记识别其每个端口并在端口内嵌入压电晶体实现静脉-静脉体外膜氧和套管的声活性。每个晶体振动与多普勒成像信号的声学相互作用产生多普勒频移,并产生瞬时彩色标记,从而定位导管在体内的位置。这些研究使超声可被用于图像引导,并作为一种可选择性导航的微创手术的方法在临床中越来越流行。 经过不断的改进,手动操纵导管系统从刚开始只可以通过手柄来调节导管尖端固定变形到可通过手柄来进行尖端的大角度弯曲变形,再到导管可用超声来进行图像引导,外科医生通过显示器可追踪导管在患者体内的具体位置,这极大提高了手术的成功率。但手动操纵导管仍然有很多不足之处,例如医生需暴露在大量辐射下;医生与患者直接接触增加了患者感染的概率;医生长时间穿铅衣在术中难免手会抖动,这很可能给患者带来术后并发症等。 2.2 磁驱动导管系统 其远端具有(电)磁性元件,通过调节内部或外部磁场来调节磁力的大小和方向并通过控制磁场的强度和方向将磁性驱动导管尖端导入体内,主要分为外部磁驱动导管系统(又称机器人导管系统)和内部磁驱动导管系统。 2.2.1 内部磁驱动导管系统 其主要是将电磁铁加入到导管尖端,利用导管尖端自身产生的电磁场来实现自身的弯曲变形,但是利用这种方式想要达到多自由度变形需要多个用于弯曲方向的电磁铁、磁活性元件以及能量供应。早在2009年就有科学家提出在导管尖端加入电磁铁,使用生物相容性热塑性材料和不锈钢编织复合材料来制造导管轴并提出了一种二自由度导管,他们在其导管末端植入4个电磁铁,彼此相对位置为90°,每2个电磁铁连接一个转向开关,允许电流供应到2个电磁铁中。因此,通电的电磁铁可以拉动附着在导管尖端的磁性元件,使导管尖端偏转。这种变形方式即使可以自由度转向,但需要复杂的设计,因此只限于理论尚未投入商业生产[10]。 2.2.2 外部磁驱动导管系统(机器人导管系统) 机器人导管系统一般由4个部分组成:推进装置、定位机械臂、操作装置和医学成像系统。如图4所示,推进装置在患者端可代替医生手指完成导管的推进、拔出及捻旋等;定位机械臂可固定推进装置实现准确定位、固定并防止抖动;操作装置使医生可以远程操作避免身体疲劳和辐射;医学成像系统可实现在术中导管的跟踪和定位。与内部磁驱动导管系统不同的是,机器人导管系统虽有与其相同的导管尖端的磁性元件,但是这些元件是由导管外部的外部磁场来控制的,它不仅可以在导管尖端加入电磁铁,也可加入永磁铁。美国食品和药物管理局(FDA)先前已经开发并批准了2种远程导管系统Niobes(Stereotaxis,St-Louis,MO,USA)和SenseisX (Hansen Medical Inc.,Mountain View,CA,USA)系统。前者在导管尖端安装了一个永磁铁,利用2个计算机控制永磁体在患者体内产生磁场,通过调节磁场的方向来控制导管尖端的灵活运动,它能准确实现导管定位;另外,由于它使用的是外部磁场驱动的软导管而不是传统的刚性导管,这极大地减少了组织损伤的概率。后者则采用机器人导向鞘系统来操纵心脏导管,它由一个带有本能运动控制器的大型工作站组成,该控制器通过记录操作员的手部运动然后利用主从控制系统将这些运动通过远程导管操纵器和导向鞘转化为导管的三维运动[20]。这2种机器人导管系统虽然可以让导管尖端达到外科医生的预期变形,但系统需要专有的护套并且费用极其昂贵,不能满足大部分患者的需求。为了解决上述2种机器人导管系统带来的昂贵费用的问题,有研究构思并开发了一种Amigot远程导管系统[20],该系统由一个手持导管手柄和一个光滑的机器人导管操纵器组成,并能够在无菌条件下通过外部机器人设备远端握住并操作不同规格的导管。与上述2种机器人导管系统相比,Amigot不需要单独的工作站或专有的导管或鞘就可以发挥同样的作用,因此,它的实施成本更低,并且很容易地集成到现有的电生理实验室中。它的另一个独特之处在于它的导管手柄可以快速摆脱系统的控制,在一些较为复杂的情况下为外科医生提供最大的灵活性。"
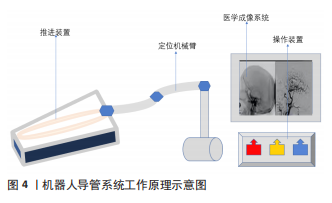

MRI驱动导管系统是一种新型的机器人导管系统,可利用MRI对导管尖端进行远程控制以及可视化。导管主体上的载流线圈提供扭矩,在MRI的磁场下通过控制通过线圈的电流来精确地控制导管[21],设计和控制MRI驱动导管需要一个足够快速和准确的导管模型。GREIGARN等[21]发明了一种伪刚体模型应用于连续体机器人中并进行了验证,这种伪刚体模型主要通过用柔性连杆充当关节将刚性连杆连接,由于柔性连杆具有弹性,可通过设计柔性连杆的数量来达到导管尖端的精准变形。由于其具有柔韧的身体并且能进入人体难以到达的部位,现被广泛应用于医疗领域。为了解决以往导管的局限性,第3代磁远程控制导管利用激光光刻技术构造了双鞍形线圈尖端,这种MRI驱动导管可在MRI下进行绘图、远程操纵、消融引导和实现病变可视化[22]。 随着机器人导管系统的不断发展,可靠的机器人结构设计仍然是一个重点关注的问题,同时机器人系统的安全性及简单性在相关系统设计中变得越来越重要。心血管介入导管系统中的金属与MRI中存在的射频场的电磁耦合对人体会产生很大的危害,为了解决这个问题,ALIPOUR等[23]发明了一种可通过充分衰减金属编织/管上的感应电流,使用微型共振浮动射频场陷阱进行内部布线并可以主动跟踪的心血管介入导管的MRI。具有丰富临床经验的外科医生在介入治疗中可达到较高的手术精度,但却无法感知导管尖端与血管壁之间的接触力,而在介入手术过程中,任何错误的操作都可能对患者的血管产生不可逆的伤害。为了最大程度上减小介入手术对患者的损伤,YIN等[24]发明了一种基于触觉的磁阻流体驱动的主从系统,并验证了对于一些毫无导管操作经验的志愿者来说,在进行操作导管的过程中,基于触觉的主从系统相较于视觉反馈更具有优越性和实用性;另外,YANG等[25]利用一种旋转手指结构来模仿外科医生旋转导丝的运动,通过杠杆结构来测量输送导丝的阻力。CHA等[26]将摩擦轮和伸缩杆结构相结合设计了一种巧妙的装配式机器人,利用电机电流的变化来评估导丝在输送过程中的阻力。ZHOU等[27]发明了一种简单的基于约束管的薄膜传感器来对弯曲进行反馈的用于经导管动脉化疗栓塞术的四自由度遥控机器人系统,该系统通过一个自定义的“S”形函数来稳定机器人导管系统的速度并开发了一种力敏感模块来解决导丝在直线输送过程中的阻力检测问题。CHOI等[28]发明了一种独特的双运动模块化滚轮的机器人导管系统,它可同时控制导管的平移和旋转运动并且具有主动夹紧功能,这能够更有效地将导管导航到所需的血管分支,并在后续的动物实验和试点临床试验中证明了该机器人导管系统的具有良好的定位精度和临床可行性。MA等[29-30]设计了一种由压力传感器、扭矩传感器、步进电机和控制器组成的主端和具有力反馈检测装置的从端的新型机器人导管系统,并在研究中将BP神经网络与传统PID控制器相结合发明了一种新型控制器,这种控制器可以更有效、智能的调节PID控制参数、更快更好地反映控制器的输出并且通过仿真实验验证了其可行性和优越性。FAGOGENIS等[31]在导管尖端将内窥镜、机器学习和图像处理算法结合起来,形成一种混合成像和触摸传感器,这不仅可以提供导管尖端所接触物体的清晰图像,同时也可以识别其所接触物体(如血液、组织及瓣膜)及其按压的强度,并将触觉视觉作为导航算法的唯一感官输入同时控制导管尖端对组织施加的力。 现机器人导管系统虽已发展较为成熟,已部分应用于临床并取得可喜的成果。机器人导管系统较手动操纵导管系统具有以下几点优势:首先,它可使外科医生实现远程操作,这使外科医生及患者都可减少射线辐射;其次,它可利用图像导航等精准定位病变位置并进行精准操作,这可使手术时间减少并且减少手术并发症;最后,它可减少医生与患者之间的接触,减少交叉感染的概率。但是机器人导管系统部分功能还未健全,例如:医生无法灵敏感受到手术过程中导管尖端的受力情况;另外,现已应用于临床的机器人导管系统只能完成固定的手术,不可灵活地应用。文章认为,机器人导管系统未来的发展趋势应该是结构更加轻巧、力感更加精准、主从运动控制更加合理。 2.3 软材料驱动导管系统 2.3.1 导电聚合物驱动导管系统 电活性聚合物可通过电化学掺杂后改变其形状,当离子被轴向驱入此类聚合物时,聚合物会沿轴向改变其体积,而当离子被横向驱入此类聚合物时,聚合物会弯曲。将由电活性聚合物制成的导管尖端置于电解质环境中,施加电流后,离子被驱使进入聚合物一侧,这可驱动导管尖端进行弯曲。与形状记忆合金相比,其响应速度快,由低电压驱动,在没有电解和热量的潮湿条件下对人体相对更安 全[32]。导电聚合物驱动导管系统的优点包括:低电压、微型化和迅速响应[33]。 早在1996年,DELLASANTA等[34]就提出了2种直径为 0.8 mm的导电聚合物导管,在一种导管中,导管壁嵌入了带有固体聚合物电解质的薄带状导电聚合物;在另一种导管中,导管壁由嵌入固体聚合物电解质弹性体基质(50%固体聚合物电解质和50%导电聚合物纤维)中的导电聚合物纤维制成,其最大弯曲角度分别为 28°和24°,这种导电聚合物导管的缺点是其刚度太低。SEWA等[35]将全氟羧酸薄膜两面进行化学镀金,在2 V输入电压下,聚合物可以在水中弯曲 90°,远端尖端位移 8 mm,这种大位移和大弯曲角度使导电聚合物应用于可操纵导管系统中成为可能。FANG等[36]发明了一种基于离子聚合物金属复合材料的用于心导管插入术的导丝。将一对平行的离子聚合物金属复合材料固定在导丝的远端,一个作为驱动器,另一个作为传感器,通过控制信号的频率对其进行控制。低频信号使导丝变形并改变其表面电阻,而高频信号保留其变形信息。利用锁定放大器对高频信号进行解调,可以测量变形。导电聚合物的主要缺点是相对较低的响应性和非线性,因此可以良好控制这种驱动将是一个巨大挑战。 2.3.2 形状记忆材料导管 形状记忆材料是一种可以根据给定的刺激(如光、温度、湿度、磁场和pH值等)改变其形状或性能的材料(合金、聚合物、凝胶或复合材料)。形状记忆合金是一种可以保持固定形状并通过热刺激恢复到另一形状的金属,镍钛合金是常用的形状记忆合金材料。HAGA等[37]在导管内层管和硅酮外层管之间放置了镍钛形状记忆合金微线圈从而使导管可进行自由弯曲。在BLANC等[38]的综述中描述了一种基于低电压驱动的导电聚合物而发明的具有可控尖端的新型驱动导管,将形状记忆凝胶作为机器人的连杆,在柔性连杆(热)和刚性连杆(冷)之间切换使导管尖端进行弯曲变形。AYVALI等[39]设计了一种单边丝驱动二自由度弯曲导管,导管具有3个通过形状记忆合金线驱动器相互连接的直不锈钢尖端部分,驱动导管与电源线直接接触,可用于前列腺和乳腺穿刺活检。LU等[40]发明了一种基于形状记忆合金的单段微型化驱动导管,通过半自动方式改善导管尖端的弯曲运动,从而减少血管壁相关损伤。SELVARA等[41]发明了一种基于双晶状结构的更高效、更安全的智能导管尖端,该导管通过将热响应水凝胶放置在嵌入加热器的柔性聚酰亚胺条上,通过调节加热器的输入功率来实现导管尖端结构的可控弯曲。这虽然暂未应用于商业导管系统之中,但为导管系统未来的发展趋势提供了具有价值的参考意义。 近年来,形状记忆聚合物因其具有低成本、质量轻、良好的生物相容性、生物降解吸收性、易驱动和性能可控等一系列优点而备受广大研究者的喜爱。目前,研究者将形状记忆聚合物与其他材料复合研制出多种可在温度控制下驱动或改变性能的产品,并将其运用至医学应用中如药物定点释放、血栓清除器以及心脏支架等。在未来,形状记忆聚合物将会更广泛的应用于可操纵导管系统中,并且它可以实现更多的适宜人体环境的驱动方法如光、pH值、水和电磁等,有较好的医学应用前景。"

| [1] 刘光,段翠海,张海军.介入手术输送系统研究进展[J].介入放射学杂志,2018,27(7):695-699. [2] TAKAYAMA T, PHELAN PJ, MATSUMURA JS. Directional tip control technique for optimal stent graft alignment in angulated proximal aortic landing zones. J Vasc Surg Cases Innov Tech. 2017;3(2):51-56. [3] LEONG BDK, JOSEPH FS. Total percutaneous femoral approach for branched custom-made device endovascular repair of thoracoabdominal aneurysm. Ann Vasc Dis. 2020;13(3):347-350. [4] MANZUR M, MAGEE GA, ZIEGLER KR, et al. Caudally directed in situ fenestrated endografting for emergent thoracoabdominal aortic aneurysm repair. J Vasc Surg Cases Innov Tech. 2021;7(3):553-557. [5] GYANO M, CSOBAY-NOVAK C. A Modified through and through guidewire steerable sheath technique for transfemoral access to visceral arteries with hostile anatomy. EJVES Vasc Forum. 2021;51:27-28. [6] MAZZACCARO D, CASTRONOVO EL, RIGHINI P, et al. Use of steerable catheters for endovascular procedures: report of a case and literature review. Catheter Cardiovasc Interv. 2020;95(5):971-977. [7] LIM G, PARK K, SUGIHARA M, et al. Future of active catheters. Sensors and actuators a: physical. 1996;56(1):113-121. [8] DE BOER J. Multi-lumen steerable catheter for therapeutically treating patient, comprises flexible catheter shaft and hub including actuators, where actuators are activated so that pressures of fluids are increased in steering lumens, US2007060997-A1. <Go to ISI>://DIIDW:2007438521. [9] WATSON JR. Asymmetric dual directional steerable catheter sheath: US, US8500733 B2. 2013. [10] ALI A, PLETTENBURG DH, BREEDVELD P. Steerable catheters in cardiology: classifying steerability and assessing future challenges. IEEE Trans Biomed Eng. 2016;63(4):679-693. [11] ALI A, SAKES A, ARKENBOUT EA, et al. Catheter steering in interventional cardiology: mechanical analysis and novel solution. Proc Inst Mech Eng H. 2019;233(12):1207-1218. [12] TANGEN GA, MANSTAD-HULAAS F, NYPAN E, et al. Manually steerable catheter with improved agility. Clin Med Insights Cardiol. 2018;12: 117954681775143. [13] MAO H, WANG F, BAO J, et al. conventional endovascular devices. Endovascular Surgery and Devices. Springer Nature. 2018. [14] MARTIN JT, HULSBERG PC, SOULE E, et al. Welcome to the new era: a completely wireless interventional procedure. Cureus. 2018;10(9): e3337. [15] POTT A, PETSCHER K, BAUMHARDT M, et al. Novel spiral mapping catheter facilitates observation of the time-to-pulmonary vein isolation during cryoballoon ablation. Heart Vessels. 2019;34(3):496-502. [16] KUMAR V, KATAYAMA M, PEAVLER R, et al. Real-Time visualization of an acoustically active injection catheter with ultrasound imaging: algorithm and in vivo validation in a swine model. IEEE Trans Biomed Eng. 2019;66(11):3212-3219. [17] KUMAR V, LIU R, KINNICK RR, et al. Unambiguous identification and visualization of an acoustically active catheter by ultrasound imaging in real time: theory, algorithm, and phantom experiments. IEEE Trans Biomed Eng. 2018;65(7):1468-1475. [18] KATAYAMA M, ZARBATANY D, CHA SS, et al. Acoustically active catheter for intracardiac navigation by color doppler ultrasonography. Ultrasound Med Biol. 2017;43(9):1888-1896. [19] BELOHLAVEK M, KATAYAMA M, VAITKUS VV, et al. A real-time color doppler marker for echocardiographic guidance of an acoustically active extracorporeal membrane oxygenation cannula. J Ultrasound Med. 2019;38(7):1875-1885. [20] SHAIKH ZA, EILENBERG MF, COHEN TJ. The amigo remote catheter system: from concept to bedside. J Innov Card Rhythm Manag. 2017; 8(8):2795-2802. [21] GREIGARN T, JACKSON R, LIU T, et al. Experimental validation of the pseudo-rigid-body model of the MRI-actuated catheter. IEEE Int Conf Robot Autom. 2017;2017:3600-3605. [22] LIU T, LOMBARD POIROT N, GREIGARN T, et al. Design of a magnetic resonance imaging guided magnetically actuated steerable catheter. J Med Device. 2017;11(2):0210041-2100411. [23] ALIPOUR A, MEYER ES, DUMOULIN CL, et al. MRI conditional actively tracked metallic electrophysiology catheters and guidewires with miniature tethered radio-frequency traps: theory, design, and validation. IEEE Trans Biomed Eng. 2020;67(6):1616-1627. [24] YIN X, GUO S, SONG Y. Magnetorheological fluids actuated haptic-based teleoperated catheter operating system. Micromachines (Basel). 2018. [25] YANG X, WANG H, SUN L, et al. Operation and force analysis of the guide wire in a minimally invasive vascular interventional surgery robot system. Chin J Mech Eng. 2015;28(2):249-257. [26] CHA HJ, YI BJ, WON JY. An assembly-type master–slave catheter and guidewire driving system for vascular intervention. Proc Inst Mech Eng H. 2016;231(1):69-79. [27] ZHOU J, MEI Z, MIAO J, et al. A remote-controlled robotic system with safety protection strategy based on force-sensing and bending feedback for transcatheter arterial chemoembolization. Micromachines. 2020;11(9):805. [28] CHOI J, PARK S, KIM YH, et al. A vascular intervention assist device using bi-motional roller cartridge structure and clinical evaluation. Biosensors (Basel). 2021;11(9):329. [29] MA X, ZHOU J, ZHANG X, et al. Design of a new catheter operating system for the surgical robot. Appl Bionics Biomech. 2021;2021(1):1-9. [30] MA X, ZHOU J, ZHANG X, et al. Development of a robotic catheter manipulation system based on BP neural network PID controller. Appl Bionics Biomech. 2020;2020:8870106. [31] FAGOGENIS G, MENCATTELLI M, MACHAIDZE Z, et al. Autonomous robotic intracardiac catheter navigation using haptic vision. Sci Robot. 2019;4(29):eaaw1977. [32] TADOKORO S, MURAKAMI T, FUJI S, et al. An elliptic friction drive element using an ICPF actuator. IEEE Control Systems Magazine. 1997; 17(3):60-68. [33] SMELA EA. Conjugated polymer actuators for biomedical applications. Adv Mater. 2010;15(6):481-494. [34] DELLASANTA A, MAZZOLDI A, DEROSSI D. Steerable microcatheters actuated by embedded conducting polymer structures. J Intell Mater Syst Struct. 1996;7(3):292-300. [35] SEWA S, ONISHI K, ASAKA K, et al. Polymer actuator driven by ion current at low voltage, applied to catheter system//Eleventh International Workshop on Micro Electro Mechanical Systems. IEEE. 1998. [36] FANG BK. Development of active guide-wire for cardiac catheterization by using ionic polymer-metal composites. Ifmbe Proceed. 2008;23(1): 340-343. [37] HAGA Y, MIZUSHIMA M, MATSUNAGA T, et al. Medical and welfare applications of shape memory alloy microcoil actuators. Smart Materials and Structures. 2005;14(5):S266-S272. [38] BLANC L, DELCHAMBRE A, LAMBERT P. Flexible medical devices: review of controllable stiffness solutions. Actuators. 2017;6(3):23. [39] AYVALI E, LIANG CP, HO M, et al. Towards a discretely actuated steerable cannula for diagnostic and therapeutic procedures. Int J Rob Res. 2012;31(5):588-603. [40] LU YH, MANI K, PANIGRAHI B, et al. A shape memory alloy-based miniaturized actuator for catheter interventions. Cardiovasc Eng Technol. 2018;9(3):405-413. [41] SELVARAJ M, TAKAHATA K. Electrothermally driven hydrogel-on-flex-circuit actuator for smart steerable catheters. Micromachines. 2020; 11(1):68. |
| [1] | Nong Fuxiang, Jiang Zhixiong, Li Yinghao, Xu Wencong, Shi Zhilan, Luo Hui, Zhang Qinglang, Zhong Shuang, Tang Meiwen. Bone cement augmented proximal femoral nail antirotation for type A3.3 intertrochanteric femoral fracturalysis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-10. |
| [2] | Pan Zhongjie, Qin Zhihong, Zheng Tiejun, Ding Xiaofei, Liao Shijie. Targeting of non-coding RNAs in the pathogenesis of the osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1441-1447. |
| [3] | Cai Zhihao, Xie Zhaoyong. Femoral neck anteversion measurement assessment: how to establish a unified method and standard [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1448-1454. |
| [4] | Dang Yi, Du Chengyan, Yao Honglin, Yuan Nenghua, Cao Jin, Xiong Shan, Zhang Dingmei, Wang Xin. Hormonal osteonecrosis and oxidative stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1469-1476. |
| [5] | Wang Ji, Zhang Min, Yang Zhongya, Zhang Long. A review of physical activity intervention in type 2 diabetes mellitus with sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1272-1277. |
| [6] | Nie Chenchen, Su Kaiqi, Gao Jing, Fan Yongfu, Ruan Xiaodi, Yuan Jie, Duan Zhaoyuan, Feng Xiaodong. The regulatory role of circular RNAs in cerebral ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1286-1291. |
| [7] | Gao Yu, Han Jiahui, Ge Xin. Immunoinflammatory microenvironment after spinal cord ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1300-1305. |
| [8] | Xu Xingxing, Wen Chaoju, Meng Maohua, Wang Qinying, Chen Jingqiao, Dong Qiang. Carbon nanomaterials in oral implant [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1062-1070. |
| [9] | Li Cheng, Zheng Guoshuang, Kuai Xiandong, Yu Weiting. Alginate scaffold in articular cartilage repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1080-1088. |
| [10] | Xu Cong, Zhao He, Sun Yan. Regeneration of facial nerve injury repaired by biomaterial nerve conduits [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1089-1095. |
| [11] | Chen Shisong, Liu Xiaohong, Xu Zhiyun. Current status and prospects of bioprosthetic heart valves [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1096-1102. |
| [12] | Lu Di, Zhang Cheng, Duan Rongquan, Liu Zongxiang. Osteoinductive properties of calcium phosphate ceramic bone repair materials [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1103-1109. |
| [13] | Shi Yehong, Wang Cheng, Chen Shijiu. Early thrombosis and prevention of small-diameter blood vessel prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1110-1116. |
| [14] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| [15] | Bai Siqi, Xiao Zhen, Liu Jing. Application potential of adipose-derived stem cells in female pelvic floor dysfunction diseases [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 921-927. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||