Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (12): 1961-1968.doi: 10.12307/2023.108
Surface treatment of dental implant materials and their antibacterial and osteoinductive ability
Wang Yuesheng1, Gao Wei2, 3, Peng Cheng1
- 1Department of Stomatology, Second Hospital of Tianjin Medical University, Tianjin 300211, China; 2Department of Interventional Therapy, Cancer Institute and Hospital, Tianjin Medical University, National Clinical Research Center for Cancer, Key Laboratory of Cancer Prevention and Therapy, Tianjin 300060, China; 3State Key Laboratory of Metastable Materials Science and Technology, Yanshan University, Qinhuangdao 066004, Hebei Province, China
-
Received:2021-11-23Accepted:2022-05-14Online:2023-04-28Published:2022-07-30 -
Contact:Gao Wei, MD, Associate chief physician, Department of Interventional Therapy, Cancer Institute and Hospital, Tianjin Medical University, National Clinical Research Center for Cancer, Key Laboratory of Cancer Prevention and Therapy, Tianjin 300060, China; State Key Laboratory of Metastable Materials Science and Technology, Yanshan University, Qinhuangdao 066004, Hebei Province, China -
About author:Wang Yuesheng, Master, Attending physician, Department of Stomatology, Second Hospital of Tianjin Medical University, Tianjin 300211, China -
Supported by:Open Project of State Key Laboratory of Metastable Materials Science and Technology of Yanshan University, Grant No. 202101 (to GW); Natural Science Foundation of Hebei Province, Grant No. C2021202002 (to GW)
CLC Number:
Cite this article
Wang Yuesheng, Gao Wei, Peng Cheng. Surface treatment of dental implant materials and their antibacterial and osteoinductive ability[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(12): 1961-1968.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

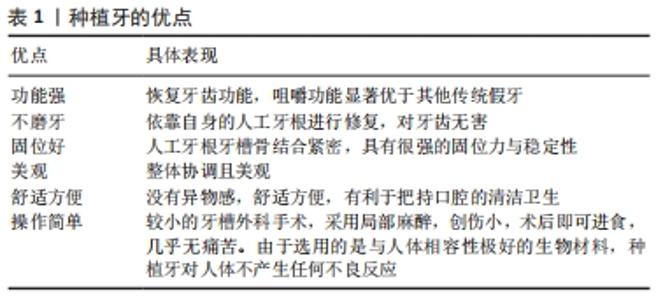
2.1.1 金属及其合金 (1)纯钛:自BRANEMARK提出骨结合理论后,纯钛及钛合金(主要是Ti-6Al-4V)一直是口腔种植体的首选材料[5]。研究表明,纯钛具有比强度低、生物相容性好、抗腐蚀性能优异等特点[6],同时因其硬度高,能充分满足牙齿咀嚼的要求,因此已作为种植体材料广泛应用于临床。 然而,钛作为种植体材料仍然存在一些弊端:①钛的颜色灰暗,能透过植入处较薄的黏膜,影响薄龈型患者的美学效果[7];②钛的弹性模量为110 GPa,比人骨的弹性模量(20-30 GPa)高,会产生应力遮挡而导致骨吸收[8];③纯钛种植体可释放钛离子导致出现牙龈炎症和牙周炎症[9];④钛可能具有免疫原性,作为过敏原,引起部分过敏症患者对金属植入物的Ⅳ型超敏反应[10]。 (2)钛合金:与纯钛相比,添加合金元素后,可提高材料的耐腐蚀性能、可加工性,降低弹性模量,尤其对于窄直径种植体,还可降低其断裂的风险[11]。临床应用较多的钛合金是Ti-6Al-4V合金。然而研究发现,Ti-6Al-4V合金会释放极微量的钒和铝离子,对人体造成危害[12]。β型钛合金是一种高熔点、高强度的合金,在正火或淬火时将高温β相保留至室温,获得介稳定的β单相组织。这类合金的主要合金元素是Nb、Zr、Ga、Mo、Ta、Cu等,是一系列β稳定性且安全无毒的合金元素,在钛的合金化领域中占据很大热点[13]。学者们开始将研究的重点放在开发无毒的钛合金,见表2[14-19]。 "


(3)钽及钽基金属:钽在体内不发生电化学腐蚀,无金属离子释放,具有良好的生物相容性,但钽的力学强度过高,限制了其在骨科和牙科领域的应用。多孔钽是一种十二面体结构的生物材料,并且具有开放孔结构。相较于钛及钛合金,多孔钽的剪切力和摩擦系数以及孔隙率都更高一些,对于骨组织和新血管的形成是非常有利的[20]。钽的氧化物具有很好的生物惰性,使其能在复杂的口腔环境中保持稳定。然而,由于价格较高,而且现阶段大多数种植体存在形式为合金或涂层,这使其应用得到了限制。 USLU等[21]通过阳极氧化技术在钽表面制备出纳米管(NT)、纳米凹坑(ND)以及纳米珊瑚(NC)形态的表面结构,以提高钽的生物活性。研究结果表明,阳极氧化后的钽表面,尤其是具有90 nm特征尺寸纳米凹坑形态的钽表面显著增强了蛋白质黏附并促进了骨细胞增殖和扩散,该结果同时证明钽本身良好的生物相容性,可应用于骨科,见图3。 "


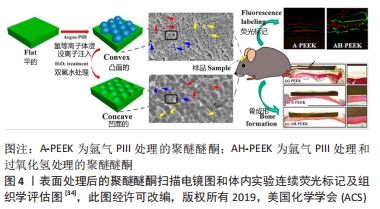
2.1.2 陶瓷 (1)氧化锆:氧化锆植入物具有良好的力学、生物学和美学性能[22]。作为一种生物陶瓷,氧化锆力学强度可以达到1 200 MPa,断裂韧性为6-10 MPa/m2[23],而且不利于菌斑附着,一定程度上达到抑菌的效果,有一部分的抑菌效果会超过钛合金种植体[24]。 另外,GANBOLD等[25]分析了氧化锆和钛植入体的表面特点以及破骨细胞的形成机制,得到了5%氧化钇稳定的四方氧化锆多晶样品,促进破骨前体细胞培养分化成破骨细胞。相对于钛,氧化锆上活化T细胞1(NFATc1)转录因子的 mRNA 表达较高,且氧化锆上 c-Fos 转录因子的蛋白表达水平也很强,说明其表面对破骨细胞增殖、分化及其黏附行为具有促进效果,可以作为牙科植入物使用。 (2)玻璃陶瓷:玻璃陶瓷是通过某些特定组成的基础玻璃,在一定的温度下进行受控核化、晶化而制得的一种含有玻璃体的多晶固相材料,具有良好的物理和生物特性。玻璃陶瓷弹性模量为(96±3) GPa,硬度为(5.27±0.26) GPa,断裂韧性为(4.77±0.27) MPa/m2,说明其具有优良的机械加工性。 SAADALDIN等[26]通过改变基材玻璃成分合成了一种适用于非金属一体式牙种植体的微晶玻璃(GC),该硅灰石玻璃陶瓷具有良好的强度、可加工型和化学稳定性,是一种很有前途的一次性牙种植体材料。另外,有研究表明玻璃陶瓷在模拟体液中浸泡后,表面可形成一层羟基磷灰石,在体外检测中,MC3T3-E1细胞在微晶玻璃表面附着、铺展和增殖,表明其具有潜在的生物活性[27]。 (3)氮化硅:氮化硅是一种合成的非氧化物陶瓷,具有良好的耐磨性、断裂韧性,自1989年起作为生物医学材料应用于临床。有许多研究表明,氮化硅可减少细菌生物膜的形成,抑制细菌的增殖,具有潜在的抗菌性能[28],可提高种植体的成功率[29]。 2.1.3 高分子材料 (1)聚醚醚酮(polyether-ether-ketone,PEEK):聚醚醚酮是一种半结晶特种高分子材料,该材料耐高温、耐化学药品腐蚀,且具有良好的力学性能和生物相容性[30],弹性模量为3.0-4.0 GPa,与纯钛相比,更接近于人骨,不会出现应力遮挡[2]。此外,聚醚醚酮可透X射线,可以避免产生伪影现象[31]。 然而,聚醚醚酮属于生物惰性材料,当被植入体内时,不利于其与周围骨组织形成良好的结合,限制了它的潜在应用。因此,学者们开始将研究的重点放在对聚醚醚酮进行改性处理以提高其生物活性[32]。早期研究中,学者们利用熔融共混和压模注塑等技术将具有生物活性的无机填料如纳米二氧化钛、纳米羟磷灰石、碳纤维等加入聚醚醚酮以形成复合材料,结果表明均有效提高了材料的生物相容性[33]。 此外,有研究者通过改变生物材料的表面纹理,达到控制细胞分化、改善基质骨整合的目的。OUYANG等[34]利用氩等离子体浸没离子注入(PIII)和后续过氧化氢处理在PEEK表面构建纳米结构,分别得到氩气PIII处理的聚醚醚酮(A-PEEK)和后续又经过氧化氢处理的聚醚醚酮(AH-PEEK)。体外结果表明,在这2个纳米结构材料表面上的细胞黏附、胶原蛋白分泌和细胞外基质沉积均得到增强;体内实验表明,通过过氧化氢处理的材料表面比仅用氩等离子体浸没离子注入处理的材料表面更有利于骨整合。该表面结构处理方法为聚醚醚酮在骨科和牙科中的应用提供了更有利的支持,见图4。 "
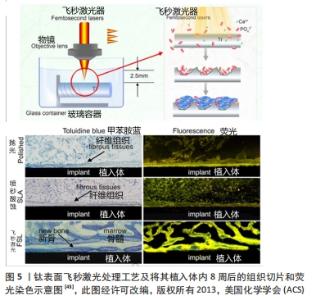
(2)聚甲基丙烯酸甲酯:聚甲基丙烯酸甲酯强度高、耐光老化,质轻而坚韧,在常温下具有优良的拉伸强度和弯曲强度,已经被应用于人造关节和人造骨[35]。近年来,有学者对其在口腔种植领域的应用进行了初步研究。 李小东等[36]分别探究了纯钛和聚甲基丙烯酸甲酯高分子材料作为牙种植材料对于人成骨细胞的细胞毒性、细胞贴壁率、相对增殖率以及种植后所引起的炎性反应等生物相容性指标,将聚甲基丙烯酸甲酯浸提液和纯钛浸提液分别与人成骨细胞共培养相比较,结果表明,纯钛和聚甲基丙烯酸甲酯浸提液培养细胞不同时程后,聚甲基丙烯酸甲酯组较纯钛组的细胞贴附率以及增殖率均较高,且种植后引发的炎症反应以及生物相容性均优于纯钛。 2.2 表面处理工艺 为了达到表面微观结构改变的现象,通过物理、化学或者是将两者结合的方法对材料表面进行改性。常用的表面处理方法可大致分为物理方法和化学方法。 2.2.1 物理方法 利用物理方法如离子注入、喷砂、激光处理等,使得植入体的表面形貌及粗糙度得到改变,因此得到了比较好的骨结合基础。 (1)离子注入:离子注入技术的基本原理是离子束入射到植入体内,离子束与植入体内的原子或分子相互作用,入射离子逐渐失去能量并最终留在植入体内,改变了其表面的成分、结构和性能。 WANG等[37]研究采用等离子体浸没离子植入技术,将镁和锌引入钛中,结果表明Mg和Zn离子的协同作用使得共植入样品培养的人牙龈成纤维细胞具有较高的增殖速率和运动性,这对植入物的软组织密封至关重要。ZHANG等[38]采用等离子体浸没离子注入技术构建了铈改性钛表面,系统研究了改性钛的力学性能、耐蚀性、抗氧化性能和成骨性能,结果表明,改性钛的表面硬度和耐蚀性明显提高,活性氧水平降低。此外,改性后的钛表面骨髓间充质干细胞的扩张、增殖、碱性磷酸酶和胶原分泌均得到改善。HUANG等[39]将氮等离子体浸没离子注入处理应用于Ti-6Al-4V钛合金,增强了种植牙的耐腐蚀性,也加快了细胞反应和抗菌黏附。 (2)喷砂处理:喷砂以压缩空气为动力,形成高速射流束,将材料高速喷射到种植体表面,以获得一定的清洁度和粗糙度,从而提高细胞的黏附和增殖能力,增强骨结合能力[40]。 VELASCO-ORTEGA等[41]将表面氧化处理和酸蚀表面喷砂处理的植入体植入新西兰兔股骨,分别对植入物和周围骨组织进行组织学和组织形态分析,体内研究结果显示,所有植入物未观察到感染迹象,表面均被新形成的骨小梁包围,12周后均显示出有大量新生骨形成。另外,与氧化处理植入体相比,喷砂处理植入体的骨种植体接触率较高,为(53.49±8.46)%,证明了通过喷砂处理的植入体的骨结合能力更好。 (3)激光处理:利用激光束在大气、真空等环境中快速加热植入体,实现局部快速加热或冷却,从而改变组织结构或引入其他材料以改善表面性能。 CHIKARAKARA等[42]对植入体进行激光表面熔化,发现处理过的表面可以促进细胞附着和增殖。 LIANG等[43]通过飞秒激光技术在钛植入物表面上生成微图案结构和钙磷沉积,结果表明,经过飞秒激光处理后,植入物表面获得了由沟槽、条纹、颗粒等组成的显微结构。体内实验组织切片表明,植入8周后的光滑表面和喷砂酸蚀植入体表面存在明显的纤维结缔组织层,而飞秒激光处理样品表面则为明显的骨组织层,见图5。 "
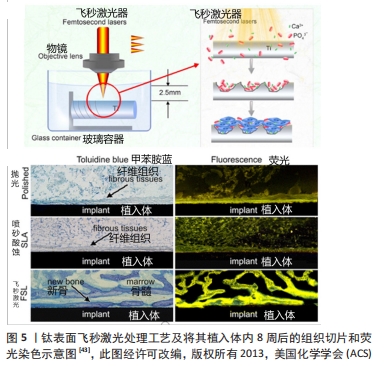
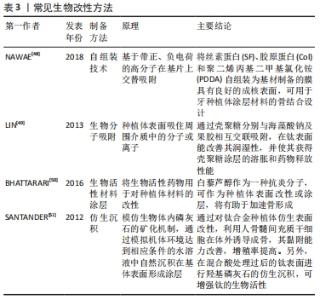
2.2.2 化学方法 化学方法是指通过与表面改性剂之间发生的化学吸附作用或化学反应,改变种植体表面的物理结构和化学性质。常用的化学方法包括阳极氧化法、微弧氧化法、溶胶凝胶法等。 (1)阳极氧化:阳极氧化是在一定的外加电流的作用下,通过使用相应的电解液和特定的工艺条件,使金属阳极表面形成氧化膜的过程。 SHARMA等[44]在含有DL-α-磷酸甘油和醋酸钙的电解液中对作为种植体的钛和钛锆合金进行阳极氧化,测试结果显示钛和钛锆合金表面氧、钙和磷元素的含量均增加,并且材料表面变得更为粗糙,使得接触角明显变小,最终使得种植体附近的成骨信号增强。KAZEK-K?SIK等[45]将钛合金置于含生物活性物质的溶液中对其表面进行阳极氧化,测试结果表明最终获得的多孔氧化层有利于MG-63骨样细胞的黏附,并且此法能够显著提升Ti-15Mo合金的亲水性。 (2)微弧氧化:微弧氧化法是通过组合所用的电解液和对应的用电参数,制造弧光放电并产生一种瞬时高温高压条件,使其在金属或其合金表面作用并生成与基底结合牢固的多孔蜂窝状微米级的氧化膜。 BAI等[46]通过多步的微弧氧化工艺,合成了具有亚微孔微弧氧化涂层的微切口性质的钛基种植体,其克服了钛基种植体对于骨整合度不足的缺陷。Li等[47]首先在钛金属表面进行微弧氧化工艺处理,其次再将合成出来的涂层置于碱性溶液中进行电化学还原,最终制备了具有特殊分层结构的表面微形貌。测试结果表明,得益于特殊结构导致的与骨之间接触面积的增大和细胞黏附性的增强,钛基种植体周围的细胞增殖和骨形成速度得到明显提升。 (3)溶胶凝胶法:溶胶凝胶法是一种将无机物或金属醇盐通过溶液、溶胶、凝胶而固化,再经热处理而形成氧化物或其他化合物的方法。 在溶胶凝胶法的基础上,有机聚合物使二氧化钛表面具有生物活性,假设通过聚对苯二甲酸乙二醇酯对其进行表面改性,骨植入体接触面可达到一定的机械稳定性、生物相容性以及良好的骨结合能力和骨传导能力。 2.2.3 生物方法 近年来种植体表面的生物改性方法也成为研究热点,其目的是在种植体上构建一层具有生物活性功能性涂层,使其具有较高的机械稳定性,同时模拟天然骨的结构和组成特性,从而更好地促进骨生长。常见方法见表3[48-51]。 "
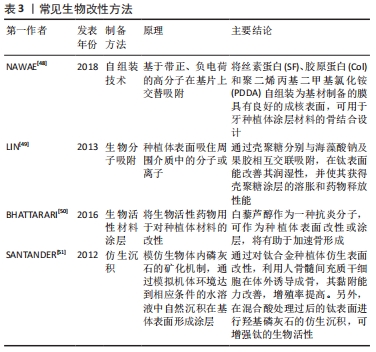

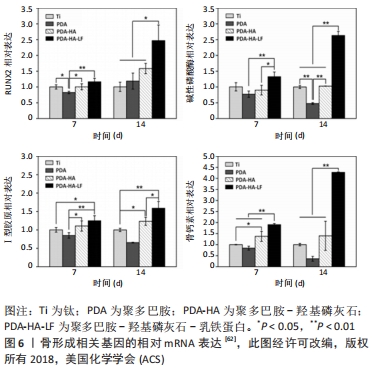
2.3 表面涂层 表面涂层技术为植入体表面覆盖上一层或者多层具有一定功能的膜,该技术不仅可以提高种植牙的生物相容性,而且对抑菌性能也能产生一定的效果。由于涂层的成分具有较大差别,被分为生物分子涂层和传统涂层[52]。 2.3.1 传统涂层 (1)银:由银涂层释放的银离子与细菌细胞膜作用,进而产生生物活性氧,会对细菌的繁殖和代谢产生非常大的影响,最终会产生杀菌的效果。含有银的涂层抗菌范围广,而且对真核细胞的伤害性比较低;与生物具有一定的相容性,动物实验证明,银电镀处理植入体周围的垂直骨吸收会有一定的降低[53]。 LI等[54]通过碱热处理的质子化效应和多巴胺的二齿螯合作用在种植体表面形成了微纳米分级结构,并负载了具有抗菌效果的银离子。纳米银颗粒在有效杀灭致病菌群的同时,还能促进早期有利的炎性反应,保证后续愈合的顺利进行。 (2)锶:锶离子能诱导免疫系统的先锋——巨噬细胞向促愈合的M2型极化,从而促进免疫调节,达到更好的愈合效果。此外,成骨细胞也受到锶离子的直接作用,分化活性增加,更快地进行胶原沉积和胞外基质矿化。通过调控两种离子的独立释放行为,实现了对骨整合初期各个阶段的调控作用。 FENBO等[55]制备了一种新型的具有微孔结构的硫酸锶软骨素/丝素蛋白(SRCS/SF)共混膜。随着硫酸锶软骨素掺杂量的增加,硫酸锶软骨素/丝素蛋白膜具有更好的力学性能和更高的保水能力。体外实验结果表明,较高含量的硫酸锶软骨素膜有利于成骨细胞的增殖。硫酸锶软骨素/丝素蛋白膜可能通过下调促炎细胞因子和降解相关分解代谢基因的表达,上调成骨因子的表达,对巨噬细胞的骨免疫反应起到积极的调节作用。 (3)石墨烯:石墨烯涂层有良好的生物相容性,并且可以通过插入切割细菌膜,也可以通过直接大量提取磷脂分子破坏细胞膜,从而杀死细菌。 邓雪阳等[56]采用层-层自组装法在碱热处理后的钛合金表面制备出具有良好亲水性和结合强度的纳米级石墨烯涂层。骨髓间充质干细胞在具有石墨烯涂层的钛片表面易于黏附,而且骨髓间充质干细胞活性保持良好。石墨烯涂层对牙龈卟啉单胞菌的杀菌率为86.34%。 LA等[57]制备载骨形态发生蛋白2和石墨烯涂层钛植入体,骨形态发生蛋白2在体内可以稳定释放,并且生物活性和蛋白质结构稳定性有所提高。在体内实验中,小鼠颅骨缺损区具有较好的成骨能力。 为了提高纳米铜纳米粒的抗菌活性和降低细胞毒性,将纳米铜较均匀地分散在还原氧化石墨烯上,同时在还原氧化石墨烯的间层中插入蒙脱土,合成了蒙脱土/还原氧化石墨烯负载纳米铜纳米粒(MMT-rGO-CuNPs),该复合材料对革兰阳性金黄色葡萄球菌的抑菌活性强于革兰阴性大肠杆菌,这可能是由于大肠杆菌外膜的保护作用,以及该复合材料对金黄色葡萄球菌的吸附作用强于大肠杆菌[58]。 (4)抗生素:抗生素指的是由细菌、霉菌或其他微生物产生的一些代谢产物或人工合成的类似物,其具有抗病原体的活性。临床医学中常用有β-内酰胺类、酰胺醇类、大环内酯类等多种抗生素。抗生素主要通过抑制细菌细胞壁的合成,干扰细胞膜上发生的反应,或者干扰蛋白质及抑制核酸的转录和复制,进而起到抑菌的效果。 RAMS等[59]利用具有邻苯二酚结构的聚多巴胺涂层辅助将抗生素头孢噻肟钠接枝到金属钛的表面,进而使该植入物实现良好的生物相容性,实验结果表明,接枝抗生素以后的金属钛可有效抑制大肠杆菌和变形链球菌的黏附和增殖。BAGHDAN等[60]通过纳米喷雾干燥技术制备可生物降解的聚乳酸-乙醇酸纳米涂层,选择诺氟沙星作为抗生素模型,研究结果显示含有诺氟沙星抗生素的纳米涂层中的活菌数下降比例高达99.83%,实现了有效抗菌的目的。 (5)羟基磷灰石:羟基磷灰石是牙齿骨骼的主要矿物质成分,具有良好的生物相容性和生物活性,被广泛应用到骨科以及牙科植入物涂层中,其在体内可以分解出钙离子和磷离子,游离的钙离子和磷离子在被植入部位的局部组织吸收后可以诱导骨内植入界面生长出新的骨组织。实验结果证实羟基磷灰石可促进骨内植物的整合,增强内植物长期使用的稳定性。 游滢滢等[61]采用溶胶凝胶法制备了羟基磷灰石和纳米含氟羟基磷灰石,将其涂覆于种植体表面进行了体外溶血实验和细胞毒性实验,结果表明各材料的溶血率均在5%以下,且细胞能够在其上很好地黏附与增殖。 SHEN等[62]受天然骨组织高度分层结构的启发,采用仿生方法和自旋辅助层接层组装技术,在钛基底表面制备了聚多巴胺辅助羟基磷灰石和乳铁蛋白多层结构(PDA-HA-LF),通过细胞实验和体外抑菌实验检测其调节骨平衡的能力和抗菌性能。图6结果表明,聚多巴胺辅助羟基磷灰石和乳铁蛋白多层修饰钛底物可上调成骨相关基因的表达。 "

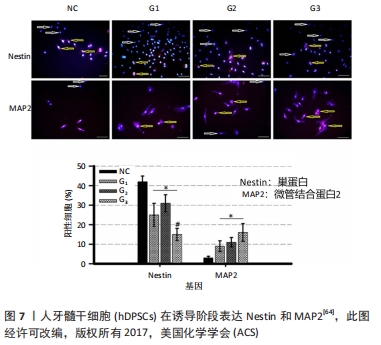
2.3.2 生物涂层 (1)壳聚糖:壳聚糖是一种含有大量阳离子的高分子碱性多糖。壳聚糖作为一种天然高分子聚合物,具有良好的生物相容性、可降解性和低免疫原性,不仅能诱导成骨细胞分化,还能抑制成纤维细胞增殖和黏附。它是一种生物多功能材料,具有良好的种植牙潜力。 PALLA-RUBIO等[63]在钛植入物表面涂覆硅和壳聚糖。体外细胞实验结果证明,复合涂层不仅对细胞没有任何毒性,而且可以促进细胞表面增殖,含质量分数为5%-10%壳聚糖的涂层具有良好的抗菌性能。 有学者提出了一种新型的壳聚糖插层蒙脱土/聚乙烯醇(OMMT/PVA)纳米纤维网作为微环境,引导人牙髓干细胞向神经元样细胞分化。通过蒙脱土与壳聚糖的离子交换反应制备了壳聚糖插层蒙脱土。将含有不同浓度壳聚糖插层蒙脱土的聚乙烯醇溶液静电纺丝,形成三维壳聚糖插层蒙脱土/聚乙烯醇纳米纤维网。在诱导后的第1天,将培养的人牙髓干细胞置于纳米纤维样品上,Nestin和MAP2特异性抗体染色结果显示阴性对照组中表达Nestin的阳性细胞高于其他实验组。相反,各组MAP2表达细胞百分比均显著高于阴性对照组,见图7,说明加入壳聚糖插层蒙脱土/聚乙烯醇纳米纤维网有利于人牙髓干细胞向神经元样细胞分化[64]。 "

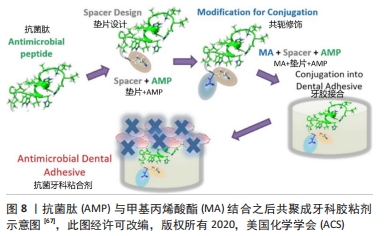
(2)抗菌肽:抗菌肽是生物体内存在的一种具有抗菌活性的肽类物质,氨基酸数目通常10-50个,常带正电荷,并具有广谱抗菌活性。抗菌肽能在细菌的质膜上起到一定的作用,能快速杀灭细菌,不易引起细菌对药物的抵抗性。它们可以单独使用或与抗生素联合使用来杀死病原体[65]。 孙丰权[66]将抗菌肽Pac-525涂覆到钛种植体表面。与不含抗菌肽的种植体进行对照,结果显示抗菌肽颗粒嵌入涂层表面的微孔中,且随抗菌肽含量的增加,抗菌效果逐渐增强,成骨细胞的黏附增殖情况均大于对照组。 XIE等[67]设计了2个不同的间隔域,将间隔结合的抗菌肽与甲基丙烯酸酯结合,得到的甲基丙烯酸酯-抗菌肽单体作为抗菌肽聚合物结合物再共聚成牙科胶粘剂。研究发现结合在树脂基质上的抗菌肽对变形链球菌具有显著的抗菌活性,见图8。 "
| [1] 杨娜.即刻种植牙的临床研究进展[J].医疗装备,2019,32(12):189-190. [2] 于婉琦,周延民,赵静辉.口腔种植体新材料的研究现状[J].国际口腔医学杂志,2019,46(4):488-496. [3] 张晨秋,王柏翔,王慧明.种植体表面抗菌技术的分类与研究进展[J].口腔医学,2020,40(3):258-261. [4] RASOULI R, BARHOUM A, ULUDAG H. A review of nanostructured surfaces and materials for dental implants: surface coating, patterning and functionalization for improved performance. Biomater Sci. 2018; 6(6):1312-1338. [5] CASTELLANO A, GIL LF, BONFANTE EA, et al. Early Healing Evaluation of Commercially Pure Titanium and Ti-6Al-4V Presenting Similar Surface Texture: An In Vivo Study. Implant Dent. 2017;26(3):338-344. [6] 马凯,赵宝红,邓春富,等.医用钛及钛合金牙种植体生物相容性及其相关抗菌性能研究进展[J].中国实用口腔科杂志,2016,9(7): 441-445. [7] TALLARICO M, PARK CJ, LUMBAU AI, et al. Customized 3D-Printed Titanium Mesh Developed to Regenerate a Complex Bone Defect in the Aesthetic Zone: A Case Report Approached with a Fully Digital Workflow. Materials (Basel). 2020;13(17):3874. [8] YANG BC, ZHOU XD, YU HY, et al. Advances in titanium dental implant surface modification. Hua Xi Kou Qiang Yi Xue Za Zhi. 2019;37(2):124-129. [9] LIU X, LI S, MENG Y, et al. Osteoclast differentiation and formation induced by titanium implantation through complement C3a. Mater Sci Eng C Mater Biol Appl. 2021;122:111932. [10] TRINDADE R, ALBREKTSSON T, GALLI S, et al. Osseointegration and foreign body reaction: Titanium implants activate the immune system and suppress bone resorption during the first 4 weeks after implantation. Clin Implant Dent Relat Res. 2018;20(1):82-91. [11] CORDEIRO JM, BARÃO VAR. Is there scientific evidence favoring the substitution of commercially pure titanium with titanium alloys for the manufacture of dental implants? Mater Sci Eng C Mater Biol Appl. 2017;71:1201-1215. [12] JIMAN PA, MOLDOVAN M, SAROSI C, et al. Surface characterization and cytotoxicity analysis of the titanium alloys for dentistry. Studia UBB Chemia. 2020;65:149-162. [13] REVATHI A, BORRÁS AD, MUÑOZ AI, et al. Degradation mechanisms and future challenges of titanium and its alloys for dental implant applications in oral environment. Mater Sci Eng C Mater Biol Appl. 2017;76:1354-1368. [14] YAN B, TAN J, WANG D, et al. Surface alloyed Ti–Zr layer constructed on titanium by Zr ion implantation for improving physicochemical and osteogenic properties. Progress in Natural Science: Materials International. 2020;30(5):635-641. [15] ZHANG Y, SUN D, CHENG J, et al. Mechanical and biological properties of Ti-(0-25 wt%)Nb alloys for biomedical implants application. Regen Biomater. 2020;7(1):119-127. [16] EL-HADAD S, SAFWAT EM, SHARAF NF. In-vitro and in-vivo, cytotoxicity evaluation of cast functionally graded biomaterials for dental implantology. Mater Sci Eng C Mater Biol Appl. 2018;93:987-995. [17] KIM HJ, JEONG YH, CHOE HC, et al. Surface morphology of TiN-coated nanotubular Ti-25Ta-xZr alloys for dental implants prepared by RF sputtering. Thin Solid Films. 2013;549:131-134. [18] HOPPE V, SZYMCZYK-ZIÓŁKOWSKA P, RUSIŃSKA M, et al. Assessment of Mechanical, Chemical, and Biological Properties of Ti-Nb-Zr Alloy for Medical Applications. Materials (Basel). 2020;14(1):126. [19] FOWLER L, MASIA N, CORNISH LA, et al. Development of Antibacterial Ti-Cux Alloys for Dental Applications: Effects of Ageing for Alloys with Up to 10 wt% Cu. Materials (Basel). 2019;12(23):4017. [20] PIGLIONICO S, BOUSQUET J, FATIMA N, et al. Porous Tantalum VS. Titanium Implants: Enhanced Mineralized Matrix Formation after Stem Cells Proliferation and Differentiation. J Clin Med. 2020;9(11):3657. [21] USLU E, MIMIROGLU D, ERCAN B. Nanofeature size and morphology of Tantalum oxide surfaces control osteoblast functions. ACS Appl Bio Mater. 2021;4(1):780-794. [22] SHARANRAJ V, RAMESHA CM, KAVYA K, et al. Zirconia: as a biocompatible biomaterial used in dental implants. Advances in Applied Ceramics. 2020;120(2):63-68. [23] HAN J, ZHANG F, VAN MEERBEEK B, et al. Laser surface texturing of zirconia-based ceramics for dental applications: A review. Mater Sci Eng C Mater Biol Appl. 2021;123:112034. [24] ROEHLING S, ASTASOV-FRAUENHOFFER M, HAUSER-GERSPACH I, et al. In Vitro Biofilm Formation on Titanium and Zirconia Implant Surfaces. J Periodontol. 2017;88(3):298-307. [25] GANBOLD B, KIM SK, HEO SJ, et al. Osteoclastogenesis Behavior of Zirconia for Dental Implant. Materials (Basel). 2019;12(5):732. [26] SAADALDIN SA, RIZKALLA AS. Synthesis and characterization of wollastonite glass-ceramics for dental implant applications. Dent Mater. 2014;30(3):364-371. [27] SAADALDIN SA, DIXON SJ, COSTA DO, et al. Synthesis of bioactive and machinable miserite glass-ceramics for dental implant applications. Dent Mater. 2013;29(6):645-655. [28] WU J, LIU Y, ZHANG H, et al. Silicon nitride as a potential candidate for dental implants: Osteogenic activities and antibacterial properties. J Mater Res. 2021;36:1866-1882. [29] BADRAN Z, STRUILLOU X, HUGHES FJ, et al. Silicon Nitride (Si3N4) Implants: The Future of Dental Implantology? J Oral Implantol. 2017; 43(3):240-244. [30] 王河军,曲弋,杨永栋,等.PEEK棒腰椎后路内固定的基础及临床应用进展[J].生物骨科材料与临床研究,2020,17(5):58-60. [31] AL-RABAB’AH M, HAMADNEH W, ALSALEM I, et al. Use of High Performance Polymers as Dental Implant Abutments and Frameworks: A Case Series Report. J Prosthodont. 2019;28(4):365-372. [32] MA Z, ZHAO X, ZHAO J, et al. Biologically Modified Polyether Ether Ketone as Dental Implant Material. Front Bioeng Biotechnol. 2020;8: 620537. [33] WANG L, HE S, WU X, et al. Polyetheretherketone/nano-fluorohydroxyapatite composite with antimicrobial activity and osseointegration properties. Biomaterials. 2014;35(25):6758-6775. [34] OUYANG L, CHEN M, WANG D, et al. Nano Textured PEEK Surface for Enhanced Osseointegration. ACS Biomater Sci Eng. 2019;5(3):1279-1289. [35] XU D, SONG W, ZHANG J, et al. Osteogenic effect of polymethyl methacrylate bone cement with surface modification of lactoferrin. J Biosci Bioeng. 2021;132(2):132-139. [36] 李小东,李新梅,孙晓晨,等.牙种植高分子材料聚甲基丙烯酸甲酯的生物相容性[J].中国组织工程研究,2015,19(47):7613-7618. [37] WANG L, LUO Q, ZHANG X, et al. Co-implantation of magnesium and zinc ions into titanium regulates the behaviors of human gingival fibroblasts. Bioact Mater. 2020;6(1):64-74. [38] ZHANG H, QIU J, LIU X. Enhanced antioxidant capability and osteogenic property of medical titanium by cerium plasma immersion ion implantation. Surfaces and Interfaces. 2021;26:101402. [39] HUANG HH, SHIAU DK, CHEN CS, et al. Nitrogen plasma immersion ion implantation treatment to enhance corrosion resistance, bone cell growth, and antibacterial adhesion of Ti-6Al-4V alloy in dental applications. Surface and Coatings Technology. 2019;365:179-188. [40] TANG X, HUANG K, DAI J, et al. Influences of surface treatments with abrasive paper and sand-blasting on surface morphology, hydrophilicity, mineralization and osteoblasts behaviors of n-CS/PK composite. Sci Rep. 2017;7(1):568. [41] VELASCO-ORTEGA E, ORTIZ-GARCÍA I, JIMÉNEZ-GUERRA A, et al. Comparison between Sandblasted Acid-Etched and Oxidized Titanium Dental Implants: In Vivo Study. Int J Mol Sci. 2019;20(13):3267. [42] CHIKARAKARA E, FITZPATRICK P, MOORE E, et al. In vitro fibroblast and pre-osteoblastic cellular responses on laser surface modified Ti-6Al-4V. Biomed Mater. 2014;10(1):015007. [43] LIANG C, WANG H, YANG J, Et al. Femtosecond laser-induced micropattern and Ca/P deposition on Ti implant surface and its acceleration on early osseointegration. ACS Appl Mater Interfaces. 2013;5(16):8179-8186. [44] SHARMA A, MCQUILLAN AJ, SHARMA LA, et al. Spark anodization of titanium-zirconium alloy: surface characterization and bioactivity assessment. J Mater Sci Mater Med. 2015;26(8):221. [45] KAZEK-KĘSIK A, NOSOL A, PŁONKA J, et al. PLGA-amoxicillin-loaded layer formed on anodized Ti alloy as a hybrid material for dental implant applications. Mater Sci Eng C Mater Biol Appl. 2019;94:998-1008. [46] BAI Y, ZHOU R, CAO J, et al. Microarc oxidation coating covered Ti implants with micro-scale gouges formed by a multi-step treatment for improving osseointegration. Mater Sci Eng C Mater Biol Appl. 2017; 76:908-917. [47] LI G, CAO H, ZHANG W, et al. Enhanced Osseointegration of Hierarchical Micro/Nanotopographic Titanium Fabricated by Microarc Oxidation and Electrochemical Treatment. ACS Appl Mater Interfaces. 2016;8(6):3840-3852. [48] NAWAE S, MEESANE J, MUENSIT N, et al. Layer-by-layer self-assembled films of silk fibroin/collagen/poly (diallyldimethylammonium chloride) as nucleating surface for osseointegration to design coated dental implant materials. Materials & Design. 2018;160:1158-1167. [49] LIN HY, CHEN JH. Osteoblast differentiation and phenotype expressions on chitosan-coated Ti-6Al-4V. Carbohydr Polym. 2013;97(2):618-626. [50] BHATTARAI G, POUDEL SB, KOOK SH, et al. Resveratrol prevents alveolar bone loss in an experimental rat model of periodontitis. Acta Biomater. 2016;29:398-408. [51] SANTANDER S, ALCAINE C, LYAHYAI J, et al. In vitro osteoinduction of human mesenchymal stem cells in biomimetic surface modified titanium alloy implants. Dent Mater J. 2012;31(5):843-850. [52] LIU MQ, GE K, JIANG L. Research progress on oral implant materials with antimicrobial properties. International Journal of Stomatology. 2018;45(5):516-521. [53] GODOY-GALLARDO M, MANZANARES-CÉSPEDES MC, SEVILLA P, et al. Evaluation of bone loss in antibacterial coated dental implants: An experimental study in dogs. Mater Sci Eng C Mater Biol Appl. 2016;69: 538-545. [54] LI D, LI Y, SHRESTHA A, et al. Effects of Programmed Local Delivery from a Micro/Nano-Hierarchical Surface on Titanium Implant on Infection Clearance and Osteogenic Induction in an Infected Bone Defect. Adv Healthc Mater. 2019;8(11):e1900002. [55] FENBO M, XINGYU X, BIN T. Strontium chondroitin sulfate/silk fibroin blend membrane containing microporous structure modulates macrophage responses for guided bone regeneration. Carbohydr Polym. 2019;213:266-275. [56] 邓雪阳,潘兰兰,胡婷,等.钛合金表面氧化石墨烯涂层的制备[J].国际口腔医学杂志,2018,45(5):539-545. [57] LA WG, PARK S, YOON HH, et al. Delivery of a therapeutic protein for bone regeneration from a substrate coated with graphene oxide. Small. 2013;9(23):4051-4060. [58] KIM JW, SHIN YC, LEE JJ, et al. The Effect of Reduced Graphene Oxide-Coated Biphasic Calcium Phosphate Bone Graft Material on Osteogenesis. Int J Mol Sci. 2017;18(8):1725. [59] RAMS TE, DEGENER JE, VAN WINKELHOFF AJ. Antibiotic resistance in human peri-implantitis microbiota. Clin Oral Implants Res. 2014; 25(1):82-90. [60] BAGHDAN E, RASCHPICHLER M, LUTFI W, et al. Nano spray dried antibacterial coatings for dental implants. Eur J Pharm Biopharm. 2019;139:59-67. [61] 游滢滢,冯云枝.纳米含氟羟基磷灰石牙种植体的生物相容性[J].中国组织工程研究,2014,18(12):1901-1906. [62] SHEN T, YANG W, SHEN X, et al. Polydopamine-Assisted Hydroxyapatite and Lactoferrin Multilayer on Titanium for Regulating Bone Balance and Enhancing Antibacterial Property. ACS Biomater Sci Eng. 2018;4(9): 3211-3223. [63] PALLA-RUBIO B, ARAÚJO-GOMES N, FERNÁNDEZ-GUTIÉRREZ M, et al. Synthesis and characterization of silica-chitosan hybrid materials as antibacterial coatings for titanium implants. Carbohydr Polym. 2019; 203:331-341. [64] GHASEMI HAMIDABADI H, REZVANI Z, NAZM BOJNORDI M, et al. Chitosan-Intercalated Montmorillonite/Poly(vinyl alcohol) Nanofibers as a Platform to Guide Neuronlike Differentiation of Human Dental Pulp Stem Cells. ACS Appl Mater Interfaces. 2017;9(13):11392-11404. [65] 李伶俐,李潇.钛基种植体表面涂层的研究进展[J].中国临床新医学,2020,13(5):527-532. [66] 孙丰权.钛种植体抗菌肽涂层的抗菌性及细胞相容性研究[D].佳木斯:佳木斯大学,2018. [67] XIE SX, SONG L, YUCA E, et al. Antimicrobial Peptide-Polymer Conjugates for Dentistry. ACS Appl Polym Mater. 2020;2(3):1134-1144. |
| [1] | Nong Fuxiang, Jiang Zhixiong, Li Yinghao, Xu Wencong, Shi Zhilan, Luo Hui, Zhang Qinglang, Zhong Shuang, Tang Meiwen. Bone cement augmented proximal femoral nail antirotation for type A3.3 intertrochanteric femoral fracturalysis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-10. |
| [2] | Pan Zhongjie, Qin Zhihong, Zheng Tiejun, Ding Xiaofei, Liao Shijie. Targeting of non-coding RNAs in the pathogenesis of the osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1441-1447. |
| [3] | Cai Zhihao, Xie Zhaoyong. Femoral neck anteversion measurement assessment: how to establish a unified method and standard [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1448-1454. |
| [4] | Dang Yi, Du Chengyan, Yao Honglin, Yuan Nenghua, Cao Jin, Xiong Shan, Zhang Dingmei, Wang Xin. Hormonal osteonecrosis and oxidative stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1469-1476. |
| [5] | Wang Ji, Zhang Min, Yang Zhongya, Zhang Long. A review of physical activity intervention in type 2 diabetes mellitus with sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1272-1277. |
| [6] | Nie Chenchen, Su Kaiqi, Gao Jing, Fan Yongfu, Ruan Xiaodi, Yuan Jie, Duan Zhaoyuan, Feng Xiaodong. The regulatory role of circular RNAs in cerebral ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1286-1291. |
| [7] | Gao Yu, Han Jiahui, Ge Xin. Immunoinflammatory microenvironment after spinal cord ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1300-1305. |
| [8] | Xu Xingxing, Wen Chaoju, Meng Maohua, Wang Qinying, Chen Jingqiao, Dong Qiang. Carbon nanomaterials in oral implant [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1062-1070. |
| [9] | Li Cheng, Zheng Guoshuang, Kuai Xiandong, Yu Weiting. Alginate scaffold in articular cartilage repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1080-1088. |
| [10] | Chen Shisong, Liu Xiaohong, Xu Zhiyun. Current status and prospects of bioprosthetic heart valves [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1096-1102. |
| [11] | Lu Di, Zhang Cheng, Duan Rongquan, Liu Zongxiang. Osteoinductive properties of calcium phosphate ceramic bone repair materials [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1103-1109. |
| [12] | Shi Yehong, Wang Cheng, Chen Shijiu. Early thrombosis and prevention of small-diameter blood vessel prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1110-1116. |
| [13] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| [14] | Bai Siqi, Xiao Zhen, Liu Jing. Application potential of adipose-derived stem cells in female pelvic floor dysfunction diseases [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 921-927. |
| [15] | Zhang Qijian, Xu Ximing. Acquisition and application of ectodermal mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 928-934. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||