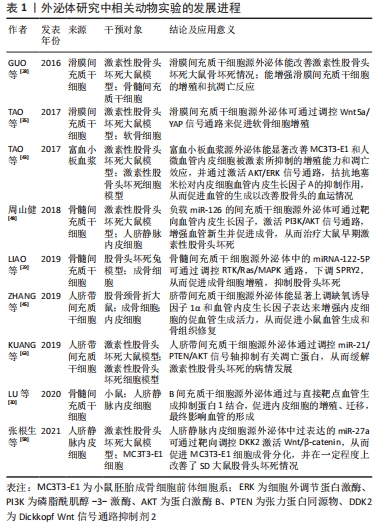
Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (19): 3056-3064.doi: 10.12307/2022.386
Previous Articles Next Articles
Regulatory mechanism of exosomes in signal communication network of steroid induced avascular necrosis of the femoral head repair
Wang Weiwei1, Ou Zhixue2, Zhang Xiaoyun1, Li Shibin1, Zhou Yi1, Li Tong1
- 1Ruikang Hospital Affiliated to Guangxi University of Traditional Chinese Medicine, Nanning 530000, Guangxi Zhuang Autonomous Region, China; 2Guilin Hospital of Traditional Chinese Medicine, Guilin 541002, Guangxi Zhuang Autonomous Region, China
-
Received:2021-07-05Revised:2021-07-26Accepted:2021-08-16Online:2022-07-08Published:2021-12-29 -
Contact:Ou Zhixue, MD, Chief physician, Guilin Hospital of Traditional Chinese Medicine, Guilin 541002, Guangxi Zhuang Autonomous Region, China Zhang Xiaoyun, Associate chief physician, Ruikang Hospital Affiliated to Guangxi University of Traditional Chinese Medicine, Nanning 530000, Guangxi Zhuang Autonomous Region, China -
About author:Wang Weiwei, Master candidate, Ruikang Hospital Affiliated to Guangxi University of Traditional Chinese Medicine, Nanning 530000, Guangxi Zhuang Autonomous Region, China -
Supported by:National Natural Science Foundation of China, No. 81960803 (to ZXY); Youth Fund of Guangxi Natural Science Foundation, No. 2020GXNSFBA159053 (to ZXY); Guangxi University Young Teachers Basic Ability Improvement Project, No. 2019KY0352 (to ZXY); Guangxi University of Traditional Chinese Medicine 2019 School-Level Scientific Research Project, No. 2019QN027 (to ZXY); Guangxi University of Traditional Chinese Medicine First-Class Subject Project, No. 2019XK026, 2019XK029 (to ZXY)
CLC Number:
Cite this article
Wang Weiwei, Ou Zhixue, Zhang Xiaoyun, Li Shibin, Zhou Yi, Li Tong. Regulatory mechanism of exosomes in signal communication network of steroid induced avascular necrosis of the femoral head repair[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(19): 3056-3064.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

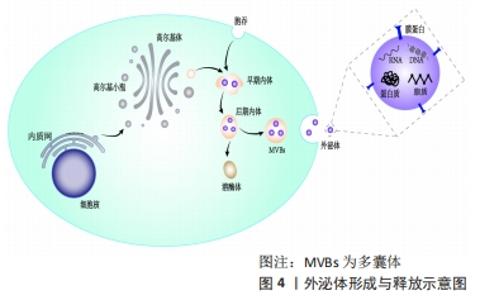
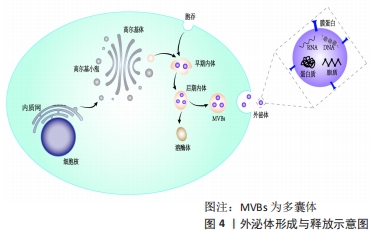
外泌体的形成存在多种机制,相关研究表明,跨膜蛋白、脂质以及syndecan-syntenin-ALIX途径,在其形成过程中起到十分重要的作用[7-10]。有研究发现,胞内四跨膜蛋白与ESCRTs作用后,促进了内囊泡的形成[8-9];ZHANG等[7]通过研究发现,外泌体膜上的鞘磷脂酶水解后,所形成的神经酰胺可促进内囊泡出芽。此外,外泌体的释放也存在多种机制,目前研究显示,Rab家族和突触蛋白在调控外泌体的释放过程中起着十分重要的作用。OSTROWSKI等[11]研究表明,抑制Rab家族相关蛋白表达水平后,Hela细胞分泌的外泌体大量减少,其中以Rab27a和Rab27b最为明显。TUCKER等[12]通过研究发现,突触蛋白可通过影响细胞质膜和多胞体的融合来调节外泌体的释放。 2.3 外泌体在激素性股骨头坏死中的应用 "

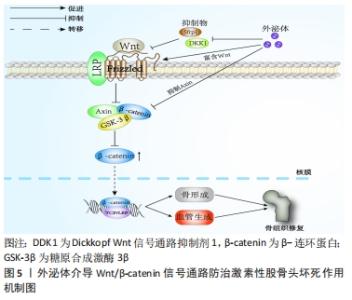
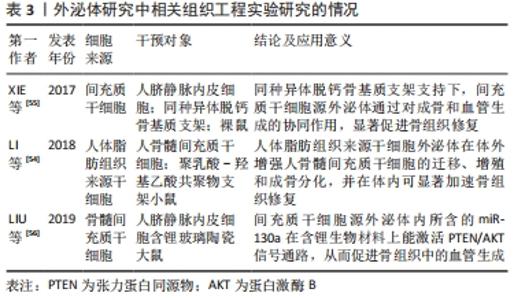
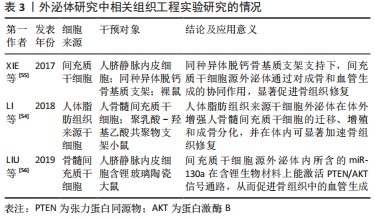
2.3.1 成骨细胞来源外泌体 成骨细胞由骨髓间充质干细胞分化而来,具有促进骨形成、愈合和重塑的功能。MIN等[13]通过蛋白质组学对小鼠MC3T3-E1细胞(成熟的成骨细胞)外泌体进行了全面分析,发现其内容物(蛋白质)主要涉及整联蛋白(Integrin)、真核起始因子2、ATP结合以及哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)信号传导4条相关成骨途径,并且还进一步指出其关键蛋白,即转化生长因子β3、骨形态发生蛋白Ⅰ型受体、ephrin-B1和低密度脂蛋白受体相关蛋白,而这些途径和蛋白质在骨组织修复过程中皆发挥着重要作用。MIN等[14]研究亦显示,矿化MC3T3-E1细胞衍生的外泌体,能上调成骨标志物的表达,如增强碱性磷酸酶和成骨特异性转录因子(runt-related transcription factor 2,RUNX2)的表达水平,并且还发现,成骨细胞外泌体中所含有的真核起始因子2B可诱导骨髓间充质干细胞的成骨分化。 除此之外,成骨细胞源外泌体中的miRNAs也被大量研究证实,在激素性股骨头坏死骨组织修复中扮演着十分重要的角色[15]。CUI等[16]研究发现,相关miRNAs在成骨细胞矿化后,上调了91个,下调了182个,而在这91个上调miRNAs中就有18种存在于其衍生的外泌体中,如miR-680、miR-677-3p和miR-3084-3p等。在其靶细胞中却发现仅有20%的miRNAs高表达,在这20%的miRNAs中,miR-667-3p,miR-6769b-5p等5个miRNAs,通过靶向β-连环蛋白(β-catenin)抑制剂体轴抑制因子1(axis inhibitor 1,Axin1)从而调控Wnt信号通路,抑制Axin1,促进β-catenin表达,最终促进成骨细胞前体的成骨分化,并进一步通过实验证明了该观点。 另外,外泌体的存在也为成骨细胞与破骨细胞之间的信号交流提供了途径。相关研究显示,成骨细胞外泌体包含骨调节相关蛋白,能刺激破骨细胞结构,从而实现骨组织细胞之间的信号交流[17]。而在这过程中,核因子κB受体活化因子配体(receptor activator of NF-κB ligand,RANKL)发挥着重要作用。RANKL是肿瘤坏死因子家族成员之一,能调控破骨细胞的激活。外泌体中的RANKL与破骨细胞前体或破骨细胞上的核因子κB受体激活因子(receptor activator of nuclear factor Kappa B,RANK)相结合,从而诱导破骨细胞或其前体分化,而两者结合过程不是通过外泌体与质膜相融合完成的,而是发生在靶细胞的表面上[18]。RANKL与RANK结合后,激活的RANK将刺激信号通过核转录因子κB送至细胞核内,c-Fos表达增强,并与活化T-细胞核因子(recombinant nuclear factor of activated T-cell cytoplasmic 1,NFATC)结合后将信号进一步传导,促使破骨细胞发生相关转录,进而促进其分化、增殖和抑制其凋亡,最终促进骨吸收。因此,作者认为Wnt经典信号传导通路和RANK-RANKL结合在成骨细胞源外泌体调控激素性股骨头坏死修复信号交流网络中发挥着重要作用,其可通过调节外泌体中相应遗传物质含量,激活Wnt信号通路以促进下游成骨标志物的表达,从而促进其前体细胞成骨分化,同时抑制RANK-RANKL相互作用,来抑制破骨细胞内RANK信号传导,进而抑制破骨细胞增殖分化,最终起到修复坏死区骨组织的作用。 2.3.2 破骨细胞来源外泌体 破骨细胞是由单核前体细胞或造血干细胞在各种信号因子的刺激下,所形成的一种高度分化的多核巨细胞,具有丰富的线粒体、高尔基体、溶酶体以及强大的细胞骨架系统,也是目前惟一明确有降解骨量作用的功能细胞。在激素性股骨头坏死病理过程中,被激活增多的破骨细胞分泌酶和酸性物质,分解吸收骨基质,使骨坏死溶解,最终导致股骨头塌陷。破骨细胞以及破骨细胞前体所衍生的外泌体,不仅在形态和大小方面相似,而且都能表达一些如CD9和CD63等外泌体标志物。但同时,在其不同时期所衍生的外泌体中,所携带的分子含量以及功能也是不同的。其中破骨前体细胞来源外泌体中RANK含量较低,而在成熟破骨细胞衍生的外泌体中就明显增高[19]。HUYNH等[20]研究发现,破骨细胞前体衍生的外泌体促进了1,25-二羟基维生素D3诱导的小鼠骨髓中破骨样多核细胞的形成,而在同一培养中,富含破骨细胞培养的外泌体却抑制了其形成,这可能是由于破骨细胞源外泌体中RANK通过类似于骨保护素的RANKL竞争性结合,抑制破骨细胞表面RANK的刺激,也有可能是利用RANK-RANKL结合将RANK丰富的外泌体靶向到RANKL承载细胞,用于调控其他分子,其具体机制有待后续研究进一步验证。由此可见,破骨细胞所衍生的外泌体是其旁分泌的重要调节因子。 Eph受体属于酪氨酸激酶受体家族成员,其细胞表面配体(ephrins)参与多种细胞通讯过程。ephrinA2-EphA2相互作用在骨组织修复起始阶段,能调控成骨细胞分化和破骨细胞形成。SUN等[21]证实了破骨细胞外泌体的表面蛋白ephrinA2与成骨细胞表面受体EphA2相结合,从而发挥相应功能。ephrinA2-EphA2的特异性结合能够将破骨细胞外泌体中大量的miRNAs运输至成骨细胞当中,从而影响成骨细胞活性。其中miR-214已被相关研究证明参与调控成骨细胞和破骨细胞。相关研究显示,miR-214可通过外泌体方式从破骨细胞转移至成骨细胞当中以抑制成骨细胞分化。WANG等[22]通过实验发现,miR-214可调节骨形成中的成骨特异性转录因子(Osterix)和成骨转录激活因子4,从而被认为与骨组织修复有关;ZHAO等[23]在骨髓单核细胞向破骨细胞方向增殖过程中,检测到其细胞内miR-214含量增多,并发现miR-214是靶向作用于张力蛋白同源物(gene of phosphate and tension homology deleted on chromsome ten,PTEN),激活磷脂酰肌醇-3-激酶(phosphatidylinositol-3-kinase,PI3K)/蛋白激酶B(protein kinase B,AKT)/NFATC1信号通路,抑制PTEN表达,进而促使AKT磷酸化水平上调,NFATC1的表达明显增加,从而促进破骨细胞增殖。由此可知,破骨细胞源外泌体的miR-214可通过多种通路的相互作用促进骨吸收,最终影响骨坏死组织修复。除了miR-214,YANG等[24]还发现,RANKL可诱导破骨细胞源性外泌体内miR-23a-5p的表达,其通过抑制RUNX2或通过Yes相关蛋白(yes-associated protein 1,YAP1)激活金属硫蛋白(metallothioneins,MTs)基因家族的长链非编码RNA成员MT1DP,来抑制成骨细胞的激活。综上所述,文章认为破骨细胞源外泌体在修复信号交流网络中,可通过ephrinA2-EphA2结合进行靶向运输,传递相关调控因子来调节靶细胞的生物活动,并通过RANKL-RANK结合,影响自身miR-214、miR-23a-5p等遗传因子的表达,调控PI3K/AKT信号通路,进而调节自身增殖、分化和凋亡,最终修复坏死区骨组织。而其中RANKL-RANK结合在破骨细胞源外泌体中是否起到类似ephrinA2-EphA2结合的靶向运输作用,则有待后续研究进行深入的探讨。 2.3.3 间充质干细胞来源外泌体 间充质干细胞来自中胚层,具有自我更新和多向分化的功能,是近些年来骨组织工程的“明星种子”,也是针对激素性股骨头坏死治疗的研究热点。现代研究结果显示,骨髓、脐带或是脂肪组织中的间充质干细胞源外泌体,均可促进间充质干细胞的成骨分化[25],其主要是通过上调相关成骨基因和促进成骨细胞增殖、迁移来实现。FANG等[26]研究证实,间充质干细胞源外泌体可通过促进成骨分化和抑制成脂分化来达到治疗股骨头坏死的效果。ZHANG等[27]研究表明骨髓间充质干细胞源外泌体可以通过调控血管生成来促进股骨头坏死区骨组织修复。GUO等[28]研究则发现,滑膜来源的间充质干细胞,可以内化为骨髓基质细胞,并增强其增殖能力和抗凋亡能力,从而预防激素诱导的股骨头坏死。 目前相关研究显示,间充质干细胞源外泌体中miRNA-122-5P和miRNA-29a在促进成骨分化、抑制破骨形成以及血管生成方面发挥重要作用。LIAO等[29]构建股骨头坏死兔模型,发现骨髓间充质干细胞源外泌体中的miRNA-122-5P通过受体酪氨酸激酶(receptor tyrosine kinase,RTK)/Ras/MAPK通路,下调sprouty同源物2(sprouty homolog 2,SPRY2),从而促进成骨细胞增殖,抑制股骨头坏死。LU等[30]报道骨髓间充质干细胞源外泌体可以运输至内皮细胞,通过与直接靶点血管抑制蛋白1结合,促进内皮细胞的增殖、迁移,最终影响血管的形成,而miRNA-29a水平在骨髓间充质干细胞源外泌体中较高。另外,其他相关研究报道,miRNA-29a可以抑制破骨形成以抵消糖皮质激素诱导的骨丢失[31]。LIAN等[32]研究则发现miR-29a通过调节p300/CBP相关因子(p300/CBP associated factor,PCAF)介导的RANKL和趋化因子配体12(C-X-C motif ligand 12,CXCL12)来抑制破骨细胞的形成。除了miRNA-122-5P和miRNA-29a,XU等[33]研究发现,在成骨分化的人骨髓间充质干细胞源外泌体中显著下调的miRNA(miR-155、miR-181a、miR-221、miR-320c 和 miR-885-5p)及其协同靶基因,均富集在MAPK和PI3K/AKT通路,而这2条通路在成骨细胞分化过程中均起到关键作用。 滑膜间充质干细胞由机体关节滑膜组织中提取而来,具备顽强的生命力,传至10代后依旧能保持其特有的细胞形态以及多能性,更因为其活性不受提取患者的年龄影响,使其成为目前骨组织修复领域颇具潜力的一种“明星种子”。其分泌的外泌体已被证实能通过促进骨髓间充质干细胞的增殖和抗凋亡作用,从而预防股骨头坏死的发生[34]。TAO等[35]研究发现滑膜间充质干细胞源外泌体中,富含Wnt5a以及Wnt5b蛋白,其通过调控Wnt5a/YAP信号通路促进软骨细胞增殖。GUO等[28]研究则将间充质干细胞源外泌体和骨髓间充质干细胞共同置于50 μmol/L大剂量激素环境中,发现前者能显著改善骨髓间充质干细胞被激素抑制的增殖能力,并且在将滑膜间充质干细胞外泌体注射至早期激素性股骨头坏死大鼠模型后可观察到相同情况。由此可见,滑膜间充质干细胞源外泌体可通过调节激素引起的骨细胞损伤机制,从而逆转激素性股骨头坏死的发生发展。 tsRNAs是通过内核裂解tRNAs产生的。近年来,这些tsRNA在多个生物学过程中广泛而保守的表达引起了人们的广泛关注。大量证据表明,tsRNAs参与翻译抑制,并在多种生理和病理现象中发挥调节作用。这些tsRNAs也影响体细胞的各种功能,如细胞增殖、癌症进展和内源性反转录因子的活性。FANG等[36]通过建立激素性股骨头坏死细胞模型以及对比正常人与激素性股骨头坏死患者的间充质干细胞源外泌体发现,223个差异表达的tsRNAs富集在Wnt信号通路上,从而参与股骨头坏死病程,并指出,其中的tsRNA-10277、tsRNA-10522和tsRNA-23731分别作用于环磷腺苷效应元件结合蛋白1(cAMP-response element binding protein,CREB1)、集落刺激因子1和NFATC2。CREB1已被证明参与大鼠骨膜源性干细胞的成骨分化[37];集落刺激因子1则在骨髓前体细胞分化为骨吸收型破骨细胞中起关键作用[38];CREB结合蛋白和骨形态发生蛋白2显著增加破骨基因集落刺激因子1的表达[39];而NFATC2则是Wnt/β-catenin通路的关键调控基因,并与成骨标志物的高表达有关。由此可知,tsRNA-10277、tsRNA-10522和tsRNA-23731是通过Wnt信号通路和成骨分化在激素性股骨头坏死进程中发挥着作用,但其真实性以及具体作用机制有待进一步探索和验证。因此,文章认为间充质干细胞源外泌体在修复信号交流网中起到广泛的信号传导作用,其通过miRNA-122-5P、miRNA-29a和tsRNAs等相关遗传物质,靶向调控Wnt和PI3K/AKT等信号通路的相关调控基因,改善骨髓间充质干细胞被激素抑制的增殖能力,促进骨髓间充质干细胞成骨分化和成骨细胞增殖,抑制破骨细胞形成,在影响坏死区骨吸收的同时还通过促进内皮细胞的增殖和迁移来进一步调节血管生成,最终促进坏死区骨组织修复,因此,间充质干细胞源外泌体的相关性研究可作为日后外泌体治疗激素性股骨头坏死的研究重点。 2.3.4 富血小板血浆来源外泌体 众所周知,富血小板血浆是一种富含多种生长因子的自体血衍生血浆,在骨组织修复、再生以及间充质干细胞分化中起着十分关键的作用[40],其在激素性股骨头坏死临床和基础研究中应用尤为广泛,能通过促进骨及血管生成,从而促进坏死区骨组织修复[41]。富血小板血浆源外泌体中同样富集多种生物活性因子,具备较为广泛的应用前景。TORREGGIANI等[42]采用经典提纯方法获取到富血小板血浆源外泌体,发现其中富含转化生长因子β1、碱性成纤维细胞生长因子以及血管内皮生长因子,能促进骨髓间充质干细胞增殖、迁移以及成骨分化。TAO等[43]将富血小板血浆源外泌体分别与骨髓间充质干细胞、人微血管内皮细胞系(HMEC-1)以及MC3T3-E1共同置于100 μmol/L大剂量激素环境中,发现富血小板血浆源外泌体能显著改善3种细胞被激素所抑制的增殖能力和凋亡效应,逆转激素对MC3T3-E1细胞、骨髓间充质干细胞成骨分化能力的抑制作用。并且还发现富血小板血浆源外泌体能激活AKT/细胞外调节蛋白激酶(extracellular regulated protein kinases,ERK)信号通路,拮抗地塞米松对内皮细胞血管内皮生长因子A的抑制作用,从而促进血管的生成以改善股骨头的血运情况。由此可见,富血小板血浆源外泌体可通过改善激素诱导的骨坏死局部微环境从而促进骨坏死组织修复。其研究也证实了在大鼠激素性股骨头坏死模型中,富血小板血浆源外泌体在抑制细胞凋亡的同时也促进了股骨头坏死区血管新生以及骨量累积。但由于目前富血小板血浆源外泌体提取技术有限,且含量不高,极大限制了其在临床上的大规模应用,因此,如何改善富血小板血浆源外泌体的提纯技术和扩大产量,就成为目前亟需解决的一大问题。 2.3.5 外泌体与血管生成 骨组织修复是一个复杂的过程,对于骨骼来说,骨量的增长离不开新生血管的形成以及氧气和营养的供给,血管形成能为骨组织修复运输养料并促进细胞增殖以及基质矿化。而间充质干细胞源外泌体中富集一系列细胞因子、生长因子、黏附分子和信号分子,譬如血管内皮生长因子、肝细胞生长因子和血管紧张素1(angiotensin 1,Ang-1)等,可调节内皮细胞中血管生成方面的基因表达以及蛋白分泌。也有相关研究者对间充质干细胞源外泌体进行了质谱分析,发现其中包含如血管内皮生长因子、转化生长因子β1和白细胞介素8等一些可溶性生长因子以及如肝细胞生长因子等一些转录因子,其通过外泌体的信息传递功能来促进血管生成。QI等[44]研究发现,人类多潜能干细胞源外泌体可以增强促进骨形成标志物如RUNX2和Ⅰ型胶原的表达,从而诱导血管再生来促进骨组织修复。而在体内实验方面,ZHANG等[45]研究亦证实,脐带间充质干细胞源外泌体能显著上调缺氧诱导因子1α和血管内皮生长因子表达来增强内皮细胞的促血管生成活力,从而促进小鼠血管生成和骨组织修复,有趣的是,在其实验当中,Osterix和Ⅰ型胶原A1等一些成骨基因的表达水平没有显著提升,这表明脐带间充质干细胞源外泌体促进骨组织修复可能只是单纯依赖于血管新生,而不是同时促进其成骨分化。这与部分研究者的看法有所不同,作者认为,造成这种情况可能与外泌体的提取、鉴定和保存的过程差异有关,后续研究可通过完善相关技术,从而对其具体作用机制进行深入了解。 另外,间充质干细胞源外泌体中还包含许多与血管生成相关的miRNA,如miRNA-125a、miRNA-126和miRNA-210等,其通过激活下游靶点促使AKT磷酸化,从而激活相关信号通路,诱使内皮细胞网状结构的发生,并结合其促增殖能力,最终影响血管的形成[46]。其中,特异性表达于内皮细胞的miR-126是目前研究较多的一种,在促进血管生成和维持血管完整性方面发挥关键调控作用。miR-126是一种内皮特异性miRNA,与血管稳态和血管生成相关。ZHANG等[47]研究在体内注射外泌体miR-126后,发现创面部位新形成的毛细血管数量显著增加,加速创面愈合;而在其体外研究中,负载miR-126的骨髓间充质干细胞源外泌体能促进人脐静脉内皮细胞的增殖、迁移和血管生成,从而起到治疗早期激素性股骨头坏死的作用[48];其将人脐静脉内皮细胞与间充质干细胞源外泌体中的miR-126孵育后,血管内皮生长因子和Ang-1的基因表达上调,并且人脐静脉内皮细胞中磷酸肌醇3激酶调控亚基2 (phosphoinositide-3-kinase regulatory subunit 2,PIK3R2)的表达水平与miR-126呈负相关,从而得知,miR-126是通过靶向血管内皮生长因子通路的负调控因子PIK3R2,激活PI3K/AKT信号通路,促进了人脐静脉内皮细胞的血管生成。除此之外,相关研究还显示外泌体可通过过表达miR-26a来促进人脐静脉内皮细胞迁移和管形成能力,并在体外激素影响下增强骨髓间充质干细胞的成骨分化,从而预防糖皮质激素诱导的股骨头坏死[49]。由此可知,无论是体内还是体外实验,皆证实了间充质干细胞源外泌体可通过调控血管生成,为坏死区骨组织修复提供养料,从而在修复信号交流网络中发挥重要作用,而PI3K/AKT信号通路在其中更是扮演着十分重要的角色。但由于外泌体在联系血管生成和骨生成方面的具体传导机制尚未阐明,缺少相关偶联机制方面的研究,因此,后续研究可将其作为外泌体治疗激素性股骨头坏死的研究重点。 2.3.6 外泌体与骨组织工程 骨组织工程学研究即致力于联合运用生物材料和细胞因子,发展能够有效修复骨缺损的新生替代材料,按照需求塑形和制备,构建与人体骨相似的骨组织。植入的组织工程复合物不仅能为坏死区的细胞生长分化提供充足的空间,还能在降解、吸收的同时逐渐被细胞增殖分化所形成的新骨所替代。而近些年来主要围绕干细胞移植和生物材料2个方面对骨组织修复展开研究,但二者皆存在一定的缺陷,如生物材料存在其毒性和免疫性易致并发症,以及干细胞存在致畸、伦理等问题[50]。外泌体的出现,则为骨组织工程提供了有益补充。一方面是因为外泌体虽来自细胞,但却不是真正意义上的细胞,它不存在传统细胞治疗的细胞来源、免疫风险、治疗时间以及医疗成本等问题[51];另一方面,外泌体不仅包含多种诱导因子,促进靶细胞增殖分化,而且和基因药物或单一蛋白相比,更具多功能性[52]。磷酸三钙是一种可生物降解的骨传导合成生物材料,已广泛应用于骨组织修复[53],但单纯的磷酸三钙因缺乏骨诱导活性而效果有限,为了解决这一缺点,研究者通常掺入一些生物活性化合物至生物材料中。而与传统的生物活性化合物(如生长因子)相比,外泌体相关疗法产生不良反应的可能性要低得多,而且它们也有足够的亲本细胞来源,以确保足够的产量。 其中,LI等[54]通过控制从聚多巴胺涂层PLGA支架中释放人体脂肪组织来源干细胞衍生的外泌体在体内临界大小的缺陷中实现显著加速骨组织修复。而除了成骨外,血管化也是骨组织修复的关键因素。在XIE等[55]的研究中,证明了在脱钙骨基质支架支持下,间充质干细胞源外泌体对成骨和血管生成的协同作用,促血管生成活性显著促进骨组织修复。除此之外,LIU等[56]研究发现外泌体内的miR-130a在含锂生物材料上能激活PTEN/AKT信号通路,从而促进骨组织中的血管生成。在现有外泌体研究基础上,YAO等[57]研究应用一种与常规外泌体相比具有高产、相似结构和生物标志物的新型外泌体模拟物(exosome mimetics,EMs)来构建工程基因激活基质用于局部治疗,利用EMs包覆血管内皮生长因子165质粒DNA,并与同轴静电纺丝制备的核-壳纳米纤维膜灵活结合,从而诱导血管化骨再生。EMs比自然分泌的外泌体产量高约28倍,并具有CD63和TSG101的外泌体特异性膜蛋白。外泌体内不包含MHC Ⅰ类或Ⅱ类蛋白,因此它们应用于非免疫兼容动物不会引起明显的免疫反应。由此可见,外泌体不仅能弥补干细胞与生物材料在治疗激素性股骨头坏死方面的相关缺陷,其自身保护以及运载遗传物质的结构与机制研究也是今后骨组织修复领域的一大热点,具有十分广泛的应用前景。 2.4 外泌体调控经典信号通路治疗激素性股骨头坏死的作用机制 根据相关实验研究表明,目前外泌体在激素性股骨头坏死骨组织修复过程中有多条信号通路参与,其中主要以干预Wnt/β-catenin和PI3K/AKT等通路来促进骨形成、抑制骨吸收以及促进血管形成,从而起到骨骼修复和血管生成的治疗作用。 2.4.1 Wnt/β-catenin信号通路 Wnt/β-catenin信号通路是目前Wnt信号传导途径中最为经典的通路之一,已被证实在治疗激素性股骨头坏死方面发挥着重要的作用。其由信号蛋白、跨膜受体、胞质蛋白、转录因子和下游靶基因构成,Frizzled为Wnt/β-catenin信号蛋白的受体,LRP5/6为辅助受体。当胞外存在Sfrp1、Dickkopf Wnt信号通路抑制剂1(Dickkopf Wnt signaling pathway inhibitor 1,DKK1)等特异性抑制物时,Wnt蛋白与其受体LRP5/6、Frizzled的结合受到抑制,而胞质内β-catenin将会与细胞支架蛋白(Axin)、糖原合成激酶3β(Glycogen synthase kinase-3β,GSK-3β)以及大肠腺瘤样息肉蛋白结合形成β-catenin降解复合物,此时Wnt/β-catenin信号通路处于失活状态,其通道并未开放。而当胞外抑制物不存在时,Wnt蛋白将正常与其受体LRP5/6、Frizzled相结合,激活胞质内散乱的蛋白,抑制GSK-3β活性,并阻碍β-catenin降解复合物的形成,抑制β-catenin磷酸化,使得胞内游离β-catenin增多,而当其数量达到阈值时,就可向核内转移并与TCF/LEF转录复合物结合,从而激活靶基因,活化Wnt/β-catenin信号通路,从而促进骨髓间充质干细胞成骨分化、加快成骨细胞增殖以及抑制成骨细胞凋亡等,最终修复坏死骨组织。CUI等[16]研究通过将外泌体(由矿化的前成骨细胞衍生)与小鼠骨髓基质细胞(ST2)共同培养发现,ST2表面出现了成骨标志,并通过激活Wnt信号通路,上调碱性磷酸酶、RUNX2表达,发现其矿化程度也随之增加。张根生等[58]研究则发现血管内皮细胞源外泌体中过表达的miR-27a可通过靶向调控DKK2促进MC3T3-E1细胞成骨分化,并在一定程度上改善了SD大鼠股骨头坏死情况。由此可见,外泌体通过Wnt/β-catenin信号传导途径在促进骨形成以及血管生成方面发挥重要作用,见图5。"
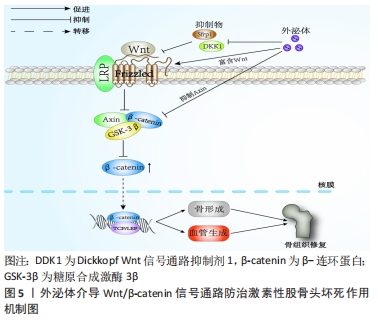
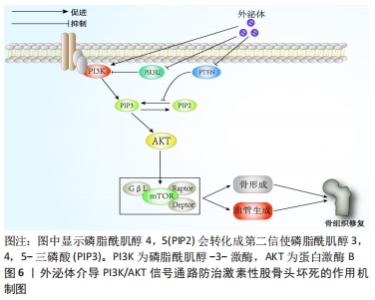
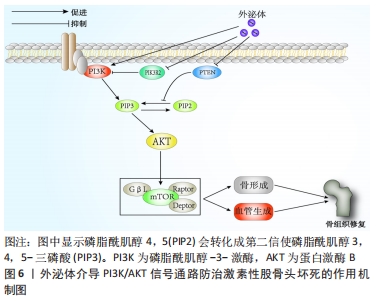
2.4.2 PI3K/AKT信号通路 此通路参与多种生物性活动,如细胞增生、凋亡以及血管生成等,并通过与多个信号通路相关联,激活相关因子调控细胞,从而调节细胞代谢平衡以及促进骨组织修复。PI3K在受到上游激活信号后,其胞膜上的磷脂酰肌醇4,5(phosphatidylinositol-4,5-bisphosphate,PIP2)会转化成第二信使磷脂酰肌醇3,4,5-三磷酸(phosphatidylinositol-3,4,5-bisphosphate,PIP3),并作用于靶基因AKT,PIP3与AKT相结合,活化AKT[59],传递信号至下游效应分子mTOR,进而调节下游多种激酶并激活介导它们,影响细胞的分化和代谢效果,最终对血管内皮修复以及激素性股骨头坏死等多种疾病起到调控作用。其中,SESSA等[60]发现miR-126可以通过调节PIK3R2来增强Ang-1的表达,从而微调血管的稳定和成熟。WALTERS等[61]将人诱导多能干细胞与β-TCP结合,在前者衍生的外泌体干预下,通过PI3K/AKT信号通路显著增强了人骨髓干细胞的成骨分化以促进骨再生。XUE等[62]通过激活PI3K/AKT信号通路,下调成骨细胞中caspase-3的表达,从而减轻地塞米松诱导的成骨细胞凋亡;KUANG等[63]研究发现人脐带间充质干细胞源外泌体通过调控miR-21/PTEN/AKT信号轴抑制有关凋亡蛋白,如BAD和caspase-3等,而激素恰好又是通过抑制AKT磷酸化,从而诱导骨细胞凋亡,进而促使BAD磷酸化诱导骨细胞凋亡,最终导致激素性股骨头坏死。由此可见,外泌体通过介导PI3K/AKT信号通路,无论在细胞增殖、凋亡以及血管生成方面,还是结合骨组织工程应用上,对于治疗激素性股骨头坏死都具有十分重要的研究价值,见图6。"
| [1] 曾宪峰,王进东,梁鼎天,等.补肾活血汤联合西医治疗早中期非创伤性股骨头缺血坏死(肾虚血瘀)随机平行对照研究[J].实用中医内科杂志,2019,33(5):38-41. [2] RECORD M, SUBRA C, SILVENTE P, et al. Exosomes as intercellular signalosomes and pharmacological effectors. Biochem Pharmacol. 2011; 81(10):1171-1182. [3] PISHAVAR E, LUO H, NASERIFAR M, et al. Advanced hydrogels as exosome delivery systems for osteogenic differentiation of mscs: application in bone regeneration. Int J Mol Sci. 2021;22(12):6203. [4] 贾亚超.外泌体及纳米微粒促进牵张成骨骨再生的研究[D].上海:上海交通大学,2019. [5] 魏松乔,郭澍,佟爽,等.脂肪干细胞-丝素/壳聚糖支架复合物在外泌体诱导下的体外成骨效应[J].中国医科大学学报,2019,48(10):891-895. [6] 陈义庆,郭澍,佟爽,等.可注射水凝胶负载脂肪来源干细胞外泌体促进骨再生[J].中国美容整形外科杂志,2019,30(4):206-209. [7] ZHANG Y, LIU YF, LIU HY, et al. Exosomes: biogenesis, biologic function and clinical potential. Cell Biosci. 2019;9:19. [8] MARIA FB, ZHE Z, EVA M, et al. Syndecan-syntenin-ALIX regulates the biogenesis of exosomes. Nat Cell Biol. 2012;14(7):677-685. [9] PEREZ-HERNANDEZ D, GUTIÉRREZ-VÁZQUEZ C, JORGE I, et al. The intracellular interactome of tetraspanin-enriched microdomains reveals their function as sorting machineries toward exosomes. J Biol Chem. 2013; 288(17):11649-11661. [10] ROUCOURT B, MEEUSSEN S, BAO J, et al. Heparanase activates the syndecan-syntenin-ALIX exosome pathway. Cell Res. 2015;25(4):412-428. [11] OSTROWSKI M, CARMO NB, KRUMEICH S, et al. Rab27a and Rab27b control different steps of the exosome secretion pathway. Nat Cell Biol. 2010;12(1): 19-30. [12] TUCKER WC, CHAPMAN ER. Role of synaptotagmin in Ca2+-triggered exocytosis. Biochem J. 2002;366(Pt 1):1-13. [13] MIN G, WU YZ, KE RH, et al. Value of osteoblast-derived exosomes in bone diseases. J Craniofac Surg. 2017;28(4):866-870. [14] MIN G, KE RH, CAI TY, et al. Identification and proteomic analysis of osteoblast-derived exosomes. Biochem Biophys Res Commun. 2015;467(1): 27-32. [15] YOSHIHIRO N, SHIGERU M, HIROYUKI I, et al. Mesenchymal-stem-cell-derived exosomes accelerate skeletal muscle regeneration. FEBS Lett. 2015; 589(11):1257-1265. [16] CUI YZ, LUAN J, LI HY, et al. Exosomes derived from mineralizing osteoblasts promote ST2 cell osteogenic differentiation by alteration of microRNA expression. FEBS Lett. 2016;590(1):185-192. [17] BIRMINGHAM E, NIEBUR GL, MCHUGH PE, et al. Osteogenic differentiation of mesenchymal stem cells is regulated by osteocyte and osteoblast cells in a simplified bone niche. Eur Cell Mater. 2012;23:13-27. [18] DENG L, WANG Y, PENG Y, et al. Osteoblast-derived microvesicles: a novel mechanism for communication between osteoblasts and osteoclasts. Bone. 2015;79:37-42. [19] TAVEMA S, PUCCI M, GIALLOMBADO M, et al. Amphiregulin contained in NSCLC-exosomes induces osteoclast differentiation through the activation of EGFR pathway. Sci Rep. 2017;7(1):3170. [20] HUYNH N, VONMOSS L, SMITH D, et al. Characterization of regulatory extracellular vesicles from osteoclasts. J Dent Res. 2016;95(6):673-679. [21] SUN WJ, ZHAO CY, Li YH, et al. Osteoclast-derived microRNA-containing exosomes selectively inhibit osteoblast activity. Cell Discov. 2016;2:16015. [22] WANG XG, GUO BS, QI L, et al. miR-214 targets ATF4 to inhibit bone formation. Nat Med. 2013;19(1):93-100. [23] ZHAO C, SUN W, ZHANG P, et al. miR-214 promotes osteoclastogenesis by targeting Pten/PI3k/Akt pathway. RNA Biol. 2015;12(3):343-353. [24] YANG JX, XIE P, LI YS, et al. Osteoclast-derived miR-23a-5p-containing exosomes inhibit osteogenic differentiation by regulating Runx2. Cell Signal. 2020;70:109504. [25] XQ WANG, OMAR O, FORUGH V, et al. Mesenchymal stem cell-derived exosomes have altered microRNA profiles and induce osteogenic differentiation depending on the stage of differentiation. PLoS One. 2018; 13(2):e0193059. [26] FANG SH, LI YF, CHEN P. Osteogenic effect of bone marrow mesenchymal stem cell-derived exosomes on steroid-induced osteonecrosis of the femoral head. Drug Des Devel Ther. 2018;13:45-55. [27] ZHANG C, SU Y, DING H, et al. Mesenchymal stem cells-derived and siRNAs-encapsulated exosomes inhibit osteonecrosis of the femoral head. J Cell Mol Med. 2020;24(17):9605-9612. [28] GUO SC, TAO SC, YIN WJ, et al. Exosomes from human synovial-derived mesenchymal stem cells prevent glucocorticoid-induced osteonecrosis of the femoral head in the rat. Int J Biol Sci. 2016;12(10):1262-1272. [29] LIAO W, NING Y, XU HJ, et al. BMSC-derived exosomes carrying microRNA-122-5p promote proliferation of osteoblasts in osteonecrosis of the femoral head. Clin Sci (Lond). 2019;133(18):1955-1975. [30] LU GD, CHENG P, LIU T, et al. BMSC-derived exosomal miR-29a promotes angiogenesis and osteogenesis. Front Cell Dev Biol. 2020;8:608521. [31] WU RW, LIAN WS, CHEN YS, et al. MicroRNA-29a counteracts glucocorticoid induction of bone loss through repressing TNFSF13b modulation of osteoclastogenesis. Int J Mol Sci. 2019;20(20):5141. [32] LIAN WS, KO JY, CHEN YS, et al. MicroRNA-29a represses osteoclast formation and protects against osteoporosis by regulating PCAF-mediated RANKL and CXCL12. Cell Death Dis. 2019;10(10):705. [33] XU JF, YANG GH, PAN XH, et al. Altered microRNA expression profile in exosomes during osteogenic differentiation of human bone marrow-derived mesenchymal stem cells. PLoS One. 2014;9(12):e114627. [34] 郭尚春.外泌体对组织修复的作用及其机制研究[D].上海:上海交通大学,2016. [35] TAO SC, YUAN T, ZHANG YL, et al. Exosomes derived from miR-140-5p-overexpressing human synovial mesenchymal stem cells enhance cartilage tissue regeneration and prevent osteoarthritis of the knee in a rat model. Theranostics. 2017;7(1):180-195. [36] FANG SH, HE TM, JIANG J, et al. Osteogenic effect of tsRNA-10277-loaded exosome derived from bone mesenchymal stem cells on steroid-induced osteonecrosis of the femoral head. Drug Des Devel Ther. 2020;14: 4579-4591. [37] ZHANG YF, XU JK, YE CR, et al. Implant-derived magnesium induces local neuronal production of CGRP to improve bone-fracture healing in rats. Nat Med. 2016;22(10):1160-1169. [38] YOSHIDA H, HAYASHI SI, KUNISADA T. The murine mutation osteopetrosis is in the coding region of the macrophage colony stimulating factor gene. Nature. 1990;345(6274):442–444. [39] GHOSH CN, SINGHA PK, WOODRUFF K, et al. Concerted action of Smad and CREB-binding protein regulates bone morphogenetic protein-2-stimulated osteoblastic colony-stimulating factor-1 expression. J Biol Chem. 2006;281(29):20160-20170. [40] GABRIELA F, YANG SY. Application of platelet-rich plasma with stem cells in bone and periodontal tissue engineering. Bone Res. 2016;4:16036. [41] TONG SC, YIN JM, LIU J. Platelet-rich plasma has beneficial effects in mice with osteonecrosis of the femoral head by promoting angiogenesis. Exp Ther Med. 2018;15(2):1781-1788. [42] TORREGGIANI E, PERUT F, RONCUZZI L, et al. Exosomes: novel effectors of human platelet lysate activity. Eur Cell Mater. 2014;28:137-151. [43] TAO SC, YUAN T, RUI BY, et al. Exosomes derived from human platelet-rich plasma prevent apoptosis induced by glucocorticoid-associated endoplasmic reticulum stress in rat osteonecrosis of the femoral head via the Akt/Bad/Bcl-2 signal pathway. Theranostics. 2017;7(3):733-750. [44] QI X, ZHANG JY, YUAN H, et al. Exosomes secreted by human-induced pluripotent stem cell-derived mesenchymal stem cells repair critical-sized bone defects through enhanced angiogenesis and osteogenesis in osteoporotic rats. Int J Biol Sci. 2016;12(7):836-849. [45] ZHANG YT, HAO ZC, WANG PF, et al. Exosomes from human umbilical cord mesenchymal stem cells enhance fracture healing through HIF-1α-mediated promotion of angiogenesis in a rat model of stabilized fracture. Cell Prolif. 2019;52(2):e12570. [46] TENG XM, CHEN L, CHEN WQ, et al. Mesenchymal stem cell-derived exosomes improve the microenvironment of infarcted myocardium contributing to angiogenesis and anti-inflammation. Cell Physiol Biochem. 2015;37(6):2415-2424. [47] ZHANG L, OUYANG PR, HE GL, et al. Exosomes from microRNA-126 overexpressing mesenchymal stem cells promote angiogenesis by targeting the PIK3R2-mediated PI3K/Akt signalling pathway. J Cell Mol Med. 2021; 25(4):2148-2162. [48] 周山健.负载miR-126的外泌体对大鼠早期激素诱导的缺血性股骨头坏死的治疗作用[D].锦州:锦州医科大学,2018. [49] ZUO RT, KONG LC, WANG MW, et al. Exosomes derived from human CD34+ stem cells transfected with miR-26a prevent glucocorticoid-induced osteonecrosis of the femoral head by promoting angiogenesis and osteogenesis. Stem Cell Res Ther. 2019;10(1):321. [50] FLEURY A, MARTINEZ MC, LE LS. Extracellular vesicles as therapeutic tools in cardiovascular diseases. Front Immunol. 2014;5:370. [51] ZHANG SP, KRISTEEN YWT, SHANG JC, et al. MSC exosomes alleviate temporomandibular joint osteoarthritis by attenuating inflammation and restoring matrix homeostasis. Biomaterials. 2019;200:35-47. [52] YUAN X, Chen L, YAN CC, et al. Circulating exosomal mir-20b-5p inhibition restores wnt9b signaling and reverses diabetes-associated impaired wound healing. Small. 2020;16(3):e1904044. [53] WATARU K, MASASHI O, TAKAMASA K, et al. First-in-human study and clinical case reports of the alveolar bone regeneration with the secretome from human mesenchymal stem cells. Head Face Med. 2016;12:5. [54] LI WY, LIU YS, ZHANG P, et al. Tissue-engineered bone immobilized with human adipose stem cells-derived exosomes promotes bone regeneration. ACS Appl Mater Interfaces. 2018;10(6):5240-5254. [55] XIE H, WANG ZX, ZHANG LM, et al. Extracellular vesicle-functionalized decalcified bone matrix scaffolds with enhanced pro-angiogenic and pro-bone regeneration activities. Sci Rep. 2017;7:45622. [56] LIU L, LIU YQ, FENG C, et al. Lithium-containing biomaterials stimulate bone marrow stromal cell-derived exosomal miR-130a secretion to promote angiogenesis. Biomaterials. 2019;192:523-536. [57] YAO Z, LIN TY, LI YW, et al. Exosome-mimetics as an engineered gene-activated matrix induces in-situ vascularized osteogenesis. Biomaterials. 2020;247:119985. [58] 张根生,刘瑞宇,党晓谦,等.miR-27a过表达的血管内皮细胞来源外泌体改善股骨头坏死实验研究[J].中国修复重建外科杂志,2021,35(3): 356-365. [59] 宋世雷,陈跃平,章晓云.PI3K/AKT信号通路调控股骨头坏死的相关机制[J].中国组织工程研究,2020,24(3):408-415. [60] SESSA R, SEANO G, DI BL, et al. The miR-126 regulates angiopoietin-1 signaling and vessel maturation by targeting p85β. Biochim Biophys Acta. 2012;1823(10):1925-1935. [61] WALTERS N, NGUYEN LTH, ZHANG JJ, et al. Extracellular vesicles as mediators of in vitro neutrophil swarming on a large-scale microparticle array. Lab Chip. 2019;19(17):2874-2884. [62] XUE XH, FENG ZH, LIi ZX, et al. Salidroside inhibits steroid-induced avascular necrosis of the femoral head via the PI3K/Akt signaling pathway: In vitro and in vivo studies. Mol Med Rep. 2018;17(3):3751-3757. [63] KUANG MJ, HUANG Y, ZHAO XG, et al. Exosomes derived from Wharton’s jelly of human umbilical cord mesenchymal stem cells reduce osteocyte apoptosis in glucocorticoid-induced osteonecrosis of the femoral head in rats via the miR-21-PTEN-AKT signalling pathway. Int J Biol Sci. 2019;15(9): 1861-1871. |
| [1] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [2] | Zhang Lichuang, Xu Hao, Ma Yinghui, Xiong Mengting, Han Haihui, Bao Jiamin, Zhai Weitao, Liang Qianqian. Mechanism and prospects of regulating lymphatic reflux function in the treatment of rheumatoid arthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1459-1466. |
| [3] | Xiao Hao, Liu Jing, Zhou Jun. Research progress of pulsed electromagnetic field in the treatment of postmenopausal osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1266-1271. |
| [4] | Wang Jing, Xiong Shan, Cao Jin, Feng Linwei, Wang Xin. Role and mechanism of interleukin-3 in bone metabolism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1260-1265. |
| [5] | Tian Chuan, Zhu Xiangqing, Yang Zailing, Yan Donghai, Li Ye, Wang Yanying, Yang Yukun, He Jie, Lü Guanke, Cai Xuemin, Shu Liping, He Zhixu, Pan Xinghua. Bone marrow mesenchymal stem cells regulate ovarian aging in macaques [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 985-991. |
| [6] | Wu Weiyue, Guo Xiaodong, Bao Chongyun. Application of engineered exosomes in bone repair and regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1102-1106. |
| [7] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [8] | Hou Jingying, Guo Tianzhu, Yu Menglei, Long Huibao, Wu Hao. Hypoxia preconditioning targets and downregulates miR-195 and promotes bone marrow mesenchymal stem cell survival and pro-angiogenic potential by activating MALAT1 [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1005-1011. |
| [9] | Liang Xuezhen, Yang Xi, Li Jiacheng, Luo Di, Xu Bo, Li Gang. Bushen Huoxue capsule regulates osteogenic and adipogenic differentiation of rat bone marrow mesenchymal stem cells via Hedgehog signaling pathway [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1020-1026. |
| [10] | Wen Dandan, Li Qiang, Shen Caiqi, Ji Zhe, Jin Peisheng. Nocardia rubra cell wall skeleton for extemal use improves the viability of adipogenic mesenchymal stem cells and promotes diabetes wound repair [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1038-1044. |
| [11] | Zhu Bingbing, Deng Jianghua, Chen Jingjing, Mu Xiaoling. Interleukin-8 receptor enhances the migration and adhesion of umbilical cord mesenchymal stem cells to injured endothelium [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1045-1050. |
| [12] | Zhang Yujie, Yang Jiandong, Cai Jun, Zhu Shoulei, Tian Yuan. Mechanism by which allicin inhibits proliferation and promotes apoptosis of rat vascular endothelial cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1080-1084. |
| [13] | Fang Xiaolei, Leng Jun, Zhang Chen, Liu Huimin, Guo Wen. Systematic evaluation of different therapeutic effects of mesenchymal stem cell transplantation in the treatment of ischemic stroke [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1085-1092. |
| [14] | Guo Jia, Ding Qionghua, Liu Ze, Lü Siyi, Zhou Quancheng, Gao Yuhua, Bai Chunyu. Biological characteristics and immunoregulation of exosomes derived from mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1093-1101. |
| [15] | Kang Kunlong, Wang Xintao. Research hotspot of biological scaffold materials promoting osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 597-603. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||