Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (24): 3894-3901.doi: 10.12307/2021.099
Previous Articles Next Articles
Effect of Wnt/beta-catenin signaling pathway on osteoblasts under the action of wear particles
Wang Qiufei1, Gu Ye1, Peng Yuqin1, Xue Feng1, Ju Rong1, Zhu Feng2, Wang Yijun2, Geng Dechun2, Xu Yaozeng2
- 1Department of Orthopedics, Changshu No. 1 People’s Hospital, Changshu Hospital Affiliated to Soochow University, Changshu 215500, Jiangsu Province, China; 2Department of Orthopedics, The First Affiliated Hospital of Soochow University, Suzhou 215006, Jiangsu Province, China
-
Received:2020-10-14Revised:2020-10-17Accepted:2020-11-26Online:2021-08-28Published:2021-03-17 -
Contact:Gu Ye, MD, Associate chief physician, Department of Orthopedics, Changshu No. 1 People’s Hospital, Changshu Hospital Affiliated to Soochow University, Changshu 215500, Jiangsu Province, China -
About author:Wang Qiufei, Master, Attending physician, Department of Orthopedics, Changshu No. 1 People’s Hospital, Changshu Hospital Affiliated to Soochow University, Changshu 215500, Jiangsu Province, China -
Supported by:the Jiangsu Province Youth Medical Key Talents Funding Project, No. QNRC2016751 (to GDC); the Six-One Project Funded Project of Jiangsu Province, No. LQY2016033 (to GDC); the Clinical Diagnosis and Treatment of Key Diseases in Suzhou, No. LCZX201824 (to XF, GY); the Science and Technology Project of Changshu Health Commission, No. csws201907 (to GY); the Changshu Science and Technology Development Plan Project, No. CS201817 (to GY)
CLC Number:
Cite this article
Wang Qiufei, Gu Ye, Peng Yuqin, Xue Feng, Ju Rong, Zhu Feng, Wang Yijun, Geng Dechun, Xu Yaozeng. Effect of Wnt/beta-catenin signaling pathway on osteoblasts under the action of wear particles[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(24): 3894-3901.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
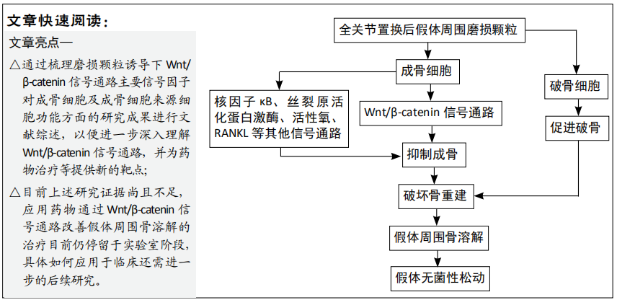
2.1 关节置换术后无菌性松动与假体周围骨溶解 TJA术后假体周围无菌性松动是人工假体中远期失效并导致翻修的重要原因,也是制约人工假体使用年限的主要因素。假体周围微环境的动态变化引起了上述结果,多种致病因素均参与其中,但仍未完全阐明假体周围无菌性松动的发生机制。大量研究表明,很多独立或相互联系的因素均可引起无菌性松动[5-6],大致可以总结为两大类:①生物学因素,即由磨损颗粒引起的细胞因子及趋化因子的分泌、细胞酶的活化、细胞致敏反应等细胞生物学反应;②机械性因素,包括手术入路和方式、假体材料、设计和安装、假体磨损、应力遮挡、循环负荷以及假体周围液压增高等因素。尽管这些机械因素均通过直接或间接的方式诱导机械性骨溶解,但目前普遍认为生物学因素,尤其是磨损颗粒诱导的假体周围骨溶解是引起假体无菌性松动的主要原因。 2.1.1 假体周围骨溶解 TJA术后随着假体和骨界面之间的微动以及假体各部件之间的长期磨损,假体周围会蓄积大量的磨损颗粒,包括聚甲基丙烯酸甲酯、金属和陶瓷颗粒等微米级、纳米级颗粒,而这些磨损颗粒可以通过直接或间接作用损害人工假体本身进一步加剧假体局部的磨损,从而陷入恶性循环并最终导致大量磨损颗粒在假体周围局部蓄积。假体周围磨损颗粒能诱导假体周围组织发生过表达的慢性炎症反应,假体-骨界面周围的成骨细胞、破骨细胞、巨噬细胞、成纤维细胞、淋巴细胞等细胞吞噬或内化磨损颗粒后,通过自分泌或旁分泌的形式释放大量促炎性细胞因子及趋化因子,如白细胞介素(白细胞介素1α、白细胞介素1β、白细胞介素6、白细胞介素18)以及肿瘤坏死因子α等,进而募集更多的炎性细胞参与到假体周围的慢性炎症反应。人工假体周围持续的慢性炎症反应抑制了其周围成骨细胞的分化与生成,可减弱成骨细胞的成骨作用并且诱导破骨细胞的形成,加强破骨细胞的骨吸收作用,最终导致假体周围骨重建的平衡状态被打破,诱导假体周围骨溶解的发生[3-6]。 2.1.2 磨损颗粒影响下成骨细胞与假体周围骨溶解 成骨细胞是由具有内外骨膜中及骨髓基质内多能性的间充质干细胞分化而来,成骨细胞系主要由不成熟的成骨前体细胞、正在分化的成骨细胞以及成熟的具备骨基质生成能力的成骨细胞等构成。成骨细胞是骨组织中主要的骨形成细胞,其通过分泌包括骨钙素、碱性磷酸酶和大量的Ⅰ型胶原来参与骨基质的生成,其中Ⅰ型胶原构成90%的有机骨基质。 目前认为磨损颗粒可直接作用于成骨细胞,造成细胞表型发生改变及其相应基因的转变,进而影响细胞内蛋白表达异常,最终表现为成骨细胞矿化能力及增殖能力减弱而导致假体周围骨溶解。另外当磨损颗粒作用于成骨细胞后可以促使骨吸收因子表达出现上调,如RANKL、白细胞介素1β、前列腺素E2等,而抑制骨吸收因子则出现表达下调,如骨保护素等,可以促进破骨细胞被过度活化,进而增强了局部骨破坏和骨吸收作用[6-7] 。因此进一步理解成骨细胞在假体周围骨溶解过程中所起的作用,将有助于发现干预假体周围骨溶解及无菌性松动的新治疗靶点。 当假体-骨界面周围磨损颗粒增多时,尽管成骨细胞是非吞噬细胞类细胞,但它仍可以通过细胞吞噬或者微胞饮现象,网格蛋白以及小凹蛋白等介导的内化作用将磨损颗粒转移至胞质内,从而引起磨损颗粒对成骨细胞功能的影响。BURTON等[8]通过细胞吞噬抑制剂细胞松弛素D预处理,通过抑制颗粒内化从而减轻颗粒与成骨细胞直接作用,进而引起的细胞活性、分化和炎症反应。目前大量研究均证实,不同颗粒大小、材质的磨损颗粒被成骨细胞吞噬或内化后能直接损伤成骨细胞细胞器并有可能造成DNA损伤、激活DNA修复、破坏细胞骨架的结构及功能,影响成骨细胞存活能力、增殖、黏附及迁移等细胞活动,并且成骨细胞的分化及矿化能力也受磨损颗粒影响出现下降。甚至有研究发现磨损钛颗粒可以下调间充质干细胞向成骨细胞分化的过程。研究显示成骨细胞与磨损颗粒接触后,碱性磷酸酶、Runx2、Osterix等早期成骨相关的基因及晚期成骨相关的骨钙素表达降低,并且成骨细胞合成Ⅰ型胶原蛋白及调节基质矿化的能力也明显下降[9]。另外成骨相关的转录因子,如骨桥蛋白、转化生长因子β1、sp7、骨钙素、FRA-2、Dlx5和Dkk1等的表达不同程度降低,而破骨相关的转录因子,如骨形态发生蛋白3、壳硬化蛋白和Msx2等则表达增高[10]。另外成骨细胞也可以分泌细胞外骨基质和效应物如基质降解蛋白酶、金属蛋白酶抑制剂参与到假体周围的骨重建和骨基质平衡中。人工假体周围磨损颗粒刺激成骨细胞后,破坏成骨细胞中基质降解蛋白酶和金属蛋白酶抑制剂之间的平衡,继发骨重建失衡,最终导致假体周围骨溶解的发生。综上所述,磨损颗粒可以通过直接作用于成骨细胞,影响成骨细胞成骨分化和矿化能力,进而破坏骨重建和骨基质平衡,并最终导致假体周围骨溶解形成。 磨损颗粒诱导的假体周围慢性炎症主要是通过激活巨噬细胞尤其是M1巨噬细胞来实现的,但成骨细胞、骨细胞、成纤维细胞和树突状细胞也参与了部分炎症形成过程。当磨损颗粒激活成骨细胞,并促进成骨细胞分泌炎症递质时,成骨细胞促炎细胞因子(包括肿瘤坏死因子α、白细胞介素1、白细胞介素6和巨噬细胞集落刺激因子)的分泌及相关基因的表达以时间和浓度依赖的方式显著上升。而这些促炎因子进一步激活了破骨细胞,促进破骨细胞骨破坏,最终导致假体周围骨溶解的形成。在这些炎性因子中肿瘤坏死因子α是主要的促炎因子,其通过自分泌和旁分泌信号通路控制白细胞介素1、白细胞介素6等其他促炎递质的释放。另外,肿瘤坏死因子α和白细胞介素1β还能通过成骨细胞改变骨基质的构成,改变骨基质平衡状态,进一步影响假体周围骨溶解的形成。在磨损颗粒刺激下,细胞趋化因子通过募集局部和全身的炎性细胞来激活假体周围的炎症反应,在假体周围骨溶解起到了关键性作用。尽管目前认为巨噬细胞和间充质干细胞是细胞趋化因子的主要来源,但成骨细胞也能产生单核细胞趋化蛋白1以及白细胞介素8。当磨损颗粒刺激成骨细胞时,成骨细胞内单核细胞趋化蛋白1和白细胞介素8 mRNA的表达及蛋白的分泌都以时间和浓度依赖的方式显著上升,而趋化因子的分泌促进了假体周围慢性炎症的进展,并最终影响了假体周围骨溶解的进程。 2.1.3 信号通路在成骨细胞诱导假体周围骨溶解过程中的作用 在磨损颗粒刺激成骨细胞诱导假体周围骨溶解的过程中,核因子κB、丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)、活性氧、RANKL以及Wnt/β-catenin等多种信号通路均涉及其中。核因子κB信号通路是免疫反应的主要调节机制之一,通过该信号通路可以调节Ⅰ型胶原蛋白的产生,并显著激活促炎细胞因子(肿瘤坏死因子α、白细胞介素1β和白细胞介素6)和趋化因子(白细胞介素8、单核细胞趋化蛋白1),进而促进炎症反应进行。FRITZ等[11]通过研究暴露在钛颗粒中的MG-63细胞发现,不仅促进转录因子核因子κB绑定至白细胞介素8启动子上,而且激活了MAPK(ERK、JNK和p38)信号通路。 MAPK和核因子κB信号通路可以通过上调炎性细胞因子和趋化因子的产生,促进慢性炎症的发生,并下调成骨细胞胶原蛋白的合成。而MAPK信号通路还涉及破坏成骨细胞内核因子κB受体活化因子配体的受体激活剂/骨保护素G的平衡状态,增加基质降解蛋白酶生成,最终破骨细胞的生成增加而细胞外骨基质沉积的过程受到抑制。而研究也表明,p38-MAPK信号通路在基质降解蛋白酶2 mRNA诱导条件下能够调节成骨细胞的活动[12],将MC3T3E-1细胞与钛颗粒共培养后激活p38-MAPK信号通路并触发基质降解蛋白酶2的表达;而通过p38抑制剂SB203580预处理,抵抗了钛微粒诱导的基质降解蛋白酶2 mRNA表达及蛋白分泌。同时SB203580也能在体内实验中,通过下调核因子κB受体活化因子配体的受体激活剂/骨保护素G和基质降解蛋白酶9/肿瘤坏死因子α在小鼠骨溶解模型中抑制钛微粒诱导的炎性骨溶解。 成骨细胞内的磨损颗粒也能发挥细胞毒性作用,通过活性氧的产生诱导细胞凋亡。活性氧不仅导致了溶酶体的通透性增加和组织蛋白酶B的释放,还导致了线粒体功能障碍及DNA损伤。此外凋亡蛋白酶(半胱氨酸蛋白酶)依赖性的成骨细胞凋亡已被报道,这归因于促凋亡蛋白(Bax、半胱氨酸蛋白酶3和半胱氨酸蛋白酶9)表达降低和抗凋亡蛋白(Bcl-2)、细胞肿瘤抗原p53表达增高。 成骨细胞还可以通过核因子κB受体活化因子配体的受体激活剂依赖的信号通路来影响假体周围骨溶解进程。核因子κB受体活化因子配体的受体激活剂通过与破骨细胞前体细胞膜表面的核因子κB受体活化因子配体受体相结合,触发级联的胞内核因子κB信号通路,进而激活破骨细胞,这对破骨细胞的分化至关重要[13]。而成骨细胞分泌的骨保护素则是抑制核因子κB受体活化因子配体的受体激活剂活性的破骨抑制因子。核因子κB受体活化因子配体的受体激活剂/骨保护素G比值是破骨细胞激活及破骨功能的重要衡量标志。研究表明多种磨损颗粒诱导处理后成骨细胞及周围组织细胞中明显出现核因子κB受体活化因子配体的受体激活剂/骨保护素G的比值增高[14]。而通过在超高分子量聚乙烯诱导骨质溶解模型内局部应用核因子κB受体活化因子配体的受体激活剂 siRNA可以抑制骨溶解并促进骨形成。 磨损颗粒还可以通过抑制成骨细胞内Wnt/β-catenin和骨形态发生蛋白信号通路,干扰成骨细胞分化并最终导致骨形成减少和骨吸收增加。NAM等[9]研究发现,磨损颗粒主要通过Wnt/β-catenin及骨形态发生蛋白/smad 信号通路诱导成骨细胞分化能力降低,而这两条通路均可被成骨原细胞所抑制。另外有研究表明,在大鼠假体周围骨溶解的动物模型中应用GSK-3β抑制剂AR28后,通过Wnt/β-catenin和骨形态发生蛋白2信号通路调节可以上调成骨细胞分化、加速成骨修复并减轻破骨细胞生成[15]。以上的研究主要结果与作者所在研究团队中GENG等[16]、GU等[17]的前期研究结果相符,并且发现磨损颗粒能够抑制GSK-3β(pSer9)磷酸化,通过GSK-3β/β-catenin通路进一步抑制成骨细胞分化,加剧骨溶解。随着研究团队进一步研究发现钛颗粒能抑制MC3T3-E1的成骨分化,而且体内研究也证实,在磨损颗粒引起的骨溶解局部骨钙素阳性的成熟成骨细胞数量显著降低[18]。 综上所述,TJA术后出现局部假体周围骨溶解,进而导致无菌性松动不仅因为磨损颗粒导致成骨细胞成骨、矿化能力减弱,而且与成骨细胞通过多种细胞因子和趋化因子引起级联反应造成破骨细胞过度活化有关,所以成骨细胞在假体周围骨溶解及无菌性松动中起着重要作用。目前研究表明多种信号通路均涉及其中,作者所在研究团队在既往研究中也发现Wnt/β-catenin信号通路在磨损颗粒与成骨细胞相互作用后抑制其胞分化、成骨能力等细胞功能,在诱导假体周围骨溶解及无菌性松动过程中起到了重要作用,其中GSK-3β和β-catenin是Wnt/β-catenin信号通路重要的负性调控因子及下游枢纽信号分子,其表达量也反映了这一信号通路的激活水平。尽管Wnt/β-catenin信号通路在磨损颗粒抑制成骨细胞能力中所起的作用及具体机制目前尚不完全明确,但可能是今后药物干预治疗的新靶点。 2.2 Wnt/β-catenin信号通路及其重要信号分子 2.2.1 Wnt/β-catenin信号通路的分子学机制 Wnt信号通路调节在包括增殖、修复、组织发育以及新陈代谢等细胞和生物的过程中起着核心作用。而Wnt/β-catenin是Wnt信号通路中研究最深入的通路,又被成为Wnt经典信号通路。当细胞膜外存在Wnt信号分子(包括Wnt 1、Wnt 2、Wnt 3、Wnt 3a、Wnt 8、Wnt Sb等)时可通过Frizzled受体或辅助受体Lrp5/Lrp6膜受体构象将细胞外信号传递入细胞内,并作用于细胞内GSK-3β。GSK-3β磷酸化失活后抑制了GSK-3β与轴蛋白、腺瘤病大肠杆菌、蛋白磷酸酶2A与酪蛋白激酶1α形成 β-catenin 降解复合体(腺瘤病大肠杆菌-GSK-3β-轴蛋白复合体),并抑制了腺瘤病大肠杆菌-GSK-3β-轴蛋白复合体磷酸化β-catenin的过程,进而导致细胞质内游离的β-catenin浓集。胞质内增多的β-catenin可以通过核转位功能,进入细胞核内与T细胞转录因子/淋巴增强因子共同结合形成复合体,进而激活信号通路靶基因转录。但当存在Wnt配体蛋白抑制剂等因素,Wnt配体蛋白与跨膜受体结合受抑制后,腺瘤病大肠杆菌-GSK-3β-轴蛋白复合体通过将β-catenin磷酸化,而磷酸化的β-catenin被β-TrCP靶向泛素化而达到降解,随后将其送至蛋白酶体进行消化。细胞质内游离β-catenin水平降低,从而抑制信号通路靶基因转录,进而发挥调控作用。 2.2.2 GSK-3β在信号通路中的作用及对成骨细胞的影响GSK-3是一种丝氨酸/苏氨酸蛋白激酶,主要包含GSK-3α和GSK-3β两种亚型。GSK-3最早在小鼠骨骼肌细胞中发现,其在细胞的生殖、分化、凋亡、定位等多种细胞生物学活动中通过调节蛋白的表达而发挥重要作用。GSK-3分布于所有真核生物的细胞中,但GSK-3α和GSK-3β蛋白水平表达并不一致。GSK-3α蛋白高表达于肺、肾、卵巢和睾丸,GSK-3β蛋白则高表达于肺、肾和脑组织中。近期有研究表明GSK-3β在骨组织也存在高表达,并且与骨量的调控密切相关[16]。GSK-3β与轴蛋白、腺瘤病大肠杆菌、蛋白磷酸酶2A以及酪蛋白激酶1α形成β-catenin降解复合体,降解胞质中的β-catenin。当GSK-3β蛋白失活时,胞质内β-catenin逐渐累积,继而增加β-catenin的核转位,当细胞核内β-catenin增加时,通过转录增加了控制成骨细胞分化的主要转录因子Runx2的转录性增加分化。Arioka等[19]通过在体外实验研究GSK-3β两种抑制剂LiCl和SB216763对间充质祖细胞C3H10T1/2细胞的成骨发育和破骨细胞前体RAW-D细胞破骨发育的影响发现,GSK-3β抑制剂促进了成骨细胞分化,激活了Wnt/β-catenin信号通路,进而诱导Runx2表达增高,同时抑制破骨细胞的破骨分化。Loiselle等[20]也发现在GSK-3缺失的小鼠体内β-catenin和Runx2表达水平升高,而与野生型小鼠相比,损伤后GSK-3缺失的小鼠骨再生率更高;而口服GSK-3β的选择性抑制剂也能够增加骨量、促进骨折愈合及骨痂形成;GSK-3β基因敲除的杂合子小鼠的成骨能力也明显增强。与之结果类似,ETHERIDGE等[21]研究发现,通过抑制GSK-3β可以激活Wnt/β-catenin信号通路,进而促进间充质干细胞的增殖并抑制其分化为成骨细胞,并最终减少磷酸酶的表达,降低碱性磷酸酶的活性。综上所述,GSK-3β是Wnt/β-catenin通路中重要的负性调控因子,其与轴蛋白、腺瘤病大肠杆菌等形成的降解复合体可负性调控胞质内游离β-catenin的浓度,进而影响影响下游基因转录过程,是调节β-catenin蛋白表达的关键性靶点。 2.2.3 β-catenin在信号通路中的作用及对成骨细胞的影响 β-catenin是由CTNNBI基因表达的产物,大小约88 kD,它是Wnt/β-catenin信号通路中的关键因子,广泛分布于细胞中,以细胞质内含量最多。β-catenin与细胞核内T细胞转录因 子/淋巴增强因子形成复合物,调控Wnt/β-catenin通路靶基因转录。HANG等[22]研究发现,当抑制Wnt/β-catenin通路后,胞质内β-catenin浓度增加并进入细胞核内与T细胞转录因 子/淋巴增强因子形成复合体,通过与DNA结合,进而诱导c-myc、cyclinD和Runx2等靶基因的转录,使成骨细胞的细胞周期由G1期进入S期,而成骨细胞的分化增殖也得到增强。β-catenin主要通过Wnt/β-catenin通路促进成骨细胞成熟,而其功能的缺失将会直接影响成骨细胞的增殖、分化与成熟。GLASS等[23]通过在成骨细胞发育晚期持续激活β-catenin,使其在成骨细胞中过表达,发现它的细胞活性和形态学未见明显变化,而破骨细胞生成及骨吸收则由于骨保护素生成减少而出现异常。Holmen等[24]最早成功通过敲除小鼠成骨细胞内的β-catenin的上游基因,发现由于成骨细胞减少和破骨细胞明显增加导致小鼠体内骨量明显减少,从而奠定β-catenin在信号通路中关键因子的重要地位。而将β-catenin敲除以后的Col2a1-ICAT转基因鼠体内发现,软骨细胞在关节软骨中的表达降低,软骨细胞的增殖和分化也受到抑制,并促进了软骨细胞的凋亡。进而使次级骨化中心形成减慢,并最终影响成骨。KRISHNAN等[25]也通过对β-catenin敲除实验发现,β-catenin在成骨早期,可以诱导间充质前体细胞向软骨细胞分化。KRAMER等[26]在成骨细胞特异性敲除β-catenin的转基因小鼠体内发现由于破骨细胞破骨功能增强及核因子κB受体活化因子配体的受体激活剂/骨保护素G比值的改变,导致小鼠骨髓腔变大,骨皮质变薄,但是成骨细胞数量却无明显变化。这说明β-catenin在成骨细胞中可能主要影响其分化、成骨,而在破骨细胞中主要调节其细胞活性及功能。 2.2.4 Wnt/β-catenin信号通路其他信号因子对成骨细胞的影响 通过对人类全基因组研究后,大量的骨质疏松相关易感性位点已被确定具有降低骨密度的能力。而部分位点基因编码的蛋白,例如Wnt配体Wnt4、Wnt16等、胞膜辅助受体Lrp5等、胞内成分轴蛋白1、Ctnnb1和 Gpr177等以及拮抗剂sclerostin(Sost)等,目前均已被证明与Wnt/β-catenin信号通路密切相关。 在Wnt4突变的小鼠体内软骨细胞的分化及成熟轻度受抑制,但对于成骨细胞形成及骨重建的影响尚未见文献报道。Wnt16具有很强的抗骨吸收活性,对成骨细胞和破骨细胞均有作用。在大鼠胶原Ⅰ型α1启动子的控制下,成骨细胞特异性Wnt16过表达会导致骨小梁中骨形成比皮质骨中更明显[27]。这可能是由于内源性Wnt16在骨小梁中适度表达,而在皮质骨中则是高表达。文献中有证据表明Wnt16除了可以通过Wnt/β-catenin通路表达,还可以通过不参与Ror2的Wnt/JNK通路,而后者可能与Wnt/β-catenin有关拮抗Wnt16作用有关。在许多研究中,Wnt配体在成骨细胞中的表达已经被证实对其相对表达水平进行了分析,但得出的不同的结果与Wnt配体在不同部位的表达差异有关[28]。在这些研究中结果相对一致的是Wnt5a配体,有意思的是,Wnt5a表达于成骨细胞,而其受体Ror2则表达于破骨细胞,因此Wnt5a/Ror2通路主要影响破骨细胞形成。另外,Wnt5a活性也会影响成骨细胞形成并增加脂肪形成,其对成骨细胞的影响以独立于Ro2的方式发生。OKAMOTO等[29]通过研究发现成骨细胞中的Wnt5a通过维持辅助受体Lrp5/6的表达水平来支持Wnt/β-catenin信号通路。以上结果也支持SONG等[30]的发现,Wnt/β-catenin信号通路缺失将导致成骨前体细胞向成脂细胞方向分化。Wnt3a基因的多态性与骨密度变化有关。Wnt3a杂合子小鼠的骨量会出现降低,而在体外实验中,Wnt3a具有刺激成骨细胞生成的作用。目前存在两种可能机制:其一是Wnt3a通过G蛋白亚组的Gαq/11发出信号并最终激活小鼠骨髓来源ST2细胞系中的Pkcδ;而另一种机制需要转录因子Lef1与转录共激活因子Taz的相互作用才能诱导[31]。杂合Lef1缺陷的小鼠表现出与性别和年龄依赖性的骨量减少,而骨量减少与成骨细胞活性降低有关。PARK等[32]也发现Yap/Taz也与成骨细胞中Wnt4的下游表达有关,Wnt4刺激Yap/Taz在细胞核内的积累,而Yap/Taz损耗则会影响成骨细胞Wnt4的活性。Wnt3a在成骨细胞不同的形成阶段具备不同的活性,在成骨来源细胞阶段具备抗成骨细胞系分化作用,而在成熟的成骨细胞和破骨细胞中则促进骨形成、抑制骨吸收[33],当然还有其他Wnt配体涉及成骨细胞分化及成骨,例如Wnt7b 和Wnt10b。Wnt7b过表达可以导致成骨细胞数量的增加,继而导致骨量明显增加;在体外实验中,经Wnt10b处理后成骨细胞的生成是增加的,在骨钙素控制下成骨细胞特异性Wnt10b过表达也导致小梁骨增加却不影响破骨细胞的形成;与之相反,存在wnt10b缺陷的小鼠则表现为骨小梁体积随着年龄的增长而有所减少,其原因是由于骨祖细胞随着年龄的增长而减少。 与Lrg受体结合的R-spondin蛋白家族成员被认为可以增强Wnt/β-catenin信号通路的效果。R-spondins具有骨代谢的调控作用,其中R-spondin1促进了成骨细胞分化以及骨形成,同时也抑制了破骨细胞形成。而ZHU等[34]也在体外研究中发现,R-spondin2可以通过激活MC3T3-E1细胞的Wnt/β-catenin信号通路来促进成骨,当R-spondin2关键受体LGR4功能被抑制的细胞中,R-spondin2的促成骨作用也被抑制。同时在卵巢切除小鼠体内实验中发现,R-spondin2通过与关键受体LGR4结合后促进Wnt/β-catenin信号进而促进成骨细胞形成,改善卵巢切除小鼠骨丢失情况及骨微结构。 综上所述,Wnt/β-catenin信号通路及其通路中多种信号因子对早期成骨的各个方面具有至关重要的作用,甚至包括关节发育过程中的机械感应。但是目前关于Wnt配体激活该通路的机制、包括Wnt/β-catenin信号通路在细胞外和细胞内水平调控等具体机制仍有待研究发现。 2.3 磨损颗粒诱导下Wnt/β-catenin信号通路对成骨细胞的影响 尽管目前关于Wnt/β-catenin信号通路对成骨细胞的分化、成骨、细胞代谢以及基因水平的影响,大量的研究已经深入浅出地阐明了其中可能的机制,但是对于TJA术后,在假体周围磨损颗粒积聚的影响下,Wnt/β-catenin信号通路是如何通过对成骨细胞产生影响并最终导致假体周围骨溶解、无菌性松动的具体机制目前尚不完全清楚。近年来,随着越来越多的关于磨损颗粒诱导的假体周围骨溶解条件下成骨细胞的研究进展,已经逐步揭示了部分可能机制。 LEE等[35]通过对MC3T3-E1细胞体外研究发现,钛颗粒与巨噬细胞相互作用后可以抑制骨前体细胞分化相关标志物的产生,包括抑制碱性磷酸酶活性,胶原的合成、基质矿化和骨钙素、Runx2的表达,而巨噬细胞分泌的肿瘤坏死因子α除了抑制成骨活动还能抑制Wnt/β-catenin和骨形态发生蛋白2信号通路活性。而钛或肿瘤坏死因子α诱导的骨硬化蛋白表达则是抑制Wnt/β-catenin和骨形态发生蛋白2信号通路活性的原因。另外骨硬化蛋白的过表达也可以抑制碱性磷酸酶的活性。同年LIU等[36]首次阐明骨重建在预防磨损颗粒诱导的假体无菌性松动中的重要意义,在他的研究中,通过在大鼠体内应用骨硬化蛋白抗体可以拮抗聚乙烯颗粒毒副作用,并且抑制骨硬化蛋白对Wnt/β-catenin信号通路的下调作用,进而增加成骨形成、减轻骨吸收。作者研究团队GENG等[16]、GU等[17]分别在2015及2017年通过体内和体外研究发现,钛磨损颗粒影响下的MC3T3-E1细胞表现出GSK-3β表达的上调以及β-catenin表达的抑制,导致成骨细胞生成功能的受损。另外该研究也发现,即使存在钛磨损颗粒影响,氯化锂(GSK-3β抑制剂)仍能促进β-catenin核转位并上调的β-catenin信号活性。研究显示钛磨损颗粒通过与成骨细胞及破骨细胞相互作用,降低了核因子κB受体活化因子配体的受体激活剂/骨保护素G比值及诱导了成骨细胞分化。而在体外实验中,通过ICG-001抑制剂阻断了β-catenin信号通路从而减弱了氯化锂对成骨细胞分化的保护作用,并首次提出GSK-3β/β-catenin信号通路可能是介导钛磨损颗粒诱导的假体周围骨溶解的重要机制。AMIRHOSSEINI等[15]通过研究也发现在大鼠机械性骨溶解模型中使用GSK-3β的抑制剂AR28抑制了GSK-3β活性后,通过Wnt/β-catenin和骨形态发生蛋白2信号通路的调节,可以加速骨修复,上调成骨细胞的分化,减弱破骨细胞的形成,进而抑制假体周围骨溶解。GENG等[37]通过对野生型C57BL/6j小鼠以及骨硬化蛋白敲除的C57BL/6j小鼠体外研究发现,雷尼酸锶能增加小鼠体内骨钙蛋白、Runx2、β-catenin以及骨保护蛋白的表达,降低核因子κB受体活化因子配体的受体激活剂的表达以及核因子κB受体活化因子配体的受体激活剂/骨保护素G的比值。而这些表现在骨硬化蛋白敲除的C57BL/6j小鼠体内并未发现,在野生型小鼠磨损微粒介导的骨溶解模型中雷尼酸锶能增强成骨形成并抑制破骨吸收,而这一作用主要依赖于通过下调骨硬化蛋白水平改善对典型Wnt通路的抑制作用来实现。QU等[38]通过对钛颗粒诱导下的MC3T3- E1细胞的假体周围骨溶解模型进行研究,发现钛颗粒能明显抑制生长激素释放多肽在MC3T3- E1细胞内的表达,而且生长激素释放多肽减轻了钛颗粒诱导的成骨生成损伤以及骨溶解;另外,生长激素释放多肽的保护作用可能与Wnt/β-catenin信号通路有关。同年作者所在研究团队ZHANG等[39]通过钛颗粒对C57BL/6小鼠诱导假体周围骨溶解的动物模型研究发现,钛颗粒处理后颅骨表面出现骨溶解伴骨硬化蛋白表达增加。同样在体外实验经钛颗粒处理后的MLO-Y4骨细胞中骨硬化蛋白表达增加,并且在小鼠体内骨硬化蛋白降低后,局部骨密度和骨体积都增大;组织学分析骨硬化蛋白降低后导致碱性磷酸酶显著增加以及颅骨表面转录因子阳性表达,并最终促进骨形成。在体外实验中,在骨硬化蛋白表达静默条件下,即使用钛粒子处理下MC3T3-E1细胞的活性以及矿化也明显增强;相反,减少的骨硬化蛋白的表达水平反而增加了β-catenin的表达水平。结果提示骨硬化蛋白基因表达的降低可激活Wnt/β-catenin信号通路促进骨形成,改善钛颗粒引起的骨丢失。根据作者所在研究团队最新研究表明,通过钛颗粒诱导C57BL/6小鼠发生假体周围骨溶解模型中发现,蛋白磷酸酶2A被选择性抑制后,可以通过加速成骨细胞生成和促进骨再生来改善钛颗诱导的骨破坏;另外还发现蛋白磷酸酶2A抑制后可以缓解钛颗粒对MC3T3-E1细胞中成骨分化的抑制作用,而且蛋白磷酸酶2A抑制后β-catenin表达增加并加强了β-catenin核转位;当进一步应用β-catenin的特异性抑制剂ICG-001后发现其作用减弱了蛋白磷酸酶2A抑制对β-catenin表达和核转位的影响[40],说明蛋白磷酸酶2A抑制对成骨分化产生的保护作用主要是通过激活Wnt/β-catenin信号通路来实现的。 综上所述,通过目前的研究发现磨损颗粒诱导下Wnt/β-catenin信号通路对成骨细胞功能的影响主要有以下几点:①在体外实验中,磨损颗粒诱导假体周围骨溶解、无菌性松动的病理过程中,Wnt/β-catenin信号通路激活后通过抑制成骨形成、增加破骨吸收进而影响骨重建,在磨损颗粒诱导假体周围骨溶解、无菌性松动的病理过程中起到了关键性作用。②在体外实验中,通过应用GSK-3β抑制剂氯化锂、生长激素释放多肽以及蛋白磷酸酶2A抑制可以激活Wnt/β-catenin等信号通路,促进成骨细胞分化及成骨活动;而ICG-001抑制剂阻断了β-catenin信号通路从而减弱了氯化锂对成骨细胞分化的保护作用,提示GSK-3β/β-catenin信号通路可能是介导钛磨损颗粒诱导假体周围骨溶解的重要机制。③在体内实验中,通过应用骨硬化蛋白抗体、蛋白磷酸酶2A抑制、氯化锂、AR28等方式激活Wnt/β-catenin等信号通路后,进而促进成骨形成,抑制破骨吸收,增加局部骨量及骨体积,对抗钛等磨损颗粒诱导的假体周围骨溶解作用。④基因层面,在骨硬化蛋白基因静默条件下,即使用钛粒子处理下MC3T3-E1细胞的活性以及矿化也明显增强;相反,减少的骨硬化蛋白的表达水平反而增加了β-catenin的表达水平;结果提示骨硬化蛋白基因表达的降低可激活Wnt/β-catenin信号通路促进骨形成,改善钛颗粒引起的骨丢失。 "

| [1] CAMUZARD O, BREUIL V, CARLE GF, et al. Autophagy Involvement in Aseptic Loosening of Arthroplasty Components. J Bone Joint Surg Am. 2019;101(5):466-472. [2] LIMMER A, WIRTZ DC. Osteoimmunology: Influence of the Immune System on Bone Regeneration and Consumption. Z Orthop Unfall. 2017;155(3):273-280. [3] YANG H, XU Y, ZHU M, et al. Inhibition of titanium-particle-induced inflammatory osteolysis after local administration of dopamine and suppression of osteoclastogenesis via D2-like receptor signaling pathway. Biomaterials. 2016;80:1-10. [4] BAI F, CHEN X, YANG H, et al. Acetyl-11-Keto-β-Boswellic Acid Promotes Osteoblast Differentiation by Inhibiting Tumor Necrosis Factor-α and Nuclear Factor-κB Activity. J Craniofac Surg. 2018;29(7):1996-2002. [5] GALLO J, GOODMAN SB, KONTTINEN YT, et al. Osteolysis around total knee arthroplasty: a review of pathogenetic mechanisms. Acta Biomater. 2013;9(9): 8046-8058. [6] GENG DC, XU YZ, YANG HL, et al. Inhibition of titanium particle-induced inflammatory osteolysis through inactivation of cannabinoid receptor 2 by AM630. J Biomed Mater Res A. 2010;95(1): 321-326. [7] GALLO J, GOODMAN SB, KONTTINEN YT, et al. Particle disease: biologic mechanisms of periprosthetic osteolysis in total hip arthroplasty. Innate Immun. 2013;19(2):213-224. [8] BURTON L, PAGET D, BINDER NB, et al. Orthopedic wear debris mediated inflammatory osteolysis is mediated in part by NALP3 inflammasome activation. J Orthop Res. 2013;31(1):73-80. [9] NAM JS, SHARMA AR, JAGGA S, et al. Suppression of osteogenic activity by regulation of WNT and BMP signaling during titanium particle induced osteolysis. J Biomed Mater Res A. 2017;105(3):912-926. [10] CHIU R, SMITH KE, MA GK, et al. Polymethylmethacrylate particles impair osteoprogenitor viability and expression of osteogenic transcription factors Runx2, osterix, and Dlx5. J Orthop Res. 2010;28(5):571-577. [11] FRITZ EA, JACOBS JJ, GLANT TT, et al. Chemokine IL-8 induction by particulate wear debris in osteoblasts is mediated by NF-kappaB. J Orthop Res. 2005;23(6):1249-1257. [12] CHEN D, LI Y, GUO F, et al. Protective effect of p38 MAPK inhibitor on wear debris-induced inflammatory osteolysis through downregulating RANK/RANKL in a mouse model. Genet Mol Res. 2015;14(1):40-52. [13] KIM JA, IHN HJ, PARK JY, et al. Inhibitory effects of triptolide on titanium particle-induced osteolysis and receptor activator of nuclear factor-κB ligand-mediated osteoclast differentiation. Int Orthop. 2015;39(1):173-182. [14] CÓRDOVA LA, TRICHET V, ESCRIOU V, et al. Inhibition of osteolysis and increase of bone formation after local administration of siRNA-targeting RANK in a polyethylene particle-induced osteolysis model. Acta Biomater. 2015;13:150-158. [15] AMIRHOSSEINI M, MADSEN RV, ESCOTT KJ, et al. GSK-3β inhibition suppresses instability-induced osteolysis by a dual action on osteoblast and osteoclast differentiation. J Cell Physiol. 2018;233(3):2398-2408. [16] GENG D, WU J, SHAO H, et al. Pharmaceutical inhibition of glycogen synthetase kinase 3 beta suppresses wear debris-induced osteolysis. Biomaterials. 2015;69:12-21. [17] GU Y, WANG Z, SHI J, et al. Titanium particle-induced osteogenic inhibition and bone destruction are mediated by the GSK-3β/β-catenin signal pathway. Cell Death Dis. 2017;8(6):e2878. [18] XIONG L, LIU Y, ZHU F, et al. Acetyl-11-keto-β-boswellic acid attenuates titanium particle-induced osteogenic inhibition via activation of the GSK-3β/β-catenin signaling pathway. Theranostics. 2019;9(24):7140-7155. [19] ARIOKA M, TAKAHASHI-YANAGA F, SASAKI M, et al. Acceleration of bone regeneration by local application of lithium: Wnt signal-mediated osteoblastogenesis and Wnt signal-independent suppression of osteoclastogenesis (vol 90, pg 397, 2014). Biochem Pharmacol. 2014;91(4):552-553. [20] LOISELLE AE, LLOYD SA, PAUL EM, et al. Inhibition of GSK-3β rescues the impairments in bone formation and mechanical properties associated with fracture healing in osteoblast selective connexin 43 deficient mice. PLoS One. 2013;8(11):e81399. [21] ETHERIDGE SL, SPENCER GJ, HEATH DJ, et al. Expression profiling and functional analysis of wnt signaling mechanisms in mesenchymal stem cells. Stem Cells. 2004;22(5):849-860. [22] HANG K, YE C, XU J, et al. Apelin enhances the osteogenic differentiation of human bone marrow mesenchymal stem cells partly through Wnt/β-catenin signaling pathway. Stem Cell Res Ther. 2019;10(1):189. [23] GLASS DA 2ND, BIALEK P, AHN JD, et al. Canonical Wnt signaling in differentiated osteoblasts controls osteoclast differentiation. Dev Cell. 2005;8(5):751-764. [24] HOLMEN SL, ZYLSTRA CR, MUKHERJEE A, et al. Essential role of beta-catenin in postnatal bone acquisition. J Biol Chem, 2005;280(22):21162-21168. [25] KRISHNAN V, BRYANT HU, MACDOUGALD OA. Regulation of bone mass by Wnt signaling. J Clin Invest. 2006;116(5):1202-1209. [26] KRAMER I, HALLEUX C, KELLER H, et al. Osteocyte Wnt/beta-catenin signaling is required for normal bone homeostasis. Mol Cell Biol. 2010;30(12):3071-3085. [27] ALAM I, ALKHOULI M, GERARD-O’RILEY RL, et al. Osteoblast-Specific Overexpression of Human WNT16 Increases Both Cortical and Trabecular Bone Mass and Structure in Mice. Endocrinology. 2016;157(2):722-736. [28] MARTINEAU X, ABED É, MARTEL-PELLETIER J, et al. Alteration of Wnt5a expression and of the non-canonical Wnt/PCP and Wnt/PKC-Ca2+ pathways in human osteoarthritis osteoblasts. PLoS One. 2017;12(8):e0180711. [29] OKAMOTO M, UDAGAWA N, UEHARA S, et al. Noncanonical Wnt5a enhances Wnt/β-catenin signaling during osteoblastogenesis. Sci Rep. 2014;4:4493. [30] SONG L, LIU M, ONO N, et al. Loss of wnt/β-catenin signaling causes cell fate shift of preosteoblasts from osteoblasts to adipocytes. J Bone Miner Res. 2012;27(11): 2344-2358. [31] KIDA J, HATA K, NAKAMURA E, et al. Interaction of LEF1 with TAZ is necessary for the osteoblastogenic activity of Wnt3a. Sci Rep. 2018;8(1):10375. [32] PARK HW, KIM YC, YU B, et al. Alternative Wnt Signaling Activates YAP/TAZ. Cell. 2015;162(4): 780-794. [33] XIONG J, ALMEIDA M, O’BRIEN CA. The YAP/TAZ transcriptional co-activators have opposing effects at different stages of osteoblast differentiation. Bone. 2018;112:1-9. [34] ZHU C, ZHENG XF, YANG YH, et al. LGR4 acts as a key receptor for R-spondin 2 to promote osteogenesis through Wnt signaling pathway. Cell Signal. 2016;28(8): 989-1000. [35] LEE SS, SHARMA AR, CHOI BS, et al. The effect of TNFα secreted from macrophages activated by titanium particles on osteogenic activity regulated by WNT/BMP signaling in osteoprogenitor cells. Biomaterials. 2012;33(17):4251-4263. [36] LIU S, VIRDI AS, SENA K, et al. Sclerostin antibody prevents particle-induced implant loosening by stimulating bone formation and inhibiting bone resorption in a rat model. Arthritis Rheum. 2012;64(12):4012-4020. [37] GENG T, SUN S, YU H, et al. Strontium ranelate inhibits wear particle-induced aseptic loosening in mice. Braz J Med Biol Res. 2018;51(9):e7414. [38] QU R, CHEN X, YUAN Y, et al. Ghrelin Fights Against Titanium Particle-Induced Inflammatory Osteolysis Through Activation of β-Catenin Signaling Pathway. Inflammation. 2019;42(5):1652-1665. [39] ZHANG ZH, JIA XY, FANG JY, et al. Reduction of SOST gene promotes bone formation through the Wnt/β-catenin signalling pathway and compensates particle-induced osteolysis. J Cell Mol Med. 2020;24(7): 4233-4244. [40] WANG L, BAI J, WANG Q, et al. Inhibition of protein phosphatase 2A attenuates titanium-particle induced suppression of bone formation. Int J Biol Macromol. 2020;142:142-151. [41] NILSSON A, NORGARD M, ANDERSSON G, et al. Fluid pressure induces osteoclast differentiation comparably to titanium particles but through a molecular pathway only partly involving TNFalpha. J Cell Biochem. 2012;113(4):1224-1234. [42] FAHLGREN A, BOSTROM MPG, YANG X, et al. Fluid pressure and flow as a cause of bone resorption. Acta Orthop. 2010;81(4):508-516. [43] AMIRHOSSEINI M, ANDERSSON G, ASPENBERG P, et al. Mechanical instability and titanium particles induce similar transcriptomic changes in a rat model for periprosthetic osteolysis and aseptic loosening. Bone Rep. 2017;7:17-25. [44] TANG YH, YUE ZS, LI GS, et al. Effect of β‑ecdysterone on glucocorticoid‑induced apoptosis and autophagy in osteoblasts. Mol Med Rep. 2018;17(1):158-164. [45] KANG C, WEI L, SONG B, et al. Involvement of autophagy in tantalum nanoparticle-induced osteoblast proliferation. Int. J. Nanomed. 2017;12:4323. [46] KIM IR, KIM SE, BAEK HS, et al. The role of kaempferol-induced autophagy on difffferentiation and mineralization of osteoblastic MC3T3-E1 cells. BMC Complement Altern. 2016;16:333. [47] WANG Z, LIU N, LIU K, et al. Autophagy mediated CoCrMo particle-induced peri-implant osteolysis by promoting osteoblast apoptosis. Autophagy. 2015;11(12): 2358-2369. [48] ZHANG X, YIN H, LI Z, et al. Nano-TiO 2 induces autophagy to protect against cell death through antioxidative mechanism in podocytes. Cell Biol. Toxicol. 2016;32: 513-527. [49] YANG L, MENG H, YANG M. Autophagy protects osteoblasts from advanced glycation end products-induced apoptosis through intracellular reactive oxygen species. J Mol Endocrinol. 2016;56:291-300. [50] ZHANG DY, WANG HJ, TAN YZ. Wnt/β-catenin signaling induces the aging of mesenchymal stem cells through the DNA damage response and the p53/p21 pathway. PLoS One. 2011;6(6):e21397. [51] XIA W, ZHUANG L, DENG X, et al. Long noncoding RNA-p21 modulates cellular senescence via the Wnt/β-catenin signaling pathway in mesenchymal stem cells. Mol Med Rep. 2017;16(5):7039-7047. [52] CHEN J, JIA YS, LIU GZ, et al. Role of LncRNA TUG1 in intervertebral disc degeneration and nucleus pulposus cells via regulating Wnt/β-catenin signaling pathway. Biochem Biophys Res Commun. 2017;491(3):668-674. [53] LAI XH, LEI Y, YANG J, et al. Effect of microRNA-34a/SIRT1/p53 signal pathway on notoginsenoside R1 delaying vascular endothelial cell senescence. Zhongguo Zhong Yao Za Zhi. 2018;43(3):577-584. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [3] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [4] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [5] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [6] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [7] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [8] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [9] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [10] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [11] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [12] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [13] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [14] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| [15] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||