1.1 设计 体外细胞学实验与动物实验,多组间比较采用方差分析,两两组间比较采用独立LSD-t检验。
1.2 时间及地点 实验于2021年2月至2022年3月在广东省第二中医院完成。
1.3 材料
1.3.1 实验动物 75只雄性SD大鼠,SPF级,8-10周龄,体质量(225±25) g,购自广东至远生物医药科技有限公司,动物的生产许可证号:SCXK(粤)2021-0057。经有专门技术人员检测所有大鼠生长良好,均无关节或骨骼疾病,并经适应性喂养后用于实验。喂养条件:12 h明/暗交替,相对湿度(50±5)%,温度(23±2) ℃,标准饲料,自由饮水与摄食,1周后进行后续实验。
实验动物的使用均符合广东省第二中医院基础动物实验伦理委员会的要求(2021-02-25-BNYM003)。
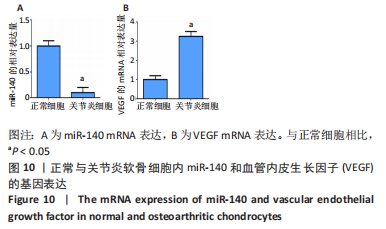
1.3.2 实验细胞 软骨细胞株ATDC5、人脐静脉血管内皮细胞株购自由吉妮欧生物科技有限公司(广州)。
1.3.3 主要试剂 温阳通络胶囊为广东省第二中医院院内制剂,由附子、桂枝、仙茅、全蝎、蜈蚣、熟地黄、蕲蛇等组成,规格0.42 g×36粒,批注文号:粤YZB-2002-012。
miR-140抑制剂(miR-140-antagomir)和miR-140抑制剂阴性对照(miR-140 antagomir-NC),miR-140-control、miR-140-mimics、RNA干扰技术沉默VEGF(siRNA-VEGF)和RNA干扰技术沉默VEGF的阴性对照(siRNA-VEGF NC)均购自苏州吉玛基因股份有限公司。
兔抗大鼠VEGF(批号:R0987)、血小板内皮细胞黏附分子(批号:T3481,CD31)、GAPDH(批号:W3568)抗体(美国Santa Cruz公司);苏木精-伊红染色(批号:CF00437)试剂盒、免疫组化(批号:CF22641)、MTT试剂盒(批号:CF45238)、蛋白质免疫印迹试剂盒(批号:CF53480)(北京中杉金桥有限公司);Ⅱ型胶原酶(批号:XD08053)、木瓜蛋白酶(批号:XD612573)、胰酶(批号:XD51723)、细胞培养基(批号:XD87346)、PBS(批号:XD26947)(上海碧云天生物技术有限公司);甲苯胺蓝染色试剂盒(批号:BR00054)、组织裂解液(批号:BR86439)、蛋白定量试剂盒(批号:BR57261)(北京天根生物科技有限公司);双荧光素酶试剂盒(批号:SK-54783,美国Promega公司);白细胞介素1β(批号:DHJ-0078)和肿瘤坏死因子α(批号:DHJ-3751)酶联免疫吸附测定实验检测试剂盒(批号:DHJ-2428)(南京建成生物技术有限公司);反转录试剂盒(批号:WF00-1A)、RNA提取试剂盒(批号:WF04-6Y)、PCR Mix试剂盒(批号:WF08-2B)(大连宝生物工程有限公司)。
1.3.4 主要仪器 低温石蜡切片机(德国莱卡公司);光学显微镜(日本Olympus公司);凝胶成像系统、电泳槽(美国Bio-Rad公司);超净工作动台(江苏荣华仪器制造有限公司)。
1.4 实验方法
1.4.1 动物实验
(1)试剂准备:分别准确量取0.5 μg的miR-140-antagomir、miR-140-antagomir-NC、siRNA-VEGF和siRNA-VEGF NC,加入5 μL的5%葡萄糖溶液配置成混合溶液,混匀,孵育后在摇晃以确保混合溶液均匀,备用[10];以10倍体积的生理盐水将温阳通络胶囊配置成温阳通络胶囊溶液,常温保存,待用。
(2)实验动物分组及处理[11]:将75只SD大鼠分为5组,分别为正常组、模型组、药物组、抑制剂组及干扰组,每组15只。
正常组:每天左后肢膝关节内注射miR-140-antagomir NC和siRNA-VEGF NC各10 nmol/L,连续注射2周,2周后随机选取3只大鼠处死,收集膝关节软骨,采用PCR检测大鼠膝关节软骨中miR-140和VEGF mRNA的表达情况。2周后灌胃给予2 mg/kg的生理盐水。
模型组:实验的1,4,7 d关节腔内注射木瓜蛋白酶复制关节炎模型;每天左后肢膝关节内注射miR-140-antagomir NC和siRNA-VEGF NC各10 nmol/L,连续注射2周,2周后随机选取3只大鼠处死,收集膝关节软骨,采用PCR检测大鼠膝关节软骨中miR-140和VEGF mRNA的表达情况。2周后灌胃给予2 mg/kg的生理盐水,连续给药4周。
药物组:实验的1,4,7 d关节腔内注射木瓜蛋白酶复制关节炎模型。每天左后肢膝关节内注射miR-140-antagomir NC和siRNA-VEGF NC各10 nmol/L,连续注射2周,2周后随机选取3只大鼠处死,收集膝关节软骨,采用PCR检测大鼠膝关节软骨中miR-140和VEGF mRNA的表达情况。2周后灌胃给予温阳通络胶囊溶液2 mg/(kg·d)[12],连续给药4周。
抑制剂组:实验的1,4,7 d关节腔内注射木瓜蛋白酶复制关节炎模型。每天左后肢关节内注射miR-140-antagomir和siRNA-VEGF NC各10 nmol/L,连续注射2周,2周后随机选取3只大鼠处死,收集膝关节软骨,采用PCR检测大鼠膝关节软骨中miR-140和VEGF mRNA的表达情况。2周后灌胃给予温阳通络胶囊溶液2 mg/(kg·d),连续给药4周。
干扰组:实验的1,4,7 d关节腔内注射木瓜蛋白酶复制关节炎模型。每天关节内注射miR-140-antagomir和siRNA-VEGF各10 nmol/L,连续注射2周,2周后随机选取3只大鼠处死,收集膝关节软骨,采用PCR检测大鼠膝关节软骨中miR-140和VEGF mRNA的表达情况。2周后灌胃给予温阳通络胶囊溶液2 mg/(kg·d),连续给药4周。
关节炎造模方法:将大鼠适应性喂养1周后,参照TOWNSEND等[13]介绍的方法复制骨关节炎模型。大鼠禁食12 h后,腹腔注射35 mg/kg的0.35%戊巴比妥钠动物麻醉,保持大鼠侧卧并伸展其左后肢,备皮,消毒,将100 μL的4%木瓜蛋白酶从髌骨下极髌腱外缘处注入左膝关节腔,注射频率:实验开始后第1,4,7 天,共注射3次。当与正常组大鼠相比,模型大鼠出现关节肿胀、跛行、身体灵活度明显下降等行为时视为造模成功[14]。

(3)观察指标
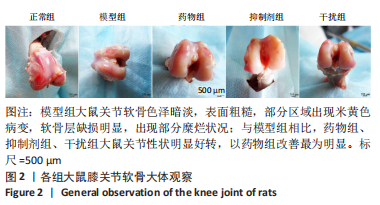
软骨大体观察:给药结束后,抽取大鼠腹主动脉血5 mL,麻醉后处死大鼠,在无菌操作台上进行解剖,暴露其病灶膝关节软骨,观察各组大鼠关节软骨外部情况,记录各组的关节软骨糜烂、溃疡及增生情况。
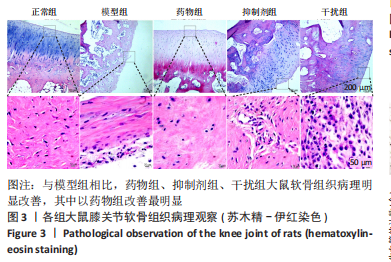
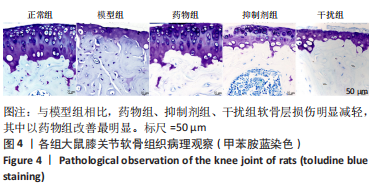
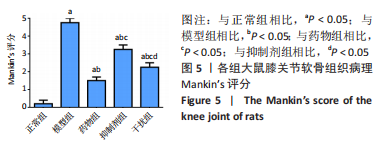
软骨组织病理观察:取大鼠膝关节,经乙二胺四乙酸钠脱钙、梯度乙醇脱水、二甲苯透明、浸蜡、包埋后,以石蜡切片机制成4-6 μm的切片,依次进行苏木精-伊红染色、甲苯胺蓝染色,上镜检测。采用Mankin′s评分评价各组大鼠软骨的病变状况[15]:软骨细胞排列整齐,数量丰富,基质未见异常,潮线完整,记为0分;软骨表面出现不规则裂隙,细胞呈现弥漫性增多,基质染色变浅,视野中出现多重潮线,记为1分;裂隙至肌层,细胞呈现簇状生长,基质染色更为减退,软骨下血管增生至肌层,记为2分;裂隙浸入辐射层,软骨细胞数量锐减,基质染色趋于消失,记为3分;裂隙已经浸至钙化层,基质染色近乎消失,记为4分;软骨层明显脱落,记为5分。Mankin′s评分越高说明软骨损伤越严重。
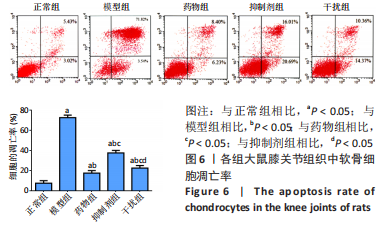
软骨组织细胞凋亡:取大鼠膝关节组织,40 g/L多聚甲醛中固定72 h,置于10%乙二胺四乙酸中脱钙6 周,胰酶消化,收集细胞悬液,离心后弃上清,PBS冲洗,膜联蛋白V和碘化丙啶双重染色[16],上流式细胞仪检测。
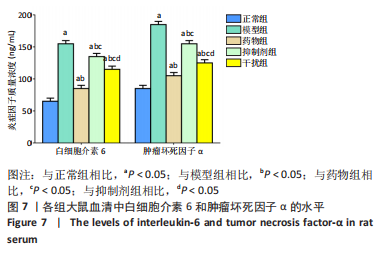
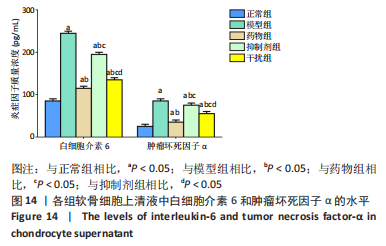
ELISA法检测炎性因子水平:取大鼠血液样本,室温下3 000 r/min离心30 min,按ELISA操作要求检测炎性因子白细胞介素6和肿瘤坏死因子α水平。
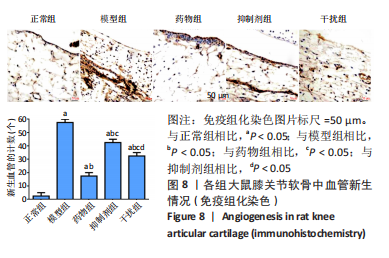
免疫组化染色:取大鼠膝关节组织,常规固定,经包埋、切片后,按免疫组化试剂盒要求进行实验操作,加入一抗CD31(1∶500),二抗(1∶1 500)显微镜下观察血管新生的情况,Image J图像处理软件统计分析新生血管(MVD)的数量[17]。
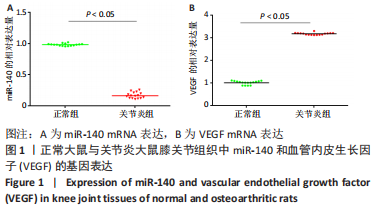
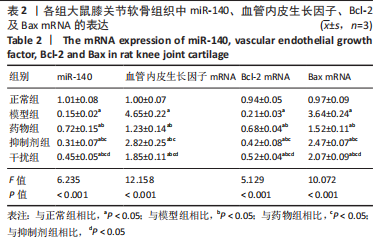
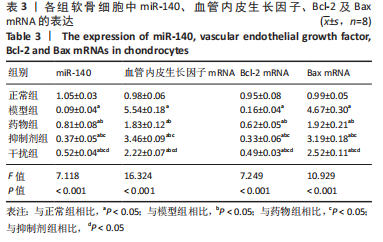
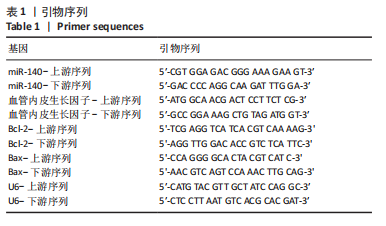
qRT-PCR检测:取大鼠膝关节组织,常规提取标本中的总RNA,NanoDrop ND-1000分光光度计检测总RNA的纯度和浓度后,利用TaqMan Small RNA Assays试剂盒反转录合成cDNA,以PCR仪进行扩增,反应条件:预变性,10 min 95 ℃;变性,10 s 95℃(40个循环);退火,20 s 60 ℃;延伸,15 s 72 ℃。以U6作为参照基因,检测miR-140、血管内皮生长因子、Bcl-2及Bax的基因表达,目的基因的表达以2-ΔΔCt进行表示[18-19]。引物序列见表1。
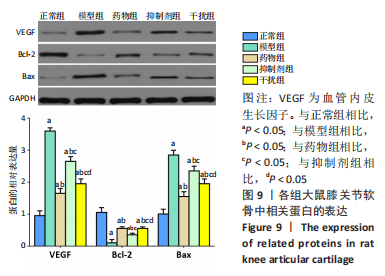
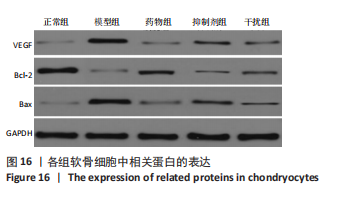
Western blot检测:检测膝关节组织VEGF、Bcl-2、Bax蛋白的表达。取大鼠膝关节组织,经RIPA蛋白裂解液裂解后,提取样本中总蛋白,Bradford试剂盒测定浓度,进行电泳分离,转膜,清洗,封闭,孵育,加入一抗VEGF、Bcl-2、Bax(1∶500),孵育过夜,加入HRP标记的IgG二抗(1∶1 000),显色[20],以GAPDH作为内参统计分析各条带的灰度值。
1.4.2 细胞实验
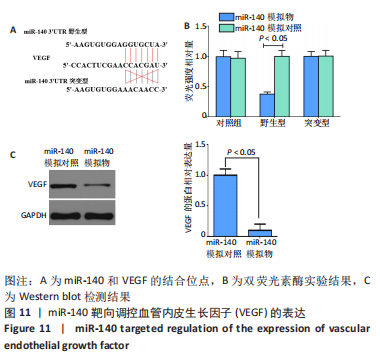
(1)双荧光素酶实验[21]:使用生物信息学数据库miRDB(http://mirdb.org/miRDB/)预测miR-140和VEGF存在靶向调控位点。推测VEGF可能为miR-140作用的靶基因。为此,进行双荧光素酶实验,构建miR-140突变型(MUT)和miR-140野生型(WT)质粒,随后插入至含VEGF-3’UTR的荧光素酶报告载体中,记为VEGF(MUT)、VEGF(WT),通过Lipofectamine2000将VEGF(MUT)、VEGF(WT)依次与miR-140模拟物阴性对照(miR-140-mimic-control)、miR-140模拟物(miR-140-mimic)miR-140-mimic共转染至软骨细胞ATDC5中,在37 ℃、体积分数5%CO2条件下培养细胞48 h,使用双重荧光素酶报告基因检测系统检测萤火虫荧光素酶活性/海肾荧光素酶的活性;同时采用Western blot检测细胞中VEGF的表达进行验证,检测步骤同上。
(2) 细胞培养:复苏软骨细胞株ATDC5,接种在含体积分数10%胎牛血清的DMEM培养基中,按要求进行消化、传代,取对数生长期的细胞进行实验。
(3)细胞实验分组与处理[22]:取对数生长期的软骨细胞ATDC5,分5组处理:正常组加入含生理盐水、0.1 mol/L miR-140-antagomir-NC和siRNA-VEGF NC的DMEM培养基;模型组加入含10 ng/mL白细胞介素1β、0.1 mol/L miR-140-antagomir-NC和siRNA-VEGF NC的DMEM培养基;药物组加入含10 ng/mL白细胞介素1β、10 mg/mL温阳通络胶囊生理盐水溶液、0.1 mol/L miR-140-antagomir-NC和siRNA-VEGF NC的DMEM培养基;抑制剂组加入含10 ng/mL白细胞介素1β、10 mg/mL温阳通络胶囊生理盐水溶液及0.1 mol/L miR-140-antagomir的DMEM培养基;干扰组加入含10 ng/mL白细胞介素1β、10 mg/mL温阳通络胶囊生理盐水溶液、0.1 mol/L miR-140-antagomir及siRNA-VEGF的DMEM培养基。所有细胞置于37℃、体积分数5%CO2细胞培养箱中培养24 h。
qRT-PCR检测:培养24 h后,检测各组细胞中miR-140、VEGF、Bcl-2及Bax mRNA的表达。
ELISA法检测炎性因子水平:培养24 h后,室温下3 000 r/min离心30 min,采用ELISA检测各组细胞上清液中白细胞介素6和肿瘤坏死因子α水平[23]。
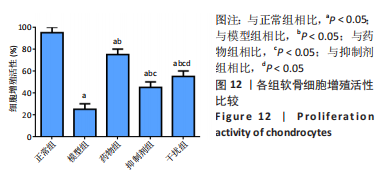
MTT法检测细胞增殖: 调整对数生长期的软骨细胞密度至3×105/孔,接种至36孔板上,按实验分组处理,置于37 ℃、体积分数5%CO2下培养24 h。加入20 μL的MTT工作液,孵育,酶标仪测量A490 nm。细胞的增殖活性=实验组的A490 nm/正常组的A490 nm×100%[24]。
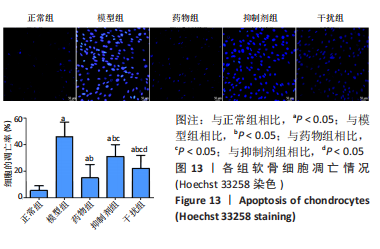
Hoechst 33258染色检测软骨细胞凋亡:调整对数生长期的软骨细胞密度至1×106/孔,按实验分组处理,置于37 ℃、体积分数5%CO2条件下培养24 h。之后以PBS充分清洗,多聚甲醛固定,加入适量Hoechst 33258染色液,室温孵育后,TE-2000荧光显微镜下观察,细胞核被染成均匀的蓝色视为正常细胞,细胞膜破裂,细胞核严重浓缩后呈现明亮的蓝色视为凋亡细胞[25]。利用图像处理软件Image J 统计分析各组细胞凋亡率。
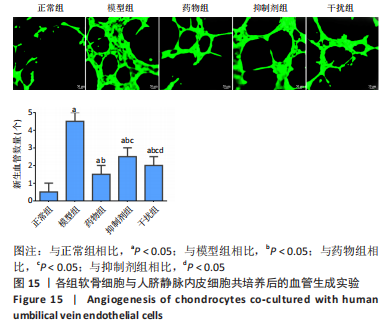
血管生成实验:调整对数生长期软骨细胞密度至1×106个/孔,按实验分组处理,同时在每组软骨细胞中加入1×106/孔的人脐静脉内皮细胞,置于37 ℃、体积分数5%CO2下孵育2 h;接种在预处理过的Matrigel基质胶中,置于37 ℃、体积分数5%CO2下培养24 h。显微镜下观察,利用Image J 软件统计新生血管数量[26]。
Western blot检测:检测细胞内VEGF、Bcl-2、Bax蛋白的表达。培养24 h后,取各组细胞,经RIPA蛋白裂解液裂解后,提取样本中总蛋白,Bradford试剂盒测定浓度,进行电泳分离,转膜,清洗,封闭,孵育,加入一抗VEGF、Bcl-2、Bax(1∶500),孵育过夜,加入HRP标记的IgG二抗(1∶1 000),显色[20],以GAPDH作为内参统计分析各条带的灰度值。
1.5 主要观察指标 ①各组大鼠膝关节软骨组织miR-140、血管内皮生长因子、Bcl-2及Bax的基因表达,软骨组织内软骨细胞凋亡及新生血管数量,血清中炎性因子水平,软骨组织病理,以及血管内皮生长因子、Bcl-2及Bax的蛋白表达;②各组软骨细胞增殖、凋亡,细胞上清中炎性因子水平,miR-140、VEGF、Bcl-2及Bax mRNA的表达,VEGF、Bcl-2、Bax蛋白的表达,以及与人脐静脉内皮细胞共培养后的新生血管数量。
1.6 统计学分析 数据分析采用软件SPSS 16.0,大鼠血清中白细胞介素6和肿瘤坏死因子α质量浓度等符合正态分布的计量资料采用x±s表示,多组间比较采用方差分析,两两组间比较采用独立LSD-t检验,P < 0.05表示差异有显著性意义。该文统计学方法已经广东食品药品职业学院统计学专家审核。