中国组织工程研究 ›› 2021, Vol. 25 ›› Issue (28): 4485-4491.doi: 10.12307/2021.062
• 组织工程软骨材料Tissue-engineered cartilage • 上一篇 下一篇
动态压力联合胰岛素样生长因子1基因转染对壳聚糖/明胶支架中兔脂肪间充质干细胞成软骨分化的影响
张传辉1,李建军2,杨 军2
- 1朝阳市中心医院骨外科,辽宁省朝阳市 122000;2中国医科大学附属盛京医院创伤骨科,辽宁省沈阳市 110004
Effect of dynamic compression combined with insulin-like growth factor-1 gene transfection on chondrogenic differentiation of rabbit adipose-derived mesenchymal stem cells in chitosan/gelatin scaffolds
Zhang Chuanhui1, Li Jianjun2, Yang Jun2
- 1Department of Orthopeadic Surgery, Chaoyang City Center Hospital, Chaoyang 122000, Liaoning Province, China; 2Department of Orthopedic Trauma, Shengjing Hospital of China Medical University, Shenyang 110004, Liaoning Province, China
摘要:

文题释义:
钙离子通道:是一种跨越细胞膜的结构,它严格控制着钙离子进入细胞的过程。软骨细胞膜上的几种通道,如受体电位香草醛亚家族4、机械敏感性离子通道和电压门控通道可被各种物理刺激激活,导致细胞外钙离子瞬时内流。
胰岛素样生长因子:是一组具有促生长作用的多肽类物质,其分泌细胞广泛分布在人体的肝、肾、脑、心和肠等组织中,胰岛素样生长因子家族有胰岛素样生长因子1和胰岛素样生长因子2两种。胰岛素样生长因子1的产生更依赖于生长激素,其促生长作用强,被认为是调节软骨形成和代谢最关键性的细胞因子。
背景:应用生物反应器体外模拟人体内生物力学环境,联合应用基因转染技术体外构建组织工程软骨是目前组织工程研究领域的新思路。对于机械应力促进脂肪间充质干细胞成软骨分化的作用机制,目前国内外尚无定论。
目的:研究动态压力与胰岛素样生长因子1(insulin-like growth factor-1,IGF-1)基因转染对诱导负载于壳聚糖/明胶复合支架上的兔脂肪间充质干细胞成软骨分化的交互作用。
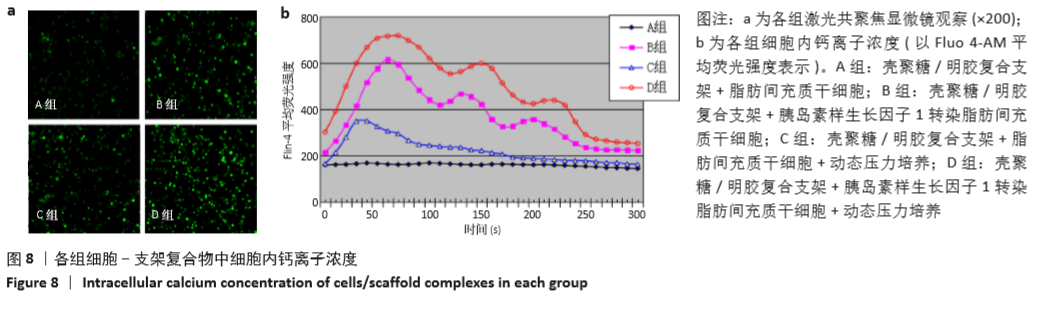
方法:将壳聚糖/明胶复合支架材料置于6孔培养板中,分4组干预:A组滴加脂肪间充质干细胞悬液,孵育4 h后加入完全培养基培养9 d;B组滴加IGF-1转染的脂肪间充质干细胞悬液,孵育4 h后加入完全培养基培养9 d;C组滴加脂肪间充质干细胞悬液,孵育4 h后加入完全培养基培养2 d,随后进行动态压力培养(2%形变,频率1 Hz),加压20 min,间歇20 min,每天6个循环周期,继续培养7 d;D组滴加IGF-1转染的脂肪间充质干细胞悬液,孵育4 h后加入完全培养基培养2 d,随后进行动态压力培养,继续培养7 d。培养结束后,检测细胞-支架复合物中细胞的增殖速度、糖胺聚糖含量、钙离子含量及软骨相关基因表达(IGF-1、Sox-9、Ⅱ型胶原、蛋白聚糖和X型胶原)。
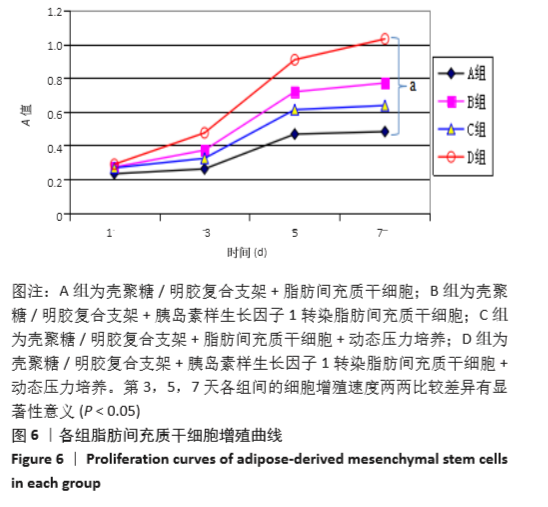
结果与结论:①各组细胞均具有较好的增殖能力,其中增殖速度由快至慢依次为D组、B组、C组、A组;②B、C、D组的糖胺聚糖、钙离子含量高于A组(P < 0.01),D组高于B、C组(P < 0.01),B组高于C组(P < 0.01);③4组间X型胶原mRNA表达无差异(P﹥0.05);B、C、D组的IGF-1、Sox-9、Ⅱ型胶原、蛋白聚糖mRNA表达高于A组(P < 0.01),D组高于B、C组(P < 0.01),B组高于C组(P < 0.01);④结果表明,动态压力联合IGF-1基因转染协同诱导壳聚糖/明胶复合支架上脂肪间充质干细胞的成软骨分化。
https://orcid.org/0000-0002-4742-2150 (张传辉)
中国组织工程研究杂志出版内容重点:生物材料;骨生物材料; 口腔生物材料; 纳米材料; 缓释材料; 材料相容性;组织工程
中图分类号: