1.1 设计 计算机模拟及体外细胞分子生物实验。
1.2 时间及地点 实验于2024年1月至2025年2月在广州中医药大学实验室完成。
1.3 材料
1.3.1 实验细胞 MC3T3-E1细胞购自中国科学院上海细胞库,后续实验所用细胞均为生长状态良好的2-10代细胞。人源髓细胞白血病细胞HL60细胞购自上海碧云天公司。
1.3.2 实验药品和试剂 芦丁(HY-N0148,MedChemExpress,美国);佛波酯(HY-18739,MedChemExpress公司,美国);α-MEM基础培养基(Hyelone公司,新西兰);RPMI-1640 培养基 (R7509-1L,Sigma-Aldrich,美国);DNaseⅠ(MedChemExpress,美国);MC3T3-E1 细胞成骨诱导分化试剂盒(MUXMT-90021,赛业,中国);碱性磷酸酶染色试剂盒(P0322M,上海碧云天公司,中国);茜素红染色液(ALIR-10001,赛业OriCell®染色液,美国);蛋白酶磷酸酶抑制剂混合物(P1045,上海碧云天公司,中国);十二烷基硫酸钠-聚丙烯酰胺凝胶配制试剂盒(PG010,上海雅酶生物医药科技有限公司,中国);ECL化学曝光液(WBKLS0100,Merck Millipore 公司,美国);Annexin V-FITC/PI凋亡检测试剂盒(C1383S,上海碧云天公司,中国);PCR引物(生工,中国);RNA抽提试剂盒(B0004D,EZBioscience,美国);PCR荧光定量试剂盒 (上海碧云天公司,中国);Runt相关转录因子2(ab192256,Abcam公司,中国);骨形态发生蛋白2(ab284387,Abcam 公司,中国);β-连环蛋白(ab32572,Abcam 公司,中国);髓过氧化物酶(AG2657,上海碧云天公司,中国);蛋白精氨酸脱亚胺酶4(F1B9L,Cell Signaling 公司,中国);中性粒细胞弹性蛋白酶(ab131260,Abcam 公司,中国);β-tubulin (ab18207,Abcam 公司,中国);辣根过氧化物酶标记羊抗兔二抗(PR30011,Proteintech 公司,美国)。
1.3.3 实验仪器 电泳仪 (BIO-RAD公司,中国);细胞培养箱(Thermo,美国);转膜仪(BIO-RAD公司,美国);细胞计数仪(上海睿钰生物科技有限公司,中国);C6流式细胞仪(BD公司,美国);多功能PCR仪(Thermo公司,美国);RNA浓度测定仪(赛默飞世尔科技有限公司,中国);荧光显微镜(OLYMPUS公司,日本);显微镜系统工作站(OLYMPUS公司,日本);恒温磁力搅拌器(司乐仪器有限公司,中国);电热恒温水槽(上海一恒科技有限公司,中国)。
1.4 实验方法
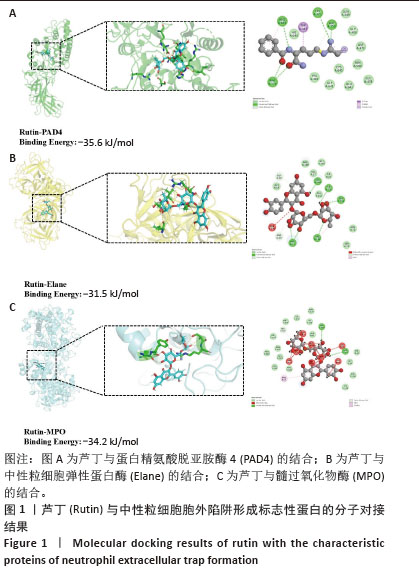
1.4.1 分子对接 在PubChem在线数据库(https://pubchem. ncbi.nlm.nih.gov/) 输入芦丁的有效成分英文名,下载芦丁(化合物化学标识符:5280805)的2D结构,采用ChemOffice软件 (版本2014)构建有效成分的3D结构使其能量最小化,保存为*mol2格式。随后从PDB数据库(https://www.rcsb.org/)分别下载蛋白精氨酸脱亚胺酶4、髓过氧化物酶、中性粒细胞弹性蛋白酶的配体PDB格式文件,用PyMOL (版本2.6.2)软件对蛋白去水分子,分离出活性中心的原配体,并确定芦丁与受体蛋白的结合位点,运用LeDock软件进行分子对接,计算结合能,使用Discovery Studio 2019和PyMOL可视化对接图像。结合能< 0 kJ/mol说明配体与受体能够自发结合,结合能≤-20.92 kJ/mol表示具有显著的受体-配体结合活性,≤-29.29 kJ/mol表示具有非常强烈的受体-配体结合活性[18]。
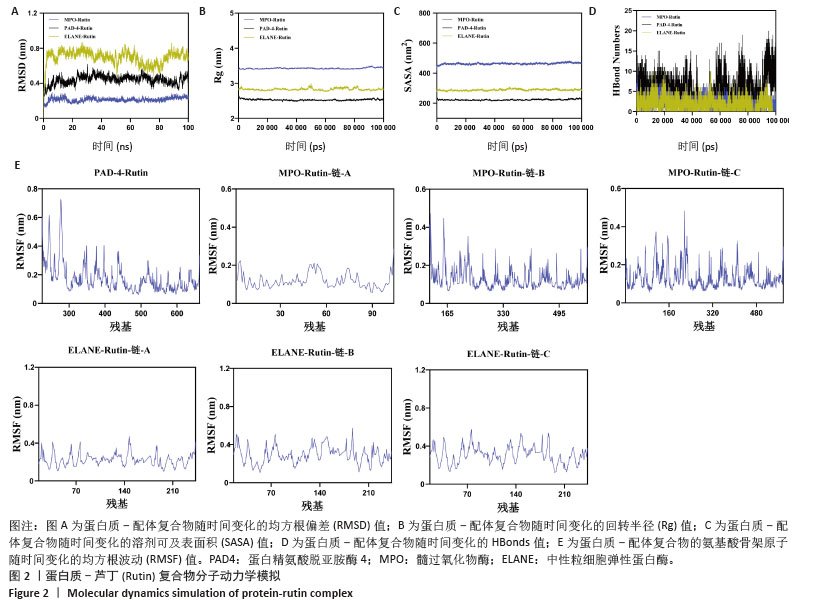
1.4.2 分子动力学模拟 使用Gromacs 2022对复合物进行100 ns分子动力学模拟。蛋白质采用CHARMM 36力场参数[19],配体拓扑结构由GAFF2力场参数构建。采用周期性边界条件,将蛋白质-配体复合物放置在立方盒中。采用TIP3P水模型将水分子填充到盒子中,形成周期边界为1.2 nm的水盒[20]。使用粒子网格Ewald和Verlet 算法计算静电相互作用。随后,进行100 000步的等温等容系综平衡和等温等压系综平衡,耦合常数为0.1 ps,持续时间为100 ps。范德华和库仑相互作用均使用1.0 nm的截止值计算。最后,系统在恒定温度(310 K)和恒压(100 kPa)下利用Gromacs 2022进行分子动力学模拟,共计时长100 ns。
1.4.3 细胞培养 第3代MC3T3-E1细胞复苏后使用含体积分数10%胎牛血清及1%青-链霉素双抗的α-MEM完全培养基,在37 ℃、体积分数5% CO2恒温培养箱中进行常规培养,培养过程中每2 d更换1次新鲜培养基,保持细胞生长密度。当细胞贴壁生长至80%-90%融合度时,按标准流程进行传代操作:首先用PBS清洗细胞3次,随后加入0.25%胰蛋白酶消化液作用2 min,待细胞回缩后加入2倍体积的完全培养基终止消化,细胞悬液经1 000 r/min离心5 min后弃上清,PBS重悬沉淀,并按1∶3比例接种至新培养皿。
HL60细胞使用含体积分数20%胎牛血清及1%青-链霉素双抗的RPMI-1640 培养基,在37 ℃、体积分数5% CO2恒温培养箱中进行常规传代培养,参考文献[21],将指数生长期的HL60细胞经1.25%二甲基亚砜持续诱导6 d分化成类中性粒细胞样细胞(Neutrophil-like cells,dHL60)。
第3代MC3T3-E1细胞以2×105/cm2密度接种到6孔板,待细胞贴壁后,将培养基更换为不含胎牛血清的RPMI-1640培养基,采用直接接触的共培养模式,向6孔板中加入dHL60细胞悬液(终细胞密度5×105/cm2)。
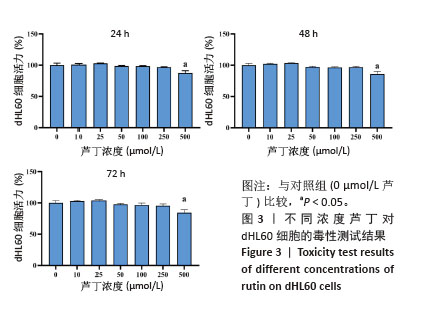
1.4.4 芦丁对dHL60细胞的毒性测试 使用二甲基亚砜将芦丁溶解配制成100 mmol/L原始溶液,依次稀释为不同浓度,经0.22 μm微孔滤膜过滤后使用。dHL60细胞以1×105个/孔密度接种于96孔板,30 min后分别加入不同浓度芦丁(1,10,25,50,100,250,500 μmol/L)或同等体积含二甲基亚砜的PBS(对照组,0 μmol/L芦丁)继续培养,每孔设置6个及以上复孔,每次实验重复3次及以上,分别在24,48,72 h时每孔加入10% CCK-8工作液20 μL,继续孵育1 h,使用酶标仪在450 nm波长下检测吸光度值并计算细胞活力,相对细胞活力=(A给药组-A空白组)/(A对照组-A空白组) ×100%。
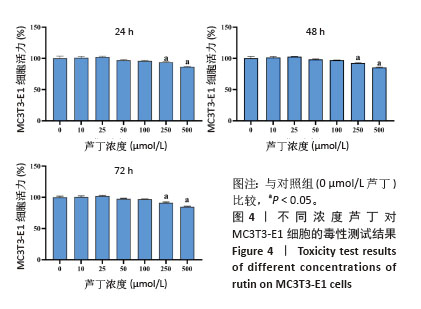
1.4.5 芦丁对MC3T3-E1细胞的毒性测试 使用二甲基亚砜将芦丁溶解配制成100 mmol/L原始溶液,依次稀释为不同浓度,经0.22 μm微孔滤膜过滤后使用。第3代MC3T3-E1细胞以1×105个/孔密度接种96孔板,30 min后分别加入不同浓度芦丁(1,10,25,50,100,250,500 μmol/L)或同等体积含二甲基亚砜的PBS (对照组,0 μmol/L芦丁)继续培养,每孔设置6个及以上复孔,每次实验重复3次及以上,分别在24,48,72 h时每孔加入10% CCK-8工作液20 μL,继续孵育1 h,使用酶标仪在450 nm波长下检测吸光度值并计算细胞活力,相对细胞活力=(A给药组-A空白组)/(A对照组-A空白组) ×100%。
1.4.6 实验分组
(1)芦丁对中性粒细胞胞外陷阱形成的影响:将1.25%二甲基亚砜诱导的dHL60细胞以5×105个/孔密度接种于12孔板中,30 min后按下述分组进行干预:①加入等体积Hank’s平衡盐溶液(空白对照组);②加入50 nmol/L佛波酯(佛波酯组);③加入50 nmol/L 佛波酯和250 μmol/L芦丁(芦丁干预组);④加入50 nmol/L佛波酯、250 μmol/L芦丁和5 U/mL DNaseⅠ (芦丁联合DNaseⅠ干预组)。佛波酯的使用浓度参考GUO等[22]的研究,DNaseⅠ的使用浓度参考MA等[23]的研究。
(2)芦丁在中性粒细胞胞外陷阱作用下对MC3T3-E1细胞成骨分化的影响:将第3代MC3T3-E1细胞以1×105个/孔密度接种于12孔板中,待细胞贴壁后弃去培养基,按照下述分组进行干预:①加入dHL60细胞(5×105个/孔)和50 nmol/L 佛波酯(中性粒细胞胞外陷阱诱导组);②加入50 nmol/L佛波酯(佛波酯对照组);③加入等体积的Hank’s平衡盐溶液(空白对照组);④加入100 μmol/L芦丁(芦丁对照组);⑤加入dHL60细胞(5×105个/孔)、50 nmol/L 佛波酯和250 μmol/L芦丁(芦丁干预组);⑥加入dHL60细胞(5×105个/孔)、50 nmol/L佛波酯、250 μmol/L芦丁和5 U/mL DNaseⅠ (芦丁联合DNaseⅠ干预组)。
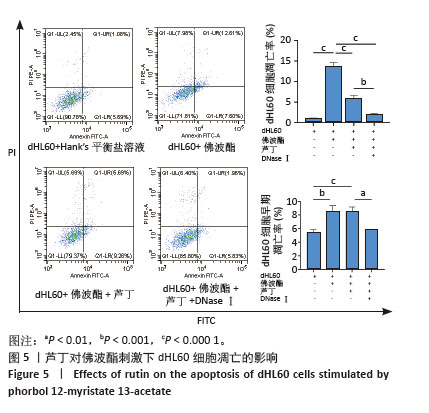
1.4.7 芦丁对佛波酯刺激下的dHL60细胞凋亡的影响 按照1.4.6(1)进行实验分组,避光孵育4 h后,离心后去上清,将细胞样品与500 μL缓冲液、5 μL Annexin V-FITC和5 μL PI 混合避光反应15 min,使用流式细胞仪检测各组dHL60细胞凋亡情况,采用CytExpert软件计算细胞凋亡率。
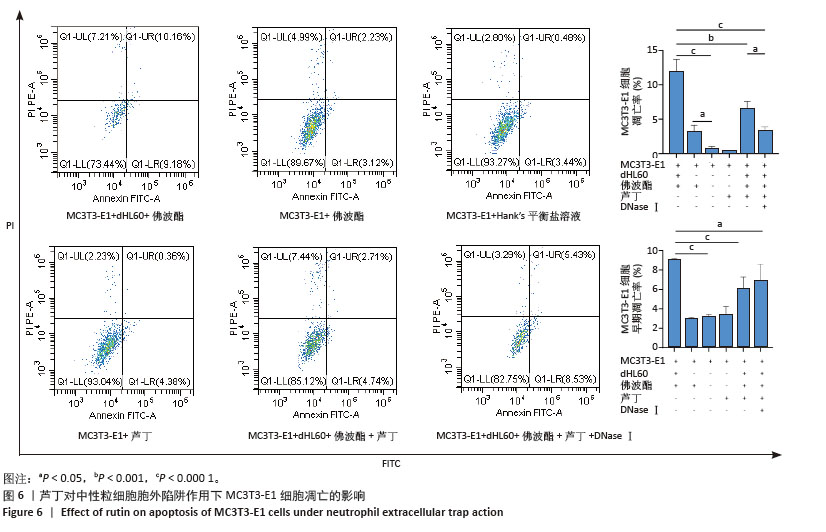
1.4.8 芦丁对中性粒细胞胞外陷阱作用下MC3T3-E1细胞凋亡的影响 按照1.4.6(2)进行实验分组干预48 h后,经胰酶消化90 s,将细胞样品与500 μL缓冲液、5 μL Annexin V-FITC和5 μL PI混合避光反应15 min,使用流式细胞仪检测各组MC3T3-E1细胞凋亡情况,采用CytExpert软件计算细胞凋亡率。
1.4.9 芦丁对中性粒细胞胞外陷阱作用下MC3T3-E1细胞成骨分化的影响
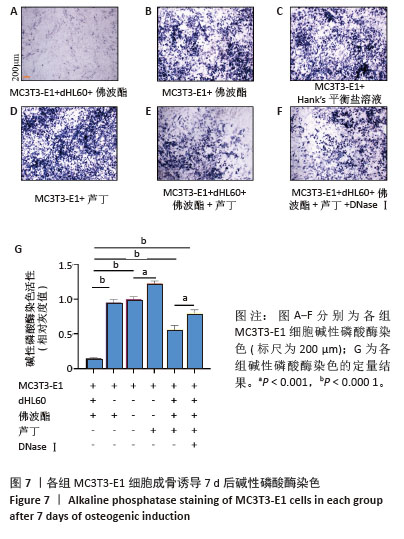
(1)碱性磷酸酶染色:根据1.4.6(2)进行实验分组干预48 h后,用成骨诱导分化试剂盒进行成骨诱导分化,每2 d换液1次。诱导至第7天时,弃培养基,PBS冲洗3次,加入4 ℃预冷的碱性磷酸酶固定液室温孵育20 min,以去离子水充分漂洗,使用1%核固红染色液室温复染5 min,显影细胞核形态,使用倒置光学显微镜采集图像,Image J软件进行灰度值分析。以对照组阳性染色区域灰度值为基准值,计算各组相对灰度值比值。
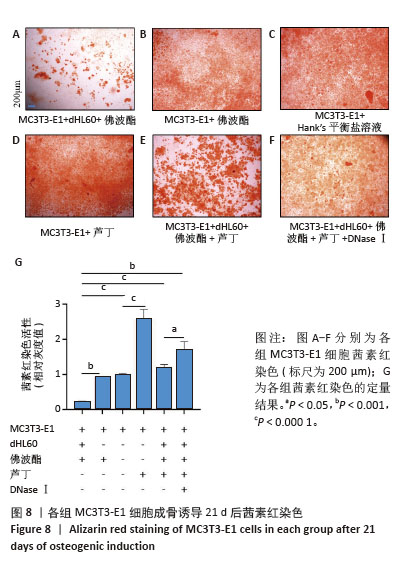
(2)茜素红染色:根据1.4.6(2)进行实验分组干预48 h后,用成骨诱导分化试剂盒进行成骨诱导分化,每2 d换液1次。诱导至第21天时,弃培养基,磷酸盐缓冲液轻柔冲洗3次,清除残留钙盐沉淀物,加入2%茜素红S染色液室温孵育30 min,染色终止后,用去离子水反复漂洗至背景透明,使用倒置光学显微镜采集图像,Image J软件进行灰度值分析。以对照组阳性染色区域灰度值为基准值,计算各组相对灰度值比值。
1.4.10 RT-qPCR检测
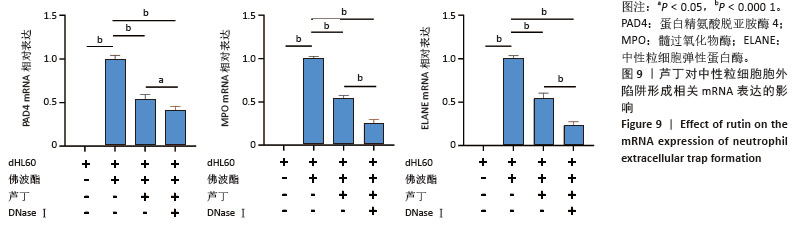
(1)芦丁对中性粒细胞胞外陷阱形成基因mRNA表达的影响:根据1.4.6(1)进行实验分组干预4 h后,使用EZBioscience提取各组dHL60细胞总RNA并检测浓度,将各组RNA浓度统一后使用试剂盒将RNA反转录为cDNA,进一步处理cDNA并进行实时荧光定量PCR检测,反应条件:94 ℃初始变性2 min,94 ℃变性 5 s,60 ℃退火30 s,共 40次循环。以GAPDH为内参基因,采用2-ΔΔCt法计算目的基因相对表达量。引物序列见表1。
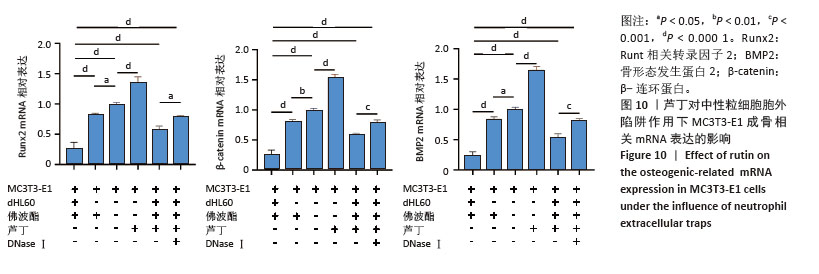
(2)芦丁对中性粒细胞胞外陷阱作用下MC3T3-E1成骨相关基因mRNA表达的影响:根据1.4.6(2)进行实验分组干预48 h后,根据成骨诱导分化试剂盒进行成骨诱导分化,每2 d换液1次。诱导至第7天,使用ZBioscience提取各组细胞总RNA并检测浓度,其余步骤同上。引物序列见表1。

1.4.11 Western blot检测
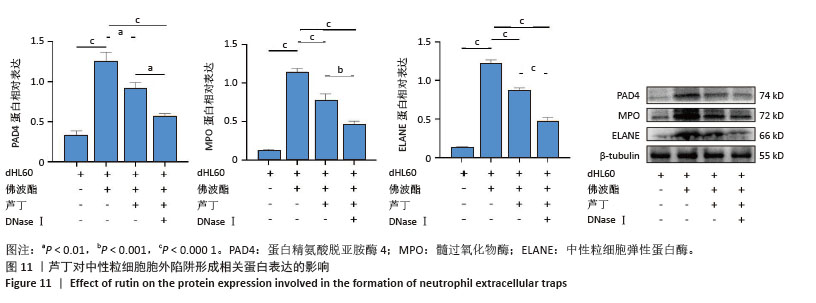
(1)芦丁对中性粒细胞胞外陷阱形成相关蛋白表达的影响:根据1.4.6(1)进行实验分组干预4 h后,用含有蛋白酶抑制剂和磷酸酶抑制剂的RIPA裂解液冰上裂解dHL60细胞30 min,4 ℃、12 000×g离心10 min,收集上清,BCA法测定蛋白浓度,以标准曲线校准后等量上样。将各组样品等量等体积加入十二烷基硫酸钠-聚丙烯酰胺凝胶电泳分离蛋白后,湿转法转移至聚偏二氟乙烯膜,用5%脱脂牛奶室温封闭1 h,Tris缓冲盐溶液-Tween 20清洗3次(10 min/次);用适当稀释度的一抗在4 ℃下过夜孵育聚偏二氟乙烯膜,一抗主要包括髓过氧化物酶(稀释比1∶2 000)、蛋白精氨酸脱亚胺酶4 (稀释比1∶2 000)、中性粒细胞弹性蛋白酶(稀释比1∶1 000),内参为β-tubulin (稀释比1∶1 000),TBST清洗PVDF膜3次,每次10 min;室温下用山羊抗兔二抗(稀释比1∶5 000)孵育1 h,TBST 清洗3次,每次10 min,ECL化学发光法显影后,使用Image J软件对各条带灰度值进行半定量分析,目的蛋白表达量标准化为β-tubulin比值(目的蛋白灰度值/β-tubulin灰度值)。
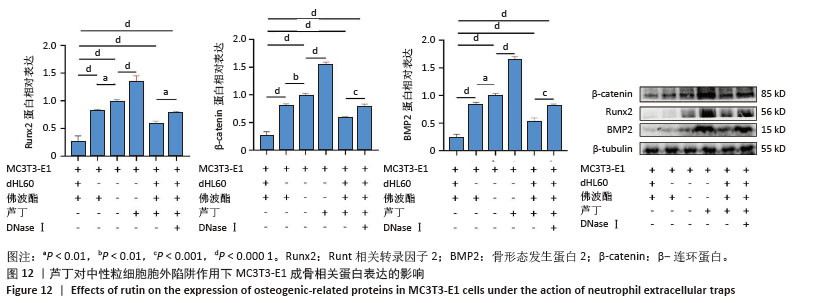
(2)芦丁对中性粒细胞胞外陷阱作用下MC3T3-E1成骨相关蛋白表达的影响:根据1.4.6(2)进行实验分组干预48 h后,使用成骨诱导分化试剂盒进行成骨诱导分化,每2 d换液1次。诱导至第7天,用RIPA裂解液裂解冰上裂解各组MC3T3-E1细胞30 min,后续其余步骤同上。一抗主要包括β-连环蛋白(稀释比1∶2 000)、Runt相关转录因子2 (稀释比1∶2 000)、骨形态发生蛋白2(稀释比1∶2 000),内参为β-tubulin (稀释比1∶1 000)。
1.5 主要观察指标 ①芦丁对佛波酯刺激下dHL60细胞中性粒细胞胞外陷阱形成的影响:各组dHL60细胞的凋亡情况,中性粒细胞胞外陷阱形成标志基因的mRNA和蛋白表达;②芦丁对中性粒细胞胞外陷阱作用下MC3T3-E1细胞的影响:各组MC3T3-E1细胞碱性磷酸酶染色与茜素红染色结果,各组MC3T3-E1细胞凋亡情况以及成骨相关基因的mRNA与蛋白表达;③芦丁靶向结合中性粒细胞胞外陷阱相关蛋白的能力:芦丁与蛋白精氨酸脱亚胺酶4、髓过氧化物酶、中性粒细胞弹性蛋白酶蛋白的结合能力。
1.6 统计学分析 采用GraphPad Prism 9 (San Diego,California,USA)软件和Image J 软件处理实验数据与作图。各组计量资料以x±s表示。对于符合正态分布且方差齐性的数据,组间比较选择独立样本t检验;若涉及多组数据比较,则采用单因素方差分析(ANOVA),并进一步通过LSD-t检验进行组间两两分析。P < 0.05为差异有显著性意义。文章统计学方法已经通过广州中医药大学生物统计学专家审核。
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程