2.1 纤毛的结构和功能
2.1.1 纤毛的结构 纤毛突出于细胞膜表面,并与之相连续。长度从几个微米到2 mm不等,直径约0.25 μm。哺乳动物纤毛主要分为运动纤毛和初级纤毛这两种类型,由纤毛膜、基质和轴丝3部分组成(见图2)。在运动纤毛的中央有一以微管为基础的轴丝,轴丝具有外围的9个双连体微管和一对中央微管(9+2结构)[4]。
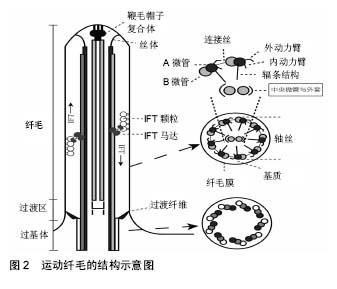
中央微管通过辐条结构与外围微管相连接,相邻的双连体微管束之间靠连接丝连接,内外动力蛋白臂分别分布在双连体微管束的内外两侧,这些蛋白质结构调控着纤毛的运动。
轴丝与位于细胞膜下的基体相连接。基体起源于中心粒,并促进增殖分裂细胞内中心体的形成[5-6]。当细胞增殖停止时,中心粒开始与高尔基体起源的囊泡接触,迁移、黏附于到细胞膜表面[7],于此部位转化为基体。基体与中心粒结构相似,由9个三联体的微管组成。纤毛轴丝顶端为“纤毛帽状复合体”,是连接轴丝顶端纤毛膜的重要结构,纤毛的组装和解聚就发生在此纤毛顶端。初级纤毛结构比较短小,通常只在电子显微镜下才能观察到[8],且初级纤毛轴丝内无中央微管结构(9+0结构)。
2.1.2 纤毛的功能 人们对纤毛功能的认识,首先基于其运动功能,如脑内室管膜纤毛,负责脑脊液循环;呼吸道纤毛,可移除呼吸道黏液及吸入的颗粒物;在相关的生殖研究中发现,随着射精的进行,数以百万计的精子通过其表面鞭毛游向输卵管;当精子细胞游到输卵管时,它们遭遇到一股由输卵管纤毛摆动形成的反向力量;胚胎节点的纤毛对确保脏器的正确位置是至关重要的[9-10]。
曾在很长一段时间内初级纤毛被认为是一种退化性细胞器,直到最近它才被确认为细胞的感应性触角。初级纤毛具有信号传导的作用,影响着动物的生长发育及各种器官的正常生理功能。初级纤毛延续于细胞膜表面并伸向胞外环境中,这样的理想位置有利于它及时察觉胞外环境中化学信号的改变,并将信号整合、传递到细胞内部,使细胞作出合适的反应与之相协调[11],例如嗅觉纤毛表面的G蛋白结合受体浓度的改变是机体识别气味的基础。初级纤毛也可感知细胞表面液体的流动,如肾集合管和肾小管上皮的纤毛可发现管内的液体流动情况,并有助于保持正常的细胞分裂模式[12-13];视网膜视杆细胞和视锥细胞通过集中于外节部分的膜相关分子感受光亮度,而外节部分即变异纤毛[14];嗅觉纤毛使人们能进一步感知外界环境,胞膜表面充满嗅觉受体蛋白,可发现环境中的化学物质并发送信号到大脑,经过处理后转化成人们的嗅觉[15]。维持哺乳动物稳态最关键的是确保胚胎发育过程中心脏解剖的正确,而发育性心脏细胞表面的纤毛对心脏形态的形成是非常重要的[16]。
2.2 纤毛结构与功能异常所致的疾病
2.2.1 原发性纤毛运动障碍(Primary ciliary dyskinesia,PCD) 纤毛在人体内广泛分布,纤毛缺陷常导致一系列的症状,即由单一病因引起的多组织受累的疾病。其中第一个被发现的是原发性纤毛运动障碍[17],它是由运动纤毛缺陷引起的。患者常有慢性支气管炎和鼻窦炎,因为呼吸道纤毛无法清除黏液和吸入的细菌、颗粒。因为反复发生的呼吸道细菌感染,患者逐渐进展为支气管扩张。男性患者常伴有不育,因为精子细胞鞭毛的运动功能受损。几乎一半的患者有内脏转位,因为节点纤毛的运动功能受损。此外,原发性纤毛运动障碍患者脑积水的发生率也大大增加,脑室内脑脊液的异常蓄积是由于室管膜纤毛的运动功能受损,阻碍脑脊液循环[18]。
随着越来越多的构成纤毛运动功能的蛋白被发现,人们逐渐发现导致原发性纤毛运动障碍发生的各种突变基因。目前,大约已有20种原发性纤毛运动障碍基因被发现,其中大多为编码外动力蛋白臂、辐条结构、连接丝、动力蛋白调节复合物以及位于胞质中用于动力蛋白臂预组装的蛋白的基因。然而,这些已知的原发性纤毛运动障碍基因只存在于半数的原发性纤毛运动障碍病例中,所以可能还有更多的原发性纤毛运动障碍基因没有被发现。
2.2.2 纤毛与不孕不育症(Infertility) 纤毛引起的不孕不育症也主要是由于其运动功能降低所致。男性精子尾部摆动是其游动动力的来源,其轴心为由9+2排列的微管组成的轴丝。当鞭毛的形成及运动功能缺陷时就会影响精子的游动,进而导致男性不育。
女性输卵管壶腹部黏膜皱襞发达,为受精发生的部位,输卵管上皮细胞主要为分泌细胞和纤毛细胞,其中纤毛细胞主要分布于黏膜皱襞的顶部。在月经周期的增殖期过程中,纤毛的高度不断增加,至卵巢排卵前后,雌激素分泌大量升高,纤毛达到最大高度,向宫腔方向的摆动频率也加快,可增强其传送功能,以将精子卵子结合成的受精卵推向宫腔并阻止细菌等有害物质进入腹膜腔,同时精子进入输卵管后游动的阻力也增加,只有少数运动能力强的精子才能达到壶腹部,以此排除畸形精子,有文献报道,在有生育力男子的精液中,畸形精子可占20%-40%。
综上,纤毛的完整性和运动性缺陷将直接影响到受精过程、受精精子质量及受精卵移动,进而导致女性不孕不育症。
Fliegauf等[13]认为即使轻微的纤毛缺陷也会导致患者的受孕率下降。此外,还有研究表明纤毛可感知激素和神经的刺激,调控女性生理周期,但详细机制还不清楚。
2.2.3 纤毛与多囊肾病(Ploycystic kidney disease PKD) 多囊肾病是常见的可危及人类生命的遗传性疾病,全球范围内已有一千多万人患有此病。
多囊肾病主要表现为常染色体显性遗传和常染色体隐形遗传。常染色体显性多囊肾病(ADPKD)主要见于成年人,发病率为1/1 000。
常染色体隐性多囊肾病(ARPKD)主要见于新生儿和孩子,发病率为1/6000,而且75%的患儿都于出生后几天内死亡。
这两种类型都有肾小管与导管上皮细胞的过度增殖,使管腔变成密闭的腔室,然后腔室扩张膨大,最终导致巨大的多囊肾脏形成和肾功能衰竭。
Pazour等[3]和Michaud等[8]分别在人和小鼠体内发现PKD1、 PKD2(多囊肾病的致病基因)编码的多囊蛋白1(PC-1)和多囊蛋白2(PC-2)共同表达于肾脏上皮细胞初级纤毛上。
多囊蛋白1和多囊蛋白2相互作用形成受体通道复合物,在调控肾脏上皮细胞增殖与分化的信号通路的早期阶段起作用。因此有学者认为:作为感觉触角的初级纤毛将这两种多囊蛋白铺置于其表面,与外界环境相接触,并中转信号到胞内。在小鼠模型中,这两种多囊蛋白突变或不能将纤毛组装成一个整体,都会因纤毛信号缺陷导致常染色体显性多囊肾病的发生。
对纤毛内转运(IFT)颗粒蛋白的测序表明在小鼠模型中IFT88的缺陷将导致常染色体隐性多囊肾病的发生。
遗传分析表明IFT88对纤毛形成是必不可少的;对基因突变小鼠肾脏进行电镜检查发现:IFT88对于肾脏集合管和肾小管上皮细胞初级纤毛的组装同样是必不可少的[3]。因此,纤毛内转运功能障碍使肾脏初级纤毛未能形成,从而导致小鼠患常染色体隐性多囊肾病。
近来发现,多囊蛋白1、多囊蛋白2在维持中心体完整性方面有重要作用,敲除多囊蛋白1在在体与离体实验中均可致中心体扩增[19],大量的中心体在看起来正常的管状细胞中积聚,表明中心体扩增为囊肿形成的早期事件。同样,在多囊蛋白2敲除的转基因小鼠成纤维细胞及胚胎间充质细胞中有中心体的扩增,表明多囊蛋白2敲除也可改变中心体的数量[20]。
中心体可为初级纤毛轴丝合成提供模板,进而参与初级纤毛的形成,并协调纤毛蛋白转运,但中心体扩增是否为纤毛病的诱因还未得到证实。
此外,肾小管上皮细胞的纤毛可感受小管内液体的流动,流体剪切力通过刺激初级纤毛及信号途径的传导来维持细胞增殖与代谢的平衡[21],当初级纤毛结构或功能缺陷时会导致肾脏上皮细胞过度增殖,导致肾脏多发囊腔的形成。
2.2.4 纤毛与失明 (Blindness) 失明是由色素性视网膜炎(感光细胞变性)引起的,与纤毛内转运缺陷相关,包括纤毛内转运颗粒蛋白和BBSome的缺陷。视网膜视杆细胞和视锥细胞有内、外节,内节是蛋白质合成的部位,外节上有膜盘,有感光作用的视蛋白就位于膜盘上。整个外节为变异纤毛,内、外节之间唯一的连接是具有9+0结构的连接纤毛。因此,所有建立和维持外节所必需的蛋白(如视蛋白)都要通过此连接纤毛[22],其中许多向外节转运的蛋白都是依赖纤毛内转运的。
20世纪90年代的研究表明,顺向纤毛内转运马达蛋白(驱动蛋白Ⅱ)位于脊椎动物连接纤毛上,敲除小鼠视网膜上的此马达蛋白将导致外节异常和视网膜变性[23]。之后的研究认为纤毛内转运颗粒蛋白位于连接纤毛上,与IFT88突变引起的小鼠多囊肾病相似,IFT88突变也可导致外节发育异常和感光细胞的凋亡[24]。
随后有研究证实缺乏其他纤毛内转运颗粒蛋白的小鼠也有相似的表现。因此,可以看出感光细胞对向外节转运的蛋白的波动极其敏感,并通过启动凋亡来杀死异常细胞,以确保消除视网膜上的异常细胞。
感光细胞的连接纤毛是一很长的纤毛过渡区域,大量的蛋白位于此区域上。研究发现似乎这些蛋白的缺陷更易导致失明,例如,过渡区的连接纤毛蛋白CEP290突变可引起莱伯氏先天性黑朦(Leber's congenital amaurosis)[25]。过渡区域似乎形成一个屏障,以阻止非纤毛蛋白进入纤毛,并允许纤毛蛋白进入纤毛。这可能解释了感光细胞的过渡区域为何如此的细长,以及为什么感光细胞对蛋白向外节的转运和分类功能缺陷如此的敏感。
2.2.5 纤毛与肿瘤(Tumor) Hedgehog(Hh)基因的同源基因有3个,分别为Shh、Ihh、Dhh[26],在不同物种的细胞增殖和内环境稳态中起着重要作用。在肿瘤发生过程中Hh信号通路被异常激活,导致细胞异常增生,最终致肿瘤的形成。
Ptch是抑癌基因[27],人类存在两种Ptch同源基因,即Ptch1和Ptch2,其中Ptch1蛋白是Hh的重要受体。Ptch1蛋白可抑制Smo(激活Hh信号传导必需的受体)进而抑制下游基因的转录,阻断Hh信号传导。几乎所有基底细胞癌亚型均有不同程度的Hh激活,其中大部分有Ptch1蛋白的缺失。
研究表明,Shh、Ptch、Smo在正常的结肠黏膜上有所表达,但在增生性病理情况下,如结肠息肉,腺瘤,腺癌中Shh、Ptch、Smo的表达水平要明显高于正常水平。在培养的离体细胞中加入外源性Shh可导致结肠上皮细胞增生,而抗Shh抗体可抑制此增生效应[28]。
此外,研究发现在小细胞癌、胰腺癌、前列腺癌、乳腺癌、恶性胶质瘤、髓母细胞瘤以及多发性骨髓瘤组织中均有Hh信号的异常激活。
初级纤毛通过由纤毛内运输介导的对于基体和轴丝Smo蛋白以及转录因子Gli1和Gli2的征募作用与Hh信号传导途径相协调,因此Hh信号传导途径依赖于初级纤毛及完整的纤毛内运输[29-30]。初级纤毛对Hh信号传导是必需的,而Hh信号传导对肿瘤的发生发展起着重要作用,这使得人们对肿瘤发病机制的研究有了新的方向。
2.2.6 纤毛与骨质疏松症(Osteoporosis) 骨是对机械负荷极其敏感的器官,它的稳态取决于骨细胞对机械负荷的感知和反应能力。
在骨组织中,骨细胞膜表面的初级纤毛可作为力学感受器,感受外界机械负荷,并将这些力学刺激转化为胞内的生化信号。
由成骨细胞和骨髓基质细胞分泌的核因子kB受体活化因子配体(RNAKL)可通过与破骨细胞前体细胞或破骨细胞表面的RANK受体结合使骨吸收增多,即促进破骨细胞的分化与激活,并抑制破骨细胞的凋亡。
骨保护素亦由成骨细胞和骨髓基质细胞分泌,可阻止RANKL与RANK的结合,起到骨保护的作用。有研究表明,在机械负荷作用于骨细胞表面时,初级纤毛可感受机械刺激并传导信号使骨保护素分泌量增多,骨保护素/RANKL比值增高,从而达到保护骨组织、抑制骨吸收的目的。通过相关基因敲除阻断初级纤毛生成后,再给予骨细胞同样大小的机械负荷,骨保护素/RANKL比值无明显变化,说明骨细胞表面的初级纤毛可感受外界机械负荷,通过调整成骨细胞和骨髓基质细胞的骨保护素、RANKL分泌量,从而抑制骨吸收[31]。
流体剪切力作用于成骨细胞时可致成骨基因的表达增加,Malone等[31]研究认为初级纤毛在其中起着至关重要的作用。在骨基质矿化开始后,成骨细胞中骨桥蛋白水平开始增加;在骨重建的过程中,骨桥蛋白在骨质线和骨膜板有较高浓度。将一定大小的流体剪切力作用成骨细胞一段时间后,骨桥蛋白基因表达量明显增加,通过相关基因敲除阻断初级纤毛生成后,再给予成骨细胞同样大小的流体剪切力,骨桥蛋白基因表达量无明显变化。此外,初级纤毛及其附属结构对成骨细胞的分化成熟也起着重要的调控作用[32]。
骨细胞与成骨细胞通过其表面的初级纤毛感受外界的机械负荷,并转化为胞内生化信号,达到保护骨细胞抑制骨吸收的目的。这种保护机制也许会为研发预防和治疗骨质疏松症的新药物提供新思路,但初级纤毛的量和功能与年龄的关系尚不清楚,因为骨质疏松症主要见于老年人。
.jpg) 文题释义:
初级纤毛:是一种广泛存在于各种细胞表面的细胞器,体形微小但结构复杂,作用强大,具有重要的感官作用,能感知细胞外机械和化学信号变化并协助其转导至细胞内部,从而引起细胞应答。
纤毛相关疾病:原发性纤毛运动障碍:纤毛在人体内广泛分布,纤毛缺陷常导致一系列的症状,即由单一病因引起的多组织受累的疾病。其中第一个被发现的是原发性纤毛运动障碍,它是由运动纤毛缺陷引起的。
文题释义:
初级纤毛:是一种广泛存在于各种细胞表面的细胞器,体形微小但结构复杂,作用强大,具有重要的感官作用,能感知细胞外机械和化学信号变化并协助其转导至细胞内部,从而引起细胞应答。
纤毛相关疾病:原发性纤毛运动障碍:纤毛在人体内广泛分布,纤毛缺陷常导致一系列的症状,即由单一病因引起的多组织受累的疾病。其中第一个被发现的是原发性纤毛运动障碍,它是由运动纤毛缺陷引起的。.jpg) 文题释义:
初级纤毛:是一种广泛存在于各种细胞表面的细胞器,体形微小但结构复杂,作用强大,具有重要的感官作用,能感知细胞外机械和化学信号变化并协助其转导至细胞内部,从而引起细胞应答。
纤毛相关疾病:原发性纤毛运动障碍:纤毛在人体内广泛分布,纤毛缺陷常导致一系列的症状,即由单一病因引起的多组织受累的疾病。其中第一个被发现的是原发性纤毛运动障碍,它是由运动纤毛缺陷引起的。
文题释义:
初级纤毛:是一种广泛存在于各种细胞表面的细胞器,体形微小但结构复杂,作用强大,具有重要的感官作用,能感知细胞外机械和化学信号变化并协助其转导至细胞内部,从而引起细胞应答。
纤毛相关疾病:原发性纤毛运动障碍:纤毛在人体内广泛分布,纤毛缺陷常导致一系列的症状,即由单一病因引起的多组织受累的疾病。其中第一个被发现的是原发性纤毛运动障碍,它是由运动纤毛缺陷引起的。
.jpg)
.jpg) 文题释义:
初级纤毛:是一种广泛存在于各种细胞表面的细胞器,体形微小但结构复杂,作用强大,具有重要的感官作用,能感知细胞外机械和化学信号变化并协助其转导至细胞内部,从而引起细胞应答。
纤毛相关疾病:原发性纤毛运动障碍:纤毛在人体内广泛分布,纤毛缺陷常导致一系列的症状,即由单一病因引起的多组织受累的疾病。其中第一个被发现的是原发性纤毛运动障碍,它是由运动纤毛缺陷引起的。
文题释义:
初级纤毛:是一种广泛存在于各种细胞表面的细胞器,体形微小但结构复杂,作用强大,具有重要的感官作用,能感知细胞外机械和化学信号变化并协助其转导至细胞内部,从而引起细胞应答。
纤毛相关疾病:原发性纤毛运动障碍:纤毛在人体内广泛分布,纤毛缺陷常导致一系列的症状,即由单一病因引起的多组织受累的疾病。其中第一个被发现的是原发性纤毛运动障碍,它是由运动纤毛缺陷引起的。