2.1 肠道菌群失调是肠易激综合征发生发展的重要环境因素 健康成人肠道内约有500种细菌,包括需氧、兼性厌氧和厌氧菌,其中双歧杆菌、嗜酸乳杆菌、粪链球菌占98%以上。正常情况下各菌属保持一定比例,维持肠道微生态系统平衡,当机体受环境、气候、饮食、用药、情绪等因素影响时,肠道微生态平衡被打乱,引起暂时或持久的菌群失调,导致肠道功能紊乱,引发多种肠道疾病[3-4]。肠道内有些细菌对人体有益,而有些则具致病性,益生菌可改善宿主肠道菌群平衡,提高宿主健康水平,致病菌则可产生毒素,侵犯黏膜,引起多种病理变化。
多项研究报道肠易激综合征患者多存在肠道菌群失调[5-6],表现为肠道菌群数量的增减,比例失调以及菌种性质的变化,如有益菌-双歧杆菌、乳酸杆菌数量减少[7-8],韦荣球菌数量增加以及小肠细菌过度增殖等,肠易激综合征患者同时存在肠道微生物定植抗力减弱,抵抗病原菌侵袭能力降低的特点[9]。另有研究证实肠易激综合征患者较之健康人群,肠道双歧杆菌和乳酸杆菌减少,类杆菌、肠杆菌、肠球菌增多[10-12]。
近年来研究发现,肠道菌群失调与肠易激综合征的发生关系密切[13]。正常情况下,肠道致病菌发挥侵袭作用,首先需突破由有益菌组成的第一道生物屏障,有益菌通过受体竞争、营养竞争、产生有害物质抑制或杀伤致病菌等方式拮抗致病菌入侵。肠易激综合征患者肠道菌群失调,有益菌数量减少而致病菌数量增多,致病菌可直接破坏肠黏膜屏障,导致通透性增高。致病菌及其
抗原易于通过肠黏膜并发生过度免疫,引起免疫细胞如肥大细胞的增殖、活化,肥大细胞被激活后可脱颗粒释放五羟色胺、前列腺素等多种活性物质,导致平滑肌收缩增强,肠道蠕动加快,出现腹泻等症状,同时干扰胃肠反射,导致内脏高敏,出现腹痛。此外,肠道菌群失调可影响机体对直肠扩张刺激的感觉阈值及内脏敏感性,McKeman等[14]研究表明婴儿双歧杆菌和短双歧杆菌可显著提高内脏高敏感模型大鼠的感觉阈值,内脏敏感性下降。另有研究应用膜片钳技术检测发现乳杆菌可通过抑制背根神经节细胞产生动作电位来改善直肠扩张刺激引起的内脏疼痛[15]。
2.2 肠道菌群与肠道黏膜免疫的相互作用及其与肠易激综合征的关系 肠道细菌以及来源于细菌的代谢产物包含了大量的免疫刺激物质如:抗原、毒素等,而肠道黏膜作为第一道免疫防线,能对来自黏膜表面的各种抗原作出诸如免疫耐受,免疫清除或免疫排斥等反应[16]。肠道免疫的效应部位主要是位于上皮内基底膜上的肠上皮内淋巴细胞(intestinal intraepithelial lymphocyte,iIEL)和位于固有层的淋巴细胞(lamina propria lymphocyte,LPL)。肠上皮内淋巴细胞是人体内最大的淋巴细胞群,是肠道免疫系统的重要组成部分。
肠上皮内淋巴细胞可通过Fas受体及穿孔素杀灭入侵的病原体和变性的上皮细胞,也能分泌一些细胞因子如白细胞介素22、白细胞介素24、白细胞介素25、肿瘤坏死因子2α、转化生长因子β来调节其他淋巴细胞与上皮细胞的功能。淋巴细胞主要包括CD4+T细胞和免疫球蛋白A+B细胞。前者可分泌下调免疫反应的细胞因子如白细胞介素10、转化生长因子β等,也能影响B细胞分泌免疫球蛋白A。
研究发现肠道菌群的鞭毛蛋白可刺激肠道固有层树突状细胞合成维甲酸[17],维甲酸又可诱导肠黏膜固有层B细胞的分化成熟而促进免疫球蛋白A。郝亚宁等[18]的实验研究发现双歧杆菌的免疫球蛋白A的阳性表达随着免疫后时间的增加而变化,双歧杆菌与抗原共同使
用,能增强机体黏膜免疫应答的能力。此外,乳酸杆菌是肿瘤坏死因子α和白细胞介素6强有力的诱导剂,可激活巨噬细胞功能,刺激机体产生免疫应答,通过巨噬细胞、T细胞、自然杀伤细胞活性的增强提高机体免疫[19]。加热灭活的双歧杆菌能刺激巨噬细胞产生过氧化氢、一氧化氮、白细胞介素6和肿瘤坏死因子α,尤其能刺激小鼠腹腔巨噬细胞白细胞介素6的分泌;嗜酸乳杆菌和瑞士乳杆菌能极显著提高感染大肠杆菌小鼠肠道内免疫球蛋白A和肠黏膜中白细胞介素2、白细胞介素4、白细胞介素6、干扰素γ的分泌量,对肠道黏膜免疫有一定的增强作用[20]。两歧双歧杆菌在体外研究中表现出较强的黏附性、抗炎能力,耐氧性双歧杆菌, 青春双歧杆菌属,或多形拟杆菌, 其中一种处理DCs, 通过减少CD4+效应T 细胞增殖和干扰素γ的分泌刺激原始T细胞成熟和发挥其功能[21]。
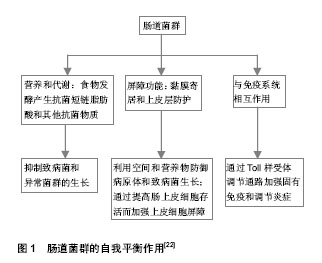
在正常情况下肠道微生物保持自我平衡的状态(肠道菌群的自我平衡作用见图1[22])。当肠道菌群与肠道免疫之间的动态平衡状态被打破后,一系列疾病将会随之发生。当肠道免疫功能下降时,肠道细菌,会出现过度繁殖、细菌移位。若肠道免疫系统失去对正常菌群某些抗原的耐受,肠道免疫被激活,肠黏膜通透性增高,导致致病菌及其抗原与黏膜下免疫细胞接触,发生免疫反应,使多种炎症细胞及免疫细胞增加和活化,同时释放多种炎性因子,使肠黏膜处于持续性低度炎症状态,导致肠道功能异常,影响机体对直肠扩张刺激的感觉阈值及内脏敏感性,诱发肠易激综合征的发生[23]。
近年来的研究证实,无论既往是否有胃肠炎病史,肠易激综合征患者肠黏膜均存在炎症细胞(肥大细胞、淋巴细胞等)浸润、细胞因子(肿瘤坏死因子、白细胞介素等)增多等肠黏膜免疫激活表现,Toll样受体4(该受体为连接先天性免疫及获得性免疫的桥梁)表达明显上调[24-25]。
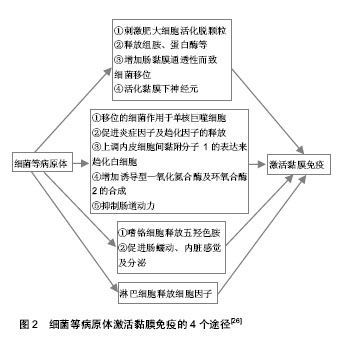
细菌等病原体可能通过以下4个途径激活黏膜免 疫[26]:①刺激肥大细胞活化脱颗粒,释放组胺、蛋白酶等,增加肠黏膜通透性而致细菌移位,活化黏膜下神经元。②移位的细菌作用于单核巨噬细胞,促进炎症因子及趋化因子的释放,通过上调内皮细胞间黏附分子1的表达来趋化白细胞,后者进一步增加诱导型一氧化氮合酶及环氧合酶2的合成,从而抑制肠道动力。③嗜铬细胞释放五羟色胺,促进肠蠕动、内脏感觉及分泌。④淋巴细胞释放细胞因子等(图2)。研究发现,部分肠易激综合征患者外周血肿瘤坏死因子α、白细胞介素1、白细胞介素6等细胞因子增加,结肠固有层上皮内淋巴细胞CD3、CD25细胞增加,黏膜活检发现存在非特异性炎症和增加的肥大细胞及中性粒细胞[27-28]。炎症细胞分泌的细胞因子和介质可能导致肠易激综合征症状的发生,已证实肠易激综合征存在促炎细胞因子的增加和抗炎性细胞因子的产生减少[29]。以核糖体RNA为基础的16S RNA等微生物技术可应用于肠道菌群在肠易激综合征发病中作用机制的研究,通过改变肠易激综合征肠道菌群的组成和阻止肠道炎症过程以及干扰肠道免疫系统的紊乱的治疗方法具有很好的前景。
3 讨论 Discussion
文章从肠道菌群及黏膜免疫角度探索艾灸治疗肠易激综合征效应机制的进行了思考。本课题组前期研究表明,艾灸治疗腹泻型肠易激综合征具有显著疗效,可明显改善腹泻型肠易激综合征患者常见临床症状如腹泻、腹痛、腹胀等,近期痊愈率为43.2%,总有效率为96%[30-31]。现代医学认为腹痛、腹胀的发病基础是胃肠道分泌、消化、吸收和运动等功能障碍。
前期研究结果表明,针灸上巨虚、天枢等穴治疗肠易激综合征,不仅能改善肠易激综合征患者的临床症状与体征,且能有效地纠正肠易激综合征肠道运动功能异常,降低肠易激综合征肠道高敏感性,能调节结肠黏膜异常升高的五羟色胺、前动力蛋白1/前动力蛋白受体1,发挥缓解内脏痛敏的镇痛作用[32-37],从而保持或恢复肠道的生理恒定性,重建机体免疫系统内环境的平衡及稳定。艾灸以多环节、多靶点的整合调节为特点,对肠易激综合征等肠腑病症的疗效已得到认可。
本课题组开展的另一项关于艾灸治疗溃疡性结肠炎的研究表明,艾灸可调节溃疡性结肠炎肠道有害菌和有益菌趋于平衡,是艾灸治疗溃疡性结肠炎的起效环节之一[2]。那么对于和溃疡性结肠炎同属于肠腑病症的肠易激综合征,艾灸的起效环节是否和调节肠道菌群有关以及调节的具体途径是怎样的,是值得探讨并深入研究的课题。作者认为可以从动物实验及临床两方面着手,借鉴现代生命科学的先进技术,结合微生物免疫学的研究进展,探讨:①艾灸对肠易激综合征患者肠道菌群构成,尤其是有益菌,有害菌的调控作用,筛选与艾灸特异性相关的肠道菌群生物标志物。②艾灸对免疫细胞及多种细胞因子表达的影响,寻找肠道菌群变化与黏膜免疫系统的相关性,阐释艾灸在维持肠道菌群和免疫稳态中发挥的作用。③从腧穴配伍(如“合募配穴”),不同灸法(如温和灸、隔物灸、麦粒灸)等角度,将经络、腧穴、辨证等中医特色理论与肠道菌群,肠道黏膜免疫相结合,为提高针灸治疗肠易激综合征的临床疗效提供理论基础和实验依据。
将灸法与现代生命科学技术相结合,为深入揭示灸法的作用机制提供新的思路与方法,也必将推动艾灸治疗肠易激综合征基础研究和临床治疗的发展。

