设计:以细胞为研究对象,随机分组。
时间及地点:于2012年9月2013年9月在华中科技大学同济医学院附属协和医院完成。
材料:
细胞培养:人单核细胞系THP-1按美国典型物培养中心(ATCC)的说明,在37 ℃、体积分数5%CO2条件下,接种于含体积分数10%胎牛血清的RPMI1640培养液中培养,隔天换液1次,培养至对数生长期。
|
THP-1单核细胞不同转染方法的比较实验所用试剂与仪器:
|
|
试剂与仪器
|
来源
|
|
人单核细胞系THP-1
|
上海细胞所
|
|
RPMI1640培养基、胎牛血清
|
Gibco公司
|
|
载体绿色荧光蛋白真核表达质粒(pEGFP-N1)
|
美国Clontech公司
|
|
DEAE-葡聚糖(二乙胺乙基葡聚糖,DEAE-Dextran)(相对分子质量500 000)
|
Pharmacia公司
|
|
阳离子脂质体Lipofectamine2000
|
美国Invitrogen公司
|
|
FuGENE 6(非脂质体配方)
|
瑞士Roche公司
|
|
阳离子聚合物梭华-sofast
|
厦门太阳马生物工程有限公司
|
|
质粒小量提取试剂盒
|
华舜公司
|
|
大肠杆菌(E.coli)DH5α
|
由本实验室保存
|
|
荧光倒置显微镜(IX70型)
|
日本Olympus
|
|
流式细胞仪(FACSort)
|
美国Becton Dickson公司
|
|
实验方法:
DEAE-Dextran法转染:具体步骤按参考文献[15]进行。转染前24 h,THP-1细胞浓度在1×109 L-1左右;置PBS、STBE、DEAE-Dextran于37 ℃水浴锅中预热;准备转染液:每1 mL STBE中,依次加入2.5 μg的样品DNA和 300 μg的DEAE-Dextran,温柔混匀;转染时,1 000 r/min 离心5 min,获得细胞沉淀,并用PBS洗2次;每(3-5)×106细胞用1 mL转染液重悬,置于37 ℃含体积分数5%CO2的培养箱中孵育20 min,每5 min混匀1次;离心去上清,用 PBS洗1次;1 500 r/min离心3-5 min,用不含血清的RPMI 1640洗1次,去掉残留的DEAE-Dextran,然后用含体积分数10%胎牛血清的RPMI1640重悬,置于37 ℃含体积分数5%CO2的培养箱中培养。
优化DEAE-Dextran法转染的不同剂量和孵育时间:转染前THP-1细胞浓度在1×109 L-1左右,转染时,THP-1细胞先用PBS洗2次,每(0.5-1.0)×106细胞在200 µL STBE中与0.5 μg质粒绿色荧光蛋白真核表达质粒、不同剂量的DEAE-Dextran混匀,37 ℃孵育不同时间,去掉残留的DEAE-Dextran,然后用正常培养基培养,24 h后收集细胞,观察指标。
比较DEAE-Dextran的不同促进剂:通过以上实验,选用DEAE-Dextran优化的剂量和孵育时间,转染后培养细胞4-6 h后,弃去培养液,加入不同促进剂,10%-20%甘油或二甲基亚砜溶液在室温孵育2.0-3.0 min,去除甘油或二甲基亚砜溶液,用PBS洗THP-1细胞2次,加培养基培养,或者按1∶1 000将100 mmol/L氯喹直接加入培养基中(氯喹终浓度100 μmol/L),孵育不超过2.5 h或出现细胞毒性前更换新鲜的培养基。
DEAE-Dextran预处理转染方法:THP-1细胞先用PBS洗2次,去除PBS,加入预先准备好的含300 mg/L DEAE-Dextran的STBE溶液,孵育20 min后。去除DEAE-Dextran,用PBS轻轻洗涤细胞2次。去除PBS,将预先准备好的含DNA的STBE溶液均匀滴加到细胞表面。细胞培养箱内孵育30 min,孵育期间经常摇动培养板以保持所有细胞湿润。最后缓慢加入细胞培养液(约稀释DNA的STBE溶液体积的10倍)继续培养。
Lipofectamine 2000试剂转染:具体步骤参见说明书。在准备混合液之前,以每孔(4-8)×105 THP-1细胞的密度接种于24孔培养板中,每孔加入0.5 mL含体积分数10%血清的RPMI1640(不含抗生素);对于要转染的每孔细胞,用 50 μL的Opti-MEM培养基稀释0.8 μg的DNA,用50 μL的 Opti-MEM培养基稀释2 µL Lipofectamine 2000,并在室温下孵育5 min。
一旦Lipofectamine 2000稀释完成后,30 min内必须和DNA溶液混合孵育;将稀释了的DNA和稀释了的 Lipofectamine 2000温柔混合,在室温下孵育20 min促使 DNA-Lipofectamine 2000混合物的形成;直接往每孔中加入DNA-Lipofectamine 2000混合物100 μL,并轻轻前后晃动培养板混匀;37 ℃、体积分数5%CO2、饱和湿度的CO2孵箱孵育4 h后,Opti-MEM更换为含体积分数10%血清的 RPMI1640中培养。
FuGENE 6试剂转染:具体步骤参见说明书。在准备混合液之前,以每孔(1-5)×105 THP-1细胞的密度接种于24孔培养板中,每孔加入0.5 mL含体积分数10%血清的RPMI1640(不含抗生素);对于要转染的每孔细胞,用20 μL的无血清培养基稀释0.6 µL的FuGENE 6,混匀,室温下孵育5 min;按照转染试剂∶DNA(μg)比例3∶1直接加入DNA,混匀并室温下孵育15 min;将以上混合液逐滴加入培养细胞的24孔板中,并轻轻前后晃动培养板混匀; 37 ℃、体积分数5%CO2、饱和湿度的CO2孵箱培养,无须更换新鲜培养基。但是,如果转染过程中需要用无血清培养基,那么可以在转染后孵育3-8 h,更换为含体积分数10%血清的RPMI1640中培养。
梭华-Sofast试剂转染:具体步骤参见说明书。在准备混合液之前,以每孔(4-8)×105 THP-1细胞的密度接种于24孔培养板中,每孔加入0.5 mL含体积分数10%血清的 RPMI1640(不含抗生素)。
梭华-Sofast/DNA复合物的制备:0.6 μg DNA质粒稀释于30 µL不含血清和抗生素的 Opti-MEM中,轻轻混匀;1.0-2.0 µL梭华-Sofast稀释于 30 µLOpti-MEM中,轻轻混匀;30 µL梭华-Sofast稀释液滴加到DNA稀释液中,一边滴加一边混匀。室温孵育 15-20 min。60 µL梭华- Sofast/DNA复合物加到每孔中并轻轻摇动使均匀混合。放置37 ℃、体积分数5%CO2、饱和湿度的CO2孵育箱孵育24-48 h后,分析报告基因转染效率。
荧光显微镜观察:于转染后在4-72 h内荧光显微镜下动态观察绿色荧光蛋白信号,阳性细胞发出明亮的绿色荧光,而阴性细胞则无。于48 h时进行显微细胞计数:每孔找3个具有代表性的视野,各观察100个细胞,计算阳性细胞的百分率。
流式细胞仪检测:于转染48 h后收集培养孔内细胞,用PBS漂洗,1 500 r/min离心5 min,混匀后采集样本,用FACSort流式细胞仪检测,每组取3个样本,每样本计数 10 000个细胞,并计算其阳性率。
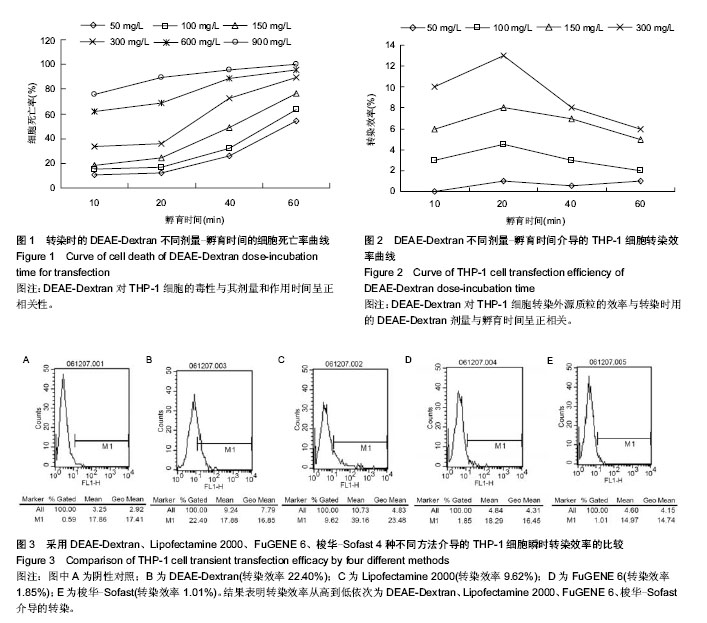
主要观察指标:①THP-1细胞用DEAE-Dextran处理后,在正常条件下生长24 h后用1%锥虫蓝染色15 min,然后用显微镜镜检,透明光亮圆形细胞为活细胞,被染上蓝紫色的细胞为死亡细胞,计数细胞死亡率,并用荧光显微镜和流式细胞仪检测转染效率。②比较DEAE-Dextran的不同剂量、孵育时间以及不同促进剂介导THP-1细胞瞬时转染的效率,从而优化DEAE-Dextran介导的THP-1细胞瞬时转染外源报告基因质粒表达的条件。③采用DEAE-Dextran、Lipofectamine 2000、FuGENE 6、梭 华-Sofast 4种不同方法转染THP-1细胞后,通过荧光显微镜下观察和流式细胞仪检测比较这4种不同转染方法的差异。