Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (30): 4890-4895.doi: 10.12307/2023.805
Previous Articles Next Articles
Synthesis and drug loading and delivery applications of chiral mesoporous silica nanoparticles
Yan Nan1, Wu Xuanjing2, Wang Ziqi2, Wu Jing2, Zhao Tongtong2, Xue Yan2, Zhao Weijie2, Wang Lijie2, Wu Zimei3, Zhang Wenqing4, Li Jing2
- 1College of Medical Applied Technology, 2School of Pharmacy, 3School of Basic Medicine, 4School of Public Health, Shenyang Medical College, Shenyang 110034, Liaoning Province, China
-
Received:2022-08-27Accepted:2022-11-23Online:2023-10-28Published:2023-04-03 -
Contact:Li Jing, MD, Associate professor, School of Pharmacy, Shenyang Medical College, Shenyang 110034, Liaoning Province, China -
About author:Yan Nan, MD, Associate professor, College of Medical Applied Technology, Shenyang Medical College, Shenyang 110034, Liaoning Province, China -
Supported by:National Natural Science Foundation of China, No. 82104114 (to LJ); Natural Fund of Liaoning Provincial Science and Technology Department, No. 2021-MS-350 (to LJ); Shenyang Science and Technology Plan Urban Governance Project, No. 21-108-9-11 (to YN); Shenyang Young and Middle Aged Scientific and Technological Innovation Talents Support Program, No. RC200238 (to YN); Liaoning Province Innovation Capacity Improvement Joint Fund Project, No. 2022-NLTS-14-06 (to YN)
CLC Number:
Cite this article
Yan Nan, Wu Xuanjing, Wang Ziqi, Wu Jing, Zhao Tongtong, Xue Yan, Zhao Weijie, Wang Lijie, Wu Zimei, Zhang Wenqing, Li Jing. Synthesis and drug loading and delivery applications of chiral mesoporous silica nanoparticles[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(30): 4890-4895.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
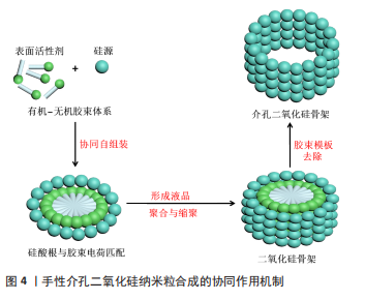
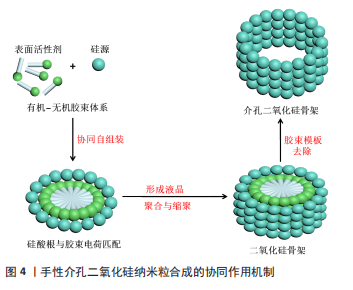
2.1 手性介孔二氧化硅纳米粒的合成 2.1.1 手性介孔二氧化硅纳米粒的合成条件 在微观尺度上,具有螺旋体形状的细菌在许多生物过程中具有优势。手性介孔二氧化硅纳米粒具有理想的拓扑结构[12]。1998年,OZIN研究团队首次报道了以硅酸盐为液晶模板时,其拓扑缺陷结构指导手性介孔二氧化硅纳米粒的合成[13]。自此,关于手性介孔二氧化硅纳米粒合成的研究与日俱增,这些研究都肯定了表面活性剂在手性介孔二氧化硅纳米粒合成中所起的重要结构导向作用。除此之外,模板也是一个不可或缺的合成条件。根据合成过程中所用的模板,可将手性介孔二氧化硅纳米粒的合成方法分为两类:硬模板法和软模板法。硬模板具有可控的形态和结构,易去除、高度有序且热稳定性好,一般为碳材料或无机粒子等结构刚性的固体材料[14];而软模板大多是两亲性分子形成的有序聚合体,其形状多样,无法控制产物的形状和尺寸,但该种方法操作简单、成本低廉,渐渐获得了人们的认可并应用[15]。手性介孔二氧化硅纳米粒被广泛用于对映选择性分辨率和手性化合物的吸附,具有理想的分离能力。在实际的合成操作中,常用的模板是表面活性剂、有机凝胶、金属纳米组分以及其他手性液晶相等,其中表面活性剂模板又分为阳离子型、阴离子型和非离子型3种。关于手性介孔二氧化硅纳米粒的制备,具有代表性研究包括:2010年,相关科研人员以两亲性分子为模板,通过溶胶-凝胶反应控制手性介孔二氧化硅纳米粒的形貌和介孔结构,得到了具有短孔道的手性介孔二氧化硅纳米带和纳米片[16];2015年,天津大学研究生路平超以非手性阳离子表面活性剂十六烷基三甲基溴化铵作为模板,正硅酸乙酯作为硅源,在极稀的氨水浓度下制备出了手性介孔二氧化硅纳米粒[17];2020年,有课题组以熊去氧胆酸/鹅去氧胆酸和阳离子表面活性剂十六烷基三甲基溴化铵为模板体系,合成了棒状手性介孔二氧化硅纳米粒[18];2021年,又有研究使用阳离子十六烷基三甲基溴化铵作为模板合成纳米颗粒,并使用L/D-酒石酸进行手性修饰的研究[19]。 2.1.2 手性介孔二氧化硅纳米粒的合成过程 手性介孔二氧化硅纳米粒的合成过程包括:表面活性剂的合成、手性介孔二氧化硅纳米粒的合成和表面活性剂的去除。上海交通大学博士靳海英[20]通过研究发现,酸与表面活性剂的摩尔比、共结构导向剂与表面活性剂的摩尔比、反应温度、表面活性剂的链长、不同的阳离子和阴离子,均对手性介孔二氧化硅纳米粒的介观结构和形貌有所影响。路平超[17]也通过研究发现,反应温度、搅拌速度、硅源和表面活性剂的用量对手性介孔二氧化硅纳米粒的形貌有影响。另外,不同的搅拌速度也会影响手性介孔二氧化硅纳米粒的合成。2013年,苏州大学的研究生蒲云月[21]以氟醇和十六烷基三甲基溴化铵作为双模板、正硅酸乙酯作为硅源,合成了手性介孔二氧化硅空心球,当氟醇与十六烷基三甲基溴化铵的摩尔比为0.4∶1、搅拌速度为 500 r/min 时,可得到外壁有介孔、内部有分层的手性介孔二氧化硅空心球;当搅拌速度为1 500 r/min 时,得到的也是类似的结构,但是外壁的介孔有序性没有前者的好,内部层数比前者的多;将不同搅拌速度条件下合成的手性介孔二氧化硅空心球于扫描电镜和透射电镜下观察,当搅拌速度为 500 r/min 时,得到是单层表面光滑的且一部分破碎的空心球,而随着搅拌速度的增加,球的表面变得不光滑,且里部的层数增加,进而得出结论:手性介孔二氧化硅空心球的层数随着搅拌速度的增加而增加。值得一提的是,2004年,上海交通大学CHE[22]教授及其课题组在《Nature》期刊上首次以手性阴离子小分子化合物十四碳-L-丙氨酸为结构导向剂、正硅酸乙酯作为硅源,通过协同自组装的方法制备了孔道高度有序的棒状手性介孔二氧化硅纳米材料,并报道了用透射电子显微镜分析手性介孔晶体结构的一般方法。 2.2 手性介孔二氧化硅纳米粒的成型机制 对于手性介孔二氧化硅纳米粒合成机制的相关研究也一直层出不穷,目前被广泛接受的是Stucky和霍启升提出的协同作用机制[23],该机制认为有机和无机物种通过协同组装最终形成了有序的排列结构。就合成手性介孔二氧化硅纳米粒的体系而言,硅酸根多聚体首先同表面活性剂通过电荷匹配作用在表面活性剂的表面层协同成核,形成有机-无机胶束聚集体,从而改变无机层的电荷密度,这使得表面活性剂的疏水链相互接近,无机物种和有机物种之间的电荷匹配控制表面活性剂的排列方式。反应的进行将改变无机层的电荷密度,整个有机和无机物种组成的固相也随之改变,最终的物相由反应进行的程度(无机部分的聚合程度)决定(图4)。"
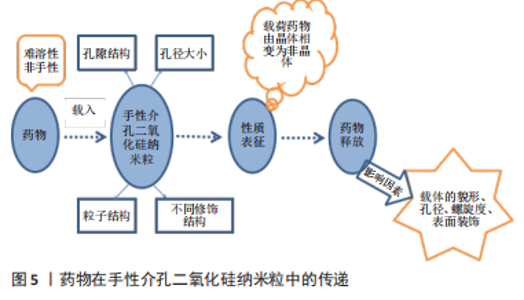
针对分子几何驱动模型,YANG等[13]曾合成具有六边形螺旋孔道的手性介孔二氧化硅纳米粒,他们从理论上揭示了特定介孔二氧化硅纳米结构形成的关键因素是硅酸盐晶种存在不同类型的拓扑缺陷。HAN等[24]以十六烷基三甲基溴化铵为模板,在不同碱性条件下成功合成了一系列具有不同螺旋度和螺旋形状的手性介孔二氧化硅纳米粒,以此来人为控制粒子的形状和螺旋度。在此基础上,有研究人员提出了熵驱动机制模型。除此之外,根据界面作用模型,手性介孔二氧化硅初生粒子间的头对头交联(即定向连接)发挥了关键性作用。KIM 等[25]认为手性介孔二氧化硅纳米粒手性形貌的产生与搅拌速度有关,研究表明泰勒涡所形成的剪切力也是螺旋结构形成的关键点。协同自组装机制也被广泛接受且用于阴离子表面活性剂模板的使用[26]。目前只有少数阴离子表面活性剂模板机制清晰透彻,还有很多表面活性剂模板的机制需要研究与探讨。除阳离子及阴离子表面活性剂外,有机凝胶模板、金属纳米组分模板和其他模板(如聚合物液晶模板),都在合成手性介孔二氧化硅纳米粒方面被广泛应用。有机凝胶模板可在适宜的合成条件下形成螺旋状聚合物。HAN等[27]成功制备由手性半胱氨酸修饰的金纳米棒为核、介孔二氧化硅为壳的核壳纳米结构,该研究发现,可通过改变金纳米棒组分的数目和长径比改变手性性能。SHOPSOWITZ等[28]利用自组装形成手性向列相结构的手性介孔二氧化硅纳米粒,该研究表明超手性分子水平自组装的影响条件主要是手性向列相液晶模板中层介晶的螺旋排列和硅源的静电相互吸引。 2.3 手性介孔二氧化硅纳米粒的性质 手性介孔二氧化硅纳米粒具有一般介孔二氧化硅纳米粒的性质[29-36],包括介孔结构、热稳定性、高比表面积和孔容、孔道可调性等。比表面积、孔容及孔径可用比表面分析仪进行测定,粒子的形貌和大小可采用扫描电子显微镜和透射电子显微镜进行测试,介孔结构可用小角X射线衍射、小角X射线散射和氮气吸附脱附等设备测试。手性介孔二氧化硅纳米粒的手性可体现在其手性形貌及手性结构,或者是通过嫁接手性小分子获得材料的分子级手性性能。手性介孔二氧化硅纳米粒的形貌可分为球形、椭球形、棒状、管状等[37],当手性介孔二氧化硅纳米粒具有手性形貌时,其表面呈现一定程度的扭曲条纹或者扭曲成螺旋形状。在手性介孔二氧化硅纳米粒中螺旋结构极其重要,有研究人员提出了“螺旋理论”[38],螺旋理论中主要阐述了各主要构象中存在的螺旋结构按方向、半径、螺距、螺仰角等,对于旋光性的贡献叠加和权重平均而得出的结果,从而定量地解释和预测手性物质的光学活性。2015年,天津大学研究生路平超[17]使用非手性阳离子表面活性剂十六烷基三甲基溴化铵作为模板、正硅酸乙酯作为硅源,在极稀的氨水浓度下制备出了手性介孔二氧化硅纳米粒,其形貌规整均匀,分散性良好,外形为棒状,头部浑圆,直径约为100 nm,长度约为350 nm,内部分布着与侧边平行的孔道,孔道直径在2.0-3.0 nm之间,孔大小为3.13 nm,比表面积为1 175 m2/g,孔容为0.986 cm3/g;透射电镜图显示样品表面存在间距一致的纹路分布,这种纹路分布是手性介孔二氧化硅纳米粒所特有的。其他手性性质如手性催化、手性识别和手性拆分等,被广泛应用于生物、化学、医学等方面。手性介孔二氧化硅纳米粒可通过自身的手性来催化不对称反应。SATO等[39]发现手性介孔二氧化硅纳米粒能够诱导烷基锌与醛类化合物的不对称反应。模板分子与硅前体接触时会形成多重作用点[40],聚合过程中这种作用点会被“记忆”下来,当模板去除后,聚合产物中便形成了许多空穴,这些空穴具有与模板分子空间构型相匹配的多重作用点,且对模板分子及其类似物具有选择识别性,因此可以手性识别和拆分对映异构体。 2.4 手性介孔二氧化硅纳米粒的载药递药性能 手性介孔二氧化硅纳米粒在药物递送系统应用研究中发挥着重要的作用,引起了人们的广泛关注。近些年来,人们发现这种纳米粒的载药研究主要与手性介孔二氧化硅纳米粒的孔隙结构、孔径大小、粒子结构以及不同的修饰结构等有关,见图5。"
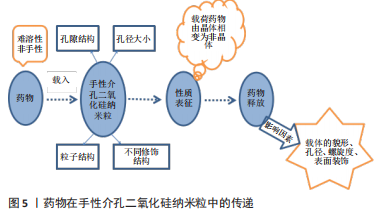
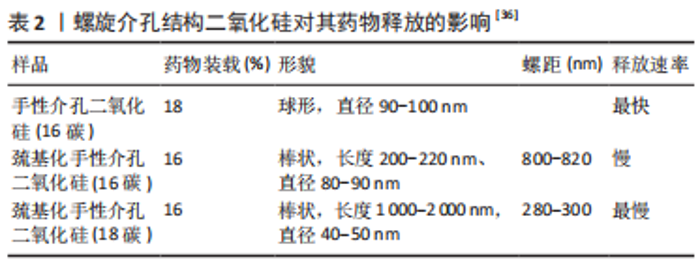
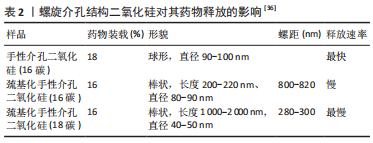
2.4.1 载体结构对载药递药能力的影响 手性介孔二氧化硅纳米粒具有有序介孔结构,同时它又属于介孔二氧化硅纳米粒,具有性能稳定、比表面积大、高孔容等性质,是作为治疗药物有效载体的不错选择。手性介孔二氧化硅纳米粒具有独特的手性性质,可体现在手性形貌及手性结构或者分子级别的手性修饰。手性介孔二氧化硅纳米粒在负载难溶性药物时可有效改善其包载能力,增大药物溶解度,进而提高生物利用度。一种以酒石酸和聚乙烯亚胺相关的手性晶体配合物为模板、支架和催化剂,在药物包载和药物释放方面都具有优势,载体因其独特的相互连通的弯曲孔道而显著提高了尼莫地平的释放量和口服吸附量,使其生物利用度提高3.26倍左右,有效延长小鼠脑缺氧存活时间10.98-17.33 min[41]。手性介孔二氧化硅纳米粒还含有扭曲的通道,可以容纳更多的药物分子,从而促进药物的负载[37]。 SPECTOR等[38]用氮气吸附解吸附分析测定手性介孔二氧化硅-3.0、手性介孔二氧化硅-1.5和手性介孔二氧化硅-1.0的等温线和孔径分布曲线,证实了高比表面积和孔容的载体更能有效包载药物,手性介孔二氧化硅-1.0的比表面积和孔容均大于手性介孔二氧化硅-3.0,其载药量更高;手性介孔二氧化硅-1.0和手性介孔二氧化硅-1.5差异不大,但手性介孔二氧化硅-1.0更具有优势;根据载药结果显示,手性介孔二氧化硅-1.0比其他两种介孔二氧化硅具有更高的载药量。王静等[40,42]为了研究螺旋介孔结构二氧化硅作为药物释放载体是否有用,他们选择不同形态和螺旋度但孔径与药物相似的手性介孔二氧化硅(16碳)和两种巯基化手性介孔二氧化硅,以阿司匹林为模型药物构建载药体系,采用体外药物溶出度进行测试。有研究者通过地西泮-手性介孔二氧化硅纳米粒载药体系的测试结果得知,手性介孔二氧化硅纳米粒包载药物可使药物以无定形的形式存在,因为手性介孔二氧化硅纳米粒的孔径能够直观地、有效地抑制药物结晶,使药物被包载后成非晶态相,所以在药物溶解度方面优于晶体药物,这也显著提高了药物的生物利用度[39,43]。 研究结果发现,螺旋介孔结构二氧化硅的形貌和螺旋度能影响药物释放速率,短而直的载体通道更有利于药物的释放,是药物载体的不错选择(表2)。"

2.4.2 修饰基团对载药递药能力的影响 手性介孔二氧化硅纳米粒可通过嫁接手性小分子实现其手性性质,亦可在具有手性形貌或手性结构的材料上进行表面基团修饰[5,44]。FAN等[8]通过嫁接手性小分子于二氧化硅骨架上合成了一种分子级左旋手性介孔二氧化硅纳米粒和右旋手性介孔二氧化硅纳米粒,并开展了两种载体载荷吲哚美辛的研究,结果表明,左旋手性介孔二氧化硅纳米粒的孔径和孔容略大于右旋手性介孔二氧化硅纳米粒,前者载药量也略高于后者,证实了该种手性介孔二氧化硅纳米粒的载药能力与载体的孔径和孔容有直接关系。此外,体外药物释放实验表明,左旋手性介孔二氧化硅纳米粒载荷吲哚美辛构建的给药系统,在添加左旋手性物质的介质中释放更快,这可能与吲哚美辛可以在载体右旋手性介孔二氧化硅纳米粒中更好地分散有关。在LI等[5]研究中,建立了以手性介孔二氧化硅纳米粒和氨基修饰手性介孔二氧化硅纳米粒为载体的吲哚美辛传递系统,两者都有很好的包载药物能力,但结果显示,氨基修饰的手性介孔二氧化硅纳米粒较手性介孔二氧化硅纳米粒拥有更高的溶出速率。两种吲哚美辛传递系统在包载药物时,都是将药物进行了非晶态相转化,这样负载引起了药物溶解度的改善,在肠道中的吸收也得到了良好改善。药物在体内的吸收因剂量不同而表现出不同的吸收方式。不同手性的介孔二氧化硅纳米粒在体内以不同的方式被吸收,将表现出差异性药理作用,有待研究者们开展一系列深入的机制探究。 2.5 手性介孔二氧化硅纳米粒的生物学评价 近年来,介孔二氧化硅材料得到了迅速发展,其研究已逐渐渗透到医学领域和生物系统[6],随之其生物安全性也成为了许多科研人员的研究重点。现有研究结果表明,对手性介孔二氧化硅纳米粒的研究尚未成熟,但手性介孔二氧化硅纳米粒是介孔二氧化硅纳米粒的分支之一,手性介孔二氧化硅纳米粒的一些基本生物学评价便可参考介孔二氧化硅纳米粒。 2.5.1 细胞毒性 根据现有研究,在人肝癌细胞和人脐静脉内皮细胞的手性介孔二氧化硅纳米粒细胞毒性实验中,将载体材料与测试细胞共孵育24 h后,手性介孔二氧化硅纳米粒不会产生显著的细胞毒性,因为即使在较高质量浓度(200 mg/mL)的情况下,实验对象仍能保持88%的细胞存活率。此外,手性介孔二氧化硅纳米粒对人脐静脉内皮细胞的毒性可以忽略不计。由于肝脏和肾脏是代谢和清除外源性物质的重要场所,因此,手性介孔二氧化硅纳米粒对肝脏和肾脏的影响也尤为重要。基于实验表明,手性介孔二氧化硅纳米粒摄入后对肝肾功能无异常影响,说明其在体内是安全的。因而可推测手性介孔二氧化硅纳米粒毒性可忽略不计[11]。在大鼠溶血实验中,手性介孔二氧化硅纳米粒和氨基修饰的手性介孔二氧化硅纳米粒的溶血率远低于10%,表明手性介孔二氧化硅纳米粒和氨基手性介孔二氧化硅纳米粒在血液循环中是安全的[5]。具有修饰基团的介孔二氧化硅纳米颗粒,通过模仿病毒表面穿透黏液层通过肠上皮的研究中没有表现出明显的毒性。而黏液层和肠上皮的障碍可以通过这些病毒模拟纳米颗粒有效地克服,用于口服难溶性药物的递送[45]。此外,介孔二氧化硅纳米粒作为阿霉素载体时并没有对其细胞毒性产生干扰,为手性介孔二氧化硅纳米粒的药效学研究提供了宝贵经验[46]。 2.5.2 生物相容性和降解 根据现有的一些研究表明,手性介孔二氧化硅纳米粒具有良好的生物可降解性和高生物相容性。手性介孔二氧化硅纳米粒在生物体内降解为硅酸后从肾脏排泄。此外,无论采用何种给药途径,纳米材料都有一定概率进入血液,因此血液相容性是生物安全性的考虑因素之一。研究表明,即使在800 mg/mL的质量浓度下,手性介孔二氧化硅纳米粒的溶血率仍低于5%,且手性介孔二氧化硅纳米粒中的极性羧基对溶血性无影响。由此可知,手性介孔二氧化硅纳米粒不会造成严重的溶血情况,并且具有良好的血液相容性,对红细胞不会产生破坏[11]。一些研究表明,润湿性与介孔二氧化硅纳米粒的结构和孔径密切相关,所以生物相容性和降解主要由润湿性决定。在模拟生理环境下,手性介孔二氧化硅纳米粒可在2-13周的时间内完全降解,并且当表面具有大量单键羟基时表现出高润湿性、高降解、低脑部分布能力[47]。降解过程作为一种界面反应,理论上比表面积和孔径较大的粒子可有效降低降解过程中的表面反应屏障,但通过实验发现,与介孔二氧化硅纳米粒相比,比表面积和孔径较小的手性介孔二氧化硅纳米粒的降解速率更快,此结果与之前的研究恰好相反[11]。 手性介孔二氧化硅纳米粒的生物安全性仍是当今社会的热门话题,现有科学成果可说明手性介孔二氧化硅纳米粒具有生物可降解性、高生物相容性和较低毒性,但其形态、粒径和孔径等生物安全性的关键影响因素需进一步研究,以便于广泛在医学领域和生物系统实践与应用。"

| [1] SHAKERAN Z, KEYHANFAR M, VARSHOSAZ J, et al. Biodegradable nanocarriers based on chitosan-modified mesoporous silica nanoparticles for delivery of methotrexate for application in breast cancer treatment. Mater Sci Eng C Mater Biol Appl. 2021;118:111526. [2] REN XN, CHENG S, LIANG Y, et al. Mesoporous silica nanospheres as nanocarriers for poorly soluble drug itraconazole with high loading capacity and enhanced bioavailability. Micropor Mesopor Mat. 2020; 305:110389. [3] NAUMOVA KA, DEMENT’EVA OV, SENCHIKHIN IN, et al. Mesoporous silica particles based on complex micelles of poorly water-soluble compounds. One simple step to multidrug carriers. Micropor Mesopor Mat. 2021;316:110911. [4] LIU RZ, WANG X, FAN N, et al. Superiority of Chiral-handed mesoporous silica nanoparticles in delivering Nimesulide. Mater Sci Eng B-Adv. 2021;269:115161. [5] LI J, GUO YG, LI H, et al. Superiority of amino-modified chiral mesoporous silica nanoparticles in delivering indomethacin. Artif Cell Nanomed B. 2018;46(5):1085-1094. [6] CHENGYI LI, HUNG R, PHARMACY SO, et al. Research progress of biodegradable inorganic mesoporous nanomaterials. J Pharm Res. 2017;36(4):222-225. [7] MARTINEZ-CARMONA M, CELA C, KUZNETSOVA VA, et al. Enantioselective effect of cysteine functionalized mesoporous silica nanoparticles in U87 MG and GM08680 human cells and Staphylococcus aureus bacteria. J Mater Chem B. 2021;9(16):3544-3553. [8] FAN N, LIU RZ, MA PP, et al. The On-Off chiral mesoporous silica nanoparticles for delivering achiral drug in chiral environment. Colloids Surf B Biointerfaces. 2019;176:122-129. [9] DAI X, MA J, CHEN N, et al. MSNs-Based Nanocomposite for Biofilm Imaging and NIR-Activated Chem/Photothermal/Photodynamic Combination Therapy. ACS Appl Bio Mater. 2021;4(3):2810-2820. [10] WU JW, SU P, HUNG J, et al. Synthesis of teicoplanin-modified hybrid magnetic mesoporous silica nanoparticles and their application in chiral separation of racemic compounds. J Colloid Interface Sci. 2013; 399(3):107-114. [11] HU BB, WANG JX, LI J, et al. Superiority of L-tartaric Acid Modified Chiral Mesoporous Silica Nanoparticle as a Drug Carrier: Structure, Wettability, Degradation, Bio-Adhesion and Biocompatibility. Int J Nanomedicine. 2020;15:601-608. [12] WANG YM, KE J, GUO XM, et al. Chiral mesoporous silica nano-screws as an efficient biomimetic oral drug delivery platform through multiple topological mechanisms. Acta Pharm Sin B. 2022;12(3):1432-1446. [13] YANG H, OZIN GA, KRESGE CT. The Role of Defects in the Formation of Mesoporous Silica Fibers, Films, and Curved Shapes. Adv Mater. 1998;10(11):883-887. [14] BECK JS, VARTULI JC, ROTH WJ, et al. A new family of mesoporous molecular sieves prepared with liquid crystal templates. J Am Chem Soc. 1992;114(27):10834-10843. [15] CHEN JF, DING HM, WANG JX, et al. Preparation and characterization of porous hollow silica nanoparticles for drug delivery application. Biomaterials. 2004;25(4):723-727. [16] YAN ZJ, LI BZ, WANG SB, et al. Preparation of mesoporous silica nanoribbons and nanoflakes with short pore channels using a chiral amphiphile. J Nanosci Nanotechnol. 2010;10(10):6732-6738. [17] 路平超.手性/空心棒状介孔纳米二氧化硅的制备[D].天津:天津大学,2015. [18] JIANG X, CUI MS, ZHANG W, et al. Design of chiral mesoporous silica nanorods using ursodeoxycholic acid/chenodeoxycholic acid and CTAB as templates for chiral-selective release of achiral drugs. Mater Lett. 2021;285:129144. [19] WU LL, GOU KJ, GUO XM, et al. Dual response to pH and chiral microenvironments for the release of a flurbiprofen-loaded chiral self-assembled mesoporous silica drug delivery system. Colloids Surf B Biointerfaces. 2021;199:111501. [20] 靳海英.手性阴离子表面活性剂结构导向法合成手性介孔材料[D].上海:上海交通大学,2009. [21] 蒲云月.手性介孔二氧化硅的制备及应用[D].苏州:苏州大学,2014. [22] CHE SN, LIU Z, OHSUNA T, et al. Synthesis and characterization of chiral mesoporous silica. Nature. 2004;429(6989):281-284. [23] SUN Q, KOOYMAN PJ, GROSSMANN JG, et al. The formation of well‐defined hollow silica spheres with multilamellar shell structure. Adv Mater. 2003;15(13):1097-1100. [24] HAN Y, ZHAN L, YING JY. Entropy-Driven Helical Mesostructure Formation with Achiral Cationic Surfactant Templates. Adv Mater. 2007;19(18):2454-2459. [25] KIM WJ, YANG SM. Helical Mesostructured Tubules from Taylor Vortex-Assisted Surfactant Templates. Adv Mater. 2001;13(15):1191-1195. [26] ZHANG L, QIAO SZ, JIN YG, et al. Hydrophobic functional group initiated helical mesostructured silica for controlled drug release. Adv Funct Mater. 2008;18(23):3834-3842. [27] HAN B, SHI L, GAO X, et al. Ultra-stable silica-coated chiral Au-nanorod assemblies: Core–shell nanostructures with enhanced chiroptical properties. Nano Res. 2016;9(2):451-457. [28] SHOPSOWITZ KE, QI H, HAMAD WY, et al. Free-Standing Mesoporous Silica Films With Tunable Chiral Nematic Structures. Nature. 2010; 468(7322):422-425. [29] 王宁.基于介孔氧化硅纳米粒子的表面修饰与功能化研究[D].上海:中国科学院大学(中国科学院上海硅酸盐研究所),2018. [30] SUN LJ, WANG DG, CHEN Y, et al. Core-shell hierarchical mesostructured silica nanoparticles for gene/chemo-synergetic stepwise therapy of multidrug-resistant cancer. Biomaterials. 2017;133:219-228. [31] QIU HB, CHE SN. Chiral mesoporous silica: Chiral construction and imprinting via cooperative self-assembly of amphiphiles and silica precursors. Chem Soc Rev. 2011;40(3):1259-1268. [32] VEGA E, MARZABADI C, KAZAKEYICH Y, et al. Synthesis of chiral mesoporous silicas with oligo(saccharide) surfaces and their use in separation of stereoisomers. J Colloid Interface Sci. 2011;359(2):542-544. [33] YOKOI T, OGAWA K, LU D, et al. Preparation of Chiral Mesoporous Materials with Helicity Perfectly Controlled. Chem Mater. 2011;23(8): 2014-2016. [34] QIU HB, INOUE Y, CHE SN. Supramolecular Chiral Transcription and Recognition by Mesoporous Silica Prepared by Chiral Imprinting of a Helical Micelle. Angew Chem Int Ed Engl. 2009;48(17):3069-3072. [35] YOKOI T, YAMATAKA Y, ARA Y, et al. Synthesis of chiral mesoporous silica by using chiral anionic surfactants. Micropor Mesopor Mat. 2007; 103(1-3):20-28. [36] LIU WJ, ZHU ZN, KE D, et al. Gold nanorod@chiral mesoporous silica core-shell nanoparticles with unique optical properties. J Am Chem Soc. 2013;135(26):9659. [37] 汤兑海. 介孔二氧化硅纳米材料的合成及其在催化和药物释放方面的应用[D].长春:吉林大学,2012. [38] SPECTOR MS, PRICE RR, SCHNUR JM. Chiral Lipid Tubules. Adv Mater. 1999;11(4):337-340. [39] SATO I, KADOWAKI K, URABE H, et al. Highly enantioselective synthesis of organic compound using right-and left-handed helical silica. Tetrahedron Lett. 2003;44(4):721-724. [40] 王静,刘爽,张春,等.手性纳米二氧化硅的制备和应用[J].化学进展,2011,23(4):669-678. [41] XIN W, WANG YM, BIAN Y, et al. Facile synthesis of PEI-based crystalline templated mesoporous silica with molecular chirality for improved oral delivery of the poorly water-soluble drug. Drug Deliv. 2021;28(1):894-905. [42] GAO ZB, LV XQ, FU YF, et al. Chiral mesoporous silica synthesized by a facile strategy for loading and releasing poorly water-soluble drug. Drug Dev Ind Pharm. 2020;46(7):1177-1184. [43] 王健鑫,柯佳,王玉美,等.手性介孔二氧化硅载体对地西泮溶出行为的改善[J].实用药物与临床,2019,22(12):1299-1302. [44] WANG X, LI C, FAN N, et al. Amino functionalized chiral mesoporous silica nanoparticles for improved loading and release of poorly water-soluble drug. Asian J Pharm Sci. 2019;14(4):405-412. [45] ZHANG Y, XIONG MT, NI XM, et al. Virus-Mimicking Mesoporous Silica Nanoparticles with an Electrically Neutral and Hydrophilic Surface to Improve the Oral Absorption of Insulin by Breaking Through Dual Barriers of the Mucus Layer and the Intestinal Epithelium. ACS Appl Mater Interfaces. 2021;13(15):18077-18088. [46] LI J, DU XT, ZHENG N, et al. Contribution of carboxyl modified chiral mesoporous silica nanoparticles in delivering doxorubicin hydrochloride in vitro: pH-response controlled release, enhanced drug cellular uptake and cytotoxicity. Colloids Surf B Biointerfaces. 2016;141:374-381. [47] LI H, WU XQ, YANG BX, et al. Evaluation of biomimetically synthesized mesoporous silica nanoparticles as drug carriers: structure, wettability, degradation, biocompatibility and brain distribution. Mater Sci Eng C Mater Biol Appl. 2019;94:453-464. [48] GOU KJ, WANG YM, XIE LL, et al. Synthesis, structural properties, biosafety and applications of chiral mesoporous silica nanostructures. Chem Eng J. 2020;421:127862. [49] CUI MS, ZHANG W, XIE LY, et al. Chiral mesoporous silica materials: A review on synthetic strategies and applications. Molecules. 2020; 25(17):3899. |
| [1] | Zhao Shuai, Li Dongyao, Wei Suiyan, Cao Yijing, Xu Yan, Xu Guoqiang. Biocompatibility of poly(vinylidene fluoride) piezoelectric bionic periosteum prepared by electrospinning [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(4): 730-737. |
| [2] | Liu Hanfeng, Wang Jingjing, Yu Yunsheng. Artificial exosomes in treatment of myocardial infarction: current status and prospects [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1118-1123. |
| [3] | Yin Tong, Yang Jilei, Li Yourui, Liu Zhuoran, Jiang Ming. Application of core-shell structured nanofibers in oral tissue regeneration [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 766-770. |
| [4] | Liu Anhong, Cai Mengmeng, Han Xiao, Wang Zhanhui. Research status on element selection of medical magnesium alloy [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 777-782. |
| [5] | Tian Xin, Liu Tao, Yang Huilin, He Fan. In vitro evaluation of sustained release Kartogenin by gelatin methacryloyl microspheres for repairing nucleus pulposus degeneration [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 724-730. |
| [6] | Tan Junjie, Du Jiaheng, Wen Zhenyu, Yan Jiyuan, He Kui, Duan Ke, Yin Yiran, Li Zhong. Antibacterial magnesium oxide-calcium phosphate composite coating prepared by combining electrodeposition and sol-gel impregnation [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(29): 4663-4670. |
| [7] | Zheng Heishu, Zhang Yingjuan, Wei Yanhua, Huang Hui, Ma Xiangyu, Liao Hongbing. Antibacterial performance of cerium oxide nanoenzyme against Escherichia coli [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(22): 3496-3501. |
| [8] | Chen Mingxue, Niu Jianhua, Lin Haiyan, Wu Gang, Wan Ben. Physicochemical properties and cytocompatibility of biomimetically precipitated nanocrystalline calcium phosphate granules [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(22): 3502-3508. |
| [9] | Tang Ziniu, Chu Fengcheng, Wu Kang, Zhang Lin, Bai Yanjie, Lin Xiao, Yang Huilin, Zhou Huan, Liu Huiling, Yang Lei. Application of strontium polyphosphate with both radiopaque and osteogenic functions in calcium phosphate cement [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(22): 3539-3547. |
| [10] | Ilham • Maimaitiabudula, Huang Xiaoxia, Li Luyao, Teng Yong. Polymer-based antibiotic sustained-release carrier in treatment of chronic osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(22): 3597-3602. |
| [11] | Liu Chang, Li Linhua, Fu Ping . Research and development of nanoparticles with active targeting ability in nonneoplastic kidney disease [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(22): 3603-3608. |
| [12] | Wang Xindong, Liang Chengzhi, Zhang Yongxian. Functional characteristics and clinical applications of MXene nanoparticles in wound healing [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(17): 2739-2746. |
| [13] | Zhang Shuzhi, Qu Pengfei, Han Junquan, Wang Hong. Research and application of electrospinning drug delivery systems containing traditional Chinese medicine [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(17): 2759-2765. |
| [14] | Guo Yuxin, Wang Hao, Li Mingqi, Chen Yueying, Pan Juhong, Huang Xin, Wang Zhiwen, Zhou Qing. Ultrasound-optimized hydrogel scaffold used to promote transdermal delivery of gold nanoparticles [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(15): 2330-2337. |
| [15] | Lyu Shangyi, He Huiyu, Wufanbieke · Baheti, Yang Quan, Ma Lisha, Han Xiangzhen. Physicochemical properties and biocompatibility of graphene oxide-hydroxyapatite composite coating materials [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(10): 1477-1483. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||

