Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (34): 5544-5551.doi: 10.12307/2021.253
Previous Articles Next Articles
Analysis methods and transdermal absorption of collagen peptides
Hua Jinglin, Xie Yingying, Xu Heran, Zhang Xiaona, Wang Min
- School of Chemistry and Materials Engineering, Beijing Technology and Business University, Beijing 100048, China
-
Received:2020-07-29Revised:2020-07-30Accepted:2020-09-20Online:2021-12-08Published:2021-07-28 -
Contact:Wang Min, MD, Associate professor, School of Chemistry and Materials Engineering, Beijing Technology and Business University, Beijing 100048, China -
About author:Hua Jinglin, Master candidate, School of Chemistry and Materials Engineering, Beijing Technology and Business University, Beijing 100048, China
CLC Number:
Cite this article
Hua Jinglin, Xie Yingying, Xu Heran, Zhang Xiaona, Wang Min. Analysis methods and transdermal absorption of collagen peptides[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(34): 5544-5551.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

2.1 胶原蛋白与胶原蛋白肽的结构 胶原蛋白又称胶原,是由3条具有独立性的左手螺旋α-肽链通过紧密缠绕而形成的右旋三重结构,结构中二硫键、氢键的相互作用保障了胶 原的机械强度[3-4]。组成胶原结构的3条肽链可以相同(同源三聚体),也可以不同(异源三聚体),异源三聚体胶原蛋白更为常见。胶原蛋白肽是胶原蛋白水解的产物,成分组成与胶原蛋白一致,它们的区别在于胶原蛋白是高分子且具有三螺旋空间结构,而胶原蛋白肽是小分子。明胶也是胶原蛋白水解的产物,不同之处在于明胶的水解条件是高温部分水解,其不具备生物活性且分子质量更大,在15 000-250 000 Da之间。胶原蛋白及其水解产物之间的关系和结构变化如图2所示。"

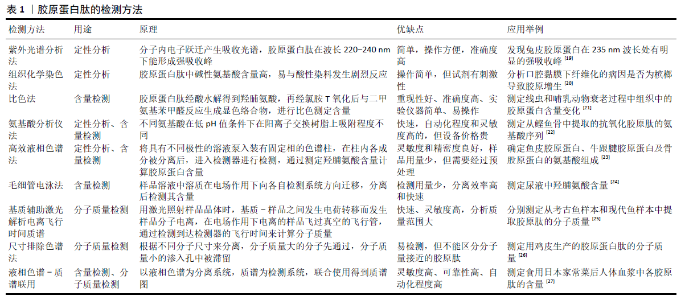
胶原蛋白及胶原蛋白肽中含有甘氨酸-X-Y重复序列,甘氨酸(Gly)是三肽中的固定组成,X、Y位可以是任意氨基酸,以脯氨酸(Pro)和羟脯氨酸(Hyp)居多,所以胶原蛋白中甘氨酸占比最高,且含有丰富的脯氨酸和羟脯氨酸,含有少量的半胱氨酸(Cys)和色氨酸(Trp)及特有的羟赖氨酸(Hyl)[5]。利用这一特性可对胶原及胶原肽进行定性和定量分析检测。 2.2 胶原蛋白肽的来源及制备 胶原蛋白肽的获取方式主要有以下3种:从天然生物体中提取;化学合成及重组DNA技术;体外胶原蛋白水解[6]。科学研究中往往需要特定结构或功能的胶原肽,若该胶原肽难以采用人工合成或人工合成复杂费力时,就会选择从天然生物体中提取的方法。ELANGO等[7]为获得成骨潜能更优异的胶原肽,选择直接从马哈鱼骨中提取天然胶原蛋白肽。然而天然生物体含有的活性肽含量很少,目前主要应用于实验研究,很难进行大批量工业生产。化学合成法及重组DNA技术多用于合成药理级肽或长肽但成本较高。体外胶原蛋白水解法是将胶原蛋白水解成分子质量较低的多肽,是当前主流的制备胶原蛋白肽的方式。 体外胶原蛋白水解法通常有3个步骤:原料预处理、胶原蛋白提取、胶原蛋白水解[8]。原料预处理的目的是去除非胶原物质,破坏三螺旋结构以便提取胶原蛋白,其中用氢氧化钠预处理最为常见[9]。胶原蛋白提取的目的是提高水解敏感性和胶原蛋白纯度,提取方式有酶提法、酸提法、碱提取法、热水提取法和盐提法[10]。胶原蛋白水解的方法分为酶解法、化学法、亚临界水水解法。化学法利用酸或碱断开肽键,反应偏剧烈,易影响肽的活性,且用碱性试剂在水解过程中易发生消旋作用,产生有毒物质。亚临界水水解法利用亚临界状态下的水做催化剂水解蛋白质生成肽,不引入其他化学物质,反应时间短,但需要先进的设备[11]。酶解法利用酶水解蛋白质生成肽,反应条件温和、得率高、环境污染小[12],因此酶解法是工业上最常用的水解胶原蛋白的方法。 酶解法又分为3种:单酶酶解法、分步酶解法、混合酶解法[13]。实验室中研究胶原肽特性时常会用到酶解法制备胶原肽,MEI等[14]以鲑鱼和罗非鱼皮为原料,用碱性蛋白酶将其酶解得到的胶原肽可促进创面愈合;JEEVITHAN等[15]用芽孢杆菌耐热蛋白酶将鲸鲨软骨胶原蛋白酶解得到低分子质量胶原蛋白肽,并用电泳分离出来3种不同分子质量的胶原肽。 2.3 胶原蛋白肽分析方法 在科研或工业化生产过程中往往需要对所制备的胶原蛋白肽进行定性和定量分析检测,包括测定胶原肽含量、分子质量等。胶原蛋白肽作为胶原蛋白水解产物,可根据胶原蛋白的检测方法进行分析。 胶原蛋白肽的定性分析方法主要有紫外光谱分析法、胶原纤维染色法和磷酸盐缓冲盐溶液检测法等[16]。在某些特定情况下需要鉴定特殊状态的胶原蛋白肽,所用方法也有所不同,例如在胶原疾病学领域需要准确检测出带有电荷的胶原蛋白肽。SUN等[17]利用石墨烯氧化物辅助构建了一种聚合诱导发射探针,该探针对带电荷的胶原肽具有高度选择性,且不受其他生物分子的干扰。 羟脯氨酸是胶原蛋白及胶原蛋白肽的特异氨基酸,在一般动物蛋白质中不存在或者含量很低,因此常根据羟脯氨酸的含量乘以换算系数计算胶原蛋白含量[18]。不同来源胶原肽羟脯氨酸含量不同,换算系数也不同。利用羟脯氨酸测定胶原肽含量的方法有比色法、氨基酸分析仪法、高效液相色谱法、毛细管电泳法等,其中比色法、电泳法较多用于含量检测,而氨基酸分析仪法和高效液相色谱法还可用于分析胶原蛋白的氨基酸组成。 胶原蛋白水解产物成分复杂,分子质量分布较广,人们利用现代分析检测方法对胶原蛋白肽进行分子质量的检测和控制。胶原蛋白肽分子质量检测方法有凝胶电泳法、尺寸排除色谱法、高效液相色谱与电喷雾-质谱联用、液相色 谱-质谱联用、基质辅助激光解析电离飞行时间质谱,其中基质辅助激光解析电离飞行时间质谱具有快速、灵敏度高,分析质量范围大的优点,被作为检测胶原蛋白水解物分子质量的最佳方法。 胶原蛋白肽的检测方法众多,原理和应用侧重各不相同,上述检测方法的原理、优缺点及应用实例如表1所示。"


2.4 胶原蛋白肽的功能特性及应用 2.4.1 胶原蛋白肽在生物医药中的应用 胶原蛋白肽因其良好的生物相容性和低免疫原性在生物医药领域上应用广泛。临床研究表明,胶原蛋白肽具有降血压、保护胃黏膜、有助于术后恢复等功效。血管紧张素转换酶是一种外肽酶,在血管紧张素Ⅰ转化为血管紧张素Ⅱ的过程中起到催化的作用,并能使缓激肽失活,与高血压的发病密切相关[28]。陈胜军 等[29]通过双酶复合水解罗非鱼鱼皮胶原蛋白制得了抑制血管紧张素转换酶活性的胶原肽,体外对血管紧张素转换酶的抑制率可达68.6%。FAHMI等[30]以鲷鱼鱼鳞为原料,使用碱性蛋白酶进行处理并水解为胶原蛋白肽,使自发性高血压的大鼠口服300 mg/kg,结果表明胶原肽对于血管紧张素转换酶活性有抑制作用,且起到降低血压的作用。甄润英等[31]探究了羊骨胶原肽对实验性高血压大鼠血压和血脂的影响,结果表明在不影响心率的条件下,通过给予羊骨胶原肽能起到降血压的作用,对血脂无明显影响。 胶原蛋白能够活化细胞功能,可以加速血红蛋白和红细胞生成,常被应用于术后恢复和创伤愈合,可用作严重烧伤治疗中的人造皮肤替代物,原料来源包括牛、猪、马或人类,有时与硅酮、糖胺聚糖、成纤维细胞、生长因子和其他物质一起使用。ZHANG等[32]通过体外抓痕实验和家兔深层部分烫伤创面实验探究尼罗罗非鱼皮肤胶原蛋白肽在伤口护理中的应用,发现该胶原肽具备较好的促创面愈合活性。CHEN等[33]发现,从阿拉斯加鳕鱼皮中提取的胶原蛋白肽可对小鼠烧伤后的肠道起到保护作用。MASHIKO等[34]采用新型重组人胶原蛋白肽支架作为生物材料载体进行细胞再生治疗,实验结果表明该支架表现出与细胞因子相似的调节细胞生长和免疫生物学作用,可作为局部生物材料敷料和干细胞及血管内皮细胞的生物载体,用于修复因放射治疗损伤的细胞或组织。 胶原蛋白肽因其优良特性在医学领域上应用广泛。人体自身的骨骼、肌肉、软组织、血管等组织结构都富含胶原蛋白,因此补充胶原肽可作为骨骼、肌肉、血管损伤修复或疾病预防的辅助治疗剂。ELANGO等[7]从马哈鱼骨中直接提取了一种具有良好成骨性能的胶原蛋白肽,实验发现该胶原蛋白肽可促进骨髓间充质干细胞的增殖分化,通过蛋白质和mRNA表达情况发现骨髓间充质干细胞中碱性磷酸酶、骨钙素等成骨生物标志物水平显著上升,进一步阐明该胶原蛋白肽具有成骨作用的假说。医学上一般使用雌激素治疗骨质疏松症,但GAO等[35]发现钙螯合胶原多肽治疗骨质疏松症的效果显著优于雌激素,且钙螯合胶原多肽更安全,无不良反应,该实验对象为去卵巢大鼠。PHILLIPS等[36]研究发现,男性老年肌肉萎缩症患者每天连续摄入15 g的胶原蛋白肽可使增肌训练取得更好的效果。LGASE等[37]通过实验证明,每天坚持摄入一定量的猪肉胶原蛋白肽有助于预防老年人动脉硬化。 胶原蛋白复合材料在生物医学领域已经应用成熟,尤其在骨组织工程方面。胶原蛋白肽复合材料的研究近些年初见成效,水凝胶一直被广泛应用于伤口愈合领域,壳聚糖/胶原肽/氧化魔芋复合水凝胶[38]、羟甲基壳聚糖/胶原肽/氧化魔芋复合水凝胶等具有优异的生物相容性[39],且安全性高、经济适用性好,在创面敷料上具有广阔的应用前景。鱼胶原蛋白肽/透明质酸水凝胶等可作为性能优异、价格实惠的组织工程支架[40]。胶原蛋白肽与金属螯合物在生物医学方面也有应用。刘安军等[41]发现胶原蛋白肽-铬(Ⅲ)螯合物对小鼠肝脏内超氧化物歧化酶的提高有所帮助。胶原肽-铁螯合物可以作为一种易于消化吸收且生物利用率高的补铁剂[42]。 胶原蛋白肽还有许多其他处于探索阶段的功能。WOO等[43]证实了从鳐鱼皮中提取的胶原蛋白肽通过抑制脂肪积累和调节脂质代谢等途径发挥减脂作用,但该实验对象为小鼠,在人体能否发挥减脂功效需要进一步验证。WANG等[44]从鸡胸软骨中提取了具有抗炎、抗氧化和抑制软骨细胞凋亡作用的胶原蛋白肽。通过文献调研发现,当前胶原蛋白肽在医学领域研究的实验对象大部分是动物或细胞,初步证明了胶原肽在内科、外科和骨科等领域的巨大潜力,但在人体上是否能达到同样的效果还有待商榷,如何应用于人体还需进一步的深入研究和探索。 2.4.2 胶原蛋白肽在食品中的应用 在食品工业中胶原蛋白肽可作为肉类、糖果和乳制品等的食品添加剂,用于改善食品的口感,延长保质期和保持颜色。NGUYEN等[45]用亲和吸附法从猪皮肤胶原蛋白水解物中分离出一种独特的胶原肽,只需添加3 g/L的该猪皮胶原肽就能显著改善被冷冻4周后面团的烘焙和质地特性,结果表明该猪皮胶原肽具较强的抗冻和低温保护活性,在食品保鲜等方面有潜在应用价值。 市售胶原肽类保健品的功能主要集中在促进软骨再生、强健骨骼、补充钙质及预防骨质疏松。胶原蛋白肽含有大量的甘氨酸和脯氨酸,摄入人体后可促进软骨细胞中生成大量的Ⅱ型胶原蛋白和蛋白多糖,二者对刺激软骨再生及受损软骨修复具有重要作用。骨骼的主要成分是胶原和羟基磷酸钙,补充胶原蛋白肽可有效抑制骨骼强度的降低,维持骨骼机 能[46]。此外,胶原蛋白的羟脯氨酸可以把血浆中的钙运输到骨细胞。单纯补钙而不注重胶原蛋白的摄入,无法达到防治骨质疏松的目的。蒋挺大[47]提出补钙要建立在补足胶原蛋白的基础上,当人体摄入足够的胶原蛋白就能在一定程度上保证正常的钙质需求量。 市场上还有很多可以改善皮肤状态、减少皱纹的胶原蛋白饮品。DO-UN等[48]实验证明通过口服一种胶原蛋肽 (1 000 mg/d,共12周)有效改善了40-60岁女性群体的光老化皮肤健康;摄入6周后显著改善了皮肤水合作用,摄入12周后皮肤皱纹减少、弹性增加,而且该胶原蛋白肽制剂可以被受试者很好地耐受。 2.4.3 胶原蛋白肽在化妆品中的应用 胶原蛋白及胶原蛋白肽有抗氧化、保湿、美白等功效,是化妆品原料研究的热点。水产动物中提取的胶原蛋白肽与人皮肤胶原蛋白的结构相似,与皮肤有很好的相容性,且其有甘氨酸等天然保湿因子,可渗透进表皮层滋养皮肤,位于胶原分子外侧的大量亲水基团可与角质层中的水结合锁住水分,使之具有良好的保湿功效[49]。李幸[50]研究发现,利用鳕鱼皮制备不同分子质量的胶原蛋白水解物均能有效抑制水分和透明质酸流失,且能消除自由基,有效缓解皮肤粗糙、胶原纤维减少、松弛等问题,同时水解物的分子质量越小效果越明显。KANG等[51]发现口服胶原蛋白肽可缓解紫外线照射引起的皮肤水分流失和产生皱纹等皮肤问题。 不少文献中都有对动物来源的胶原蛋白和多肽的抗氧化及延缓衰老的功效进行了研究。郭德斌等[52]研究了湿法粉碎并用碱性蛋白酶水解获得鸭皮胶原蛋白肽的抗氧化活性,当添加质量浓度为16 g/L时,其羟基自由基清除能力、还原力和氮自由基清除力分别为65.22%,79.36%和77.45%。BENJAKUL等[53]比较了不同水解过程对用石斑鱼皮所生产的胶原蛋白肽抗氧化活性的影响,结果表明两步法可提高胶原蛋白肽的产率、羟脯氨酸回收率、α-氨基含量和抗氧化活性,因此通过适当的水解、干燥等工艺组合可以得到抗氧化胶原蛋白肽。 胶原蛋白肽具有美白作用的原因是:其酪氨酸残基可同皮肤中的酪氨酸共同竞争与酪氨酸酶活性中心结合的机会,以此抑制酪氨酸酶对皮肤中酪氨酸的催化作用,阻止皮肤中黑色素形成,达到美白的目的。同时胶原蛋白肽可以增加皮肤弹性,从而减少光散射形成的阴影现象,提高皮肤的亮度,达到美白效果[54]。 现今化妆品市场中的胶原和胶原肽产品种类繁多,有许多添加了胶原和胶原肽的面膜、眼霜和护霜。在国外也有胶原蛋白肽在美容方面的一些深入研究,有实验证明0.01%小分子胶原蛋白肽原液就有较好的抗辐射作用,且能形成良好的保水层,提供皮肤所需水分[55]。 胶原蛋白肽产品在行业中也存在着一些问题,比如有些企业推出产品时涉嫌夸大宣传,宣称的功能与产品本身不符,如逆生长,而有的产品实际所含胶原蛋白含量与宣传不符,如2013年有报道指出,Fancl胶原蛋白果味饮料中的胶原含量远低于宣称的量,甚至在汤某倍健胶原蛋白粉未检出胶原蛋白的特征氨基酸——羟脯氨酸[56]。胶原蛋白肽产品仍存在着安全风险,动物源病毒、细菌、毒素使得动物各类组织作为获取胶原蛋白肽来源的风险增大,所以一定要严格把控胶原蛋白肽原料制备中的安全风险问题,必须严格遵守行业中的相关标准规范。 2.4.4 胶原蛋白肽产品的发展趋势 近年来,各类媒体的宣传使得消费者对胶原蛋白的认知逐渐加深,添加胶原蛋白已经成为不少相关产品的卖点,然而吸收性更胜一筹的胶原蛋白肽还未被国内消费者熟知,当前市场上的胶原蛋白肽产品主要集中于保健品和美容护肤行业,若要增强市场竞争力,未来胶原蛋白肽需向创新型和高品质型方向发展。 市场上胶原蛋白肽产品众多,但产品品质参差不齐。国内于2020-06-29新发布的《化妆品监督管理条例》规定了化妆品的功效宣称应当有充分的科学依据,这要求企业不仅应关注产品的使用安全性,更需要重视其宣称的功效性。当敷料或化妆品等将胶原蛋白肽作为主要功效原料时,透皮吸收的效果对其功效发挥有极大的影响,因此探究如何提升胶原蛋白肽的透皮吸收性能并对其进行有效科学的评价极为重要。 2.5 胶原蛋白肽的透皮吸收 2.5.1 透皮吸收概论 皮肤由表皮、真皮、皮下组织、皮脂腺和汗腺组成[57]。皮肤限制物质进出的屏障作用主要来源于角质层的紧密结构,小分子物质、兼具脂溶性和水溶性的物质更易于渗透,一些特定物质可自由穿过角质层[58]。 一般情况下,特定药品中的药物成分可通过透皮吸收到达血液,进入体循环,而化妆品的透皮吸收大多只能停留在表皮层。在使用过程中化妆品的功效成分作用于皮肤表面或者到达不同皮肤层,在该部位积聚并发挥功效性作用的过程即为透皮吸收。与药物“透皮吸收”不同,化妆品功效性成分是以积聚并作用在皮肤层为最终目的,不需要进入体循 环[59]。 透皮吸收主要有角质层、毛囊、汗管及皮脂腺4条途径,其中毛囊、汗管和皮脂腺常被称为旁路途径,因为皮肤附属器与整个皮肤表面积的比不足1%,难以通过角质层的大分子物质和离子型物质可以经这3个途径进入皮肤。角质层透皮途径又可分为2种:细胞间途径与跨细胞途径。 细胞间途径:化学物质通过角质细胞间连续分布的细胞间质透入皮下。虽然细胞间隙面积只有角质层面积的0.01%-1%,但因其疏松的结构,容积可达角质层容积的30%左右。该途径的主要阻力来源于细胞间隙的脂质,阻力小于跨细胞途径,所以在经皮渗透中起主要作用,通常脂溶性、非极性物质易通过此途径扩散。 跨细胞途径:化学物质直接穿过角质细胞和细胞间隙。角质细胞是已死亡的扁平无核细胞,它的细胞膜是致密的交联网状蛋白架构,胞内含大量整齐排列的微丝角蛋白和丝蛋白,这两者都不利于化学物质扩散,但因其占有较大的扩散面积,该途径仍有重要作用。一般认为,水溶性和极性物质容易从角质细胞经皮渗透[59]。 透皮吸收理论主要有扩散理论、渗透压理论、水合理论、相似相溶理论和结构变化理论[60],如表2所示。不同的透皮吸收机制从不同的角度解释皮肤屏障打开的过程,同时它们互补互足、相辅相成。 2.5.2 胶原蛋白肽常用透皮评价方法 扩散池法:目前应用最为广泛的体外评价方法,其步骤如下:将离体皮肤或人工皮肤模型固定在扩散池上,将实验样品溶解作为供给液添加到供给池内,使皮肤角质层与供给液充分接触,皮肤底面与接受池中的接收液充分接触,定时收取接收液进行分析,最后通过计算透皮率来评价试验样品的透皮吸收性[62]。扩散池可分为动态和静态两类:静态扩散池的代表是Franz扩散池和Valia-Chien(V-C)扩散池,此类扩散池组成结构简单,出现故障的概率低;动态扩散池是在静态扩散池的基础结构上增加了由进口管、出口管和接收池组成的动态流动系统,更能模拟真实的生理条件[63]。应用在透皮吸收实验中的离体皮肤来源包括动物、人体及三维重组皮肤模型,由于法律法规和人伦道德的约束,人类离体皮肤较难获得,而三维重组皮肤模型成本高且不含毛囊、汗腺等结构,所以常用动物皮肤进行实验。一般大鼠、小鼠离体皮肤选自腹部或背部,猪离体皮肤常选自耳部或腹部[64]。用扩散池法评价胶原蛋白肽的透皮吸收时,常用胶原蛋白肽对离体皮肤的累积渗透量或透皮速率作为评价透皮性能的指标。 刘楚怡等[65]用酶解法分别将海蜇、牛骨和鳕鱼皮胶原制备成不同分子质量(<1 kD和1-3 kD)的胶原肽,利用扩散池法考察时间、分子质量和质量浓度对胶原蛋白肽透皮吸收的影响,研究结果表明:①6种胶原肽的单位面积累积透过量(Q)均随时间延长而增大,透皮速率都随时间延长而下降,且在质量浓度均为10 g/L时24 h内透皮吸收能力由小到大为鳕鱼皮胶原肽(1-3 kD)、牛骨胶原肽(1-3 kD)、海蜇胶原肽(1-3 kD)、海蜇胶原肽(<1 kD)、牛骨胶原肽(<1 kD)、鳕鱼皮胶原肽(<1 kD);②胶原蛋白肽分子质量越大,透皮吸收能力小;③海蜇和牛骨胶原肽随质量浓度增加透皮吸收能力增大,而鳕鱼皮胶原肽随着质量浓度增加累积透过量减小,推测是因为胶原肽的黏性随着质量浓度增加而增大减慢了透皮过程。 ZHANG等[66]用扩散池系统检测了鹿筋胶原蛋白水解物对小鼠皮肤透皮作用中经皮蛋白质含量和经皮速率,研究结果表明鹿筋胶原蛋白水解物对小鼠表皮和真皮有渗透作用,相对渗透率为8%,接收池中采集24 h鹿筋胶原蛋白水解物的分子质量分布为5-13 Da,占比91.55%。 胶带剥离技术光谱法:角质层作为皮肤的屏障,将待测物质涂抹于皮肤一段时间后,使用胶带粘贴获得皮肤角质层,再分析胶带中特定物质的含量。该方法可以实现同一时间内研究同一志愿者多个取样点的透皮吸收情况,但不适用于测定具有快速挥发性和快速渗透性的样品。万青华[67]使用胶带剥离技术考察L-抗坏血酸布洛芬酯和布洛芬在猪皮角质层中的渗透分布情况,检测胶带上L-抗坏血酸布洛芬酯和布洛芬的含量发现,L-抗坏血酸布洛芬酯穿过皮肤角质层的速度和深度均大于布洛芬,证明经皮外用给药时L-抗坏血酸布洛芬酯更有优势。 光谱法:可对透皮吸收进入角质层中的化合物进行快速、无创的直接测定。随着光谱方法和成像技术的不断完善,共聚焦拉曼光谱法、傅里叶变换红外光谱法和荧光寿命显微成像法等实时的检测方法在透皮吸收中的应用越来越广泛,但并不是每种物质都有适合的光谱检测波段和特征峰,所以光谱法还存在着问题[61]。 共聚焦拉曼显微镜可以追踪进入皮肤的特殊物质,更有针对性地检测目标物透皮吸收情况,但要求这个物质的拉曼光谱具备一定特殊的峰值。尹雅宁等[68]实验发现,皮肤组织真皮层内胶原蛋白的拉曼特征峰为1 248 cm-1。LIU等[69]用共聚焦拉曼光谱法测定了熊果苷的皮肤穿透深度及穿透量。目前用共聚焦拉曼显微镜测胶原蛋白肽透皮吸收的研究还比较少,尤其是对于特定范围分子质量的目标物定量检测较难准确实现,但这是一个理论可行的方法,还需进一步实验探索。 荧光寿命显微成像法是将已标记过的胶原肽涂敷在动物皮肤上,一段时间后取下相应的皮肤,冷冻切片,置于荧光显微镜下观测胶原肽在皮肤内的扩散路径。另外,生物电子显微镜可直接观察样品涂抹前后的皮肤模型超微结构,并对比分析样品对皮肤超微结构的影响,以此评价透皮传输效 果[70]。刘楚怡等[65]将<1 kD和1-3 kD的牛骨胶原肽进行异硫氰酸荧光素标记后,取一定量的胶原肽水溶液于无纺布上,固定在已脱毛的小鼠皮肤上,待各样品分别作用15,30,60,120 min后取下小鼠皮肤冷冻切片,固定后在荧光显微镜下观察不同时间的荧光分布,进而直观反映胶原肽在皮肤中的透皮吸收过程。 生物组织中具有长程非中心对称的分子可产生很强的二次谐波,如胶原蛋白、弹力纤维等,因此可利用真皮层中胶原的二次谐波信号作为皮肤组织的结构内参,进行样品的皮肤吸收定位。孙娅楠等[71]用二次谐波结合双光子荧光成像方法成功观察到胶原蛋白肽透皮吸收深度。 功效检测法:通过化妆品的使用功效来评价其透皮传输效果,这是一种近似“反推法”。林婕等[70]用Lab法和红黑色素检测法对比含有促渗剂与不含促渗剂产品配方的美白效果,从而评价促渗剂对于美白功效成分的促渗作用。胶原蛋白肽具有美白、保湿、缓解皱纹等作用,可测涂抹胶原肽产品前后皮肤水分含量、经皮水分散失、Lab值、皱纹深度、皱纹面积等差异来反推其透皮吸收性能。 目前,已有许多对不同来源胶原蛋白肽透皮吸收的研究,但实际应用的研究方法仍主要借鉴药物经皮渗透的研究方法。为研究胶原蛋白肽透皮吸收具体情况,可以尝试将不同的检测方法和分析手段联用,从而对胶原肽在皮肤中的存留时间、降解后的去向及代谢途径进一步探究。"

| [1] 陈华,易湘茜,陈忻,等.海洋胶原蛋白肽的制备及生物活性研究进展[J].中国食物与营养,2010(8):57-60. [2] 宋芹,陈封政,颜军,等.一种胶原蛋白寡肽体外透皮吸收性能研究[J].成都大学学报(自然科学版),2011,30(1):8-10,14. [3] WU S, KANG H. Advances in research and application of fish scale collagen. J Agric Sci Technol. 2017;18(12):2543-2546,2553. [4] 石金扣.水解胶原蛋白分子量控制技术的研究[J].科学与财富, 2019(2):36. [5] 焦道龙,陆剑锋,张伟伟,等.水产动物胶原蛋白的研究现状及发展趋势[J].食品科学,2009,30(17):334-338. [6] 贾雪婷,孙佳明,张辉.从生物体中获得胶原蛋白的研究进展[J].吉林中医药,2013,33(10):1034-1035,1048. [7] ELANGO J, ROBINSON J, ZHANG J, et al. Collagen peptide upregulates osteoblast genesis from bone marrow mesenchymal stem cells through MAPK- Runx2. Cells-Basel. 2019;8:446-461. [8] HONG H, FAN H, CHALAMAIAH M, et al. Preparation of low-molecular-weight, collagen hydrolysates (pep-tides): Current progress, challenges, and future perspectives. Food Chem X. 2019;301:1-10. [9] LIU D, WEI G, LI T, et al. Effects of alkaline pretreatments and acid extraction conditions on the ac-id-soluble collagen from grass carp (Ctenopharyngodon idella) skin. Food Chem. 2015;172(apr.1):836-843. [10] 刘俊佳.胶原蛋白肽产业现状及发展趋势[J].养生保健指南, 2019(7):321. [11] POWELL T, BOWRA S, COOPER HJ. Subcritical water hydrolysis of peptides: Amino acid side-chain modifications. J Am Soc Mass Spectrom. 2017;28(9):1775-1796. [12] 朱德誉,公维洁,卓先勤,等.鱼皮胶原蛋白肽的制备与应用研究进展[J].农产品加工,2019(7):84-85,89. [13] 张崟,郭思亚,熊伟,等.胶原蛋白酶解制备肽工艺研究进展[J].中国调味品,2018,43(2):89-95. [14] MEI F, LIU J, WU J, et al. Collagen peptides isolated from Salmon salar and Tilapia nilotica skin ac-celerate wound healing by altering cutaneous microbiome colonization via up-regulated NOD2 and BD14. J Agric Food Chem. 2020:1-27. [15] JEEVITHAN E, JINGYI Z, BAO B, et al. Biocompatibility assessment of type-II collagen and its polypep-tide for tissue engineering: effect of collagen’s molecular weight and glycoprotein content on tumor necro-sis factor (Fas/Apo-1) receptor activation in human acute T-lymphocyte leukemia cell line. RSC Adv. 2016;6:14236-14246. [16] 袁野,李佳林.胶原蛋白检测方法研究进展[J].明胶科学与技术, 2014(4):16-21. [17] SUN X, QIAO Y, LI W, et al. A graphene oxide-aided triple helical aggregation-induced emission biosensor for highly specific detection of charged collagen peptides. J Mater Chem B. 2020;8(6):1-8. [18] 邓浩,党政,尹青春,等.胶原蛋白的研究进展[J].广州化工,2019, 47(18):27-30. [19] 马明思,张宇昊,马良,等.兔皮胶原蛋白的微观结构及不同因素对其聚集特性的影响[J].食品与机械,2017,33(2):11-16. [20] KANNEGANTI S, KATTAPPAGARI KK, TANUJA K, et al. Oral submucous fibrosis: Clinical and histopathological correlation of collagen fibers using Masson’s trichrome and Van Gieson stains. J Dr NTR Univ Health Sci. 2018;7(3):181. [21] TEUSCHER AC, STATZER C, PANTASIS S, et al. Assessing collagen deposition during aging in mammalian tissue and in Caenorhabditis elegans. New York, Humana Press, 2019:169-188. [22] DING D, DU B, ZHANG C, et al. Isolation and identification of an antioxidant collagen peptide from skipjack tuna (Katsuwonus pelamis) bone. RSC Adv. 2019;9(46):27032-27041. [23] GAUZA-WŁODARCZYK M, KUBISZ L, WŁODARCZYK D. Amino acid composition in determination of collagen origin and assessment of physical factors effects. Int J Biol Macromol. 2017;104:987-991. [24] 冯刚,温群英,王洪海.柱前衍生-毛细管电泳法测定尿液中的羟脯氨酸[J].理化检验-化学分册,2016,52(8):879-883. [25] RICHTER KK, MCGRATH K, MASSON-MACLEAN E, et al. What’s the catch? Archaeological application of rapid collagen-based species identification for Pacific Salmon. J Archaeol Sci. 2020;116:105-116. [26] HONG H, ROY BC, CHALAMAIAH M, et al. Pretreatment with formic acid enhances the production of small peptides from highly cross-linked collagen of spent hens. Food Chem. 2018;258:174-180. [27] ASAI T, TAKAHASHI A, ITO K, et al. Amount of collagen in the meat contained in Japanese daily dishes and the collagen peptide content in human blood after ingestion of cooked fish meat. J Agric Food Chem. 2019;67(10):2831-2838. [28] 曾丽,李丽,王加斌,等.水产胶原蛋白肽功能活性及其制备工艺研究进展[J].浙江海洋学院学报(自然科学版),2013,32(2):163-168. [29] 陈胜军,李来好,曾名勇,等.罗非鱼鱼皮胶原蛋白降血压酶解液的制备与活性研究[J].食品科学,2005,26(8):229-233. [30] FAHMI A, MORIMURA S, GUO HC, et al. Production of angiotensin Ⅰ converting enzyme inhibitory peptides from sea bream scales. Process Biochem. 2004;39(10):1195-1200. [31] 甄润英,马俪珍,姜帆,等.羊骨胶原肽对实验性高血压大鼠血压和血脂的影响[J].营养学报,2008,30(5):512-514,519. [32] ZHANG H, PING Y, ZHOU C, et al. Marine collagen peptides from the skin of Nile tilapia (Oreochromis niloticus): Characterization and wound healing evaluation. Mar Drugs. 2017;15(4):102. [33] CHEN Q, GAO X, ZHANG H, et al. Collagen peptides administration in early enteral nutrition intervention attenuates burn-induced intestinal barrier disruption: Effects on tight junction structure. Funct Food. 2019; 55:167-174. [34] MASHIKO T, TAKADA H, WU SH, et al. Therapeutic effects of a recombinant human collagen peptide bioscaffold with human adipose‐derived stem cells on impaired wound healing after radiotherapy. Tissue Eng Regen Med. 2018;12(5):1186-1194. [35] GAO W, SHEN Y, CHENG Z, et al. Comparison of the ameliorating effect of collagen peptide chelated calcium and estrogen on the bone quality in ovariectomized rats. Zhongguo Shi Yan Dong Wu Xue Bao. 2017; 25(3):256-262. [36] PHILLIPS SM, TIPTON KD, VAN LOON LJC, et al. Exceptional body composition changes attributed to collagen peptide supplementation and resistance training in older sarcopenic men. J Nutr. 2016;116(3): 569-570. [37] LGASE M, KOHARA K, OKADA Y, et al. A double-blind, placebo-controlled, randomised clinical study of the effect of pork collagen peptide supplementation on atherosclerosis in healthy older individuals. Biosci Biotechnol Biochem. 2018;82(5):893-895. [38] LIU L, WEN H, RAO Z, et al. Preparation and characterization of chitosan–collagen peptide/oxidized konjac glucomannan hydrogel. Int J Biol Macromol. 2018;108:376-382. [39] ZHANG C, YANG X, HU W, et al. Preparation and characterization of carboxymethyl chitosan/collagen peptide/oxidized konjac composite hydrogel. Int J Biol Macromol. 2020;149:31-40. [40] 魏志君,施春英,程连强,等.鱼胶原蛋白肽-透明质酸水凝胶制备及其生物相容性[J].青岛大学学报(医学版),2017,53(5):600-603. [41] 刘安军,王维君,曹东旭,等.胶原蛋白多肽-铬(Ⅲ)螯合物对小鼠肝脏SOD表达的影响[J].食品研究与开发,2007,28(12):22-25. [42] 蔡冰娜,陈忻,潘剑宇,等.响应面法优化鳕鱼皮胶原蛋白肽螯合铁工艺[J].食品科学,2012(2):48-52. [43] WOO M, SONG YO, KANG KH, et al. Anti-obesity effects of collagen peptide derived from skate (Raja kenojei) skin through regulation of lipid metabolism. Mar Drugs. 2018;16(9):306-318. [44] WANG J, LUO D, LIANG M, et al. Spectrum-effect relationships between high-performance liquid chromatography (HPLC) fingerprints and the antioxidant and anti-inflammatory activities of collagen peptides. Molecules. 2018;23(12):3257-3274. [45] NGUYEN CT, YUAN M, YU JS, et al. Isolation of ice structuring collagen peptide by ice affinity adsorption, its ice binding mechanism and bread making performance in frozen dough. J Food Biochem. 2018;42(3):1-9. [46] 郭兆锋,刘爱青.水解胶原蛋白在保健食品和化妆品中的应用进展(一)[J].中国生物美容,2009(4):70-73. [47] 蒋挺大.胶原蛋白[M].北京:化学工业出版社,2001. [48] DO-UN K, HEE-CHUL C, JIA C, et al. Oral intake of low-molecular-weight collagen peptide improves hydration, elasticity, and wrinkling in human skin: A randomized, double-blind, placebo-controlled study. Nutrients. 2018;10(7):826-839. [49] JAYACHANDRAN V, SUKUMARAN A, SE-KWON K, et al. Marine fish proteins and peptides for cosmeceuticals: A review. Mar Drugs. 2017; 15:142-160 [50] 李幸.鳕鱼皮胶原肽保湿护肤效果的研究[D].青岛:中国海洋大学,2014. [51] KANG MC, YUMNAM S, KIM SY. Oral intake of collagen peptide attenuates ultraviolet B irradiation-induced skin dehydration in vivo by regulating hyaluronic acid synthesis. Int J Mol Sci. 2018;19(11): 3551-3563. [52] 郭德斌,苏婷,郭振,等.鸭皮胶原蛋白肽的制备及抗氧化活性[J].浙江农业科学,2019,60(7):1226-1229,1233. [53] BENJAKUL S, KARNJANAPRATUM S, VISESSANGUAN W. Production and characterization of odorless ant oxidative hydrolyzed collagen from seabass (Lates calcarifer) skin without descaling. Waste Biomass Valorization. 2018;9(4):549-559. [54] HSU KC, KIM HC, PARK SI, et al. Cosmetic composition for whitening and improving the resilience of skin[P]. U.S.: 9770404B2, 2017-9-26. [55] 天津市天大天福生物技术有限公司.一种胶原蛋白及胶原多肽的提取方法及在化妆品中的应用[P].中国:201711079709, 2018-03-23.http://cprs.patentstar.com.cn/Search/Detail?ANE=7CDA4DBA6DCA8ABA4CBA9DGADEIA9DDF2A AABHHAAEFA7FCA [56] 《京华时报》.胶原蛋白含量不符无添加丸美等7大品牌或虚假宣传[J].广西质量监督导报,2013(10):10-10. [57] WERTZ PW. Lipids and barrier function of the skin. Acta Derm Venereol. 1999; 208:7-11. [58] BARTOSOVA L, BAJGAR J. Transdermal drug delivery in vitro using diffusion cells. Curr Med Chem. 2012;19:4671-4677. [59] 林婕,何聪芬,董银卯.化妆品功效成分的透皮吸收途径与技术[J].中国化妆品,2009(2):90-97. [60] 林婕,何聪芬,董银卯.化妆品功效成分的透皮吸收机理[J].日用化学工业,2009,39(4):275-278. [61] 宋艳青,盘瑶,赵华.化妆品透皮吸收试验方法概述[J].日用化学工业,2019,49(12):824-829,838. [62] HOLMGAARD R, BENFELDT E, NIELSEN JB. Percutaneous penetration: methodological considerations. Basic Clin Pharmaco Toxicol. 2014; 115(1): 101-109. [63] RUELA ALM, PERISSINATO AG, LINO MES, et al. Evaluation of skin absorption of drugs from topical and transdermal formulations. J Pharm Sci. 2016;52(3):527-544. [64] VAN GELE M, GEUSENS B, BROCHEZ L, et al. Three-dimensional skin models as tools for transdermal drug delivery: Challenges and limitations. Expert Opin Drug Deliv. 2011;8(6):705-720. [65] 刘楚怡,隋海松,车帅,等.海蜇、牛骨和鳕鱼皮胶原肽的透皮吸收性能研究[J].日用化学工业,2017,47(3):164-167,177. [66] ZHANG H, PAN D, DONG Y, et al. Transdermal permeation effect of collagen hydrolysates of deer sinew on mouse skin, ex vitro, and antioxidant activity, increased type I collagen secretion of percutaneous pro-teins in NIH/3T3 cells. J Cosmet Dermatol. 2020;19(2):519-528. [67] 万青华.L-抗坏血酸布洛芬酯(L-AI)的表面化学及皮肤渗透研究[D].无锡: 江南大学,2016:1-39. [68] 尹亚宁,王爽,龚宇泽,等.皮肤组织显微共聚焦拉曼光谱成像研究[J].激光生物学报,2016,25(5):391-397. [69] LIU J, YANG L, PANG J, et al. Research on skin penetration of β-arbutin by confocal Raman spectroscopy. China Surfactants Deterg Cosmet. 2019;49(7):452-455. [70] 林婕,何聪芬,董银卯.化妆品中的透皮传输[J].中国美容医学, 2009,18(8):1197-1200. [71] 孙娅楠,赵静,李超华,等.二次谐波结合双光子荧光成像方法观察人源胶原蛋白透皮吸收情况[J].激光生物学报,2017,26(1):24-29. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [3] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [4] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [5] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [6] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [7] | Jiang Hongying, Zhu Liang, Yu Xi, Huang Jing, Xiang Xiaona, Lan Zhengyan, He Hongchen. Effect of platelet-rich plasma on pressure ulcers after spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1149-1153. |
| [8] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [9] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [10] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [11] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [12] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [13] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [14] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [15] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||