Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (11): 1765-1771.doi: 10.12307/2022.363
Previous Articles Next Articles
Regulatory role and mechanism of non-coding RNA on steroid-induced osteonecrosis of the femoral head
Huang Yangjun, Zhou Honghai, Chen Longhao, Li Jilin, Lu Qingwang, Li Dongyang, He Xinyu
- School of Orthopedics and Traumatology, Guangxi University of Traditional Chinese Medicine, Nanning 530001, Guangxi Zhuang Autonomous Region, China
-
Received:2021-01-04Revised:2021-01-18Accepted:2021-03-07Online:2022-04-18Published:2021-12-13 -
Contact:Zhou Honghai, MD, Professor, Chief physician, School of Orthopedics and Traumatology, Guangxi University of Traditional Chinese Medicine, Nanning 530001, Guangxi Zhuang Autonomous Region, China -
About author:Huang Yangjun, Master candidate, School of Orthopedics and Traumatology, Guangxi University of Traditional Chinese Medicine, Nanning 530001, Guangxi Zhuang Autonomous Region, China Chen Longhao, Master, School of Orthopedics and Traumatology, Guangxi University of Traditional Chinese Medicine, Nanning 530001, Guangxi Zhuang Autonomous Region, China Huang Yangjun and Chen Longhao contributed equally to this work. -
Supported by:the National Natural Science Foundation of China (Regional Project), No. 81660800 (to ZHH)
CLC Number:
Cite this article
Huang Yangjun, Zhou Honghai, Chen Longhao, Li Jilin, Lu Qingwang, Li Dongyang, He Xinyu. Regulatory role and mechanism of non-coding RNA on steroid-induced osteonecrosis of the femoral head[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(11): 1765-1771.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
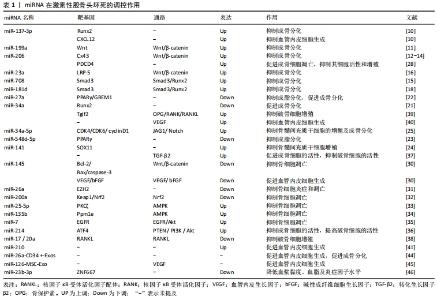
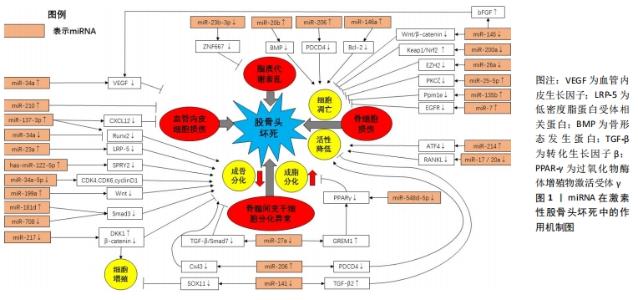
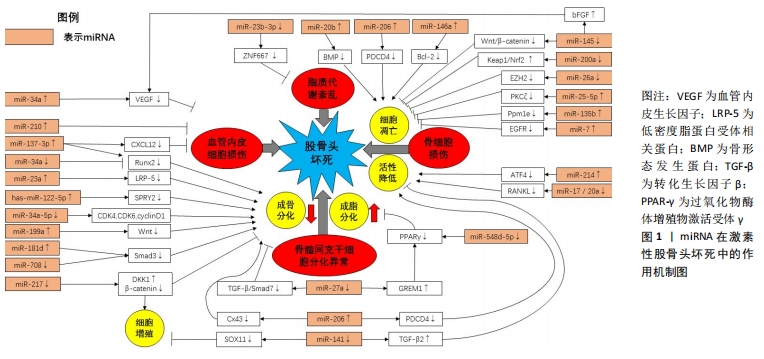
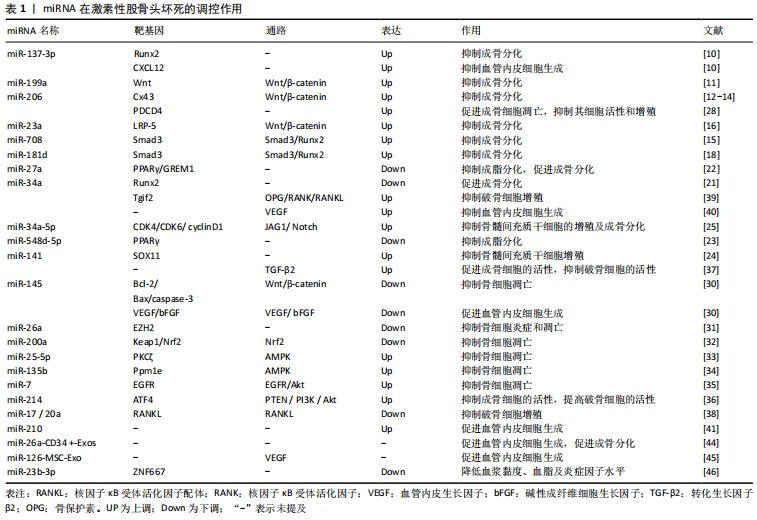
miRNA是一类内源性非编码调控的单链小分子RNA,在发育、细胞增殖、分化和凋亡等多种生理过程中发挥重要调控作用。2012年,国内学者首次报道了miRNA在激素性股骨头坏死的患者血浆中的差异表达,研究显示共有27个差异表达的miRNA,其中15个表达上调,12个表达下调 [4],提示miRNA可能参与了激素性股骨头坏死的调控过程。 骨髓间充质干细胞是一种具有高度增殖与多分化能力的多能干细胞,在特定环境下可分化为成骨细胞、软骨细胞、脂肪细胞等中胚层细胞。激素可抑制骨髓间充质干细胞成骨分化,使成骨细胞数量减少,诱导骨质疏松与坏死;并促进了成脂分化,使脂肪细胞数量增加,占据股骨头的骨髓腔,导致骨髓中的造血细胞死亡,进而发生缺血性坏死。故骨髓间充质干细胞的成骨、成脂分化异常被认为是激素性股骨头坏死的诱发因素之一,而miRNA在该过程中发挥重要调节作用。 2.1.1 miRNA调控骨髓间充质干细胞成骨分化 激素可抑制骨髓间充质干细胞成骨分化过程,减少骨形成,诱发激素性股骨头坏死,miRNA的表达在激素诱导的骨髓间充质干细胞成骨分化过程中发挥重要调控作用。 Wnt/β-catenin信号通路是一条在进化中高度保守的信号通路,通过结合靶基因[如Runt相关转录因子2(runt-related transcription factor 2,Runx2)、Osterix等]激活下游信号,发挥成骨细胞增殖、分化、抑制骨细胞凋亡等调控作用,miR-23a、miR-199a可通过调控Wnt/β-catenin信号通路在骨髓间充质干细胞成骨分化过程发挥重要作用。李涛 [5]从接受全髋关节置换术激素性股骨头坏死患者的股骨头组织内取出骨髓并获取骨髓间充质干细胞,通过基因芯片筛选发现激素促进了miR-23a的表达,过表达的miR-23a通过抑制靶基因LRP-5,影响Wnt蛋白与LRP-5共受体的结合,降低β-catenin蛋白水平,导致Wnt/β-catenin信号通路传导出现障碍,从而抑制骨髓间充质干细胞的成骨分化。SHI等 [6]在激素处理的MC3T3-E1细胞中发现miR-199a表达明显上调,转染miR-199a模拟物将降低β-catenin的表达,抑制Wnt通路传导,进而抑制成骨分化。故miR-23a、miR-199a通过调控Wnt/β-catenin信号通路在骨髓间充质干细胞成骨分化过程中发挥负调节作用。 Runx2被认为是成骨细胞形成的关键因子,通过激活转化生长因子β/骨形态发生蛋白信号通路在骨形成中发挥重要调控作用。研究发现,miR-137-3p、miR-206、miR-708、miR-181d、miR-34a通过靶向调控Runx2影响骨髓间充质干细胞的成骨分化过程。KONG等 [7]研究显示,miR-137-3p在激素性股骨头坏死大鼠坏死的股骨头组织中呈高表达,双重荧光素酶测定法提示miR-137-3p靶向Runx2;体外实验中miR-137-3p抑制剂增加了骨髓间充质干细胞成骨标记物碱性磷酸酶的活性及Runx2的表达,促进成骨分化,而过表达miR-137-3p模拟物则得到相反的结果。席源 [8]发现miR-206在激素性股骨头坏死动物模型的股骨头组织中表达增加,激素可能通过miR-206下调靶蛋白Cx43水平,抑制 ERK1/2-Runx2转导,进而引起成骨分化障碍。郝铖 [9]证实在激素干预的骨髓间充质干细胞中miR-708的表达上调,抑制 miR-708可在体外促进成骨,提示miR-708负调控成骨分化过程,该机制可能与增强Smad3蛋白的表达,激活转化生长因子β相关信号通路等一系列细胞内信号转导作用,调控下游Runx2的活性有关。XIE等 [10]发现在激素性股骨头坏死患者骨髓中,高表达的miR-181d可通过Smad3/Runx2调控轴抑制成骨细胞分化,进一步说明Smad3/Runx2调控轴的准确性。此外,ZHA等 [11]研究发现,miR-34a在激素诱导的骨髓间充质干细胞中表达降低,转染miR-34a抑制剂则强烈降低Runx2和Osterix的表达,加剧激素对成骨分化的抑制作用。由此可知,miR-137-3p、miR-206、miR-708、miR-181d、miR-34a通过靶向调控Runx2在骨髓间充质干细胞的成骨分化过程发挥双向调节作用。 上述研究表明,miRNA可通过调控Runx2、Wnt/β-catenin信号通路在激素诱导的骨髓间充质干细胞成骨分化过程中起到了双向调节作用。 2.1.2 miRNA调控骨髓间充质干细胞成脂分化 激素在降低骨髓间充质干细胞成骨潜能的同时,也增加了其成脂分化能力,而促进成脂分化可导致脂肪细胞增多、沉积,占据骨髓腔隙,最终导致股骨头缺血性坏死,故骨髓间充质干细胞的成脂分化也是诱发激素性股骨头坏死的危险因素之一。 过氧化物酶体增殖物激活受体γ(peroxisome proliferator-activated receptor gamma,PPARγ)是成脂分化的关键转录因子,miR-27a、miR-548d-5p可影响PPARγ的表达。谷晨熙 [12]在激素诱导的大鼠股骨头坏死模型中发现,miR-27a的表达显著下调,通过生物信息学研究发现PPARγ和GREM1是miR-27a的靶基因,进一步实验显示miRNA-27a通过作用于PPARγ和GREM1的3’UTR区,负调控其表达,有效抑制了骨髓间充质干细胞的成脂分化过程。SUN等 [13]也得出了相似的结论,研究者在激素诱导的骨髓间充质干细胞中发现miR-548d-5p表达水平下降,蛋白质印迹分析表明,miR-548d-5p的过表达显著降低了PPARγ的细胞水平,并减少了细胞甘油酸酯含量,以抑制激素诱导的成脂分化过程。因此,miR-27a、miR-548d-5p均通过抑制成脂分化因子PPARγ来抑制骨髓间充质干细胞成脂分化过程。 2.1.3 miRNA调控骨髓间充质干细胞增殖 骨髓间充质干细胞增殖异常也将影响其成骨成脂分化。KANG等 [14]研究显示,miR-34a-5p在激素处理的骨髓间充质干细胞中被上调,miR-34a-5p模拟物促进了激素对骨髓间充质干细胞增殖的抑制作用,进而抑制其成骨分化过程,其机制可能与靶向调节CDK4、CDK6及cyclin D1,抑制JAG1/Notch信号表达相关。还有研究表明 ,miR-141可通过靶向调节转录因子SOX11抑制骨髓间充质干细胞的增殖,而miR-141抑制组的结果则相反[15]。故可知,miR-141、miR-34a-5p均通过调控骨髓间充质干细胞增殖来影响成骨成脂分化过程。 2.2 miRNA调控骨细胞代谢 成骨细胞与破骨细胞是维持骨组织稳态的重要组成,在骨形成与骨吸收中发挥重要作用。激素可增加细胞毒性,诱导骨细胞凋亡,减少其活性,导致骨细胞代谢能力下降,骨转换减少,骨质疏松,使股骨头承重区域更易发生塌陷。故骨细胞代谢在激素性股骨头坏死发病过程中也发挥重要作用,而miRNA可通过调控骨细胞凋亡及细胞活性的方式参与调节骨细胞代谢。 2.2.1 miRNA调控骨细胞凋亡 细胞凋亡是细胞通过主动结束生命的方式来清除受损及衰老细胞以维护内环境稳定的过程。激素可诱发骨细胞凋亡,使骨小梁稀疏,骨质减少,导致骨组织在外力作用下更易发生折断,是诱发激素性股骨头坏死的高危因素之一,miRNA在激素诱导的骨细胞凋亡过程中起到了重要的调节作用。 抑制骨细胞凋亡可保护骨细胞免受激素侵害,从而减缓激素性股骨头坏死的发展。LI等 [16]通过大肠杆菌内毒素结合大剂量类固醇脉冲试验建立大鼠激素性股骨头坏死模型后发现,miR-26a的表达较弱,EZH2的表达较高,通过Targetscan靶点预测证实了EZH2是miR-26a的靶基因,而升高的miR-26a可抑制EZH2的表达,进而抑制骨细胞炎症和凋亡。FAN等 [17]通过实验研究证实了miR-25-5p可靶向调控PKCζ的3’非翻译区(UTR),以激活AMPK信号传导发挥抗氧化功能,抑制成骨细胞凋亡,增加细胞活性,进而保护成骨细胞免受激素侵害。该研究团队还报道了miR-135b通过靶向抑制Ppm1e表达激活AMPK信号,miR-7通过抑制靶基因EGFR激活EGFR/Akt信号传导,进而发挥相似的作用 [18-19]。TIAN 等 [20]在激素诱导的股骨头坏死家兔模型中发现,miR-145通过靶向沉默Wnt/β-catenin信号通路的下游基因Bcl-2、Bax及caspase-3抑制了骨细胞凋亡。ZHAO等 [21]报道了miR-200a介导的抑制因子Keap1、Nrf2也可抑制激素诱导的活性氧生成和成骨细胞的凋亡。 然而,也有少数miRNA促进了这一过程。张在恒 [22]研究发现,在激素性股骨头坏死患者的骨组织中miR-206、PDCD4的表达异常,PDCD4是细胞凋亡发生过程的一个重要调控蛋白,miR-206可直接结合PDCD4基因的启动子序列并抑制其表达,促进成骨细胞凋亡并且抑制其细胞活性和增殖。由此可知,miRNA在激素诱导的骨细胞凋亡过程中起到了双向调节作用。 2.2.2 miRNA调控骨细胞活性 长期大量使用激素可降低成骨细胞和破骨细胞的活性,造成骨细胞数量减少,导致骨小梁稀疏,进而引起股骨头承重区域塌陷,甚至坏死。WANG等 [23]报道,miR-214可直接靶向调控ATF4表达以抑制成骨细胞活性,并通过调控PTEN/PI3K/Akt通路发挥作用来促进破骨细胞功能。TIAN等 [24]发现,抑制miR-141可导致激素性股骨头坏死大鼠股骨头组织中转化生长因子β2的表达升高。此外,沉默miR-141或过表达的转化生长因子β2抑制了激素性股骨头坏死大鼠的骨细胞凋亡,促进成骨细胞的活性并抑制破骨细胞的活性。SHi等 [25]通过大鼠体内、体外实验发现miR-17/20a对核因子κB受体活化因子配体(receptor activator of NF-kB ligand,RANKL)具有靶向抑制作用,RANKL通过与骨保护素(osteoprotegerin,OPG)调节的核因子κB受体激活剂结合,促进了破骨细胞的形成,增强骨吸收功能并维持骨稳态,该实验中miR-17/20a通过阻断RANKL的表达来抑制破骨细胞的生成。PENG等 [26]研究表明,miR-34a可以负调控转化生长因子β引导因子2(Tgif2)和OPG/RANK/RANKL信号通路,miR-34a通过下调Tgif2表达,抑制OPG/RANK/RANKL信号通路的转导,抑制破骨细胞增殖。上述研究表明,miRNA在调控骨细胞活性,维持股骨头稳态上发挥重要作用。 2.3 miRNA调控血管内皮细胞生成 糖皮质激素的过度使用会导致血管内皮细胞的损伤和功能障碍,故血管内皮细胞的损伤被认为是激素诱导股骨头坏死的潜在机制之一,而血管生成是激素性股骨头坏死修复过程的关键。因此,血管内皮细胞的迁移、凋亡、增殖和相互连接发生任何变化都可能对激素性股骨头坏死的发展产生重大影响。 血管内皮生长因子信号通路是调控内皮细胞增殖、迁移和血管生成的关键因素。研究表明,人脐静脉内皮细胞中血管内皮生长因子的表达可被激素抑制,而miR-34a的转染可抑制血管内皮生长因子的分泌,这表明血管内皮生长因子可能是miR-34a在激素抑制血管生成中的调控靶标 [27]。TIAN等[20]研究中也发现miR-145的沉默可以增加血管内皮生长因子和成纤维细胞生长因子的表达水平,成纤维细胞生长因子主要参与血管(特别是微血管)的再生,血管内皮生长因子与成纤维细胞生长因子结合协同促进血管内皮细胞生成。YUAN等 [28]通过亚硫酸氢盐测序(BSP)发现,miR-210的上调与其序列内部的2个CpG位点的甲基化状态相关,DNA甲基转移酶抑制剂可促进miR-210表达,上调血管内皮生长因子、成纤维细胞生长因子、肿瘤坏死因子α和增殖细胞核抗原(PCNA)的表达,增加血管内皮细胞的活力和分化,进而调节激素性股骨头坏死中的血管生成。KONG等[7]指出,miR-137-3p与CXCL12存在靶向关系,沉默miR-137-3p可上调CXCL12,显著增加循环内皮祖细胞的数量,促进血管内皮细胞生成。 此外,外泌体(Exo)来源的miRNA对血管生成也有促进作用。CD34+干细胞是一组血管祖细胞,具有非凡的血管生成特性,移植CD34+干细胞来源的外泌体(CD34+-Exos)可以通过促进新血管形成来治疗缺血性疾病。ZUO等 [29]用携带miR-26a基因的慢病毒转染CD34+干细胞发现,CD34+-Exo的促血管生成作用和miR-26a的促成骨分化作用在miR-26a-CD34+-Exo中结合在一起,在逆转激素诱导的激素性股骨头坏死的致病过程中起协同作用。周山健 [30]的研究也证实了这一观点,该团队从过表达miR-126的骨髓间充质干细胞中获得高含量的miR-126-MSC-Exo,通过体外实验得知,miR-126-MSC-Exo可促进人脐静脉内皮细胞的增殖、迁移及内皮细胞因子血管内皮生长因子的表达,提示miR-126-MSC-Exo可以促进内皮细胞生成,改善股骨头的血供,从而增强骨质沉积来减缓激素性股骨头坏死的发展,表明microRNA与细胞外泌体的结合可以促进内皮细胞生成,改善股骨头的血供,为激素性股骨头坏死的防治提供了新思路。 2.4 miRNA调控脂质代谢 脂质代谢异常也是激素性股骨头坏死发病的重要危险因素之一,激素可诱导脂质代谢紊乱,引起血脂增高并导致高脂血症,使体内血液趋于停滞,脂肪细胞沉积、堵塞于微血管及骨髓内,形成脂肪栓塞,导致局部血瘀,进而引起股骨头缺血性坏死。研究发现,miRNA对脂质代谢具有调控作用。miR-23b-3p可靶向抑制ZNF667,从而降低血浆黏度、血脂及促炎性细胞因子(白细胞介素6)、肿瘤坏死因子α水平,在激素性股骨头坏死诱导的组织损伤和血脂形成中具有保护作用 [31]。 以上研究表明,miRNA可以通过调节靶向基因的表达,以调控骨髓间充质干细胞分化、骨细胞代谢、血管内皮细胞生成及脂质代谢的途径参与激素性股骨头坏死的发生发展,见表1,图1。"
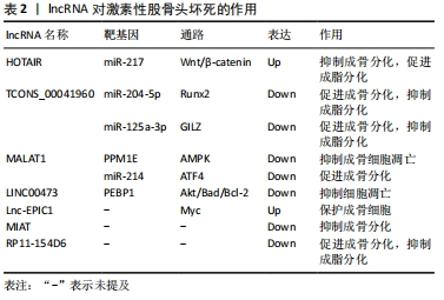
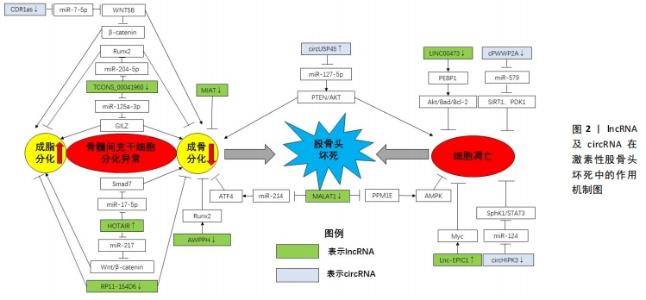
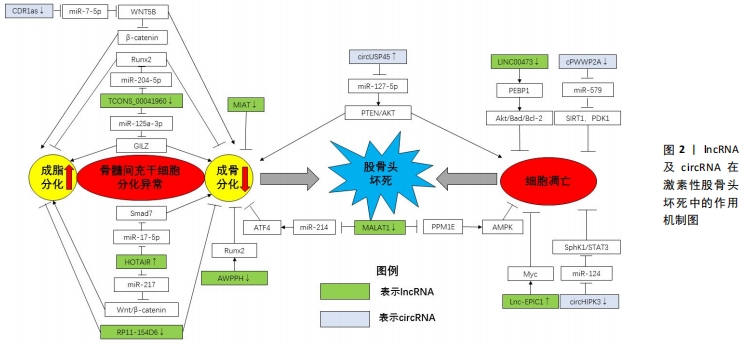
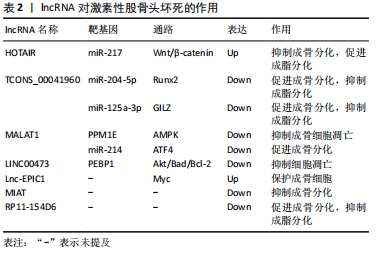
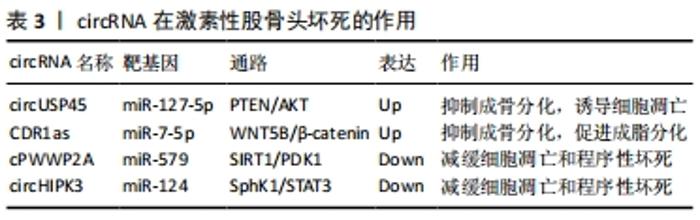
故干扰miRNA的异常表达可能是延缓激素性股骨头坏死进展的有效治疗方法。此外,外泌体与miRNA结合带来的协同作用对于治疗激素性股骨头坏死也有良好的发展前景。 2.5 lncRNA与激素性股骨头坏死的关系 长链非编码RNA (long non-conding RNA,lncRNA)是一类不参与蛋白质编码的调节性RNA,其长度超过200个核苷酸,可通过海绵化miRNA来介导其生物学功能 [32]。研究发现,lncRNA主要通过海绵化miRNA激活靶向通路来参与激素性股骨头坏死的调控过程[33-46]。 2.5.1 lncRNA调控骨髓间充质干细胞分化 lncRNA在骨髓间充质干细胞成骨、成脂分化中发挥重要调控作用。2017年,QINGYU等 [33]首次利用芯片和生物信息学研究了激素性股骨头坏死患者骨髓间充质干细胞的lncRNA表达谱,揭示了40余条具有显著差异的信号通路,尤其是调节骨髓间充质干细胞多能性的信号通路。CNC和ceRNA网络表明激素性股骨头坏死患者中lncRNA RP1-193H18.2,MALAT1和HOTAIR与骨髓间充质干细胞的异常成骨和成脂分化有关,王庆宇[34]对此进行了验证实验,发现HOTAIR可通过结合miRNA-217来调控Wnt/β-catenin 信号通路的关键基因OCT4、β-catenin及其抑制蛋白DKK1的表达,以抑制骨髓间充质干细胞的成骨分化,促进其成脂分化。HUANG等 [35]研究人员模拟了激素抑制骨髓间充质干细胞成骨分化的过程,并使用双重萤光素酶报告基因测定法来确认MALAT1和miR-214以及miR-214和ATF4之间的结合关系,结果显示,MALAT1的过表达可使miR-214海绵化以上调ATF4来促进成骨细胞分化,证实了MALAT1可以通过调控miR-214-ATF4轴改善激素诱导的骨髓间充质干细胞成骨分化抑制作用。进一步证明了WANG等实验结果的准确性。尚国伟 [36]在激素诱导异常分化的大鼠骨髓间充质干细胞中发现TCONS_00041960的表达显著下调,而miR-204-5p、miR-125a-3p的表达显著上调,通过进一步验证实验表明,TCONS_00041960通过下调miR-204-5p的表达以调控Runx2的表达,及下调miR-125a-3p的表达以调控亮氨酸拉链蛋白(GILZ),进而抑制骨髓间充质干细胞的成脂分化,促进其成骨分化。此外,还有研究报道,在激素性股骨头坏死患者的坏死组织中的MIAT水平显著高于非坏死组织中的MIAT,在骨髓间充质干细胞的成骨分化过程中,MIAT的表达水平逐渐降低,提示MIAT的异常过表达可能会抑制骨髓间充质干细胞的成骨分化 [37];RP11-154D6在骨髓间充质干细胞成骨分化过程中上调,在成脂分化过程中下调,提示RP11-154D6可能通过介导骨髓间充质干细胞的分化来参与激素性股骨头坏死的发病过 程[38],但其具体调控机制还有待深入研究。 2.5.2 lncRNA调控骨细胞凋亡 在骨细胞凋亡过程中,lncRNA可通过下调某些基因的表达,激活具有抗炎作用的相关通路,抑制激素诱导的骨细胞凋亡。FAN等[39]研究人员发现,在接受激素治疗的人成骨细胞和坏死的股骨头组织中,Lnc-MALAT1表达被下调了,提示MALAT1可能参与了激素性股骨头坏死的发病过程。随后,通过qPCR分析及进一步验证实验后发现,在激素处理的OB-6和hFOB1.19成骨细胞以及原代人成骨细胞中下调的MALAT1抑制了激素诱导的细胞死亡和凋亡,其机制可能是通过下调PPM1E来激活AMPK信号传导,活化的AMPK可激活Nrf2信号通路,增加Nrf2活性从而减弱氧化应激反应,抑制活性氧的产生和氧化损伤,提高成骨细胞抗氧化能力,抑制激素诱导的细胞死亡和凋亡,从而保护人成骨细胞免受激素损害。XU等 [40]在激素性股骨头坏死患者的骨髓间充质干细胞中发现LINC00473的表达明显下调,而上调LINC00473可减弱激素对骨髓间充质干细胞增殖和凋亡的抑制作用,其作用机制是通过介导磷脂酰乙醇胺结合蛋白1(PEBP1)激活Akt/Bad/Bcl-2信号通路,抑制激素诱导的细胞凋亡,保护骨髓间充质干细胞。相似的,Lnc-EPIC1通过调节Myc的表达可以保护人成骨细胞免受激素损伤 [41]。 由上述报道可知,lncRNA主要通过海绵化miRNA来激活下游信号通路以调控骨髓间充质干细胞分化及细胞凋亡的方式参与激素性股骨头坏死的发生发展过程,见表2。为激素性股骨头坏死的治疗提供了潜在的作用靶点。但目前关于lncRNA与激素性股骨头坏死的相关研究较少,其作用机制研究也有待深入。"
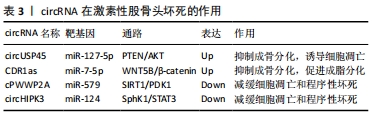
2.6 circRNA与激素性股骨头坏死 早在1976年,环状RNA(circRNA)就首次在RNA病毒中作为类病毒被发现 [42]。近年来,随着RNA测序技术和生物信息学的发展,越来越多的circRNA被发现、报道,其生物功能及调控机制也逐渐深入。目前的研究发现,circRNA是首尾端以3’、5’-磷酸二酯键形成的闭合环状分子,结构稳定,不易被RNA核酸外切酶降解,其通过充当miRNA海绵、RNA结合蛋白的海绵,与蛋白产生交互作用发挥其生物功能 [43]。一项最新的实验研究发现,共有345个circRNA在激素性股骨头坏死患者和健康个体的外周血中出现异位表达,其中229个circRNA被上调,而116个circRNA被下调 [44],提示circRNA可能参与了激素性股骨头坏死发病过程。 AKT信号是PI3K/AKT信号通路下游的效应器,主要参与调控细胞存活、增殖、生长、分化等生理过程,而PTEN基因是调控AKT信号的抑制分子,PTEN的激活可抑制AKT相关的磷酸化过程,从而抑制细胞的增殖与分化。KUANG等 [45]通过实验发现,circUSP45在激素性股骨头坏死中高表达,高表达的circUSP45可通过PTEN/AKT信号通路使miR-127-5p海绵化,并上调PTEN的表达而抑制AKT途径,进而诱导骨髓间充质干细胞的凋亡并抑制其增殖和成骨分化能力,诱发激素性股骨头坏死,提示circUSP45-miR-127-5p-PTEN/AKT信号级联的调控与激素性股骨头坏死的发病密切相关。高陈扬 [46]通过生信分析及进一步验证实验发现,在激素性股骨头坏死的骨髓间充质干细胞中,circRNA CDR1as呈高表达,并通过竞争性吸附miR-7-5p,以减轻miR-7-5p对WNT5B的抑制,上调WNT5B,降低Wnt/β-catenin信号通路中的β-catenin蛋白水平进而促进骨髓间充质干细胞成脂分化,抑制其成骨分化的功能,提示CDR1as-miR-7-5p-WNT5B/β-catenin调控轴通过促进骨髓间充质干细胞成脂分化的途径参与了激素性股骨头坏死。HONG等 [47]研究发现,在长期服用激素的患者以及激素处理的坏死股骨头组织的人类成骨细胞中,circRNA cPWWP2A被下调。在OB-6成骨细胞和原代人成骨细胞中,异位表达的cPWWP2A可以有效抑制激素诱导miR-579在细胞的积累,下调沉默信息调节因子1(SIRT1)与3-磷酸肌醇依赖性蛋白激酶1(PDK1)的表达以减缓细胞凋亡和程序性坏死的过程。ZHU等 [48]报道,在激素诱导的人类成骨细胞及坏死的股骨头组织中,circRNA HIPK3的过表达减弱了激素对成骨细胞中的凋亡活化的诱导,而沉默circHIPK3则会引起miR-124在成骨细胞的积累及miR-124的生存靶标鞘氨醇激酶1(SPHK1)和信号转导、转录激活因子3(STAT3)表达的上调,增强激素对成骨细胞的细胞毒性,从而抑制成骨细胞增殖。因此,cPWWP2A- miR-579- SIRT1/PDK1、circHIPK3-miR-124- SphK1/STAT3级联可能是保护人类成骨细胞免受激素侵害的新型靶标。 以上研究提示,circRNA主要通过调控骨髓间充质干细胞分化及减缓细胞凋亡和程序性坏死来参与激素性股骨头坏死的发病过程,提示circRNA在激素性股骨头坏死的启动机制中具有潜在作用,见表3。"
| [1] CUI L, ZHUANG Q, LIN J, et al.Multicentric epidemiologic study on six thousand three hundred and ninety five cases of femoral head osteonecrosis in China. Int Orthop. 2016;40(2):267-276. [2] VAN DER JAGT D, MOKETE L, PIETRZAK J, et al. Osteonecrosis of the Femoral Head: Evaluation and Treatment. J Am Acad Orthop Surg. 2015;23(2):69-70. [3] 李时斌, 赖渝, 周毅,等. 激素性股骨头坏死发病机制及相关信号通路的靶点效应[J]. 中国组织工程研究,2021,25(6):935-941. [4] 王兴山. 循环microRNA与激素性股骨头坏死相关性的初步研究[D].北京:北京协和医学院,2012. [5] 李涛. 人激素性股骨头坏死骨髓间充质干细胞差异表达miRNA筛选与miRNA-23a抑制干细胞成骨分化及机制研究[D].北京:北京协和医学院, 2015. [6] SHI C, HUANG P, KANG H, et al. Glucocorticoid inhibits cell proliferation in differentiating osteoblasts by microRNA-199a targeting of WNT signaling. J Mol Endocrinol. 2015;54(3):325-337. [7] KONG L, ZUO R, WANG M, et al. Silencing MicroRNA-137-3p, which Targets RUNX2 and CXCL12 Prevents Steroid-induced Osteonecrosis of the Femoral Head by Facilitating Osteogenesis and Angiogenesis. Int J Biol Sci. 2020;16(4):655-670. [8] 席源. MicroRNA-206通过Cx43-ERK1/2信号通路调控成骨分化在激素性股骨头坏死中的作用研究[D].南宁:广西医科大学,2019. [9] 郝铖. MiR-708通过靶基因SMAD3抑制间充质干细胞成骨分化并促进激素性股骨头坏死[D].武汉:华中科技大学,2016. [10] XIE Y, HU JZ, SHI ZY. MiR-181d promotes steroid-induced osteonecrosis of the femoral head by targeting SMAD3 to inhibit osteogenic differentiation of hBMSCs. Eur Rev Med Pharmacol. 2018;22(13):4053-4062. [11] ZHA X, SUN B, ZHANG R, et al. Regulatory effect of microRNA-34a on osteogenesis and angiogenesis in glucocorticoid-induced osteonecrosis of the femoral head. J Orthop Res. 2018;36(1):417-424. [12] 谷晨熙. miR-27a双靶向调控PPARγ与GREM1阻止激素诱导大鼠BMSCs成脂分化并促进其成骨分化的实验研究[D].郑州:郑州大学, 2017. [13] SUN J, WANG Y, LI Y, et al. Downregulation of PPARγ by miR-548d-5p suppresses the adipogenic differentiation of human bone marrow mesenchymal stem cells and enhances their osteogenic potential. J Transl Med. 2014;12:168. [14] KANG H , CHEN H , HUANG P , et al. Glucocorticoids impair bone formation of bone marrow stromal stem cells by reciprocally regulating microRNA-34a-5p. Osteoporos Int. 2016;27(4):1493-1505. [15] MENG CY, XUE F, ZHAO ZQ,et al. Influence of MicroRNA‐141 on Inhibition of the Proliferation of Bone Marrow Mesenchymal Stem Cells in Steroid‐Induced Osteonecrosis via SOX11. Orthop Surg. 2020;12(1):277-285. [16] LI G, LIU H, ZHANG X, et al. The protective effects of microRNA-26a in steroid-induced osteonecrosis of the femoral head by repressing EZH2. Cell cycle. 2020;19(1):1-16. [17] FAN JB, LIU W, ZHU XH, et al. microRNA-25 targets PKCζ and protects osteoblastic cells from dexamethasone via activating AMPK signaling. Oncotarget. 2017;8(2):3226-3236. [18] FAN JB, RUAN JW, LIU W, et al. miR-135b expression downregulates Ppm1e to activate AMPK signaling and protect osteoblastic cells from dexamethasone. Oncotarget. 2016;7(43):70613-70622. [19] FAN JB, LIU W, ZHU XH, et al. microRNA-7 inhibition protects human osteoblasts from dexamethasone via activation of epidermal growth factor receptor signaling. Mol Cell Biochem. 2019;460(1-2):113-121. [20] TIAN ZJ, LIU BY, ZHANG YT, et al. MiR-145 silencing promotes steroid-induced avascular necrosis of the femoral head repair via upregulating VEGF. 2017;21(17):3763-3769. [21] ZHAO S, MAO L, WANG SG, et al. MicroRNA-200a activates Nrf2 signaling to protect osteoblasts from dexamethasone. Oncotarget. 2017;8(62):104867-104876. [22] 张在恒. MicroRNA-206调控激素性股骨头缺血性坏死进程的分子机制研究及Dixdc1b基因骨骼发育调控功能的初步探讨[D].广州:南方医科大学,2018. [23] WANG C, SUN W, LING S, et al. AAV-Anti-miR-214 Prevents Collapse of the Femoral Head in Osteonecrosis by Regulating Osteoblast and Osteoclast Activities. Mol Ther Nucleic Acids. 2019;18:841-850. [24] TIAN L , SUN S , LI W , et al. Down-regulated microRNA-141 facilitates osteoblast activity and inhibits osteoclast activity to ameliorate osteonecrosis of the femoral head via up-regulating TGF-β2. Cell Cycle. 2020;19(7):772-786. [25] SHI C, QI J, HUANG P, et al. MicroRNA-17/20a inhibits glucocorticoid-induced osteoclast differentiation and function through targeting RANKL expression in osteoblast cells. Bone. 2014;68:67-75. [26] PENG WX, YE C, DONG WT, et al. MicroRNA-34a alleviates steroid-induced avascular necrosis of femoral head by targeting Tgif2 through OPG/RANK/RANKL signaling pathway. Exp Biol Med (Maywood). 2017;242(12):1234-1243. [27] ZHA X, SUN B, ZHANG R, et al. Regulatory effect of microRNA-34a on osteogenesis and angiogenesis in glucocorticoid-induced osteonecrosis of the femoral head. J Orthop Res. 2018;36(1):417-424. [28] YUAN HF, CHRISTINA VR, GUO CA, et al. Involvement of MicroRNA-210 Demethylation in Steroid-associated Osteonecrosis of the Femoral Head. Sci Rep. 2016;6:20046. [29] ZUO R, KONG L, WANG M, et al. Exosomes derived from human CD34+ stem cells transfected with miR-26a prevent glucocorticoid-induced osteonecrosis of the femoral head by promoting angiogenesis and osteogenesis. Stem Cell Res Ther. 2019;10(1):321. [30] 周山健. 负载miR-126的外泌体对大鼠早期激素诱导的缺血性股骨头坏死的治疗作用[D].锦州:锦州医科大学,2018. [31] LIU Y, ZONG Y, SHAN H, et al. MicroRNA-23b-3p participates in steroid-induced osteonecrosis of the femoral head by suppressing ZNF667 expression. Steroids. 2020;163:108709. [32] MARCHESE FP, RAIMONDI I, HUARTE M. The multidimensional mechanisms of long noncod-ing RNA function. Genome Biol. 2017;18(1):206. [33] QINGYU W, QIWEI Y, GAOYANG C, et al. LncRNA expression profiling of BMSCs in osteonecrosis of the femoral head associated with increased adipogenic and decreased osteogenic differentiation. Sci Rep. 2018;8(1): 9127. [34] 王庆宇. 激素性股骨头坏死BMSCs lncRNA异常表达谱及lncRNA HOTAIR在BMSCs成骨/成脂异常转分化作用机理的研究[D].长春:吉林大学, 2018. [35] HUANG XZ, HUANG J, LI WZ, et al. LncRNA-MALAT1 promotes osteogenic differentiation through regulating ATF4 by sponging miR-214: Implication of steroid-induced avascular necrosis of the femoral head. Steroids.2020;154:108533. [36] 尚国伟. LncRNA TCONS_00041960阻止激素诱导大鼠BMSCs成脂分化并促进成骨分化的实验研究[D].郑州:郑州大学,2018. [37] FANG B, LI Y, CHEN C, et al. Huo Xue Tong Luo capsule ameliorates osteonecrosis of femoral head through inhibiting lncRNA-Miat. J Ethnopharmacol. 2019;238:111862. [38] XIANG S, LI Z, WENG X. The role of lncRNA RP11-154D6 in steroid-induced osteonecrosis of the femoral head through BMSC regulation. J Cell Biochem. 2019;120(10):18435-18445. [39] FAN JB, ZHANG Y, LIU W, et al. Long Non-Coding RNA MALAT1 Protects Human Osteoblasts from Dexamethasone-Induced Injury via Activation of PPM1E-AMPK Signaling. Cell Physiol Biochem. 2018;51(1):31-45. [40] XU Y, JIANG Y, WANG Y, et al. LINC00473 rescues human bone marrow mesenchymal stem cells from apoptosis induced by dexamethasone through the PEBP1‑mediated Akt/Bad/Bcl‑2 signaling pathway.J Int J Mol Med. 2020;47(1):171-182. [41] 张向阳. LncRNA EPIC1保护成骨细胞免受地塞米松损伤[D].苏州:苏州大学, 2019. [42] SANGER HL. Viroids are single-stranded covalently closed circularRNA molecules existing as highly base-paired rod-like structuresJ . Proc Natl Acad Sci USA.1976;73 (11):3852-3856. [43] HUANG A, ZHENG H, WU Z, et al. Circular RNA-protein interactions: Functions, mechanisms, and identification. Theranostics. 2020;10(8):3503-3517. [44] ZHU Z, DU W, YU H, et al. Expression Profile Analysis of Differentially Expressed Circular RNAs in Steroid-Induced Osteonecrosis of the Femoral Head. Dis markers. 2019;2019:8759642. [45] KUANG MJ, XING F, WANG D, et al. CircUSP45 inhibited osteogenesis in glucocorticoid-induced osteonecrosis of femoral head by sponging miR-127-5p through PTEN/AKT signal pathway: Experimental studies. Biochem Biophys Res Commun. 2019;509(1):255-261. [46] 陈高扬. 环状RNA CDR1as在激素性股骨头坏死BMSCs成骨/成脂异常转分化中的分子机理及信号通路的研究[D].长春:吉林大学,2019. [47] HONG H, SUN Y, DENG H, et al. Dysregulation of cPWWP2A-miR-579 axis mediates dexamethasone-induced cytotoxicity in human osteoblasts. Biochem Biophys Res Commun. 2019;517(3):491-498. [48] ZHU CY, YAO C, ZHU LQ, et al. Dexamethasone-induced cytotoxicity in human osteoblasts is associated with circular RNA HIPK3 downregulation. Biochem Biophys Res Commun. 2019;516(3):645-652. |
| [1] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [2] | Jiang Huanchang, Zhang Zhaofei, Liang De, Jiang Xiaobing, Yang Xiaodong, Liu Zhixiang. Comparison of advantages between unilateral multidirectional curved and straight vertebroplasty in the treatment of thoracolumbar osteoporotic vertebral compression fracture [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1407-1411. |
| [3] | Xue Yadong, Zhou Xinshe, Pei Lijia, Meng Fanyu, Li Jian, Wang Jinzi . Reconstruction of Paprosky III type acetabular defect by autogenous iliac bone block combined with titanium plate: providing a strong initial fixation for the prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1424-1428. |
| [4] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhou Qian, Zhang Qiang, Chen Qiu. Human salivary components and osteoporosis/osteopenia [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1439-1444. |
| [5] | Jin Tao, Liu Lin, Zhu Xiaoyan, Shi Yucong, Niu Jianxiong, Zhang Tongtong, Wu Shujin, Yang Qingshan. Osteoarthritis and mitochondrial abnormalities [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1452-1458. |
| [6] | Zhang Lichuang, Xu Hao, Ma Yinghui, Xiong Mengting, Han Haihui, Bao Jiamin, Zhai Weitao, Liang Qianqian. Mechanism and prospects of regulating lymphatic reflux function in the treatment of rheumatoid arthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1459-1466. |
| [7] | Li Huo, Wang Peng, Gao Jianming, Jiang Haoran, Lu Xiaobo, Peng Jiang. Relationship between revascularization and internal microstructure changes in osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1323-1328. |
| [8] | Wang Jing, Xiong Shan, Cao Jin, Feng Linwei, Wang Xin. Role and mechanism of interleukin-3 in bone metabolism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1260-1265. |
| [9] | Xiao Hao, Liu Jing, Zhou Jun. Research progress of pulsed electromagnetic field in the treatment of postmenopausal osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1266-1271. |
| [10] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhang Qiang, Liu Jing, Shao Ming. Acupuncture for Parkinson’s disease: an insight into the action mechanism in animal experiments [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1272-1277. |
| [11] | Wu Bingshuang, Wang Zhi, Tang Yi, Tang Xiaoyu, Li Qi. Anterior cruciate ligament reconstruction: from enthesis to tendon-to-bone healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1293-1298. |
| [12] | Li Wei, Zhu Hanmin, Wang Xin, Gao Xue, Cui Jing, Liu Yuxin, Huang Shuming. Effect of Zuogui Wan on bone morphogenetic protein 2 signaling pathway in ovariectomized osteoporosis mice [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1173-1179. |
| [13] | Tian Chuan, Zhu Xiangqing, Yang Zailing, Yan Donghai, Li Ye, Wang Yanying, Yang Yukun, He Jie, Lü Guanke, Cai Xuemin, Shu Liping, He Zhixu, Pan Xinghua. Bone marrow mesenchymal stem cells regulate ovarian aging in macaques [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 985-991. |
| [14] | Fang Xiaolei, Leng Jun, Zhang Chen, Liu Huimin, Guo Wen. Systematic evaluation of different therapeutic effects of mesenchymal stem cell transplantation in the treatment of ischemic stroke [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1085-1092. |
| [15] | Guo Jia, Ding Qionghua, Liu Ze, Lü Siyi, Zhou Quancheng, Gao Yuhua, Bai Chunyu. Biological characteristics and immunoregulation of exosomes derived from mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1093-1101. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||