Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (14): 2245-2250.doi: 10.3969/j.issn.2095-4344.0702
Previous Articles Next Articles
Composite scaffolds for bone tissue engineering: application review and future direction
Xu Gui-wen1, Wurikaixi Aiyiti1, Teng Yong2
- 1School of Mechanical Engineering, Xinjiang University, Urumqi 830047, Xinjiang Uygur Autonomous Region, China; 2Orthopedic Center of PLA, Urumqi General Hospital of Lanzhou Military Region, Urumqi 830000, Xinjiang Uygur Autonomous Region, China
-
Received:2017-12-22Online:2018-05-18Published:2018-05-18 -
Contact:Wurikaixi Aiyiti, Ph.D., Professor, School of Mechanical Engineering, Xinjiang University, Urumqi 830047, Xinjiang Uygur Autonomous Region, China -
About author:Xu Gui-wen, Master candidate, School of Mechanical Engineering, Xinjiang University, Urumqi 830047, Xinjiang Uygur Autonomous Region, China -
Supported by:the National Natural Science Foundation of China, No. 51165044
CLC Number:
Cite this article
Xu Gui-wen, Wurikaixi Aiyiti, Teng Yong. Composite scaffolds for bone tissue engineering: application review and future direction[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(14): 2245-2250.
share this article
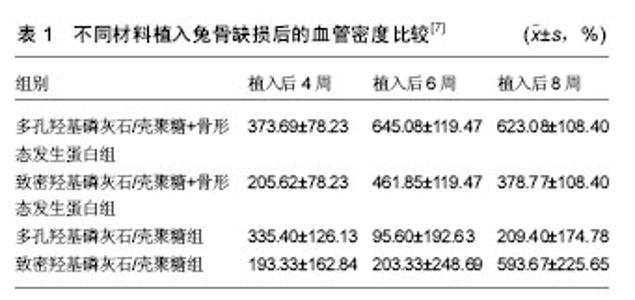
2.1 人工骨的复合形式 骨组织工程中常用的骨修复材料主要有金属、陶瓷、聚合物等。支架材料的选取、空间结构的构建、细胞与支架材料间的相互作用及机制等一直是骨组织工程学研究的核心内容。单一材料人工骨在力学性能、降解速度控制及诱导刺激骨骼生长等方面有所欠缺。单一结构人工骨在仿生设计、孔隙率及三维 贯通的可控孔隙结构等方面难以达到要求。单一功能人工骨在生物活性与力学强度、养料运输与代谢产物排放、支架降解与组织生长速率及血管化等功能之间的相互匹配还有待改进。复合型人工骨综合考虑材料、结构、功能之间的各种因素,取长补短,使之具有更好的生物学功能。 2.1.1 材料复合化研究 羟基磷灰石的生物相容性好,能与骨形成较强的键合,将其与骨形态发生蛋白(BMP)结合,可使材料具有骨诱导活性和骨传导作用。尹庆水 等[3]将天然海珊瑚碳酸钙转变成珊瑚羟基磷灰石人工骨,并与骨形态发生蛋白和几丁糖复合,将其植入大白鼠体内显示出显著的成骨诱导作用且炎症反应轻。王浩等[4]将胶原、羟基磷灰石、硫酸软骨素复合构建成三维多孔支架,再吸附以骨形态发生蛋白2形成骨修复材料,种植骨髓基质干细胞于材料表面进行动物实验,结果显示骨修复材料在植入局部保持完整的支架结构,具有利于细胞黏附和增殖的多孔结构。李冀等[5]将同种异体皮质骨粉与聚乳酸在超临界CO2作用下复合成多孔骨替代材料,植入动物体内具有良好的生物相容性和骨修复缺损能力。由于羟基磷灰石力学性能差,一般只能用作非负荷性骨缺损填充。 羟基磷灰石/高聚物复合材料中的羟基磷灰石粉末可提高聚合物的抗压强度。Thein-Han等[6]通过冷冻和冻干制备可生物降解的壳聚糖-羟基磷灰石复合材料支架。多孔的结构和孔径为50-125 μm,细胞附着显著增强,加入壳聚糖后,有利于降解。人自然骨中的羟基磷灰石主要是纳米级针状单晶体结构,彭超等[7]制备了纳米羟基磷灰石/壳聚糖-骨形态发生蛋白复合人工骨,初步探讨其植入后成骨与血管化的关系及孔径对再血管化的影响(表1)。"

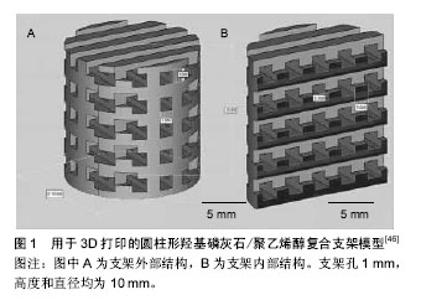
硫酸钙具有良好的生物相容性和可降解性,但缺乏诱导成骨活性。张永莉等[8]将硫酸钙与明胶组合构制可吸收复合生物材料。通过表面细胞培养显示出支架良好的细胞黏附性和生物相容性,且硫酸钙吸收后能够形成可供细胞生长的多孔支架。聚氨基酸是由有机高分子聚合物与生物活性无机钙盐复合而成的双相复合材料,赵增辉等[9]采用原位熔融缩聚法合成聚氨基酸/硫酸钙复合材料,植入兔体内无明显排异反应,有新生骨长入材料内部,与宿主骨形成牢固的骨性愈合。 磷酸钙骨水泥有良好的生物相容性和降解性。孙明林等[10]将磷酸钙与骨形态发生蛋白复合成人工骨。骨再生不仅有骨形态发生蛋白的参与,其他因子也发挥着重要的作用。刘洪等[11]在磷酸钙中加入神经生长因子(NGF),磷酸钙降解的同时释放出神经生长因子促进骨生长。针对磷酸钙脆性大、强度低等缺点,连芩等[12]采用壳聚糖纤维为增强体改善磷酸钙的力学性能。使复合材料人工骨的初始强度满足要求,同时壳聚糖纤维降解形成的多孔结构可促进骨长入。史雪婷等[13]以聚磷酸钙纤维为增强材料,以α-磷酸三钙/纳米羟基磷灰石为基体,制备纤维增强骨水泥复合材料。Minamiguchi等[14]研制了聚乳酸-羟基乙酸共聚物与抗冲洗型AC颗粒组成的三维支架,显示具有aw-AC的聚乳酸-羟基乙酸共聚物复合支架表现出比聚乳酸-羟基乙酸共聚物支架更大的强度和稳定性。 目前人工骨材料基础与应用研究均已取得明显进展,部分人工骨材料已进入临床应用阶段,且取得良好效果,生物材料在临床上治疗骨缺损的作用越来越受到重视,但是仍然存在材料加工困难、力学性能差、孔隙率低、孔隙连通性差等缺点。以磷酸钙或羟基磷灰石等为主体的复合人工骨由于降解慢或不能降解,在骨缺损区长期滞留,阻碍了新骨长入,量大时更为明显,同时降解物产物引起局部酸碱变化导致炎性反应,不利于细胞生长,且材料本身对细胞的亲和力有待加强。石墨烯及其衍生物已受到生物医学应用的关注,其具有显著的性能,如高表面积、高机械强度和易于功能化[15]。这类生物相容的碳基材料允许干细胞附着,可诱导和维持干细胞生长和谱系分化。此外,还具有促进成骨分化的能力,并且可与其他材料如聚合物、陶瓷和金属等组合,以进一步提高其应用价值。因此,骨传导材料复合化的研究,考虑各种性能之间的相互匹配将展现出巨大的生物医学应用潜力。 2.1.2 结构复合化研究 骨的机械性能与其分层结构和纳米级无机相及有机相的精确组织有关[16]。如纳米羟基磷灰石与聚己内酯复合构建人工骨支架,具有良好的微观结构。通过模拟天然细胞外基质特征,制备纳米纤维明胶基质,合成纳米纤维明胶/磷灰石复合支架[17],可改善表面积和机械强度。考虑到支架的热敏性,Venkatesana等[18]用壳聚糖/羟基磷灰石与硫酸软骨素和支链淀粉制备骨支架,较壳聚糖支架孔隙率和吸水/保留能力降低,而热稳定性增加。Fu等[19]制备了一种由三嵌段聚乙二醇-聚己内酯-聚乙二醇共聚物、胶原和纳米羟基磷灰石组成的三组分仿生水凝胶复合材料,表现出互连多孔结构。聚合物具有很好的生物性能而强度较低,Lei等[20]制造新型3D聚己内酯-20%磷酸三钙复合支架,在模拟体液中浸泡实验显示有磷灰石层结晶逐渐形成。Khan等[21]用聚环氧乙烷连接的明胶和磷酸三钙制备复合支架并将壳聚糖引入支架中,以改善人造骨基质的性质,结果显示在微结构中,磷酸三钙颗粒均匀地分散在交联的明胶/壳聚糖支架之间。对于复合支架的生物活性研究,Sabersamandari等[22]合成了具有半互穿网络的纤维-聚丙烯酰胺/纳米羟基磷灰石的纳米复合材料支架,在模拟体液中新的磷灰石颗粒可以其表面生长。Kavya等[23]制备了壳聚糖、明胶和纳米二氧化硅的3D纳米复合支架,更利于细胞附着增殖。 此外,用生物玻璃混合物制备具有互连孔隙的无定形复合支架,成骨细胞也表现出良好的附着、增殖和分化。可使用亚微米生物玻璃纤维作为有机相,明胶/胶原作为无机相,结合交联剂增强其机械性能。金属材料方面,钛及其合金由于其良好的生物相容性与机械强度和优良的耐腐蚀性而得到了广泛应用。对于承重部位的骨缺损修复,刘亚雄等[24]提出了一种钛框架-磷酸钙-骨形态发生蛋白复合结构的人工骨;作者所在课题组也成功研制出钛合金-生物陶瓷复合结构人工骨支架,钛合金网架结构对提高复合结构支架的力学性能效果显著[25]。由于此类结构易导致应力屏蔽,乌日开西等[26]对金属与陶瓷复合结构人工骨中金属支架的设计进行了研究,对关节置换后假体与股骨之间力的传递规律进行数值模拟研究,设计出了力学特性符合受力规律的钛合金支架结构。 人工骨从最开始的单一结构到复合结构,实现了功能上的巨大提升,再结合纳米技术进行仿生设计及有机材料与无机材料的复合[27]。目前,人工骨在骨缺损区作为空隙的填充物,有利于血管和成骨细胞的长入,提供了骨形成所需的空间,并阻止软组织长入。但多为孔隙结构非可控形式,其机械性能较差,难以起到机械支撑作用,尚不能用于修复重建大段骨缺损和关节缺损,仅用于填充植骨或脊柱融合等。3D打印技术能够准确控制空间孔隙的分布、走向及连通性等结构特征,被广泛应用于支架制备中。而如果将3D打印技术与纳米技术相结合,实现组织工程化人工骨支架材料的纳米级3D打印将展现出更大前景。 2.1.3 功能复合化研究 对人工骨材料和结构的研究是为了实现其功能。人工骨在功能上应更大程度实现对天然骨的仿生设计,并考虑各种性能之间的相互匹配,最终诱导人骨生成的同时逐渐对植入人工骨爬行代替。在胶原中添加壳聚糖和羟基磷灰石,可有效促进成骨细胞形成。而α-半水硫酸钙与骨基质明胶复合时,α-半水硫酸钙抗压性能差,降解速度过快,且骨组织在其上附着是二维模式。碳纳米管具有三维空间互联多孔网状结构,有利于成骨细胞长入,并具有低密度、高强度、高弹性模量等特性。楼毅等[28]研制出α-半水硫酸钙/碳纳米管复合材料,具有优良的生物相容性。 在人工骨研究中,对材料的生物相容性、孔隙形貌、降解性能和机械强度等都有要求。磷酸钙和磷酸三钙的力学强度差,加入可降解高分子材料,既能保证人工骨具有一定的孔隙率和骨诱导特性又能保持一定的强度和韧性。赵萍等[29]采用羧甲基壳聚糖作为添加剂,制得羧甲基壳聚糖α-磷酸三钙骨水泥生物复合材料,用于提高骨水泥的力学性能。徐尚龙等[30]采用聚左旋乳酸支架增强结构,以磷酸钙为复合填充材料,制备了复合增强结构人工骨,提高了承载能力。为改善β-磷酸三钙支架结构稳定性,Yang等[31]研制出β-磷酸三钙/聚甘油癸二酸酯支架,其具有良好的互连多孔结构和良好的机械性能及生物相容性。利用快速成型技术,马兴等[32]制备出聚乳酸-聚羟乙酸/磷酸三钙复合人工骨载体,并对载体表面修饰,以改进生物相容性,进而复合牛骨形态发生蛋白以制备仿生活性人工骨。在软骨修复方面,Wang等[33]制备与聚乳酸-聚羟乙酸微球结合的胶原/丝素蛋白复合支架,植入兔体内显示可增强关节软骨再生和修复软骨与周围软骨之间的整合。 天然骨在的结构、功能、营养、代谢方面均十分复杂,从骨科临床角度,要求人工材料达到如此高的仿生水平很难实现。近年来,骨组织工程领域迅速发展,体外和体内研究已解释了细胞分化成成骨细胞的潜力及生长因子、生物材料的作用,这些研究大多揭示了生物相容性、生物降解性、骨诱导能力、骨传导性、成骨性及力学性质。然而,使用生物材料完全更换有缺陷的骨骼仍然没有实现,使用细胞治疗创建功能性骨骼仍然是一个挑战。材料科学、组织工程学和纳米技术及3D打印技术的快速发展,使各种组织工程化构建的复合型人工骨相继研制成功[34]。人工骨材料生产工艺的提高,复合化研究的不断发展,学科间的相互结合,将实现结构和性质类似于人体组织并具有多种生物活性的生物医学功能,为人工骨修复材料的开发与骨缺损修复治疗带来新的希望。 2.2 复合人工骨的制备工艺方法 人工骨的制备工艺方法也是骨修复的关键,寻找合适的人工骨合成方法一直是骨科研究的重要课题。其主要可分传统技术及3D打印技术(也被称为快速成型技术)。 2.2.1 传统技术 传统的骨修复工艺方法主要有:纤维粘接法、相分离法、溶液浇铸/粒子沥滤法、静电纺丝法、气体发泡法等。孙明林等[10]将磷酸钙粉末与含骨形态发生蛋白的固化液按比例调和,观察表面结构及孔径,控制凝固时间得到抗压强度及弹性模量、溶解度、缓释作用、孔隙率等符合要求的磷酸钙/骨形态发生蛋白复合人工骨。罗庆平等[35]用磷酸单酯偶联剂对羟基磷灰石进行表面预处理,再将改性后的羟基磷灰石与高密度聚乙烯熔融共混来制备羟基磷灰石/高密度聚乙烯复合人工骨材料。为改善黏弹性和各向异性,Mathieu等[36]通过超临界CO2发泡处理聚乳酸和羟基磷灰石或β-磷酸三钙制成的开孔复合泡沫。通过CT分析内部结构,证明了在发泡方向的孔隙形态学各向异性。此外,压缩试验显示出机械性能的各向异性。 史雪婷等[13]利用固相反应法和湿法反应法分别制得α-磷酸三钙和纳米羟基磷灰石粉末,然后将其与聚磷酸钙纤维复合制成骨水泥试样。赵萍等[29]用碳纤维为增强相,采用硝酸液态氧化法对碳纤维进行表面处理,制得的碳纤维增强磷酸钙生物复合材料。於娟等[37]以纳米羟基磷灰石/壳聚糖复合材料作为骨水泥的固相粉体,将柠檬酸、醋酸等作为液相,制得羧甲基壳聚糖/α-磷酸三钙骨水泥生物复合材料。酆波等[38]采用真空吸附法将骨形态发生蛋白7多肽与支架材料复合,制备了壳聚糖/纳米羟基磷灰石/胶原复合支架材料。Sabersamandari 等[22]将微晶纤维素溶于N,N-二甲基甲酰胺和氯化锂混合物中,以过硫酸盐作为引发剂,纳米羟基磷灰石粉末作为单体和交联剂,合成半三维贯通网络结构纳米复合材料支架。 在传统的制造过程中有高温、高压或使用有机溶剂,同时操作步骤较复杂,需要模具或裁剪才能获取三维立体结构,因而常常造成型支架三维立体结构精度欠佳,难以形成可控孔隙结构,不能保证孔隙之间的完全贯通,以实现孔隙梯度和材料梯度结构的成形,且不便于定制化制造。 2.2.2 3D打印技术 3D打印技术也被称为快速成型技术、增材制造技术等,是一种利用逐层堆积原理制作零件的先进制造技术,商品化的设备出现于20世纪80年代末期。由于具有直接由CAD数据制成三维实体、不受零件复杂程度的限制、无需要传统的刀具和夹具等优势,在制造、医疗、建筑、艺术等领域得到了越来越多的应用。3D打印为实现支架微结构可控、多材料复合、细胞支架一体化制备等提供了有力的技术支撑。在满足个性化支架宏观结构的同时,能够兼顾细胞附着和组织生长。结合有限元分析可预先对支架结构进行优化[39]。由于能够打印设计出成分可控且相互连接[40],具有孔径梯度的支架而变得流行[41]。Tarafder等[42]通过3D打印制备出内部结构可控的多孔磷酸三钙支架,并通过微波烧结提高其机械强度。采用低温3D打印可增强支架性能,使用定制的3D打印机开发具有不同内部孔隙率的仿生聚己内酯支架[43-44]。Lu等[45]通过3DP致孔剂法制备聚己内酯/β-磷酸三钙的复合支架。显示出了良好的生物相容性和生物降解后和机械性能。结构设计之外,复合材料3D打印也是人工骨研究的重点。Cox等[46]提出了通过3D打印羟基磷灰石和聚乙烯醇复合粉末制备骨组织支架 (图1)。为突破支架材料生物功能的限制,Pati等[47]通过模拟骨微环境细胞外基质来修饰3D打印合成支架的生物功能。为使通过3D打印制备的支架更具生物活性,考虑在支架表层涂覆细胞亲和材料,Kao等[48]开发聚多巴胺涂层的复合支架聚多巴胺/聚乳酸,来增强人类脂肪干细胞的细胞黏附、增殖和分化及促进细胞外基质的分泌。人体组织细胞外基质是天然纳米复合材料,细胞在 纳米级特征材料中表现最佳。设计类似于细胞微环境组分的纳米材料并结合3D打印技术,通过增加表面积、添加纳米粗糙度、改变表面化学等增强材料的仿生特性[49]。 用于组织工程支架的3D打印技术是一个正在快速发展的研究领域,开发3D打印支架的主要目的是创建与植入部位天然微环境特性相似的支架。相对而言,3D打印技术能够同时打印出负载着细胞、生长因子、蛋白质等生物活性物质的复合材料支架,但生物材料的研发依然是生物3D打印技术的重点之一。 2.2.3 制备工艺对比 传统制备法的主要缺点是不能精确控制支架孔隙的尺寸、形状和空间分布,而且孔的连通性不能得到保证,加工精度和重复性差。模具挤出成形法精度较高,支架重复性好,但成形材料的种类有限,而且加工中存在高温过程,对材料性能影响较大。同时往往成形的是单管道,无法成形具有仿生结构的复杂管网系。因此,这些传统的支架成形技术难以适应组织工程的需要,其应用也逐渐被现代成形技术所取代。 3D打印技术使用零件的三维CAD模型直接成形,加工柔性大,包括形状和尺寸的高度灵活性及优良的精度和良好的表面质量,可精确控制空间分布、高再现性和材料适应性,并可根据患者需求定制设计,提高了组织工程支架的适应性。此外,由于各个材料层之间的熔合,保证良好的结构完整性,在组织工程中应用愈发广泛。将3D打印制备法和微细结构制备法相结合,可更好地满足组织工程支架对宏观结构及微细结构的要求。"
| [1] Schieker M,Seitz H,Drosse I,et al.Biomaterials as Scaffold for Bone Tissue Engineering. Eur J Trauma Emerg Surg.2006;32(2):114-124.[2] Boonlom T,Nattapon C,Kriskrai S,et al.Bone tissue engineering scaffolding: computer-aided scaffolding techniques.Prog Biomater. 2014;3(2):61-102.[3] 尹庆水,张余,李兆麟,等.复合珊瑚羟基磷灰石人工骨的研制及其成骨效应[J].中华创伤骨科杂,2004, 6(1):92-102.[4] 王浩,张里程,石涛,等.胶原-羟基磷灰石-硫酸软骨素-骨形态发生蛋白骨修复材料的性质评估[J].北京大学学报(医学版),2011,43(5):730-734.[5] 李冀,何丽娜,张育敏,等.超临界流体技术复合人工骨生物替代材料修复腔隙性骨缺损[J].中国组织工程研究与临床康复,2008,12(41):8042-8046. [6] Thein-Han WW,Misra RD.Biomimetic chitosan-nanohydroxyapatite composite scaffolds for bone tissue engineering.Acta Biomater. 2009; 5(4):1182-1197. [7] 彭超,杨天府.纳米羟基磷灰石/壳聚糖复合人工骨的成骨及再血管化[J].中国组织工程研究与临床康复,2007,11(40):8025-8029. [8] 张永莉,霍书娟,高建平,等.明胶/硫酸钙复合生物材料[J].高分子材料科学与工程,2006,22(1):215-217.[9] 赵增辉,蒋电明,苏保,等.复合骨修复材料-聚氨基酸/硫酸钙的生物相容性研究[J].功能材料,2011,42(5):807-811. [10] 孙明林,胡蕴玉,雷伟,等.磷酸钙骨水泥/BMP复合人工骨的理化性能及缓释作用[J].第三军医大学学报,2001,23(7):800-802.[11] 刘洪,臧小方,赵自平,等.磷酸钙骨水泥与外源性神经生长因子复合移植修复兔桡骨缺损[J].中国组织工程研究与临床康复,2008,12(41): 8037-8041.[12] 连芩,李涤尘,李爱民,等.壳聚糖纤维/磷酸钙骨水泥复合材料人工骨的力学性能[J].机械工程学报,2008,44(6):49-53.[13] 史雪婷,徐立新,石宗利.聚磷酸钙纤维增强α-磷酸三钙/纳米羟基磷灰石骨水泥复合材料的力学性能[J].中国组织工程研究与临床康复, 2010, 14(51):9535-9538.[14] Minamiguchi S,Takechi M,Yuasa T,et al.Basic research on aw-AC/PLGA composite scaffolds for bone tissue engineering.J Mater Sci Mater Med.2008;19(3):1165-1172.[15] Dubey N,Bentini R,Islam I,et al.Graphene: A Versatile Carbon-Based Material for Bone Tissue Engineering.Stem Cells Int.2015; 2015: 804213.[16] Liu Y,Luo D,Wang T.Hierarchical Structures of Bone and Bioinspired Bone Tissue Engineering. Small.2016;12(34):4611-4632.[17] Liu X,Smith LA,Hu J,et al.Biomimetic nanofibrous gelatin/apatite composite scaffolds for bone tissue engineering.Biomaterials.2009; 30(12):2252-2258.[18] Venkatesan J,Pallela R,Bhatnagar I,et al.Chitosan-Amylopectin/hydroxyapatite and chitosan-chondroitin sulphate/hydroxyapatite composite scaffolds for bone tissue engineering.Int J Biol Macromol. 2012;51(5):1033-1042. [19] Fu S,Ni P,Wang B,et al.Injectable and thermo-sensitive PEG-PCL-PEG copolymer/collagen/n-HA hydrogel composite for guided bone regeneration.Biomaterials.2012;33(19):4801-4809. [20] Lei Y,Rai B,Ho KH,et al.In vitro degradation of novel bioactive polycaprolactone—20% tricalcium phosphate composite scaffolds for bone engineering.Mater Sci Eng C Mater Biol Appl.2007;27(2): 293-298.[21] Khan MN,Islam JM,Khan MA.Fabrication and characterization of gelatin-based biocompatible porous composite scaffold for bone tissue engineering.J Biomed Mater Res A.2012;100(11):3020-3028.[22] Sabersamandari S,Sabersamandari S,Kiyazar S,et al.In vitro evaluation for apatite-forming ability of cellulose-based nanocomposite scaffolds for bone tissue engineering.Int J Biol Macromol. 2016;86: 434-442..[23] Kavya KC,Jayakumar R,Nair S,et al.Fabrication and characterization of chitosan/gelatin/nSiO2, composite scaffold for bone tissue engineering. Int J Biol Macromol.2013;59(4):255-263.[24] 刘亚雄,李涤尘,卢秉恒,等.具有钛框架增强结构人工骨的降解规律[J].西安交通大学学报,2005,39(1):9-12. [25] 杨文静,王娟,乌日开西•艾依提,滕勇.基于3D打印的钛合金-生物陶瓷复合结构人工骨支架设计[J].电加工与模具,2016,(03):47-51.[26] 乌日开西•艾依提,赵梦雅,王娟,滕勇.复合结构组织工程化人工骨的金属支架结构设计研究[J].新疆大学学报:自然科学版,2014(4):394-397. [27] Chung EH,Gilbert M,Virdi AS,et al.Biomimetic artificial ECMs stimulate bone regeneration.J Biomed Mater Res A.2006;79(4):815-826.[28] 楼毅,潘宗友,吴瑞凯,等.α半水硫酸钙复合功能化多壁碳纳米管骨修复材料生物相容性[J].生物工程学报,2012,28(3):340-348. [29] 赵萍,赵太荣,任学华,等.羧甲基壳聚糖/磷酸钙骨水泥生物复合材料探讨[J].陶瓷学报,2012,33(2):149-152.[30] 徐尚龙,李涤尘,陈中中,等.PLLA/CPC复合支架增强结构设计及制备[J].机械工程学报,2005,41(12): 122-125. [31] Yang K,Zhang J,Ma X,et al.β-Tricalcium phosphate/poly(glycerol sebacate) scaffolds with robust mechanical property for bone tissue engineering.Mater Sci Eng C Mater Biol Appl.2015;56:37-47.[32] 马兴,胡蕴玉,吴小明,等.聚酯/磷酸三钙人工骨载体的表面修饰及不同骨移植材料的比较研究[J].生物医学工程学杂志,2008,25(3):571-577. [33] Wang J,Yang Q,Cheng N,et al.Collagen/silk fibroin composite scaffold incorporated with PLGA microsphere for cartilage repair.Mater Sci Eng C Mater Biol Appl.2016,61:705-711.[34] Lipowiecki M,Ryvolová M,Töttösi Á,et al.Permeability of rapid prototyped artificial bone scaffold structures.J Biomed Mater Res A. 2014;102(11):4127-4135.[35] 罗庆平,刘桂香,杨世源,等.磷酸单酯偶联剂改性羟基磷灰石/高密度聚乙烯复合人工骨材料的制备和性能[J].复合材料学报,2006,23(1):80-84. [36] Mathieu LM,Mueller TL,Bourban PE,et al.Architecture and properties of anisotropic polymer composite scaffolds for bone tissue engineering. Biomaterials.2006;27(6):905-916.[37] 於娟,周钢,杨欣,等.可注射型纳米羟基磷灰石/壳聚糖复合材料骨水泥的研究[J].生物物理学报,2010,26(8):759-767. [38] 酆波,胡冬煦,张阳德,等.仿生支架材料骨形态发生蛋白7多肽/壳聚糖/纳米羟基磷灰石/胶原的制备及其细胞相容性[J].中国组织工程研究与临床康复,2011,15(8):1392-1396.[39] 吴任东,杨辉,张磊,等.组织工程支架快速成形技术研究现状[J].机械工程学报,2011,47(5):170-176.[40] Bose S,Vahabzadeh S,Bandyopadhyay A. Bone tissue engineering using 3D printing.Mater Today. 2013;16(12):496-504.[41] Sobral JM,Caridade SG,Sousa RA,et al.Three-dimensional plotted scaffolds with controlled pore size gradients:Effect of scaffold geometry on mechanical performance and cell seeding efficiency.Acta Biomaterialia.2011;7(3):1009-1018.[42] Tarafder S,Balla VK,Davies NM,et al.Microwave-sintered 3D printed tricalcium phosphate scaffolds for bone tissue engineering.J Tissue Eng Regen Med.2013;7(8):631-641.[43] Inzana JA,Olvera D,Fuller SM,et al.3D printing of composite calcium phosphate and collagen scaffolds for bone regeneration. Biomaterials. 2014;35(13):4026-4034.[44] Temple JP,Hutton DL,Hung BP,et al.Engineering anatomically shaped vascularized bone grafts with hASCs and 3D-printed PCL scaffolds.J Biomed Mater Res A.2014;102(12):4317-4325.[45] Lu L,Zhang Q,Wootton D,et al.Biocompatibility and biodegradation studies of PCL/β-TCP bone tissue scaffold fabricated by structural porogen method.J Mater Sci Mater Med.2012;23(9):2217-2226.[46] Cox SC,Thornby JA,Gibbons GJ,et al.3D printing of porous hydroxyapatite scaffolds intended for use in bone tissue engineering applications.Mater Sci Eng C Mater Biol Appl.2015;47:237-247.[47] Pati F,Song TH,Rijal G,et al.Ornamenting 3D printed scaffolds with cell-laid extracellular matrix for bone tissue regeneration.Biomaterials. 2015;37:230-241.[48] Kao CT,Lin CC,Chen YW,et al.Poly(dopamine) coating of 3D printed poly(lactic acid) scaffolds for bone tissue engineering.Mater Sci Eng C Mater Biol Appl.2015;56:165-173.[49] O'Brien CM,Holmes B,Faucett S,et al.Three-dimensional printing of nanomaterial scaffolds for complex tissue regeneration.Tissue Eng Part B Rev.2015;21(1):103-114. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [11] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [12] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [13] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [14] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| [15] | Liu Liyong, Zhou Lei. Research and development status and development trend of hydrogel in tissue engineering based on patent information [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3527-3533. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||