Chinese Journal of Tissue Engineering Research ›› 2015, Vol. 19 ›› Issue (6): 962-968.doi: 10.3969/j.issn.2095-4344.2015.06.025
Previous Articles Next Articles
Stem cell marker LGR5: a new target for cancer therapy
Gao Fei, Wei Yan-cai, Yang Chen
- Department of Nuclear Medicine, Suzhou Hospital Affiliated to Nanjing Medical university, Suzhou 215000, Jiangsu Province, China
-
Received:2015-01-12Online:2015-02-05Published:2015-02-05 -
Contact:Yang Chen, M.D., Chief docimaster, Department of Nuclear Medicine, Suzhou Hospital Affiliated to Nanjing Medical university, Suzhou 215000, Jiangsu Province, China -
About author:Gao Fei, Master, Docimaster, Department of Nuclear Medicine, Suzhou Hospital Affiliated to Nanjing Medical university, Suzhou 215000, Jiangsu Province, China
CLC Number:
Cite this article
Gao Fei, Wei Yan-cai, Yang Chen. Stem cell marker LGR5: a new target for cancer therapy[J]. Chinese Journal of Tissue Engineering Research, 2015, 19(6): 962-968.
share this article
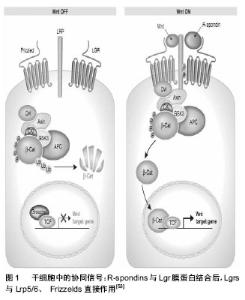
2.1 LGR5的生物学特征 2.1.1 LGR5的结构特征 人LGR5位于染色体12q22-23,cDNA全长4 208 bp,含有22个外显子和21个内含子,转录产生8个不同的mRNA,其中5个为选择性剪切体,可读框编码由907个氨基酸残基组成的多肽链,其中信号肽21个,外功能区540个,跨膜区263个,C-端尾部83个。编码产物LGR5蛋白结构特征为:外功能区有18个富含亮氨酸重复序列,N-端和C-端尾部侧翼富含半胱氨酸序列,有4个糖基化位点,7次α螺旋跨膜区高度保守[3-4]。 2.1.2 LGR5的表达 研究表明,LGR5在人体内分布广泛,大脑、脊髓、乳腺、毛囊、眼睛、生殖器官及胃肠道等都有表达,但在正常组织中局限性表达。Barker等[7]通过原位杂交发现LGR5表达在小肠隐窝基底柱状细胞,结肠隐窝及胃腺体底部。而在多种肿瘤组织中,LGR5弥散性表达。 2.2 LGR5与干细胞 干细胞是存在于动物和人的一种特殊功能细胞,具有多向分化潜能和自我更新能力。这种特性使其在再生医学、组织工程的实验研究及临床治疗应用中体现了重要的价值。成体干细胞的发育等级较低,是指存在于一种已经分化组织中的未分化细胞。最新研究显示LGR5有作为成体干细胞特异性标记的潜能性。 2.2.1 LGR5与肠道干细胞 肠黏膜上皮是哺乳动物机体代谢最为活跃的场所,肠上皮细胞终身进行着不间断的自我更新,3-5 d更新1次。肠黏膜上皮之所以能终身进行不间断的更新,是因为位于肠道隐窝部位的肠道干细胞及定向祖细胞保持着旺盛的分化能力,凋亡脱落及受损坏死的细胞与干细胞的增殖分化保持着动态平衡,由此可见肠上皮干细胞在维持肠道屏障结构和功能的完整以及损伤后的修复中扮演着重要的角色。 最新研究显示LGR5是小肠干细胞标记物。原位杂交试验表明,LGR5特异表达在小肠隐窝基底柱状细胞(crypt base columnar cells,CBC),这些细胞散在分布于潘氏细胞间[7]。为观察LGR5+CBC及其子代细胞,Barker等[7]在LGR5第一个外显子插入GFP和它莫西芬诱导的Cre重组酶,通过示踪实验发现LGR5+CBC可以自我更新并分化出小肠上皮中的所有细胞类型。形态学上,LGR5+CBC的特点是稀少的胞质和楔形的核朝向隐窝腔,很容易和毗邻的潘氏细胞相区别。增殖标记物Ki-67在CBC几乎都是阳性,M期标记物磷酸-组蛋白H3偶尔表达,表明这些细胞呈现典型的周期变化。由此Barker等[7]认为LGR5+CBC具有长期维持上皮自我更新的特性,可以分化产生肠上皮中所有细胞类型,还具有凋亡抑制性及高度增殖活性。此外,研究发现,LGR5+CBC在体外可形成隐窝-绒毛结构[9]。 结肠干细胞位于结肠隐窝基底部,维持结肠黏膜上皮的正常再生。2007年首次提出LGR5是结直肠干细胞的标记物,研究表明LGR5只在结肠隐窝基底细胞特异性表达,LGR5+细胞具有干细胞活性,可分化产生结肠上皮所有细胞类型,证明了这些细胞的多潜能性[7]。 上述研究表明LGR5+细胞是小肠、结肠的干细胞,LGR5可能是小肠和结肠干细胞的特异性标记分子。 2.2.2 LGR5与胃干细胞 胃黏膜上皮凹陷形成胃腺,根据其所在部位与结构的不同,分为胃底腺、贲门腺和幽门腺。研究表明,在新生小鼠中,LGR5表达在胃体部和幽门腺底部,出生几周后,LGR5在胃体部的表达即消失,只表达在幽门腺底部。谱系追踪实验表明胃腺来源于LGR5+细胞,LGR5+使胃上皮保持长期自我更新。在体外培养系统中,单个LGR5+细胞可以形成类似成熟幽门上皮的组织[10]。这些研究表明LGR5+细胞是维持胃上皮自我更新的干细胞,LGR5是胃多能干细胞的标记物。对胃干细胞培养方法及其标记物LGR5的研究,有利于了解胃上皮更新机制、炎症/感染和癌症的发生发展。 2.2.3 LGR5与毛囊干细胞 毛囊干细胞位于毛囊隆突区,对毛囊的周期性生长,表皮和皮脂腺的更新以及皮肤损伤后修复有着至关重要的作用。目前国内外主要采用的毛囊干细胞标记物有整合素、角蛋白、CD34、CD200等,而LGR5是最新发现的标记物。LGR5基因限制表达在毛囊干细胞不对称分裂时保持非随机共分离的姐妹染色单体上[11]。基因微阵列分析显示LGR5 mRNA高表达于成人毛囊的隆突区[12]。研究发现从毛囊Bulge区分离得到的LGR5+细胞增殖活跃,具有多分化潜能,能分化为毛囊、表皮和皮脂腺[13]。体外移植和标志谱系实验表明,LGR5+细胞可以形成毛囊结构。因此,LGR5可能是毛囊干细胞的标志物。 2.2.4 LGR5与乳腺干细胞 Welm等[14]在电镜下研究了乳腺干细胞的形态和位置,他们认为位于乳腺基底部位未分化的小淡染细胞(small light cells,SLC)为乳腺干细胞,而细胞形态较复杂的仍处于未分化状态的大淡染细胞(undifferentiated large light cells,ULLC)为乳腺祖细胞。虽然乳腺组织中存在干细胞,但目前尚缺乏特异性的乳腺干细胞标记物。目前,候选的乳腺干细胞标记分子有:干细胞抗原1(Stem cell antigen 1,Sca-1)、ABCG2/Bcrp l、滞留细胞标记分子、细胞角蛋白CK6和CK19、细胞表面分子CD24和CD29、Musashi-1、乙醛脱氢酶1等[15-18]。Barker等发现乳腺基底上皮层有LGR5表达,LGR5是否为乳腺的干细胞标记物还需进一步证实。 2.3 LGR5与肿瘤 肿瘤干细胞与成体正常干细胞特性相似,耐毒性损伤和放化疗,并可能与治疗后的复发和侵入转移有关。LGR5是新兴的肿瘤干细胞表面标志物,与肿瘤的形成和发展有很大的相关性,可以作为新的治疗靶点。 2.3.1 LGR5在结直肠癌中的表达 结直肠癌是人类最常见的消化道恶性肿瘤之一,在欧美发达国家其发病率居于恶性肿瘤第二,在亚洲地区,尤其是经济发达地区,呈现快速增长趋势,占国内肿瘤死因的第4-6位,尽管结直肠癌的诊疗水平不断提高,但术后高复发率及转移仍是待解决的问题[19]。结直肠癌干细胞已被认为是结直肠癌复发的根源,因此研究结直肠癌干细胞的标志分子及其功能十分重要[20]。 McClanaha等[20]利用cDNA微阵列分析15例结肠肿瘤和对应正常组织的基因表达情况,结果LGR5在结肠肿瘤中表达率为73%(11/15)。实时定量PCR检测结肠原发肿瘤,结果显示肿瘤组织中LGR5 mRNA表达水平明显高于对应的正常组织(P < 0.000 1),在结肠原发肿瘤组织中LGR5上调64%[21]。免疫组化结果显示LGR5主要定位于细胞质中,在癌旁正常结肠黏膜中局限表达在隐窝基底部,而在结肠腺瘤和结直肠癌中的表达呈递增趋势。建立LGR5转基因鼠模型,发现在APC基因缺失后,大鼠于实验30周出现结肠腺瘤[22]。上述结果提示LGR5阳性干细胞与肿瘤的发生发展密切相关,可能是结直肠癌的肿瘤干细胞标志物,在临床中可作为肿瘤筛选和分型的参考指标。 LGR5在结直肠癌转移灶来源的细胞株上的表达比原发癌来源的细胞株上高[23]。采用免疫组织化学方法检测169例结直肠癌患者术后组织石蜡切片标本,分析LGR5表达与临床病理特征之间的联系,并采用Kaplan-Meier法分析LGR5表达与患者生存预后的关系,伴有淋巴结转移的组织中 LGR5蛋白的表达水平明显高于无淋巴结转移的组织,即在 Dukes C/D期组织中的表达水平明显高于Dukes A/B期(P < 0.05),且其表达与肿瘤远处结转移以及分化程度有关。LGR5高表达的患者术后100个月生存率明显低于低表达或者阴性表达的患者[24-27]。因此,LGR5在结直肠癌组织中的表达水平与肿瘤分期、转移、分化程度相关,高表达LGR5的结直肠癌患者预后不良,LGR5可以作为判定结直肠癌发展水平及预后的一个新指标。 2.3.2 LGR5在胃癌中的表达 幽门螺旋杆菌(Hp)是胃癌最主要的致病因素,近期研究表明幽门螺旋杆菌感染的胃癌组织中LGR5+细胞数增加,且LGR5+上皮细胞比LGR5-上皮细胞对幽门螺旋杆菌感染导致的DNA损伤更敏感[28]。通过免疫染色法检测LGR5在正常胃组织和癌前病变组织中表达的差异,发现LGR5在正常胃组织中局限表达于基底部,而在癌前病变组织中表达明显升高,且LGR5+细胞不局限于基底部,表明LGR5+细胞离开干细胞巢是胃癌形成和恶化的早期事件[29]。Simon等[30]从转录水平(实时定量PCR)和翻译水平(免疫组化)探讨了LGR5在胃癌中的表达情况和肿瘤生物学意义。结果显示正常胃组织中仅散在存在少量LGR5+细胞,而相应癌组织中LGR5+细胞明显增多,复染实验显示LGR5与公认的干细胞标记分子CD44,Musashi-1,ADAM17共表达。胃癌的发展过程与LGR5+细胞的位置分布相关:在正常胃黏膜中,LGR5+细胞主要分布在颈黏液区,在肠化生组织中,LGR5+细胞分布在隐窝基底部,而在胃癌组织中,LGR5+细胞分布在管腔表面、肿瘤中心、浸润边缘。胃癌中LGR5的表达与局部肿瘤生长和淋巴转移显著相关,且LGR5高表达的胃癌患者生存期短。胃癌中LGR5局限表达于胃干细胞所在部位,且与公认的干细胞标记分子共表达,提示LGR5+胃癌细胞可能具有胃癌干细胞特性。 2.3.3 LGR5在肺癌中的表达 肺癌位居世界范围内肿瘤致死率首位,也是中国常见的恶性肿瘤之一,近年来发病率呈不断上升趋势。2013年GLOBOCAN资料显示,肺癌死亡比例占肿瘤性致死人数的18%(约1 400 000例)。研究表明,肺癌中也存在肿瘤干细胞[31-32]。Ryuge等[33]利用免疫组织化学方法检测了266例非小细胞肺癌患者组织切片中LGR5的表达及与临床病理参数的关系,研究发现,仅在16例腺癌中检测到LGR5的表达,且肿瘤体积大(size> 5 cm,P=0.033)、高TNM分期(stage Ⅱ/Ⅲ,P=0.025)及不表达TTF-1(P=0.042)的患者肿瘤组织高表达LGR5,高表达LGR5患者的预后差(P=0.026),但LGR5的表达不是生存率的独立预测指标。该研究表明LGR5与非小细胞肺癌发展进程密切相关,为肺癌干细胞研究打开新的视角,但LGR5是否为肺癌干细胞标记物仍需进一步研究。 2.3.4 LGR5在卵巢癌中的表达 RT-PCR分析结果表明在卵巢原发肿瘤中LGR5表达上调53%(18/33),且其表达水平与肿瘤的组织分级有关,在卵巢肿瘤Ⅰ、Ⅱ期表达水平有不同的上调,而在Ⅲ、Ⅳ期表达下调,可见LGR5的表达上调也许是肿瘤形成的早期事件[34]。用免疫组化的方法检测LGR5在正常卵巢及卵巢癌组织中的表达情况,结果显示LGR5在卵巢癌组织中的表达显著提高[35],表明LGR5与卵巢原发肿瘤的发生发展密切相关。 2.3.5 LGR5在肝癌中的表达 RT-PCR结果显示LGR5 mRNA在正常肝组织中呈低水平表达,而在肝细胞癌中表达显著上调(P=0.000 3)[36]。Fukuma等[37]建立了稳定表达LGR5-FLAG的肝癌细胞株,观察发现过表达LGR5的肝癌细胞形态发生变化,克隆形成率增高,抗细胞毒性药物能力增强,迁移力降低,下调肝癌细胞株中LGR5的表达则相反。McClanahan等[20]利用RNA干扰抑制肝癌细胞中LGR5的表达,发现抑制LGR5表达可诱导人肝癌细胞的凋亡。临床病例资料显示LGR5在肝癌患者中的过度表达常伴随着Wnt信号通路中的关键分子β-catenin第三外显子突变,将突变的β-catenin导入小鼠肝脏中,将导致小鼠LGR5表达上调,因此LGR5很可能是Wnt信号途径的目标基因,在肝细胞癌的发生发展中发挥作用[36]。 2.3.6 LGR5在基底细胞癌中的表达 LGR5与基底细胞癌(basal cell carcinoma,BCC)的发生密切相关。Tanese等[38]利用DNA微阵列分析人类BCC病例,结果显示LGR5表达上调,且原位杂交实验证实了LGR5表达上调。实时定量RT-PCR技术检测表明基底细胞癌组织中LGR5 mRNA的表达水平明显高于正常组织。敲除LGR5基因导致小鼠BCC细胞株增殖受抑制,将过表达LGR5基因的人角质化HaCaT细胞株移植到免疫缺陷小鼠中会导致肿瘤形成。相关研究还发现,抑制小鼠BCC细胞株Hedgehog信号通路可引起内在的LGR5上调,激活小鼠NIH3T3细胞株Hedgehog信号可引起内在的LGR5下调。这些结果显示LGR5可能参与了体内除Wnt信号通路以外多种信号途径的转导,其表达会下调Hedgehog信号,引起细胞增殖和肿瘤形成。 2.3.7 LGR5在食管病变中的表达 研究显示,Barrett食管中有LGR5表达,在Barrett食管相关高度异型增生和食管腺癌中,其表达较Barrett食管显著增强,并与食管腺癌预后不良独立相关,提示LGR5有作为Barrett食管相关异型增生和食管腺癌生物学标记的潜能[39]。免疫组化方法检测LGR5在Barrett食管、早期食管鳞癌和轻度食管炎组织中的表达情况,结果显示LGR5表达于腺体细胞的细胞质和鳞状细胞的细胞核,且Barrett食管组织腺上皮LGR5表达评分显著高于轻度食管炎组织(65.00±1.95,2.55±1.70,P=0.049),早期食管鳞癌癌灶组织LGR5表达评分显著高于相应癌旁组织(5.39±0.61,3.06±1.06,P=0.000),原位癌、黏膜内癌与黏膜下癌间LGR5表达评分差异无显著性意义(5.00±0.63、5.56±0.53和6.00±0.58,P=0.174)[40]。生存单因素分析显示高表达LGR5的食管腺癌患者5年生存期差[41]。LGR5在Barrett食管、轻度食管炎组织和早期食管鳞癌中的表达呈上升趋势,提示LGR5在Barrett食管向食管鳞癌的发展过程中起关键作用。 2.4 LGR5的配体及其信号通路 Wnt途径是细胞发育和调节生长的一个关键途径,参与人体胚胎发育、干细胞的增殖分化以及肿瘤的形成。Wnt信号最关键的步骤是β-catenin的稳定化和稳定的β-catenin进入细胞核,与T细胞因子(T cell factor/lymphoid enhancer factor, TCF/LEF)家族成员结合,调节Wnt信号通路靶基因的表达[42-43]。Wnt途径关键分子的突变或表达异常会引起各种疾病。在大部分结直肠癌中都观察到Wnt途径的活化以及β-catenin在细胞质中的积累,β-catenin在细胞质中积累后转移到细胞核中,与细胞核中的转录因子,如TCF/LEF结合,调节Wnt信号通路靶基因表达,下游靶基因的不正常表达会导致细胞异常增殖,甚至致瘤。在正常结直肠黏膜中β-catenin主要表达在细胞膜上,而在结直肠腺瘤和结直肠腺癌中,β-catenin在细胞核中的表达呈递增趋势(81%),表明Wnt/β-catenin信号通路参与结直肠癌的发生发展。研究表明,在结直肠癌中LGR5的表达与β-catenin的表达正相关,这表明LGR5可能作为下游分子通过Wnt/β-catenin信号途径在结直肠癌的发生中发挥作用[25]。Van der Flie等[44]发现有大约80种Wnt信号通路的靶基因与结直肠癌的发生有关,其中LGR5作为Wnt信号通路中β-catenin/TCF-4的靶基因,当Wnt信号通路异常激活时,引起LGR5的表达显著升高,可能对肠上皮细胞的恶性转化起到重要作用。敲除LGR5会导致小肠中Wnt/β-catenin信号失调,表现为Wnt/β-catenin信号增强时上皮细胞增殖不加快,提示LGR5对细胞的快速增殖是必须的[45]。有临床资料显示部分肝细胞癌患者中LGR5的过度表达与β-catenin第三外显子的突变密切相关。体外培养小鼠肝细胞并导入突变的β-catenin也发现LGR5的表达上调,Wnt通路的异常激活,引起LGR5表达上调,可能导致肝细胞的异常增生和肿瘤的形成[36]。因此LGR5作为Wnt信号通路的靶基因,在Wnt通路激活以后,引起LGR5表达的上调,可能对细胞的增殖分化和肿瘤的发生起到重要作用。 LGR5是Wnt信号靶基因,与人体正常生长发育和疾病相关,但尚未发现其配体,一直被认为是G蛋白偶联受体超家族的孤儿受体,近期研究表明R-spondins(RSPOs)是LGR5的高亲和力配体。RSPOs 蛋白家族由4种分泌性蛋白组成(RSPO1-4),他们是Wnt/β-catenin信号的增强剂,其作用可被胞外Wnt受体阻断剂DKK1阻断[46-48],在干细胞的生长发育中起重要作用。研究表明RSPOs可通过增强Wnt/β-catenin信号,刺激小肠隐窝干细胞的生长[47,49-50]。在体外培养的小肠隐窝中加入RSPO1导致LGR5+细胞Wnt/β-catenin信号增强,细胞增殖增加,体内高表达RSPO1也会引起LGR5+细胞大量特异的增殖[47,50]。 Carmon等[51]利用传统的生化方法发现RSPOs可与表达Lgr4和LGR5的细胞结合,并且Lgrs与R-spondins间存在相互作用,敲除LGR5会使R-spondins诱导的Lrp6磷酸化作用消失,但过表达LGR5并不能增强Lrp6磷酸化作用,反而限制了磷酸化的最高水平和刺激的可持续时间,即β-连环蛋白的稳定化。De lau等[52]发现RSPOs还可与Lgr6结合,并进一步研究了RSPOs、Lgr蛋白、Lrp、Frizzelds间的相互作用,免疫共沉淀结果表明细胞表面Wnt通路复合物Frizzeld5/7、Lrp5/6和Lgr4 LGR5间存在功能关联。研究表明,R-spondin/Lgr可能是通过与Lrp相互作用直接刺激Wnt途径,而没有进一步产生单独的胞内信号。研究者认为RSPOs要传导信号,必须与Lgr蛋白结合,Lgr蛋白募集结合了Wnt信号受体激动剂的Frizzled/LRPs复合物,成功激活通路后,导致LRP受体磷酸化,最终干扰关键分子β-catenin的降解(图1)[53]。总之,R-spondins通过与Lgr4、LGR5、Lgr6相互作用增强Wnt信号,其机制仍不十分清楚,但Lgrs与Lrp5/6、Frizzelds的作用表明它们是Wnt配体的关键受体复合物。"
| [1] Clarke MF, Dick JE, Dirks PB,et al.Cancer stem cells--perspectives on current status and future directions: AACR Workshop on cancer stem cells.Cancer Res. 2006; 66(19):9339-9344. [2] Brabletz S, Schmalhofer O, Brabletz T.Gastrointestinal stem cells in development and cancer.J Pathol. 2009;217(2): 307-317. [3] Hsu SY, Liang SG, Hsueh AJ.Characterization of two LGR genes homologous to gonadotropin and thyrotropin receptors with extracellular leucine-rich repeats and a G protein-coupled, seven-transmembrane region.Mol Endocrinol. 1998;12(12):1830-1845. [4] McDonald T, Wang R, Bailey W,et al.Identification and cloning of an orphan G protein-coupled receptor of the glycoprotein hormone receptor subfamily.Biochem Biophys Res Commun. 1998;247(2):266-270. [5] Chen JD1, Pan J, McCallum RW.Clinical significance of gastric myoelectrical dysrhythmias.Dig Dis. 1995;13(5):275- 290. [6] Verne GN, Soldevia-Pico C, Robinson ME,et al.Autonomic dysfunction and gastroparesis in cirrhosis.J Clin Gastroenterol. 2004;38(1):72-76. [7] Barker N, van Es JH, Kuipers J,et al.Identification of stem cells in small intestine and colon by marker gene Lgr5.Nature. 2007;449(7165):1003-1007. [8] Kemper K, Prasetyanti PR, De Lau W,et al.Monoclonal antibodies against Lgr5 identify human colorectal cancer stem cells.Stem Cells. 2012;30(11):2378-2386. [9] Sato T, Vries RG, Snippert HJ,et al.Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche.Nature. 2009;459(7244):262-265. [10] Barker N, Huch M, Kujala P,et al.Lgr5(+ve) stem cells drive self-renewal in the stomach and build long-lived gastric units in vitro.Cell Stem Cell. 2010;6(1):25-36. [11] Huh YH, King J, Cohen J,et al. SACK-expanded hair follicle stem cells display asymmetric nuclear Lgr5 expression with non-random sister chromatid segregation.Sci Rep. 2011;1: 176. [12] Morris RJ, Liu Y, Marles L, et al.Capturing and profiling adult hair follicle stem cells.Nat Biotechnol. 2004;22(4):411-417. [13] Jaks V, Barker N, Kasper M,et al. Lgr5 marks cycling, yet long-lived, hair follicle stem cells.Nat Genet. 2008;40(11): 1291-1299. [14] Welm BE, Tepera SB, Venezia T,et al.Sca-1(pos) cells in the mouse mammary gland represent an enriched progenitor cell population.Dev Biol. 2002;245(1):42-56. [15] 朱悦,孙保存.乳腺干细胞标记物的研究进展[J].中国肿瘤临床, 2007,34(15):874-876. [16] Visvader JE, Lindeman GJ.Mammary stem cells and mammopoiesis.Cancer Res. 2006;66(20):9798-9801. [17] Stingl J, Eirew P, Ricketson I,et al.Purification and unique properties of mammary epithelial stem cells.Nature. 2006; 439(7079):993-997. [18] Ginestier C, Hur MH, Charafe-Jauffret E,et al.ALDH1 is a marker of normal and malignant human mammary stem cells and a predictor of poor clinical outcome.Cell Stem Cell. 2007; 1(5):555-567. [19] Meropol NJ, Berger NA.Colon cancer recurrence: insights from the interface between epidemiology, laboratory science, and clinical medicine.J Natl Cancer Inst. 2012;104(22): 1697-1698. [20] McClanahan T, Koseoglu S, Smith K,et al.Identification of overexpression of orphan G protein-coupled receptor GPR49 in human colon and ovarian primary tumors.Cancer Biol Ther. 2006;5(4):419-426. [21] Takahashi H, Ishii H, Nishida N,et al.Significance of Lgr5(+ve) cancer stem cells in the colon and rectum.Ann Surg Oncol. 2011;18(4):1166-1174. [22] Barker N, Ridgway RA, van Es JH, et al.Crypt stem cells as the cells-of-origin of intestinal cancer.Nature. 2009;457(7229): 608-611. [23] Uchida H, Yamazaki K, Fukuma M, et al.Overexpression of leucine-rich repeat-containing G protein-coupled receptor 5 in colorectal cancer.Cancer Sci. 2010;101(7):1731-1737. [24] Saigusa S, Inoue Y, Tanaka K,et al.Significant correlation between LKB1 and LGR5 gene expression and the association with poor recurrence-free survival in rectal cancer after preoperative chemoradiotherapy.J Cancer Res Clin Oncol. 2013;139(1):131-138. [25] Fan XS, Wu HY, Yu HP,et al.Expression of Lgr5 in human colorectal carcinogenesis and its potential correlation with beta-catenin.Int J Colorectal Dis. 2010;25(5):583-590. [26] 彭亮,梁纯,梁燕,等.结直肠癌LGR5表达对患者预后的影响[J].现代消化及介入治疗,2010,15(5):284-287. [27] Wu XS, Xi HQ, Chen L.Lgr5 is a potential marker of colorectal carcinoma stem cells that correlates with patient survival. World J Surg Oncol. 2012;10:244. [28] Uehara T, Ma D, Yao Y,et al. H. pylori infection is associated with DNA damage of Lgr5-positive epithelial stem cells in the stomach of patients with gastric cancer.Dig Dis Sci. 2013; 58(1): 140-149. [29] Becker L, Huang Q, Mashimo H.Immunostaining of Lgr5, an intestinal stem cell marker, in normal and premalignant human gastrointestinal tissue.ScientificWorldJournal. 2008;8: 1168-1176. [30] Simon E, Petke D, Böger C,et al.The spatial distribution of LGR5+ cells correlates with gastric cancer progression.PLoS One. 2012;7(4):e35486. [31] Sullivan JP, Minna JD, Shay JW.Evidence for self-renewing lung cancer stem cells and their implications in tumor initiation, progression, and targeted therapy.Cancer Metastasis Rev. 2010;29(1):61-72. [32] ] Kim CF, Jackson EL, Woolfenden AE, et al.Identification of bronchioalveolar stem cells in normal lung and lung cancer. Cell. 2005;121(6):823-835. [33] Ryuge S, Sato Y, Jiang SX,et al.The clinicopathological significance of Lgr5 expression in lung adenocarcinoma.Lung Cancer. 2013;82(1):143-148. [34] McClanahan T, Koseoglu S, Smith K,et al.Identification of overexpression of orphan G protein-coupled receptor GPR49 in human colon and ovarian primary tumors.Cancer Biol Ther. 2006;5(4):419-426. [35] Amsterdam A, Raanan C, Schreiber L, et al. Localization of the stem cell markers LGR5 and Nanog in the normal and the cancerous human ovary and their inter-relationship.Acta Histochem. 2013;115(4):330-338. [36] Yamamoto Y, Sakamoto M, Fujii G,et al.Overexpression of orphan G-protein-coupled receptor, Gpr49, in human hepatocellular carcinomas with beta-catenin mutations. Hepatology. 2003;37(3):528-533. [37] Fukuma M, Tanese K, Effendi K,et al.Leucine-rich repeat-containing G protein-coupled receptor 5 regulates epithelial cell phenotype and survival of hepatocellular carcinoma cells.Exp Cell Res. 2013;319(3):113-121. [38] Tanese K, Fukuma M, Yamada T,et al.G-protein-coupled receptor GPR49 is up-regulated in basal cell carcinoma and promotes cell proliferation and tumor formation.Am J Pathol. 2008;173(3):835-843. [39] Becker L, Huang Q, Mashimo H.Lgr5, an intestinal stem cell marker, is abnormally expressed in Barrett's esophagus and esophageal adenocarcinoma.Dis Esophagus. 2010;23(2): 168-174. [40] 丁黎葭,陈世耀,纪元,等.LGR5 在 Barrett 食管和早期食管鳞癌中的表达[J].胃肠病学,2011,16(6):328-331. [41] von Rahden BH, Kircher S, Lazariotou M,et al.LgR5 expression and cancer stem cell hypothesis: clue to define the true origin of esophageal adenocarcinomas with and without Barrett's esophagus. J Exp Clin Cancer Res. 2011;30: 23. [42] Katoh M, Katoh M.WNT signaling pathway and stem cell signaling network.Clin Cancer Res. 2007;13(14):4042-4045. [43] Birchmeier W.Stem cells: Orphan receptors find a home. Nature. 2011;476(7360):287-288. [44] Van der Flier LG, Sabates-Bellver J, Oving I,et al.The Intestinal Wnt/TCF Signature.Gastroenterology. 2007;132(2): 628-632. [45] Garcia MI, Ghiani M, Lefort A,et al.LGR5 deficiency deregulates Wnt signaling and leads to precocious Paneth cell differentiation in the fetal intestine.Dev Biol. 2009;331(1): 58-67. [46] Kazanskaya O, Glinka A, del Barco Barrantes I,et al. R-Spondin2 is a secreted activator of Wnt/beta-catenin signaling and is required for Xenopus myogenesis.Dev Cell. 2004;7(4):525-534. [47] Kim KA, Kakitani M, Zhao J,et al.Mitogenic influence of human R-spondin1 on the intestinal epithelium.Science. 2005; 309(5738):1256-1259. [48] Nam JS, Turcotte TJ, Smith PF,et al.Mouse cristin/R-spondin family proteins are novel ligands for the Frizzled 8 and LRP6 receptors and activate beta-catenin-dependent gene expression. J Biol Chem. 2006;281(19):13247-13257. [49] Kim KA, Zhao J, Andarmani S,et al.R-Spondin proteins: a novel link to beta-catenin activation.Cell Cycle. 2006;5(1): 23-26. [50] Ootani A, Li X, Sangiorgi E,et al.Sustained in vitro intestinal epithelial culture within a Wnt-dependent stem cell niche.Nat Med. 2009;15(6):701-706. [51] Carmon KS, Gong X, Lin Q,et al.R-spondins function as ligands of the orphan receptors LGR4 and LGR5 to regulate Wnt/beta-catenin signaling.Proc Natl Acad Sci U S A. 2011; 108(28):11452-11457. [52] de Lau W, Barker N, Low TY,et al.Lgr5 homologues associate with Wnt receptors and mediate R-spondin signalling.Nature. 2011;476(7360):293-297. [53] Schuijers J, Clevers H.Adult mammalian stem cells: the role of Wnt, Lgr5 and R-spondins.EMBO J. 2012;31(12):2685- 2696. [54] Morita H, Mazerbourg S, Bouley DM,et al.Neonatal lethality of LGR5 null mice is associated with ankyloglossia and gastrointestinal distension.Mol Cell Biol. 2004;24(22):9736- 9743. [55] Walker F, Zhang HH, Odorizzi A,et al.LGR5 is a negative regulator of tumourigenicity, antagonizes Wnt signalling and regulates cell adhesion in colorectal cancer cell lines.PLoS One. 2011;6(7):e22733. |
| [1] | Zhang Yingying, Wang Yinglei, Meng Lin, Xiao Lin, Li Zhonghai, Zhao Zhankui, Wu Houke. RNA interferes with Id2 gene expression to inhibit proliferation and invasion of PC-3 prostate cancer stem cells [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(9): 1342-1348. |
| [2] | Han Mingli, Lü Pengwei, Qian Xueke, Yang Xue, Yang Yunqing, Gu Yuanting. MicroRNA-10b regulates aldehyde dehydrogenase 1 mRNA and protein expression in breast cancer MCF-7 cell line [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(9): 1349-1353. |
| [3] | Zha Luqin, Han Bengao, Zhang Chaojie. Metformin regulates proliferation and apoptosis of gastric cancer stem cells through the Akt pathway [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(5): 657-662. |
| [4] | Xie Dongke, He Xia, Liao Kainan. Inhibitory effects and mechanisms of tetrandrine on proliferation and stemness marker expression of neuroblastoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(5): 729-733. |
| [5] | Cheng Haiyan, Long Heming, Xie Xiaoying, Li Feng. ciRS-7 regulates the stemness of cervical cancer stem cells: effects and mechanisms [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(13): 2009-2015. |
| [6] | Xia Rongjun, Ou Yingfu, Xing Weishan, Zheng Linlin, Yu Shengjin, Lin Lijuan. Long non-coding RNA H19 promotes proliferation and invasion of gastric cancer stem cells [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(13): 2022-2027. |
| [7] | Qi Minjun, Wu Xiaopeng, Zhou Zhongxing, Jiang Xiaodong. miR-142-3p effect on the stemness of bladder cancer stem cells via regulation of S1PR3 [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(13): 2028-2034. |
| [8] | Zhang Zhen-hua, Su Zi-jie, Kan Yun-zhen, Liu Qiu-yu. Effects of leukemia inhibitory factor receptor overexpression on stemness maintenance and lung metastasis in vivo of thyroid cancer stem cells [J]. Chinese Journal of Tissue Engineering Research, 2018, 22(9): 1376-1381. |
| [9] | Han Fang-zheng, Zhang Xiao-lin, Dong Wei-yi, Xie Yun-ting. Co-expression of CD24 and CD44 in gastric carcinoma and its influence on clinicopathological parameters and prognosis [J]. Chinese Journal of Tissue Engineering Research, 2018, 22(29): 4625-4630. |
| [10] | Zhao Wei, Tang Hui, Shao Chuan, Qiao Fei. Insulin-like growth factor binding protein-2 promotes the proliferation, migration and invasion of glioma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2018, 22(29): 4631-4636. |
| [11] | Yu Xiao-yu, Wu Di, Wang Jing, Li Fei, Bai Xu-le, Zhao Feng-shu, Dou Jun. Isolation and biological identification of tumor stem cells from ovarian cancer ID8 cell lines [J]. Chinese Journal of Tissue Engineering Research, 2018, 22(29): 4687-4691. |
| [12] | He Xin-zhi, Lu Guan-ming, Pu Jian, Wei Zhong-heng, Ma Yan-fei, Chen Yong-cheng, Qin Qiang, Huang Qian-fang, Luo Zhi-zhai. miR-93 effects on the proliferation, apoptosis and invasion of tumor stem cells in thyroid papillary carcinoma [J]. Chinese Journal of Tissue Engineering Research, 2018, 22(25): 3987-3992. |
| [13] | Yao Bin, Zhang Qing-hua. Effects of Wnt/beta-catenin signaling pathway on the proliferation, migration and invasion of ovarian cancer stem cells [J]. Chinese Journal of Tissue Engineering Research, 2018, 22(25): 4001-4006. |
| [14] | Luo Qiong, Gao Guo-xiang, Qin Shi-yun. Drug-loaded tumor exosomes combined with radiotherapy inhibit the proliferation of breast cancer stem cells [J]. Chinese Journal of Tissue Engineering Research, 2018, 22(21): 3286-3291. |
| [15] | Guo Rui, Dai Jian-feng, Luo Yu-ming, Zhao Hai-ming, Tang Peng. Regulation of Smad4 by miRNA-196a-5p influences gastric cancer stem cell characteristics [J]. Chinese Journal of Tissue Engineering Research, 2018, 22(21): 3310-3315. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||