Chinese Journal of Tissue Engineering Research ›› 2017, Vol. 21 ›› Issue (34): 5558-5564.doi: 10.3969/j.issn.2095-4344.2017.34.024
Previous Articles Next Articles
Application of bone grafting and tissue engineering scaffold in oral implantation involving maxillary sinus elevation
- 1Second Affiliated Hospital of Xingtai Medical College, Xingtai 054000, Hebei Province, China; 2Department of Psychology, Chengde Medical University, Chengde 067000, Hebei Province, China; 3Worker’s Hospital of Xiandewang Branch Office of Jinzhong Energy Xingtai Mining Industry Group Co., Ltd., Xingtai 054103, Hebei Province, China; 4Health Team of Hetian Detachment of Xinjiang Armed Police Corps, Hetian 848011, Xinjiang Uygur Autonomous Region, China; 5Xingtai Medical College, Xingtai 054000, Hebei Province, China
-
Received:2017-06-28Online:2017-12-08Published:2018-01-04 -
Contact:Li Rui-yu, Professor, Chief physician, Second Affiliated Hospital of Xingtai Medical College, Xingtai 054000, Hebei Province, China -
About author:Li Lin-feng, Associate chief physician, Second Affiliated Hospital of Xingtai Medical College, Xingtai 054000, Hebei Province, China -
Supported by:the Funded Project of Henan Provincial Administration of Traditional Chinese Medicine, No. 2014115
CLC Number:
Cite this article
Li Lin-feng, Li Yue, Li Rui-yu, Hao Yue-ling, Li Meng, Zhang Jun-hui, Dang Ying, Li Bing, Wang Wen-jie.
share this article
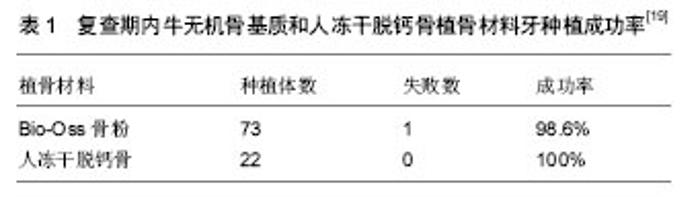
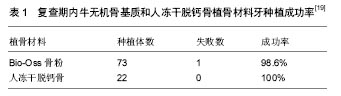
2.1 自体骨和异体骨在上颌窦提升种植体植入中的作用 2.1.1 自体骨 自体骨为取自患者自身的骨,包括松质骨、皮质骨或带血管的骨瓣移植等,是目前植骨的金标准,因为它是惟一具有成骨性、骨诱导性和骨引导性的植骨替代材料。严宁等[9]对7例牙槽骨高度不足的上颌后牙种植进行上颌窦提升、植自体骨并同期种植,6个月后X射线片显示自体骨已改建形成了新骨,增加了牙槽骨高度,满足了种植要求,并与种植体骨形成紧密的骨性结合;种植体植入6个月后进行二期修复,说明植自体骨提升上颌窦增加了上颌后牙区的牙槽骨高度,拓展了种植的适应证,方法简单。自体骨的具体取骨部位可选择下颌颏部联合处、上颌结节、下颌升支、颅顶和髂前上棘等,其成骨能力最强,效果最稳定,一直被视为植骨的最佳选择。应用自体骨移植物进行上颌窦提升,其优点是操作简便、手术区视野清晰、取骨方便、松质骨较多、抗感染能力强,可获得长期存活率,保证种植体周围骨量充足[10]。有研究对25例上颌严重萎缩牙缺失患者在种植体植入前用自体骨植入进行上颌窦提升,种植体10年存活率为94.48%,应用自体骨进行上颌窦提升以增加骨量,保证牙种植体周围长期稳定性[11]。有研究将自体骨移植物移植到种植体的上方,以确保种植体周围窦膜不会塌陷,结果显示所有种植体稳定,没有种植体丢失,放射学评估显示3个月后的骨增长为(3.2±0.9) mm,1年后的骨增长为(3.6±0.9) mm,说明自体骨移植物具有良好的骨形成和骨整合性[12]。动物实验应用自体骨进行上颌窦提升并同期植入种植体,结果显示骨形成从窦底部开始,在种植体周围有骨桥蛋白的表达[13]。也有研究用颊脂肪垫对6例患者进行上颌窦提升,植入后7.2个月放射学和组织学上观察到上颌窦的新骨形成,植入物存活率达95%,说明颊脂肪垫可作为自体成骨移植物材料提高上颌窦提升成功率[14]。然而自体骨移植需开辟第二术区增加了患者痛苦,会对供区造成创伤,由于自体骨移植存在不足,有关自体骨移植替代物,如异种移植物、同种异体移植物和异体移植物或人工骨材料的研究显得非常必要。 2.1.2 异体骨 同种异体骨最大的优势是含有骨形态发生蛋白,能够促进骨生长,同种异体骨移植是较好的选择。沈庆赋等[15]应用同种异体冻干骨颗粒在18例上颌牙列缺损,上颌窦骨量不足,需要行上颌窦提升植骨的临床病例中上颌窦提升延期或同期种植,结果显示种植体牢固,随访32个月没有种植体松动,脱落情况发生,效果较好。冷冻干燥表面脱钙异体骨,既有一定的力学支持能力又有骨诱导作用,且可塑性强,适用于上颌窦提升中作为植骨材料,能室温保藏,携带方便,易于临床应用[16]。有研究从供体收集新鲜冷冻骨,比较上颌窦移植新鲜冷冻骨和自体骨移植对新骨形成的影响,分别应用新鲜冷冻骨和自体骨进行上颌窦移植后6个月植入牙种植体,结果新鲜冷冻骨和自体骨移植有新骨形成,牙种植体存活率相似[17]。以往研究的同种异体骨多为颗粒,有研究用可注射性的同种异体骨移植物用于上颌窦提升,并比较了颗粒同种异体骨移植材料和可注射制剂同种异体骨移植物的移植效果,结果显示无论使用何种形式同种异体骨移植材料所有种植体都成功种植,可注射制剂同种异体骨移植物移植所用时间少于颗粒同种异体骨移植材料,因此注射制剂同种异体移植物材料可替代颗粒形式的同种异体移植骨,以降低操作时间[18]。 邓飞龙等[19]采用牛无机骨基质和人冻干脱钙骨对56例患者共60侧上颌窦行植骨提升术,同期或延期行牙种植,结果显示在所植入95枚种植体中共有1枚种植体松动脱落,其余种植体均与新形成骨组织形成良好的骨结合,种植体周围未见明显骨吸收阴影,种植体3年成功率为98.9%(表1),说明牛无机骨基质骨粉和同种异体冻干脱钙骨作为上颌窦底植骨提升移植材料是可行的。经过脱蛋白处理保留无机骨成分,主要障碍是免疫排斥反应,抗原性引起的免疫排斥反应是导致异体骨移植失败的主要因素。脱矿处理是降低或消除异体骨移植抗原的有效方法之一,全脱矿异体骨具有抗原性低、骨诱导能力强的特点。有研究用去蛋白牛骨矿物质或自体骨移植物提升上颌窦,从胫骨收集自体骨移植物,将相同剂量的自体骨移植物或去蛋白牛骨矿物质颗粒置于窦黏膜下,并将种植体植入到升高的上颌窦中,植入后7 d,在去蛋白牛骨矿物质颗粒和自体骨移植物植入位置发现新形成的矿化骨,去蛋白牛骨矿物质颗粒和自体骨移植物置入有助于种植体的愈合[20]。有研究将对19例后牙上颌骨骨质萎缩和垂直骨高度≤4 mm的患者用无机牛骨与自体骨复合植入用于上颌窦提升,结果显示新形成骨量较高,种植体植入该部位后有足够的稳定性,种植体存活率达到92.86%[21]。有研究分别应用去蛋白牛骨基质移植物与自体骨移植物进行上颌窦提升中,随后分别植入32个和27个种植体,结果显示去蛋白牛骨基质移植有2个种植体失效,自体骨移植未见种植体失效,去蛋白牛骨基质移植组有1例发生并发症,自体骨移植组有2例发生并发症,两组在垂直骨高度上无显著差异[23]。用牛异种移植物用于上颌窦提升6个月后可见新骨形成,可为种植体提供良好的植入位置,促进种植体修复[22]。"
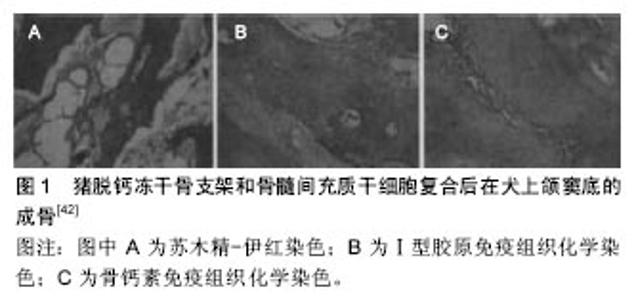
2.2 人工骨在上颌窦提升种植体植入中的作用 由于上颌后牙区的皮质骨厚度、骨密度和宽度每个人之间都有差异,因此临床上上颌窦底骨高度不足的情况,应根据上颌窦提升高度不同选用不同的充填材料,用合成移植物材料进行上颌窦提升,随后常规植入牙种植体,可改善骨-种植体物接触率[24]。陈璐等[25]通过上颌窦闭合式提升自体骨复合人工骨移植同期植入种植体,结果说明成骨时间短,操作简便,能维持种植体的长期稳定。章宏毅等[26]采用传统成骨诱导剂+人工骨粉提升上颌窦底的方法,发现在快速成骨及成骨的有效性方面明显优于单纯的人工骨粉上颌窦底填充法。有研究在37例患者窦区植入生物玻璃和/或同种异体移植物,随后植入40个牙种植体,并观察牙种植体植入后周围移植物骨高度,结果显示经过39.2个月随访所有牙种植体都达到临床稳定性,窦区玻璃和/或同种异体移植物骨高度为(7.0±1.9) mm,随访植物骨高度降低至(4.6±1.9) mm,上颌窦提升过程中生物玻璃和/或同种异体移植物都先经过重建随后有所收缩,但可保证种植体稳定性[27]。 羟基磷灰石可作为上颌窦提升填充物,以自体骨和牛源性羟基磷灰石作为上颌窦提升材料,随后植入钛种植体,观察骨再生情况及骨-种植体结合率,结果发现各移植物组都发现新骨形成,在矿物质成分、骨-种植体结合率上没有显著差异,但自体骨移植组矿物质成分在4-8周显著下降,但各种材料种植体植入的效果满意[28]。有研究用羟基磷灰石粉末胶原膜作为人工骨移植材料,上颌窦提升后将羟基磷灰石粉末胶原膜置于升高的窦黏膜上,经过4或8周的愈合期进行种植体植入。结果显示种植体周围大量新骨形成,并显示骨整合[29]。有研究颌窦提升用纳米晶体羟基磷灰石颗粒填充,结果显示在窦区有新骨形成,是自体骨和异种骨移植材料的理想替代材料[30]。 β-磷酸三钙作为上颌窦增强移植物可增加骨量,并无炎症反应,未见牙种植体种植失败[31]。在牙种植体放置之前将磷酸三钙用于上颌窦底部抬高可增加骨高度,促进新骨形成。有研究分析了纳米羟基磷灰石和纳米β-磷酸三钙晶体复合物在上颌窦提升中的应用,种植体植入后显示出良好的稳定性,平均观察21.45个月后,纳米羟基磷灰石和纳米β-磷酸三钙晶体复合物显示出良好的骨整合和种植体周围骨稳定性[32]。同样有研究用由60%羟基磷灰石和40%β-磷酸三钙组成的合成双相磷酸钙用于上颌窦提升,评价骨形成的质量和数量,在6个月的愈合期之后于种植体放置前进行活检,结果显示合成的双相磷酸钙有较好的稳定性,其填充后可利于随后的牙种植体植入,新形成的骨具有小梁结构且与替代材料紧密接触,双相磷酸钙具有骨传导性质[33]。 上颌窦抬高的目的是增加该区域中的骨高度,以用于支撑牙种植体植入修复牙缺损修复。用磷酸钙骨水泥作为填充材料,良好的生物相容性使其与骨紧密接触,有很好的骨传导能力,可作为上颌窦提升填充材料[34]。应用双相微孔和大孔磷酸钙结合纤维蛋白封闭剂进行上颌窦提升后,上颌窦有20%新骨形成,多为层状骨,种植体植入后1年移植物高度保持稳定,新生骨形成质量与,种植成功率与自体骨类似。用双相微孔和大孔磷酸钙结合纤维蛋白封闭剂复合进行上颌窦提升安全,且耐受和良好,支持骨再生[35]。有研究比较了去蛋白化的牛骨同种异体移植物和双相磷酸钙的骨形成情况,对5例上颌骨萎缩患者分别应用去蛋白化的牛骨同种异体移植物和双相磷酸钙)进行上颌窦提升,3-8个月后植入32个牙种植体,结果显示种植体均成功植入并达到稳定性。去蛋白化的牛骨同种异体移植物和双相磷酸钙移植后骨量、移植物体积、骨矿化程度相似,但经活检发现双相磷酸钙移植物检比牛骨同种异体移植物具有相对更多的类骨质[36]。有研究评估了新型合成双相磷酸钙或脱蛋白牛骨用作上颌窦提升后种植体植入的成功率。在窦膜抬高后填充合成双相磷酸钙或脱蛋白牛骨,移植后各有1个种植体丢失,总存活率为96.8%,两种移植材料种植体周围骨丢失未见明显差异[37]。但也有研究显示上颌窦提升中应用骨移植材料未见明显优势,该研究比较了上颌窦提升中应用和未应用双相磷酸钙移植物对新骨形成和种植体稳定性的影响,测量骨-种植体接触率、牙槽骨高度、骨密度和移植材料密度,评估种植体稳定性,结果应用和未应用双相磷酸钙移植物均发现有新骨形成,但未应用双相磷酸钙移植物其骨-种植体接触率和骨密度高于应用双相磷酸钙移植物,未应用双相磷酸钙移植物有自发新骨形成和更好的骨-种植体接触率[38]。 2.3 组织工程生物支架材料在上颌窦提升种植体植入中的作用 近年来,随着组织工程学的发展,使组织工程化骨替代其他植骨替代材料用于修复种植体植入区的骨量不足成为可能,并将成为口腔种植中最理想的植骨替代材料。到目前为止,组织工程骨在上颌窦提升中的研究报道不多,因此有必要探讨组织工程骨在上颌窦这一特殊生理环境中的成骨效果及新生骨与同期种植体的整合情况。骨髓间充质干细胞是来自骨髓的具有多分化潜能的细胞,在特定分化条件下可分化为成骨、软骨、脂肪、肌肉等细胞。骨髓间充质干细胞复合无机小牛骨粉、透明质酸、磷酸三钙等的组织工程骨可诱导新骨的形成,在四肢及颌面部的应用已取得成功。将牛骨矿物分别与自体单核干细胞的自体骨髓浓缩物或自体骨结合进行上颌窦提升,与牛骨矿物结合自体骨移植相比,牛骨矿物结合自体单核干细胞移植的骨形成率较高,所有种植体都达到临床稳定性,将骨髓间充质干细胞种植于牛骨矿物上可诱导足够的新骨形成,与牛骨矿物结合自体骨移植相比,能有效完成种植体植入[39-40]。培养成骨细胞样细胞,将培养的细胞接种在去矿物质的牛骨基质或脱水矿化骨制成的支架上并进行移植,移植5个月后去矿物质的牛骨基质表现为层状骨和类骨质,12个月后表现为纤维结缔组织,脱水矿化骨支架在移植5个月后发现炎症和骨吸收,12个月后可见包封脱水矿化骨支架残余物的松质骨形成,支架材料的制备及生物力学稳定性可能会影响移植后的新骨形成[41]。余优成等[42]观察猪脱钙冻干骨支架和骨髓间充质干细胞复合后在犬上颌窦底的成骨情况,结果发现应用冻干脱钙骨支架与骨髓间充质干细胞复合的组织工程复合物在上颌窦提升时,具有良好的成骨能力,可形成正常骨组织,种植体均可与组织工程人工骨发生骨整合,效果良好(图1)。研究认为将无机材料作为组织工程支架材料有利于种子细胞的黏附和增殖,具有良好的生物相容性,在兔上颌窦底提升中,无机材料可作为骨替代材料成功用于其中,而利用组织工程学的方法将骨髓间充质干细胞与材料复合,可有效促进上颌窦中新骨的形成[43]。骨髓间充质干细胞在体外与无机小牛骨粉复合良好;组织工程骨在犬上颌窦提升中成骨早,新生骨量多,与同期种植体结合良好[44]。有研究将成年间充质干细胞加载到双相羟基磷灰石/β-磷酸三钙复合支架上进行上颌窦抬高,上颌窦抬高后3个月测量骨高度并植入30个种植体,结果显示30个种植体有28个获得成功,羟基磷灰石/β-磷酸三钙复合支架有类骨质和骨形成,没有炎性细胞浸润,骨再生率为41.34%,所有种植体在4个月后达到临床骨整合,骨高度增加,间充质干细胞与双相羟基磷灰石/β-磷酸三钙等骨源性生物材料复合可促进骨形成,使种植体成功植入[45]。有研究用组织工程骨复合物磷酸钙水泥支架结合骨髓基质细胞进行上颌窦提升同时牙种植体植入,结果显示3个月的愈合期后,与单独磷酸钙水泥或自体骨移植相比,组织工程磷酸钙水泥支架结合骨髓基质细胞复合物可促进早期骨形成和矿化,并最大限度地保持上颌窦骨高度和体积,促进骨形成,提高骨-种植体接触率,说明组织工程磷酸钙水泥/骨髓基质细胞复合可用于上颌窦提升并同期种植体植入,组织工程骨可增强植入物的稳定性,对改善口腔功能有重要意义[46]。 生长因子是组织工程构建的主要因素,在上颌窦底提升中与生物材料复合,为上颌窦底升高提供了可能和保障,影响牙种植效果。富血小板血浆含有丰富的生长因子,很多研究证明富血小板血浆能促进骨的再生与修复。有研究比较双相磷酸钙结合富血小板血浆与软化牛骨基质结合富血小板血浆在上颌窦底部升高中的效果,移植后6个月放置种植体,共放置42个种植体,同时行组织活检;1年后随访所有种植体均存活,两组新骨形成能力相似,无显著差别,与软化牛骨基质结合富血小板血浆移植组相比,双相磷酸钙结合富血小板血浆有更多的I型胶原,说明双相磷酸钙结合富血小板血浆移植随着时间的延长,骨形成能力会更强[47]。用自体富血小板血纤维蛋白作为上颌窦提升的填充材料,可促进上颌窦骨增殖。在膜和窦底部之间填充富含自体血小板的纤维蛋白,在上颌窦中窦膜抬高后放置种植体,种植体植入后6个月后在种植体下部可观察到骨组织,种植体周围新形成的骨的高度在颊侧为(2.6±2.0) mm,在腭侧为(1.3±1.8) mm[48]。有研究以浓缩生长因子作为移植材料行上颌窦内提升,观察26例患者种植体周围骨水平的改变,结果发现不同剩余牙槽骨高度组间的近、远中边缘骨水平改变比较差异无显著性意义,剩余牙槽骨高度与上颌窦提升高度对种植体周骨组织形成无明显影响,表明在上颌窦内提升时使用浓缩生长因子移植材料的同期植入种植体存留率高,种植体周围牙槽骨稳定。 骨形态发生蛋白是一组具有多种生物活性的生长因子,包括骨形态发生蛋白1-9,其中骨形态发生蛋白2-7均是转化生长因子β超基因家族的成员。体内外实验及临床试验证实骨形态发生蛋白2、骨形态发生蛋白7同源二聚体在诱导异位成骨、修复骨缺损、促进脊椎融合、加速骨联合等方面有显著作用。骨形态发生蛋白与各种生物材料复合构成的各种释放系统被用于临床的骨修复。目前,骨形态发生蛋白复合胶原释放系统的建立和应用备受业界的关注,其中骨形态发生蛋白与胶原的结合方式更是重中之重,有研究比较了载重组骨形态发生蛋白2的聚-DL-乳酸-乙醇酸明胶海绵和自体骨在上颌窦提升中的作用,结果显示载重组骨形态发生蛋白2的聚-DL-乳酸-乙醇酸明胶海绵移植后骨-种植体接触率和骨密度在12个月时较高[51]。上颌窦提升后用载有重组人骨形态发生蛋白2的可吸收胶原海绵填充,可以保证种植体成功植入,且稳定性良好[52-53]。骨形态发生蛋白对骨生成有积极影响,叶展超等[49]抽取12只犬髂部骨髓,体外分离扩增骨髓间充质干细胞,评价骨形态发生蛋白基因强化骨髓间充质干细胞复合牛无机骨基质在上颌窦底提升中的效果,认为骨形态发生蛋白基因强化骨髓间充质干细胞-牛无机骨基质复合骨应用于上颌窦底提升可获得良好的成骨效果。上颌窦提升后,移植载有人类重组DNA骨形态发生蛋白7的胶原蛋白,移植6个月后可见血管化的骨样组织,具有诱导骨形成的能力,可替代自体骨移植用于上颌窦提升提高骨量[50]。 "
| [1]Boyne PJ,James RA.Grafting of the maxillary sinus floor with autogenous marrow and bone.J Oral Surg. 1980;38(8): 613-616.[2]Beretta M,Cicciù M,Bramanti E,et al.Schneider membrane elevation in presence of sinus septa: anatomic features and surgical management.Int J Dent.2012;2012:261905.[3]Baj A,Trapella G,Lauritano D,et al.An overview on bone reconstruction of atrophic maxilla: success parameters and critical issues.J Biol Regul Homeost Agents.2016;30(2 Suppl 1):209-215.[4]Ramos-Murguialday M,Caubet J,Ramis JM,et al.Evaluation of the Ideal Implant Insertion Time in Human Bone Biopsies After Sinus Elevation Using a Combination of Autologous Bone and Graft Substitute. Int J Oral Maxillofac Implants. 2015;30(4):891-899. [5]Schulten EA,Prins HJ,Overman JR,et al.A novel approach revealing the effect of a collagenous membrane on osteoconduction in maxillary sinus floor elevation with β-tricalcium phosphate.Eur Cell Mater.2013;25:215-228.[6]Froum SJ,Wallace SS,Cho SC,et al.Histomorphometric comparison of a biphasic bone ceramic to anorganic bovine bone for sinus augmentation: 6- to 8-month postsurgical assessment of vital bone formation. A pilot study. Int J Periodontics Restorative Dent.2008;28(3):273-281.[7]Cara-Fuentes M,Machuca-Ariza J,Ruiz-Martos A,et al. Long-term outcome of dental implants after maxillary augmentation with and without bone grafting.Med Oral Patol Oral Cir Bucal.2016;21(2):e229-235.[8]Farré-Guasch E,Prins HJ,Overman JR,et al.Human maxillary sinus floor elevation as a model for bone regeneration enabling the application of one-step surgical procedures. Tissue Eng Part B Rev. 2013;19(1):69-82. [9]严宁,黄云飞,周磊.植自体骨在上颌窦提升牙种植术中的临床应用[J].实用医学杂志,2002,18(6):605-606.[10]Jungner M,Legrell PE,Lundgren S.Follow-up study of implants with turned or oxidized surfaces placed after sinus augmentation. Int J Oral Maxillofac Implants.2014;29(6):1380-1387. [11]Schmitt CM,Moest T,Lutz R,et al.Anorganic bovine bone (ABB) vs. autologous bone (AB) plus ABB in maxillary sinus grafting. A prospective non-randomized clinical and histomorphometrical trial.Clin Oral Implants Res.2015;26(9):1043-1050. [12]Raghoebar GM,Meijer HJ,Telleman G,et al.Maxillary sinus floor augmentation surgery with autogenous bone grafts as ceiling: a pilot study and test of principle.Clin Implant Dent Relat Res. 2013;15(4):550-755. [13]Jungner M,Cricchio G,Salata LA,et al.On the Early Mechanisms of Bone Formation after Maxillary Sinus Membrane Elevation: An Experimental Histological and Immunohistochemical Study. Clin Implant Dent Relat Res.2015;17(6):1092-102.[14] Falah M,Srouji S.Use of Buccal Fat Pad for Closure of Perforation and Graft Material in a Maxillary Sinus Elevation Procedure: A Preliminary Study.Int J Oral Maxillofac Implants. 2016;31(4):842-848. [15]沈庆赋,沈晓涵,陆爱萍,等.同种异体冻干骨颗粒在上颌窦提升牙种植术中的临床应用[J].临床口腔医学杂志,2011,27(2):111-112.[16]陈建钢,帅李娅,张伟,等.冷冻干燥^60钴灭菌表面脱钙异体骨修复种植周骨缺损的临床应用[J].武汉大学学报:医学版, 2004, 25(6):672-674.[17]Xavier SP,Dias RR,Sehn FP,et al.Maxillary sinus grafting with autograft vs. fresh frozen allograft: a split-mouth histo morphometric study.Clin Oral Implants Res.2015;26(9): 1080-1085. [18]Irinakis T.Efficacy of injectable demineralized bone matrix as graft material during sinus elevation surgery with simultaneous implant placement in the posterior maxilla: clinical evaluation of 49 sinuses.J Oral Maxillofac Surg. 2011; 69(1):134-141. [19]邓飞龙,曾融生,罗智斌,等.上颌窦提升术中单独应用牛无机骨基质(Bio—Oss)或人冻干脱钙骨的临床评价[J].中国口腔种植学杂志,2004,9(3):112-115.[20]De Santis E,Lang NP,Ferreira S,et al.Healing at implants installed concurrently to maxillary sinus floor elevation with Bio-Oss? or autologous bone grafts. A histo-morphometric study in rabbits. Clin Oral Implants Res.2017;28(5):503-511.[21]Schmitt C,Karasholi T,Lutz R,et al. Long-term changes in graft height after maxillary sinus augmentation, onlay bone grafting, and combination of both techniques: a long-term retrospective cohort study.Clin Oral Implants Res.2014;25(2):e38-46.[22]Calasans-Maia MD,Mourão CF,Alves AT,et al.Maxillary Sinus Augmentation with a New Xenograft: A Randomized Controlled Clinical Trial.Clin Implant Dent Relat Res.2015;17 Suppl 2:e586-93. [23]Merli M,Moscatelli M,Mariotti G,et al.Autogenous bone versus deproteinised bovine bone matrix in 1-stage lateral sinus floor elevation in the severely atrophied maxilla: a randomised controlled trial. Eur J Oral Implantol.2013;6(1):27-37.[24]Philipp A,Duncan W,Roos M,et al.Comparison of SLA? or SLActive? implants placed in the maxillary sinus with or without synthetic bone graft materials--an animal study in sheep.Clin Oral Implants Res.2014;25(10):1142-1148.[25]陈璐,周文清,吴燕平,等.β-磷酸三钙复合自体骨移植在上颌窦闭合式提升中的应用[J].上海口腔医学,2011,20(3):282-285.[26]章宏毅,周鑫才,邓亚丁,等.上颌窦底黏膜下放置传统成骨诱导剂及人工骨粉提升上颌窦底的临床观察[J].临床口腔医学杂志, 2012,28(9):553-555.[27]Chen HH,Lin YC,Lee SY,et al.Influence of Sinus Floor Configuration on Grafted Bone Remodeling After Osteotome Sinus Floor Elevation.J Periodontol. 2017; 88(1):10-16. [28]Kim YS,Kim SH,Kim KH,et al.Rabbit maxillary sinus augmentation model with simultaneous implant placement: differential responses to the graft materials. J Periodontal Implant Sci. 2012;42(6):204-211. [29]Jung UW,Unursaikhan O,Park JY,et al.Tenting effect of the elevated sinus membrane over an implant with adjunctive use of a hydroxyapatite-powdered collagen membrane in rabbits. Clin Oral Implants Res. 2015;26(6):663-670. [30]Bosshardt DD,Bornstein MM,Carrel JP,et al.Maxillary sinus grafting with a synthetic, nanocrystalline hydroxyapatite-silica gel in humans: histologic and histomorphometric results.Int J Periodontics Restorative Dent.2014;34(2):259-267. [31]Schulze-Späte U,Dietrich T,Kayal RA,et al.Analysis of bone formation after sinus augmentation using β-tricalcium phosphate.Compend Contin Educ Dent. 2012;33(5): 364-368.[32]Mertens C,Wiens D,Steveling HG,et al.Maxillary sinus-floor elevation with nanoporous biphasic bone graft material for early implant placement.Clin Implant Dent Relat Res. 2014; 16(3):365-373. [33]Frenken JW,Bouwman WF,Bravenboer N,et al.The use of Straumann Bone Ceramic in a maxillary sinus floor elevation procedure: a clinical, radiological, histological and histomorphometric evaluation with a 6-month healing period.Clin Oral Implants Res.2010;21(2):201-208. [34]Sverzut AT,Rodrigues DC,Lauria A,et al.Clinical,radiographic, and histological analyses of calcium phosphate cement as filling material in maxillary sinus lift surgery.In Oral Implants Res.2015;26(6):633-638. [35]Wagner W,Wiltfang J,Pistner H,et al.Bone formation with a biphasic calcium phosphate combined with fibrin sealant in maxillary sinus floor elevation for delayed dental implant.Clin Oral Implants Res.2012;23(9):1112-1117. [36]de Lange GL,Overman JR,Farré-Guasch E,et al.A histomorphometric and micro-computed tomography study of bone regeneration in the maxillary sinus comparing biphasic calcium phosphate and deproteinized cancellous bovine bone in a human split-mouth model.Oral Surg Oral Med Oral Pathol Oral Radiol.2014;117(1):8-22. [37]Lindgren C,Mordenfeld A,Hallman M.A prospective 1-year clinical and radiographic study of implants placed after maxillary sinus floor augmentation with synthetic biphasic calcium phosphate or deproteinized bovine bone.Clin Implant Dent Relat Res.2012;14(1):41-50. [38]Si MS,Mo JJ,Zhuang LF,et al.Osteotome sinus floor elevation with and without grafting: an animal study in Labrador dogs.Clin Oral Implants Res.2015;26(2):197-203. [39]Rickert D,Vissink A,Slot WJ,et al.Maxillary sinus floor elevation surgery with BioOss? mixed with a bone marrow concentrate or autogenous bone: test of principle on implant survival and clinical performance.Int J Oral Maxillofac Surg. 2014;43(2):243-247. [40]Rickert D,Sauerbier S,Nagursky H,et al.Maxillary sinus floor elevation with bovine bone mineral combined with either autogenous bone or autogenous stem cells: a prospective randomized clinical trial. Clin Oral Implants Res. 2011;22(3): 251-258.[41]Pradel W,Mai R,Manolo Hagedorn G,et al.The biomaterial influences the ossification after sinus floor elevation using tissue-engineered bone grafts.Biomed Tech (Berl). 2008; 53(5):224-228. [42]余优成,吴伟杰,顾章愉,等.骨组织工程技术进行犬上颌窦提升的实验研究[J].中国临床医学,2006,13(5):860-862.[43]孙小娟.osteobone复合bmscs组织工程化骨提升兔上颌窦底的研究[D].上海:上海交通大学医学院附属第九人民医院, 2008: 1-130.[44]李祥,陈松龄,黄代营,等.包绕式盖膜引导骨再生技术在上颌窦底提升同期牙种植中的成骨研究[J].中华口腔医学杂志, 2011, 46(9):547-550.[45]Shayesteh YS,Khojasteh A,Soleimani M,et al.Sinus augmentation using human mesenchymal stem cells loaded into a beta-tricalcium phosphate/hydroxyapatite scaffold. Oral Surg Oral Med Oral Pathol Oral Radiol Endod.2008;106(2):203-209. [46]Zou D,Guo L,Lu J,et al.Engineering of bone using porous calcium phosphate cement and bone marrow stromal cells for maxillary sinus augmentation with simultaneous implant placement in goats.Tissue Eng Part A. 2012;18(13-14): 1464-1478. [47]Taschieri S,Corbella S,Weinstein R,et al.Maxillary Sinus Floor Elevation Using Platelet-Rich Plasma Combined With Either Biphasic Calcium Phosphate or Deproteinized Bovine Bone.J Craniofac Surg. 2016;27(3):702-707.[48]Jeong SM,Lee CU,Son JS,et al.Simultaneous sinus lift and implantation using platelet-rich fibrin as sole grafting material.J Craniomaxillofac Surg.2014;42(6):990-994. [49]叶展超,张文斌,陈晓莉,等.基因强化组织工程骨用于上颌窦底提升的动物实验[J].中华口腔医学杂志,2012,47(2):114-117.[50]van den Bergh JP,ten Bruggenkate CM,Groeneveld HH,et al.Recombinant human bone morphogenetic protein-7 in maxillary sinus floor elevation surgery in 3 patients compared to autogenous bone grafts. A clinical pilot study.J Clin Periodontol.2000;27(9):627-636.[51]Gutwald R,Haberstroh J,Stricker A,et al.Influence of rhBMP-2 on bone formation and osseointegration in different implant systems after sinus-floor elevation. An in vivo study on sheep. J Craniomaxillofac Surg.2010;38(8):571-579. [52]Jensen OT,Cottam JR,Ringeman JL,et al.Experience with bone morphogenetic protein-2 and interpositional grafting of edentulous maxillae: a comparison of Le Fort I downfracture to full-arch (horseshoe) segmental osteotomy done in conjunction with sinus floor grafting.Int J Oral Maxillofac Implants.2013;28(6):e331-348. [53]Cottam JR,Jensen OT,Beatty L,et al.Closure of 1.5-cm alveolar oral antral fistula with intra-alveolar sinus membrane elevation and bone morphogenetic protein-2/collagen graft followed by dental implant restoration: case report.Int J Oral Maxillofac Implants.2013;28(5):e277-282. |
| [1] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [2] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [3] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [4] | He Yunying, Li Lingjie, Zhang Shuqi, Li Yuzhou, Yang Sheng, Ji Ping. Method of constructing cell spheroids based on agarose and polyacrylic molds [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 553-559. |
| [5] | He Guanyu, Xu Baoshan, Du Lilong, Zhang Tongxing, Huo Zhenxin, Shen Li. Biomimetic orientated microchannel annulus fibrosus scaffold constructed by silk fibroin [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 560-566. |
| [6] | Chen Xiaoxu, Luo Yaxin, Bi Haoran, Yang Kun. Preparation and application of acellular scaffold in tissue engineering and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 591-596. |
| [7] | Kang Kunlong, Wang Xintao. Research hotspot of biological scaffold materials promoting osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 597-603. |
| [8] | Shen Jiahua, Fu Yong. Application of graphene-based nanomaterials in stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 604-609. |
| [9] | Zhang Tong, Cai Jinchi, Yuan Zhifa, Zhao Haiyan, Han Xingwen, Wang Wenji. Hyaluronic acid-based composite hydrogel in cartilage injury caused by osteoarthritis: application and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 617-625. |
| [10] | Li Hui, Chen Lianglong. Application and characteristics of bone graft materials in the treatment of spinal tuberculosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 626-630. |
| [11] | Gao Cangjian, Yang Zhen, Liu Shuyun, Li Hao, Fu Liwei, Zhao Tianyuan, Chen Wei, Liao Zhiyao, Li Pinxue, Sui Xiang, Guo Quanyi. Electrospinning for rotator cuff repair [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 637-642. |
| [12] | Chen Jinmin, Chen Suisheng, Ding Jing, Xia Baoquan, Luo Xiaojia, Lu Chenghai. Stability of balloon dilation with injectable calcium sulfate cement for tibial plateau fractures [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 414-418. |
| [13] | Guan Jian, Jia Yanfei, Zhang Baoxin , Zhao Guozhong. Application of 4D bioprinting in tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 446-455. |
| [14] | Liu Jiali, Suo Hairui, Yang Han, Wang Ling, Xu Mingen. Influence of lay-down angles on mechanical properties of three-dimensional printed polycaprolactone scaffolds [J]. Chinese Journal of Tissue Engineering Research, 2022, 10(16): 2612-2617. |
| [15] | Huang Bo, Chen Mingxue, Peng Liqing, Luo Xujiang, Li Huo, Wang Hao, Tian Qinyu, Lu Xiaobo, Liu Shuyun, Guo Quanyi . Fabrication and biocompatibility of injectable gelatin-methacryloyl/cartilage-derived matrix particles composite hydrogel scaffold [J]. Chinese Journal of Tissue Engineering Research, 2022, 10(16): 2600-2606. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||