Chinese Journal of Tissue Engineering Research ›› 2017, Vol. 21 ›› Issue (20): 3255-3262.doi: 10.3969/j.issn.2095-4344.2017.20.022
Previous Articles Next Articles
Pathogenesis and treatment of osteoarthritis: the latest progress
Zheng Xiao-fen
- Longhua People’s Hospital of Shenzhen, Shenzhen 518109, Guangdong Province, China
-
Revised:2017-05-25Online:2017-07-18Published:2017-07-28 -
About author:Zheng Xiao-fen, Nurse-in-charge, Longhua People’s Hospital of Shenzhen, Shenzhen 518109, Guangdong Province, China -
Supported by:the Social Public Welfare Project of Science and Technology Plan of Baoan District in Shenzhen, No. 2012233
CLC Number:
Cite this article
Zheng Xiao-fen. Pathogenesis and treatment of osteoarthritis: the latest progress[J]. Chinese Journal of Tissue Engineering Research, 2017, 21(20): 3255-3262.
share this article
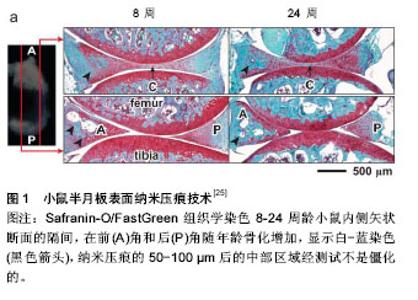
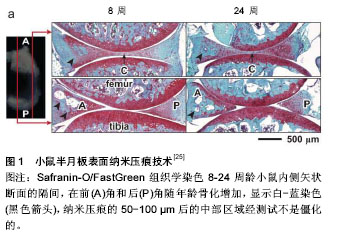
2.1 发病机制研究进展 2.1.1 软骨及软骨细胞与骨关节炎 软骨的退化,骨关节炎主要的标志之一是软骨的退化,现在国际上越来越重视这一点,大量的研究探讨引起软骨退化的诱导因子和修复软骨的方式。但是由于存在高比例的细胞外基质和软骨内缺乏血管,关节软骨很难被修复。由于缺少血管,药物也很难通过机体的血液供应输入到软骨中,只能通过基质缓慢渗透到软骨中,所以修复软骨确实耗时长久而且效果欠佳,最近有文章指出了引起骨软骨关节炎的可能的原因包括:软骨退变,自我吞噬,生物时钟改变,机械力学改变、氧化应激、内部免疫、软骨过度增生、疼痛[1],除此之外,更多学者在做相关的研究。 目前关于软骨细胞表型和骨关节炎的关系也有重大进步。在骨关节炎过程中,关节软骨细胞遭受一系列的损害,包括异常的生物力学应力、促炎性细胞因子和趋化因子以细胞外基质的大量变化。这会引发软骨细胞表型转移并扰乱软骨内稳态。有一些新途径有助于和延续这些被发现的大的表型变化。健康体内的信使核糖核酸的衰退与骨关节炎软骨细胞的信使核糖核酸水平的对比不止受合成速度所控而且还受降解率的控制(即,转录后水平上的调控)。Tew和同事[2]通过放线菌素D追踪5后的微阵列分析检验了健康人体转录组和骨关节炎人体软骨细胞中的信使核糖核酸的衰退。他们报告说,大多数软骨细胞表达的转录是稳定的,但一个子集表现出快速衰减,有趣的是,骨关节炎软骨细胞中的信使核糖核酸半衰期有一个明显的缩短趋势。短暂的转录包括转录调节中涉及的基因、细胞核的定位,或参与程序性细胞死亡的调节。此外,研究发现基因与细胞外基质流动有关,如ADAMTS-1 ADAMTS-5,ADAMTS-9,透明质酸合成酶,HAS2,硫酸乙酰肝素的磺基转移酶,HS3ST3A1,还有NFkB复合成分。这些短暂的转录总体上在骨关节炎软骨细胞中是更高度表达的,这可能意味着它们与依赖骨关节炎中的快速和灵活的基因响应过程有关联[2]。这首开先河的研究给软骨细胞表型的稳定的调节添加一个新的维度。 最近有研究认为氧分压和骨关节炎的严重程度密切相关。在软骨的氧应激反应中,血红素氧化酶起了重要的作用。转录因子Nrf2((nuclear factor (erythroid- derived2)-like 2)是血红素氧化酶的调节因子,在敲除了Nrf2的大鼠中,大鼠均得了严重的关节炎[3]。在大鼠的创伤骨关节炎模型中,萝卜硫素被用来激活Nrf2基因,降低血红素氧化酶的表达,控制骨关节炎,起得了很好的效果[4]。这些研究都表明,血红素氧化酶可能是治疗骨关节炎的新的方式。转化生长因子α是表皮生长因家族的成员,研究发现转化生长因子α能降低软骨的合成代谢[5],但是能增加软骨的降解代谢,因此可用来治疗骨关节炎的软骨退化。最近,Appleton等[6]研究中使用了一种名叫AG1478药物的干扰剂,去抑制大鼠关节炎体内的转化生长因子α,发现这种方法不但能够降低关节软骨的退化和关节炎的严重程度,而且能增加体内血清中Ⅱ型胶原前肽(CPⅡ)的水平,降低胶原蛋白降解产物(C2C)的水平。因为Ⅱ型胶原前肽是胶原合成代谢的标记物,C2C是胶原分解代谢的标记物,所以这种干扰剂有增加胶原合成,降低胶原分解的作用,这个研究证实了药物能有效的阻止创伤后骨关节炎的恶化。软骨退化后的降解产物已经被证明了能引起远期的关节的退化,降解后的碎片比如:Ⅱ型胶原、蛋白多糖、纤连蛋白能通过调节基质金属蛋白酶引起关节远期的退化。同时降解后的产物如特定的碎片、浓度、机械压力都会引进代谢的反应,进一步诱导形成骨关节炎处理这些蛋白聚糖碎片能引起抗合成代谢,增加分解代谢和抗炎症反应。在动物敲除相应的基因(MyD88)后,这些效应都消失[7]。来源软骨的纤连蛋白碎片也产生了同样的效果。 在骨关节炎中,软骨下骨的病理改变常常被认为是次要的,但是早期的软骨下骨的改变能触发骨关节炎的形成。关节炎软骨下骨的退化会引起关节面的硬化和关节面骨赘形成。所以,毫无疑问对软骨下骨的治疗和骨关节炎的预后密切相关,对软骨下骨的研究方向应该是成骨和破骨细胞的生理机制及骨的重塑过程。 2.1.2 力学与骨关节炎 力学和骨关节炎关系密切,Adouni等[8]使用下肢肌肉骨骼模型,该模型是基于步态站立中期的运动学原理建立的。胫股室的接触负荷的分配会受到膝关节内收角度的极大影响。Ateshian等[9]最近总结出了关于复杂的3D关节接触力学的新的计算算法。数字化的PE方法放宽了对模型假设的要求,比如微小应变、一系列的线性关系。这样的接触分析方法,基于多种材料的表象还能预测软骨层中张力的变化。这些方法将有望帮助医生根据获得的医学影像资料对患者进行个体化分析,并且制定出治疗方案。比如,Henak等[10]使用有限元模型以评估髋臼发育不良髋关节骨关节炎的主要诱发因素)时人类臀部的软骨的接触力学。研究结果表明,相比正常髋关节,在髋关节发育不良时,关节盂唇发挥着更为重大作用。具体而言,在髋关节发育不良时,关节盂唇承受的负荷是正常髋关节时的2.8-4倍以上。本次研究充分说明在对髋臼发育不良的患者进行手术时应该将关节盂唇保留。 步行时膝关节负荷是骨性关节病进展的一个十分重要的因素。减少外部膝关节内收力矩负荷已经成为减少关节负荷治疗的一个关键所在。然而,最近的研究表明外部膝关节屈曲负荷在内侧区室负荷问题上也发挥着显著的作用。Chehab等[11]以16例患有内侧膝关节骨性关节病的患者为样本,进行了对外部膝关节内收力矩和外部膝关节屈曲进行为期5年的前瞻性研究,该研究对膝关节软骨的变化与早期站立时的基线膝关节内收和外部膝关节屈曲存在相关性。研究还利用磁共振成像对软骨厚度以及内侧与外侧厚度比的变化(MLTR)进行了测量。其研究结果表明内侧区室的负荷约等于膝关节内收力矩负荷和膝关节屈曲负荷的合力,而不是只等于膝关节内收力矩负荷。该作者更加具体的总结到膝关节内收力矩负荷与股骨头软骨的改变更加密切相关(以MLTR变化测得的结果显示),并且在严重的骨性关节病患者中扮演着更加严重的致病因素,而KFM对胫骨软骨厚度和相对不那么严重的骨性关节病患者产生更加重大的影响。这些研究结果进一步表明单独予以减少膝关节内收力矩的干预可能是不够的,事实上,以增加患者KFM为代价的方式来减少膝关节内收力矩可能对患者的治疗效果是不利的。 Moore和Burris[12]对牛膝关节的空间位置依赖性摩擦和材料性质进行了研究。他们的研究结果表明,在不同区域的如如软骨性质存在着明显的差异,这阐明了改变关节负荷情况的损伤(如前叉韧带或半月板撕裂)会使得软骨的负荷失常,进而导致骨性关节病的进展。为了探索出受损伤的半月板对关节接触力学模式的影响,Wang等[13]通过对12具尸体的膝盖进行多方位步态模仿进而测出关节软骨和半月板承受的区域接触负荷。为准确地模仿闸门,研究人员研发出一款标准化的相互作用的算法,该算法适用于计算胫骨平台上的接触应力。他们的研究结果得出步态周期内的不同点的内侧、外侧半月板的负荷:仅在站立的早期阶段内侧半月板的后方承受负荷,而后侧半月板的的后方在站立的早期和后期均承受负荷。在对力传递和稳定状态时内侧半月板的功能的补充研究中,Walker等[14]对10名正常人膝盖进行单独压缩、压缩和前剪,或者压缩和后剪试验。他们研究发现,负荷类型不一样情况会不相同,但是平均而言,有58%的负荷是通过半月板传递的,余下的42%通过未覆盖的软骨进行传递。这些对正常膝盖的研究发现会对鉴别出存在于受损膝盖中的异常非常有帮助,并且有望帮助我们更好的理解创伤后关节炎的病理力学。 有研究证实力学改变引起半月板损伤会加剧骨关节炎,半月板合并韧带损伤的动物模型已经得以建立。Fischenich等[15]使用一个12周的兔模型,对半月板的力学变化以及发生ACL合并半月板损伤后的蛋白多糖的含量进行了探索。在此次研究中,这种联合损伤导致了半月板的弹性系数和糖胺聚糖覆盖随着时间推移而出现明显的减少。作者指出,尽管目前尚没有测量半月板力学属性的前交叉韧带(ACL)横断面单独研究,但是他们依然推测这种复核损伤很有可能加剧了骨性关节病的进展。因此,需要对这种复合关节组织损伤的影响进行进一步的研究。 目前对骨关节炎的研究中,各种肌肉骨骼组织的生物力学特性的区域变化聚焦了研究者们的目光。比如,关节软骨的平衡和动态压缩系数会增加组织浅表区到组织深表区的深度,并且与深层组织组成及组织细胞外基质超微结构存在着直接相关性。鉴于浅表区在关节润滑、以及类骨性关节病发病方面的重要作用,研究人员尤其对发育和功能相关的这一区域进行了探索。Gannon等[16]推测未成熟的软骨缺乏功能性的浅表区域,因此,只有在成熟软骨中,浅表区的切除会导致动态系数的降低。使用不同年龄段猪的膝关节的股膝沟的内侧和外侧隆起处的骨软骨核心,他们发现软骨浅表区组织会随着年龄发生巨大的变化,因此,在决定组织动态压缩刚度方面扮演着十分重要的角色。所以软骨浅表区的损伤容易导致骨关节炎。 2.1.3 疼痛与骨关节炎 有学者证实疼痛和滑膜炎关系密切,Stoppiello等[17]从29例无症状的捐助者和29例有症状捐助者(全膝关节置换)获取了内侧胫骨软骨。他们分析了两个组之间组织学特性的异同点,并发现与无症状软骨病组相比,有症状软骨病组显示出更显著的软骨细胞完整性的丢失和软骨形态的改变。 然而,与疼痛最强烈相关的特性是滑膜炎(29例有症状的膝盖中有8例显示症状严重的炎症),滑膜炎对应的神经生长因子呈阳性。这些结果表明疼痛和滑膜炎有密切的关系。 目前有很多关于骨关节炎的新型镇痛方式的研究。研究人员探索了关节疼痛和周围神经系统的关系,研究表明神经生长因子能改善骨关节炎疼痛的症状,几家公司都在研究神经生长因子抗体(抗TrkA抗体或受体阻滞剂)对骨关节炎的止痛作用。有研究表明,神经生长因子可能由滑膜细胞产生[17]。然而,软骨也可能产生神经生长因子。两组报证实刺激软骨细胞能诱导神经生长因子,其中一组证实白细胞介素1b和内脏脂肪素能诱导小鼠和人类软骨组织产生神经生长因子[18],而另外一组证实转化生长因子b能诱导牛和人类软骨细胞以ALK5/Smad2/3相依的方式产生神经生长因子mRNA[19]。后者研究有助于了解转化生长因子b在骨关节炎发病的复杂机制中所取的作用。有研究证实抑制神经生长因子能缓解和治疗实验性骨关节炎[20]。 一个研究发现了神经肽及降钙素的作用,在大鼠内侧半月板撕裂的骨关节炎模型中,这两种物质能让外围神经更加敏感。目前有学者对如何缓解骨关节炎疼痛展开了研究。一个研究发现了神经肽及降钙素相关基因缩氨酸的作用,在大鼠内侧半月板撕裂的骨关节炎模型中, 降钙素相关基因缩氨酸与外围神经敏感性相关[21]。研究人员测试了降钙素相关基因缩氨酸抗体的效用,发现抑制降钙素基因相关肽会增加疼痛减轻的时间[22]。有学者使用体内电生理学实验评估了神经元电压门控钠通道的拮抗剂的止痛效果,发现拮抗剂具有止痛的效果[23]。 2.1.4 骨关节炎病因研究的新方法 目前研究发病机制中,对半月板的研究采用了新的办法,有学者使用纳米力学原子力显微镜用于确定半月板的性能,建立了新的骨关节炎的模型。Kwok等[24]使用直径为5 mm的球形的原子力显微镜探针尖端,根据力-位移曲线压痕以评估正常的、老化的和退化的人类半月板的外部、中间以及内侧的Young氏系数。得出了不同区域和不同年龄的骨性关节病的纳米机械分布图。Li等[25]首次使用原子力显微镜的纳米压痕来确定小鼠半月板的性质(图1)。在他们的研究中,使用直径10 mm球形的原子力显微镜探针尖端检测雄性小鼠,他们观察到力和深度的线性关系主要取决于半月板表面的胶原纤维束的拉伸阻力。这些新型建模和检测的方法对研究骨关节炎有很大的帮助。"

近年来,在骨关节炎的研究中,在实验测量和细胞的时间变化模型中采用了几项新的技术,其中包括微管吸吮技术和基于原子力显微镜的纳米压痕技术。已经有学者建立了时间相关的张力松弛数据模型。此外,有研究建立了多孔弹性模型用于研究细胞内液和固体摩擦的相互作用,研究者证实,软骨细胞对应力的应变速率和骨髓基质细胞的动态振荡频率均与细胞内的多孔弹性机制有关[26-27]。这些最近的研究结果提出了有趣的假设,即细胞内细胞骨架的变形和组织中细胞外基质的变形存在相关性,细胞外基质能够支撑关节活动时产生的高张力。 目前骨关节炎中,钙信号传导机制已经成为软骨细胞机械传导研究中的热点。Lee等[28]报道了关于软骨细胞Ca2+和Piezo1和Piezo2密切相关重大发现。首先,他们发现 Piezo1/2在原猪软骨细胞中的过度表达;第二,他们观察到Piezo1/2 的共同表达能够维持动物模型中机械诱发性的Ca2+离子涌入;第三,使用无针尖原子力显微镜悬臂,将高回缩张力施加到软骨细胞能激活 Ca2+通道,Ca2+表达可以被Piezo1或Piezo2特异性siRNA抑制,这些新的研究都有助于帮助大家认识骨关节炎的机制。 2.2 骨关节炎的治疗 骨关节炎的治疗应该基于以非药物和药物联合治疗为主转向预防为主,以降低患病风险和减缓疾病进展为目标。肥胖是可以干预的最重要的危险因素,所以运动和减肥很重要。骨关节炎防治指南推荐非类固醇类抗炎药作为一线治疗膝骨性关节炎的药。尤其是对于老年患者或有并发症的患者,为避免不良反应可使用外用非类固醇类消炎药。骨关节炎的常用药物中氨基葡萄糖似乎并不比安慰剂组有效,其对骨关节炎的防治效果是不确定的。深海鱼油也并不能缓解膝骨关节炎的进展。手术干预应避免用在骨关节炎的早期阶段,关节镜手术并不能治愈骨关节炎,严重骨关节炎应考虑关节置换手术。 2.2.1 骨关节炎的干预治疗 除了止痛,所有伴或不伴并发症的骨关节炎患者的核心干涉措施应该是陆上运动、体质量管理、力量训练、游泳等水中运动,要加强患者教育和自我管理。运动是普遍推荐的临床指南,具体实施则需进行病人评估后给予个体化建议。Meta分析表明为改进关节功能和减轻疼痛,锻炼要小到中等程度,效果类似于非类固醇抗炎药和止痛药[29]。靶向肌肉强化训练结合一般有氧运动,以及基于水的运动练习对于关节功能和活动受限的患者有确实效果。伸展运动和灵活性练习则属于整体治疗膝骨性关节炎的锻炼计划的一部分,可用来维持或增加关节的运动范围。监督小组集体训练和一对一训练对缓解疼痛的效果优于家庭内部运动[30]。 助行器例如拐杖、膝盖支撑和足矫形器都可以减少疼痛和改善功能活动。肥胖是最重要的、可控制的危险因素。有研究发现:20周内体质量减轻5%可明显改善患者膝关节骨关节炎,有症状与通过饮食和训练减重10%的患者症状能得到50%的改善[31]。 2.2.2 骨关节炎的药物治疗 双膦酸盐是强有力的破骨细胞的抑制剂,现在已经广泛的使用在临床上,它能够减少骨量的丢失,可以应用在很多疾病上比如:Paget’s骨病、癌细胞转移性骨病及骨质疏松症,近10年来,有关双膦酸盐的疗效已经被严格的论证,证实了其良好的效果[32]。帕米膦酸二钠是一种双膦酸盐,在去除前交叉韧带诱发的骨关节炎动物模型中,它能短期内完全抑制骨关节炎的产生。如果长期的使用,在动物模型中,它甚至能逆转骨关节炎的病理改变[32]。实验证实,在动物骨关节炎模型中,使用阿仑膦酸钠(另外一种双膦酸盐)能抑制退变的关节软骨内的骨赘的产生和减少关节软骨下骨的骨量的丢失[32]。 药物治疗中非类固醇类抗炎药通常被认为是治疗膝骨性关节炎的首选的一线药物治疗,是缓解静息痛和整体疼痛的有效药物。但是要注意长期使用非类固醇类抗炎药引起的不良反应。每年在美国因非类固醇类消炎药导致胃肠道不良反应造成死亡和住院总人数超过 16 500人,此外它对心脑血管和肾的危害也值得关注。无论是非选择性或者是选择性非类固醇类抗炎药都有发生类似不良反应的风险,但是环氧化酶2抑制剂可降低胃肠道不良反应的发生率,对其他系统的损害有待进一步探索。质子泵抑制剂联合非类固醇类抗炎药同时使用可减少胃肠道风险。同样的Meta分析发现,相比单一使用非类固醇类抗炎药,非类固醇类抗炎药结合质子泵抑制剂可降低消化性不良反应66%的相对风险和9%的绝对风险。 非类固醇类抗炎药治疗的最佳时间尚不清楚。对19个随机研究所做的Meta分析发现[33],选择性或非选择性非类固醇类抗炎药治疗的持续时间和心血管事件的风险之间没有明显的联系,连续塞来昔布使用要比间歇给药对疼痛和关节功能的改善稍稍更有效些,但是二者因不良反应而停药的发生率相似。目前尚未有间歇给药策略与严重胃肠道或心血管不良反应相关性的研究。由于非类固醇类抗炎药的不良不良反应的现状,对乙酰氨基酚(最多4 g/d)可用于轻度至中度骨性关节炎疼痛的常规镇痛,但它不再被骨关节炎治疗指南建议为一线用药。有研究发现对乙酰氨基酚缓解骨性关节炎所致疼痛疗效欠佳[34],且超治疗量服用可增加胃肠道事件和多器官功能衰竭的风险,长时间使用对乙酰氨基酚能增加心血管事件发生的风险,与大量使用非类固醇抗炎药风险类似,二者联合用药,发生胃肠道疾病住院风险比对单独使用乙酰氨基酚和单独使用非类固醇类抗炎药均更高。 局部用药推荐常规定期外用非类固醇类抗炎药治疗。相关的局部不良反应包括皮疹、烧灼感和瘙痒。外用非类固醇类抗炎药适合局部给药,可减少胃肠道的不良反应,对膝关节和手的骨关节炎疗效优于安慰剂,疗效可与口服非类固醇抗炎药相媲美。多个配方已在研究,包括同时含有酮洛芬和双氯芬酸钠的药物[35]。老年膝关节骨关节炎患者的12个月治疗后分析也已显示了1%双氯芬酸钠钠凝胶的安全性,65岁上下两类人群总体发生心血管和胃肠道不良反应的概率类似[36]。到目前为止,大多数研究都只聚焦在膝关节骨关节炎患者,所以外用非类固醇类抗炎药对多关节骨关节炎患者的益处仍不确定。尽管如此,外用非类固醇类抗炎药日益被视为一线用药,尤其是在患者不良事件的风险增加的情况下。辣椒素作为一种替代或作为标准药物治疗的辅助手段,可以外用且有减少膝关节疼痛的效果。 关节内皮质类固醇注射可为骨关节炎患者短期缓解疼痛和改善关节功能,可以考虑用在有关节积液和局部炎症的急性发作期患者。然而,关节腔内注射如果超出4个月一次的频率给药可能导致软骨和关节破坏,并增加感染的风险。关节腔内透明质酸注射剂的好处是不确定的,在Meta分析中看到的结果不一致。临床试验表明效益不同,影响不一。最近双盲试验灵敏度分析发现仅有很少的有益作用[37],关节内糖皮质激素治疗的疗效在短期内比透明质酸更好,但透明质酸鞘内注射疗效更持久。 阿片类药物是由于合并症或禁忌证而不能耐受或坚持一线药物的患者最好的选择。全面的系统分析结果显示,为髋关节和膝关节骨关节炎患者缓解疼痛和改善关节功能,阿片类药物的经口和透皮贴剂比安慰剂组更有效。坏处是大量小到中等不良事件造成患者撤药。阿片类药物长期效用有限,其常见不良反应事件为心血管事件(HR 1.77,95%CI 1.39-2.24)和骨折(HR 4.47,95%CI 3.12-6.41),与安慰剂相比,患者使用4倍剂量更有可能停止阿片类药物不良反应(RR 4.05,95%CI 3.06-5.38)。临床上骨关节炎疼痛常是多因素共同作用所致,是经常和抑郁共存的神经病理性疼痛的疼痛综合征。在对比试验中,服用度洛西汀报道有更多的人可减少痛苦至少30%,优于服用安慰剂(65%和44%)的患者[38]。度洛西汀可以和口服非类固醇类抗炎药联合使用,用作常规骨关节炎治疗减轻疼痛和改善关节功能的辅助用药,其常见不良反应包括恶心、便秘、疲劳、口干和食欲减少。 最常用的替代治疗膝骨性关节炎的药物是氨基葡萄糖。在随机对照试验中,它具有与安慰剂治疗疼痛类似的效果。美国国立卫生研究院资助的研究发现那氨基葡萄糖在减少膝关节疼痛方面不明显优于安慰剂[39]。对于可能的解剖结构改善的效果(减慢或停止进展的软骨损伤和关节其他结构性变化)的相关证据仍存在争议。同样的情况也出现在硫酸软骨素上,它对缓解症状的效果也是不确定的,目前研究尚有争议,有研究发现长期使用硫酸软骨素能降低关节间隙宽度,但是氨基葡萄糖和软骨素组合与安慰剂组疗效相比没有统计学差异[40]。使用鱼油治疗膝骨性关节炎日益普及,虽然在类风湿关节炎中有一些试验,但在骨关节炎其使用仍不确定。二十碳五烯酸(EPA)和二十二碳六烯酸(DHA) 可减少降解酶和炎性细胞因子在体外软骨模型骨关节炎的表达,在临床研究中,鱼油小剂量及大剂量均未减缓膝关节骨关节炎的症状和进展[41]。 有许多药物治疗膝骨性关节炎,但其疗效和不良影响常限制其使用,目前尚无行之有效的疗法可用。骨关节炎研究中的焦点现在转向使用类风湿关节炎的靶向生物治疗。如慢性骨关节炎被认为是低的炎症条件,研究正在转向靶向血管生长因子、细胞因子和炎症递质。不同的药物对骨改建的作用,包括双膦酸盐和锶雷尼酸,也正在接受检验。有随机对照实验证实了雷奈酸锶减少疼痛和影像学的改变,然而不能减少心血管疾病的风险与增加疗效[42]。最近干细胞疗法治疗膝关节骨性关节炎,到目前为止,尚无支持的证据提倡这种治疗方法。澳大利亚风湿病协会和干细胞研究国际联盟都反对将当前将干细胞用于骨性关节炎。开发新疗法治疗膝骨性关节炎有它的挑战。新麻醉镇痛药如tanezumab是一种神经生长因子抑制剂,可改善髋关节和膝关节骨关节炎的疼痛,但Meta分析发现停药后少数患者出现关节加速损坏现象[43]。 2.2.3 骨关节炎的手术治疗 随着对骨关节炎认识的加深,目前认为骨关节炎治疗无有效的方式,治疗已经从传统的控制疼痛,包括提高关节活动功能和生活质量的干预措施优化到重视对疾病的预防和阻止其进展上,即从缓解症状转移到以预防为主。治疗方法以对症保守治疗为主,只有在保守治疗无效,影响工作和生活的情况下才选择手术治疗(见表1)。"

| [1] Goldring M, Berenbaum F. Emerging targets in osteoarthritis therapy. Curr Opin Pharmacol. 2015;2022:51-63.[2] Tew S, McDermott B, Fentem R, et al. Transcriptome-wide analysis of messenger RNA decay innormal and osteoarthritic human articular chondrocytes. Arthritis Rheumatol. 2014; 2066(2011):3052-3061.[3] Cai D, Yin S, Yang J, et al. Histone deacetylase inhibition activates Nrf2 and protects against osteoarthritis. Arthritis Res Ther.2015; 2017:2269.[4] Davidson RK, Jupp O, de Ferrars R, et al. Sulforaphane represses matrix-degrading proteases and protects cartilage from destruction in vitro and in vivo. Arthritis Rheum.2013; 2065:3130-3140.[5] 徐会勇. TGF-β_1与BMP-2对髁突软骨细胞Ⅱ型胶原及蛋白多糖合成的影响[D].昆明医学院, 2007.[6] Appleton C, Usmani S, Pest M, et al. Reduction in disease progression by inhibition of transforminggrowth factor alpha-CCL2 signaling in experimental posttraumatic osteoarthritis. Arthritis Rheumatol. 2015;2067:2691-2701.[7] Lees S, Golub SB, Last K, et al. Bioactivity in an aggrecan 32-mer ragment ismediated via toll-like receptor. Arthritis Rheumatol.2015;2067:1240-1249.[8] [Adouni M, Shirazi AA. Partitioning of knee joint internalforces in gait is dictated by the knee adduction angle and notby the knee adduction moment. J Biomech. 2014;2047:1696-2703.[9] Ateshian G, Henak C, Weiss J. Toward patient- specificarticular contact mechanics. J Biomech 2015;2048: 2779-2086.[10] Henak C, Abraham C, Anderson A, et al. Patient-specific analysis of cartilage and labrum mechanics in human hips with acetabular dysplasia. Osteoarthritis Cartilage. 2014; 2022:2210-2017.[11] Chehab E, Favre J, Erhart-Hledik J, et al. Baseline knee adduction and flexion moments during walking are both associated with 5 year cartilage changes in patients with medial knee osteoarthritis. Osteoarthritis Cartilage.2014; 2022:1833-1839.[12] Moore AC, Burris DL.Tribological and material properties for cartilage of and throughout the bovine stifle: support for the altered joint kinematics hypothesis of osteoarthritis. Osteoarthritis Cartilage. 2015;23(1):161-169. [13] Wang H, Chen T, Torzilli P, et al. Dynamic contact stress patterns on the tibial plateaus during simulated gait: a novel application of normalized cross correlation. J Biomech.2014; 2047:2568-2074.[14] Walker P, Arno S, Bell C, et al. Function of the medial meniscus in force transmission and stability.J Biomech.2015; 2048:1383-1388.[15] Fischenich K, Coatney G, Haverkamp J, et al. Evaluation of meniscal mechanics and proteoglycan content in a modified anterior cruciate ligament transection model. J Biomech Eng. 2014;2136:2011-2018.[16] Gannon A, Nagel T, Bell A, et al. The changing role of the superficial region in determining the dynamic compressive properties of articular cartilage during postnatal development. Osteoarthritis Cartilage 2015;2023:975-984.[17] Stoppiello L, Mapp P, Wilson D, et al. Structural associations of symptomatic knee osteoarthritis. Arthritis Rheumatol.2014; 2066(2011):3018-2027.[18] Pecchi E, Priam S, Gosset M, et al.Induction of nerve growth factor expression and release by mechanical and in?ammatory stimuli in chondrocytes:possible involvement in osteoarthritis pain. Arthritis Res Ther.2014;2016(2011):R2016.[19] Blaney Davidson EN, van Caam AP, Vitters EL, et al. TGF-beta is a potent inducer of nerve growth factor in articular cartilage via the ALK5-Smad2/3 pathway Potential role in OA related pain? Osteoarthritis Cartilage. Osteoarthritis Cartilage. 2015;23(3):478-486. [20] Ishikawa G, Koya Y, Tanaka H, et al. Long-term analgesic effect of a single dose of anti-NGF antibody on pain during motion without notable suppression of joint edema and lesion in a rat model of osteoarthritis. Osteoarthritis Cartilage: 2015; 2023(2016):925-932.[21] Bullock C, Wookey P, Bennett A, et al. Peripheral calcitonin gene-related peptide receptoractivation and mechanical sensitization of the joint in ratmodels of osteoarthritis pain. Arthritis Rheumatol.2014;2066(2018):2188-2200.[22] Benschop R, Collins E, Darling R, et al. Development of a novel antibody to calcitonin gene-related peptide for the treatment of osteoarthritis related pain. Osteoarthritis Cartilage.2014;2022(2014):578-585.[23] Rahman W, Dickenson A. Emerging targets and therapeutic approaches for the treatment of osteoarthritis pain. Curr Opin Support Palliat Care. 2015;2019(2012):124-130.[24] Kwok J, Grogan S, Meckes B, et al. Atomic force microscopy reveals age-dependent changes in nanomechanical properties of the extracellular matrix of native human menisci:implications for joint degeneration and osteoarthritis. Nanomedicine Nanotechnol Biol Med. 2014;2010:1777-1785.[25] Li Q, Doyran B, Gamer L W, et al. Biomechanical properties of murine meniscus surface via AFM-based nanoindentation. J Biomech.2015;2048:1364-1370.[26] Nguyen T, Oloyede A, Singh S, et al. Microscale consolidation analysis of relaxation behavior of single living chondrocytes subjected to varying strain-rates. J Mech Behav Biomed Mater. 2015;2049:2343-2354.[27] Lee B, Han L, Frank E, et al. Dynamic nanomechanics of individual bone marrow stromal cells and cell-matrix composites during chondrogenic differentiation. J Biomech. 2015;2048:171-175.[28] Lee W, Leddy H, Chen Y, et al. Synergy between Piezo1 and Piezo2 channels confers high-strain mechanosensitivity to articular cartilage. Proc NatlAcad Sci.2014;2111:E5114-2022.[29] Zhang W, Nuki G, Moskowitz R, et al. OARSI recommendations for the management of hip and knee osteoarthritis: Part III: Changes in evidence following systematic cumulative update of research published through January 2009. Osteoarthritis Cartilage.2010;2018:476-499.[30] Bennell K, Wrigley T, Hunt M, et al.Update on the role of muscle in the genesis and management of knee osteoarthritis. Rheum Dis Clin North Am. 2013;2039:145-176.[31] Messier S, Mihalko S, Legault C, et al. Effects of intensive diet and exercise on knee joint loads, inflammation, and clinical outcomes among overweight and obese adults with knee osteoarthritis: the IDEA randomized clinical trial. JAMA. 2013; 2310:1263-1273.[32] Laslett L, Kingsbury S, Hensor E, et al. Effect of bisphosphonate use in patients with symptomaticand radiographic knee osteoarthritis: data from the Osteoarthritis Initiative. Ann Rheum Dis. 2014;2073:824-830.[33] Chou R, McDonagh M, Nakamoto E, et al. Analgesics for osteoarthritis: an update of the 2006 comparative effectiveness review. Comparative Effectiveness Reviews.No. 38. Report No. 11-eHC076-EF. Rockville (MD). Agency for Healthcare Research and Quality (US): 2011.[34] Bannuru R, Dasi U, McAlindon T. Reassessing the role of acetaminophen in osteoarthritis: systematic review and meta-analysis. Osteoarthritis Cartilage 2010;2018 Suppl 2012:S2250.[35] Conaghan P, Dickson J, Bolten W, et al. A multicentre, randomized, placebo- and active-controlled trial comparing the efficacy and safety of topical ketoprofen in Transfersome gel (IDEA-033) with ketoprofen-free vehicle (TDT 064) and oral celecoxib for knee pain associated with osteoarthritis. Rheumatology (Oxford) 2013;2052:1303-1312.[36] Peniston J, Gold M, Wieman M, et al. Longterm tolerability of topical diclofenac sodium 1% gel for osteoarthritis in seniors and patients with comorbidities. Clin Interv Aging.2012;2017: 517-523.[37] Rutjes AW, Jüni P, da Costa BR, et al. Viscosupplementation for osteoarthritis of the knee: a systematic review and meta-analysis. Ann Intern Med: 2012;2157:180-191.[38] Chappell A, Desaiah D, Liu-Seifert H, et al.A double-blind, randomized, placebo controlled study of the efficacy and safety of duloxetine for the treatment of chronic pain due to osteoarthritis of the knee. Pain Pract 2011;2011:33-41.[39] Clegg D, Reda D, Harris C, et al. Glucosamine, chondroitin sulfate, and the two in combination for painful knee osteoarthritis.N Engl J Med: 2006;2354:795-808.[40] Fransen M, Agaliotis M, Nairn L, et al. Glucosamine and chondroitin for knee osteoarthritis: a double-blind randomized placebo-controlled clinical trial evaluating single and combination regimens. Ann Rheum Dis 2015;2074:851-888.[41] Hill C, Jones G, Lester S, et al. Effect of fish oil on structural progression in knee osteoarthritis: a two year randomized, double-blind clinical trial comparing high dose with low dose. Arthritis Rheum.2013;2065 Suppl 2010:S2914.[42] Abrahamsen B, Grove E, Vestergaard P, et al. registry-based analysis of cardiovascular risk factors and adverse outcomes in patients treated with strontium ranelate. Osteoporos Int. 2014;2025:757-762.[43] Mobashen A. The future of osteoarthritis therapeutics emerging biological therapy. Curr Rheumatol Rep.2013; 2015:385.[44] 荆立忠,潘登,杨久山. 膝骨关节炎非全膝置换手术治疗研究进展[J]. 山东医药, 2016, 56(10):105-106.[45] 陶源,徐祖健,李忠. 膝骨关节炎关节镜治疗概况[J]. 中医正骨, 2010,22(12): 41-43.[46] 王飞,陈竞清,百成,等. 胫骨高位截骨术治疗膝内翻伴膝外摆步态的疗效与不足[J].中国矫形外科杂志, 2006, 14(5): 343-345. |
| [1] | Tan Xinfang, Guo Yanxing, Qin Xiaofei, Zhang Binqing, Zhao Dongliang, Pan Kunkun, Li Yuzhuo, Chen Haoyu. Effect of uniaxial fatigue exercise on patellofemoral cartilage injury in a rabbit [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(在线): 1-6. |
| [2] | Zhang Jichao, Dong Yuefu, Mou Zhifang, Zhang Zhen, Li Bingyan, Xu Xiangjun, Li Jiayi, Ren Meng, Dong Wanpeng. Finite element analysis of biomechanical changes in the osteoarthritis knee joint in different gait flexion angles [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1357-1361. |
| [3] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [4] | Jin Tao, Liu Lin, Zhu Xiaoyan, Shi Yucong, Niu Jianxiong, Zhang Tongtong, Wu Shujin, Yang Qingshan. Osteoarthritis and mitochondrial abnormalities [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1452-1458. |
| [5] | Wu Cong, Jia Quanzhong, Liu Lun. Relationship between transforming growth factor beta1 expression and chondrocyte migration in adult articular cartilage after fragmentation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1167-1172. |
| [6] | Wang Baojuan, Zheng Shuguang, Zhang Qi, Li Tianyang. Miao medicine fumigation can delay extracellular matrix destruction in a rabbit model of knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1180-1186. |
| [7] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [8] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [9] | Liu Dongcheng, Zhao Jijun, Zhou Zihong, Wu Zhaofeng, Yu Yinghao, Chen Yuhao, Feng Dehong. Comparison of different reference methods for force line correction in open wedge high tibial osteotomy [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 827-831. |
| [10] | Zhou Jianguo, Liu Shiwei, Yuan Changhong, Bi Shengrong, Yang Guoping, Hu Weiquan, Liu Hui, Qian Rui. Total knee arthroplasty with posterior cruciate ligament retaining prosthesis in the treatment of knee osteoarthritis with knee valgus deformity [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 892-897. |
| [11] | Xu Lei, Han Xiaoqiang, Zhang Jintao, Sun Haibiao. Hyaluronic acid around articular chondrocytes: production, transformation and function characteristics [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 768-773. |
| [12] | He Junjun, Huang Zeling, Hong Zhenqiang. Interventional effect of Yanghe Decoction on synovial inflammation in a rabbit model of early knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 694-699. |
| [13] | Lin Xuchen, Zhu Hainian, Wang Zengshun, Qi Tengmin, Liu Limin, Suonan Angxiu. Effect of xanthohumol on inflammatory factors and articular cartilage in a mouse mode of osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 676-681. |
| [14] | Chen Xiaoxu, Luo Yaxin, Bi Haoran, Yang Kun. Preparation and application of acellular scaffold in tissue engineering and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 591-596. |
| [15] | Kang Kunlong, Wang Xintao. Research hotspot of biological scaffold materials promoting osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 597-603. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||