Chinese Journal of Tissue Engineering Research ›› 2016, Vol. 20 ›› Issue (43): 6530-6536.doi: 10.3969/j.issn.2095-4344.2016.43.021
Properties of sustained-release and controlled-release polymeric materials and application in the treatment of hypertension
- Department of Cardiology, Jinqiu Hospital of Liaoning Province, Shenyang 110002, Liaoning Province, China
-
Received:2016-08-22Online:2016-10-21Published:2016-10-21 -
About author:Chen Yao, Associate chief physician, Department of Cardiology, Jinqiu Hospital of Liaoning Province, Shenyang 110002, Liaoning Province, China
CLC Number:
Cite this article
Chen Yao.
share this article
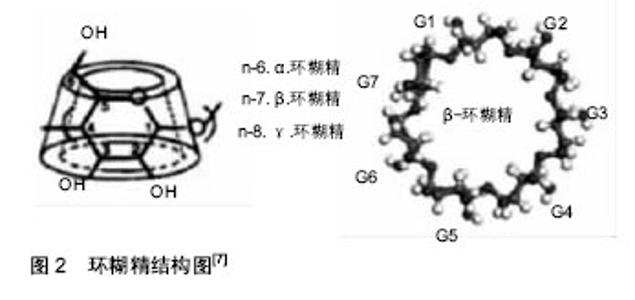
2.1 高分子缓释制剂载体材料 高分子药物载体材料需要无毒,并备良好的生物相容性和可降解性,可分为天然高分子载体材料(如多糖类、蛋白质类材料)和合成高分子载体材料(如聚乳酸、聚酸酐、多肽与氨基酸类聚合物等材料),近年出现了复合高分子载体材料。 2.1.1 天然高分子载体材料 天然高分子安全无毒,具有优良的生物相容性和易生物降解特性,无细胞毒性,作为药物载体材料得到了广泛应用,不过天然高分子材料也具有力学性能及加工性能差的缺陷。 壳聚糖及其衍生物:壳聚糖是天然存在的唯一碱性多糖,具有良好的生物相容性和可降解性,还有降血压、抗菌抗肿瘤特性,不过单纯的壳聚糖作为载体材料效果不是非常理想,所以大都是将壳聚糖与其它材料复合在一起,以获得综合性能优异的载体材料。壳聚糖可以通过化学交联、静电吸附等方法制成纳米粒子、微球、片、膜、凝胶等体系包载药物,起到缓释作用,目前已经有很多药物利用壳聚糖及其衍生物作为载体材料制备了缓释制剂,一般药物中有法莫替丁、吲哚美辛、阿司匹林、三七总皂苷、卡托普利等,抗癌药物有5-氟尿嘧啶、阿霉素、顺柏、紫杉醇等,蛋白质类药物有胰岛素、干扰素等,一些基因类药物也应用壳聚糖及其衍生物为载体。 安世昌等[4]以离子凝胶法制备壳聚糖微球,制备了能良好缓释蛋白类药物的壳聚糖纳米微球聚乳酸-羟基乙酸/纳米羟基磷灰石复合支架,体外实验显示该支架材料形态好,强度和降解速率合适,对牛血清蛋白有良好的缓释作用。刘峰等[5]以壳聚糖和三聚磷酸钠(tripolyphosphate)为原料,采用离子交联法成功制备了具有良好缓释能力的负载骨形态发生蛋白2的的壳聚糖纳米球。高婷婷[6]则对壳聚糖进行化学改性,合成制备出具有温敏性的羟丁基壳聚糖水凝胶,探究了羟丁基壳聚糖水凝胶作为胰岛素缓释载体的可行性。以上研究均证实了壳聚糖及其衍生物作为药物缓释载体材料是可行的。 环糊精及其衍生物:环糊精的结构图见图2[7],是一种环状低聚糖的总称,其中分子中含有6,7和8个葡萄糖单元的分别称为α,β和γ-环糊精,其中作为缓释载体材料最常用的是β-环糊精。约赛[8]制备了一种羧甲基壳聚糖(CMC)和羧甲基-β-环糊精(CMβ-CD)纳米粒,可作为药物缓释体系靶向递送抗癌药物。姜升阳等[9]以羟丙基-β-环糊精(HPC)及聚乙二醇(PEG)为基质制备硝苯地平骨架缓释片,在模拟胃液(pH 1.2)试验中5 h累积释放率仅为36.4%,可延长硝苯地平的体外释放时间及提高硝苯地平的生物利用度。杨黎燕等[10]采用共沉淀法制备了茶碱β环糊精聚合物微球,其体外释药规律符合一级释放方程和Korsmeyer-Peppas模型方程,具有一定缓释效果。"


丝素蛋白:丝素蛋白稳定无毒、廉价易得,具有良好的可降解性和生物相容性等特点,而且其可塑性强,可制成粉、膜、纤维、凝胶等,因此丝素蛋白是一种优良的药物缓释载体材料。叶漫文等[11]以京尼平为交联剂,应用无机乳化交联法制备缓释牛血清白蛋白的丝素蛋白-壳聚糖微球,该微球的载药率为(1.25±0.11)%,21 d的累积释放率为(75.2±2.53)%。李娟[12]开发了一种新颖的方法,使丝素蛋白在特定条件下通过自组装形成具有规整结构的蛋白基纳米微球和多孔支架材料,明显延长了药物的释放时间。王娟[13]采用离子诱导法制备了柞蚕丝素蛋白微球,这种微球的细胞相容性良好,能够支持细胞的生长和增殖;载阿霉素药物微球具有药物缓释作用,在给药3 d后仍然抑制癌细胞的生长,而对正常成纤维细胞影响不明显。 2.1.2 合成高分子载体材料 天然高分子药物载体材料具有优良的生物相容性,但其力学性能和加工性能较差,而合成高分子药物载体材料则可以弥补天然材料所存在的缺点,在药物缓释载体材料领域得到广泛应用。目前常用的合成高分子药物载体材料有聚乳酸及其共聚物[14-15]、聚酸酐及其共聚物、聚乙烯醇、聚膦腈、聚磷酸酯、多肽与氨基酸类聚合物等(表1)。"

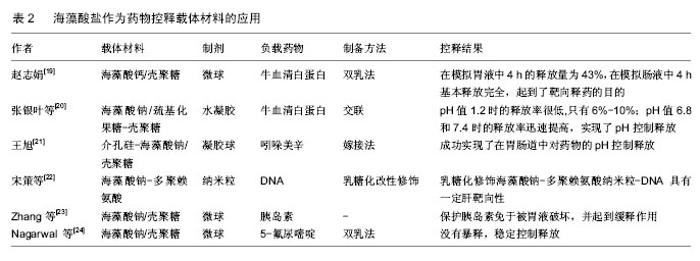
2.1.3 复合高分子缓释药物载体 在单一的聚合物用而限制了临床应用,所以对这些载体材料进行一定的改性进而改善其性能是非常必要的。目前常用的方法是将2种或多种聚合物使用接枝、交联或共混等法复合在一起,弥补材料的缺点,发挥优势,以获得性能更优良的复合高分子缓释药物载体。 何胤等[16]制备了复合异烟肼、利福平、吡嗪酰胺的聚乳酸-羟基乙酸缓释微球,体外缓释试验显示微球缓释前12 d左右,3种药物的累计缓释度均超过了50%,第12天后3药的缓释基本趋于稳定,3种药物缓释到50 d时均大于10倍MIC,提示聚乳酸-羟基乙酸微球具有优良的载药及药物缓释效果,是一种理想的复合抗结核药物缓释系统。 杨桔[17]将聚乳酸-羟基乙酸共聚物(PLGA)微球与P(NIPAAm-co-Aam)温敏凝胶复合构建了新型可控的PLGA微球/P(NIPAAm-co-Aam)水凝胶复合缓释制剂, 以牛血清白蛋白(BSA)为模型药物,制备了包封率较高且缓释效果较好的BSA微球。Fukuda等[18]的实验发现以壳聚糖、黄原胶制备复合缓释载体,对马来酸氯苯那敏的缓释可持续12 h,且不受溶液pH值和缓冲溶液影响。以上研究均证实高分子复合材料作为缓释载体的可行性,而且复合材料拓宽了缓释载体的范围,有很大的研究空间。 2.2 高分子控释制剂载体材料 药物控制释放就是将负载在高分子聚合物材料上的药物按一定的浓度和一定的速率缓慢释放得到环境中,使血药浓度长时间恒定维持在有效浓度范围。与缓释制剂相比,控释制剂更侧重控制药物的靶向释放和目的释放。可用作药物控释材料的高分子材料有很多,比如胶原、海藻酸钠、淀粉、纤维素衍生物等天然高分子材料,聚酯、聚醚、聚酰胺等人工合成高分子材料。 2.2.1 藻酸盐 海藻酸是一种线性的天然大分子多糖材料,分子链上含羧基及羟基,可与二价金属交联形成凝胶,通过选择海藻酸盐的类型、包覆剂与赋形剂制备海藻酸盐载药基体,可以使DNA、蛋白质、肽等类药物释放时间得以控制(表2)。 "
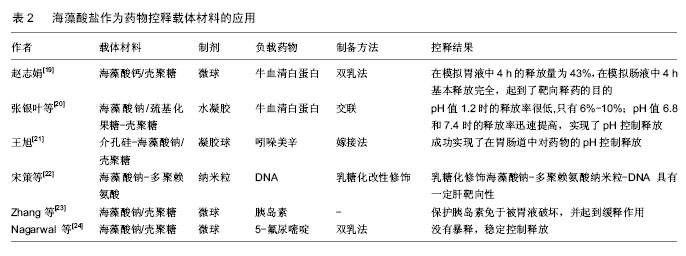
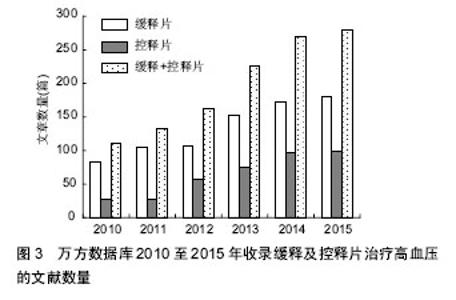
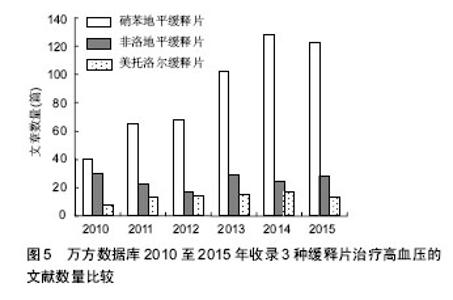
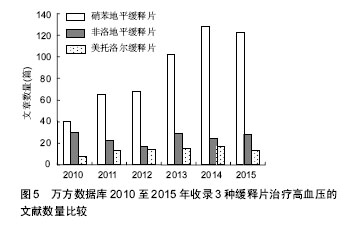
2.2.2 聚氨酯 聚氨酯(PU)是由多元醇、小分子扩链剂与异氰酸酯聚合形成的共聚物,具有良好的生物相容性和优良的物理机械性能。将聚氨酯弹性体浸在药物的水溶液中可以制成聚氨酯水凝胶,作为药物控释载体。在聚氨酯水凝胶上接枝或者利用互穿网络接上一些特殊的官能团,可制成温度敏感型聚氨酯水凝胶或pH值敏感型聚氨酯水凝胶。王素军[25]成功制备基于HO-P(LA-co-PDO)-OH的聚氨酯,其形状记忆温度在体温37 ℃左右;王孝娟[26]采用层层自组装技术,以聚胺聚氨酯(PUA)和聚苯乙烯磺酸钠(PSS)为囊壁材料,制备出具有可逆温度响应性的微胶囊,具有pH/温度双重智能响应性,而且缓释效果明显。以上研究结果说明聚氨酯在药物控释医学领域具有广泛的应用前景。 2.2.3 其他 甲基丙烯酸酯和甲基丙烯酸共聚物为溶解型聚合物,主要用于口服药物控释材料,根据溶解性的不同,药物可在胃、肠、组织或血液中靶向释放。一些非生物降解型聚合物也可作为药物控释载体材料,如聚丙烯酰胺类水凝胶,有研究者制备了一种纳米聚N-异丙基丙烯酰胺水凝胶控释材料,可磁控远程控制药物释放[27]。不过非生物降解型聚合物不能降解,所以应用不广泛[28]。还有一些可生物降解的共聚物,如不同单体聚合物互相结合,取长补短,获得性能更全面的新的药物控释材料,也是未来的发展方向[29-30]。 2.3 缓释及控释制剂在高血压治疗中的应用 高血压的治疗要求将血压稳定在目标范围内,不能上下波动,以免靶器官损害,因此患者需要服用长效的缓释或控释降压药。近年来临床缓释或控释降压药应用比较广泛。为了分析缓释或控释降压药在国内的临床应用,应用计算机检索万方数据库2010至2015年的相关文献,检索文题包含“高血压,缓释”及“高血压,控释”的文献,分析缓释及控释制剂在高血压治疗中的应用趋势,结果见图3。万方数据库收录缓释及控释片治疗高血压的文献数量从2010至2015年逐年上升,2010年111篇,2011年132篇,2012年162篇,2013年226篇,2014年270篇,2015年279篇,说明临床上高血压治疗中缓释及控释片的应用逐年普及,越来越多,所以相应的报道才会逐年增多。"
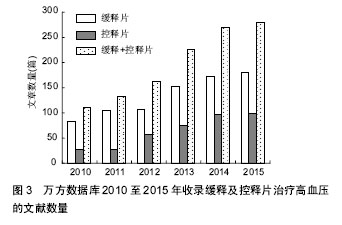
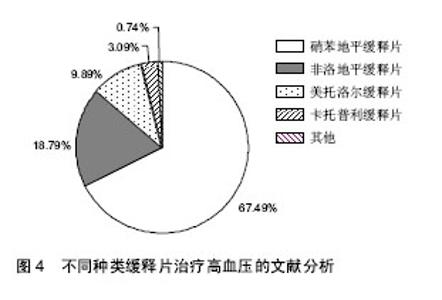
2.3.1 缓释降压制剂 从图3可知,万方数据库收录缓释片治疗高血压的文献数量也是呈上升趋势,不过至2014年(180篇)2015年(173篇)基本持平,可能是与近2年硝苯地平控释片逐渐占领市场有关。 检索2010至2015年文题包含“高血压,缓释”的文献,得到809篇缓释片治疗高血压的相关文献,进一步分析,其中硝苯地平缓释片546篇(67.49%),非洛地平缓释片152篇(18.79%),美托洛尔缓释片80篇(9.89%),卡托普利缓释片25篇(3.09%),其他缓释片占0.74%。从图4可知,治疗高血压的缓释片临床上应用最多的是硝苯地平缓释片、非洛地平缓释片(商品名波依定)和美托洛尔缓释片(商品名倍他乐克),占文献总量的95%,所以进一步分析近6年3种缓释片相关文献的发表趋势,能够代表缓释片在高血压治疗中的应用现状。图5可知,硝苯地平缓释片相关文献从2010年40篇,至2014年128篇逐年上升,2014年是2010年的3倍,所以这几年硝苯地平缓释片逐年普及,是高血压治疗中应用最多的缓释药物。2015年123篇较2014年略下降,应该是与硝苯地平控释片上市相关。非洛地平与美托洛尔缓释片6年来文献数量起伏不大。 2.3.2 控释降压制剂 相对于缓释制剂,控释制剂对药物释放要求更高,控释片在单位时间内有着比较恒定的释放剂量,以维持血药浓度恒定,效力更持久。目前高血压治疗中应用最多的是硝苯地平控释片,近6年万方数据库收录的治疗高血压的控释片相关文献基本上都是硝苯地平控释片,从图3可知,从2010年至2015年硝苯地平控释片治疗高血压文献数量也是明显上升。而相对于缓释片,硝苯地平控释片具有更好的稳定性,作用维持效果更好,相信未来控释片会拥有更大的市场份额。"

| [1]Murakami M, Saito T, Tabata Y.Controlled release of sphingosine-1-phosphate agonist with gelatin hydrogels for macrophage recruitment.Acta Biomater. 2014; 10(11):4723-4729. [2]Tomita S, Sato K, Anzai J.Layer-by-layer assembled thin films composed of carboxyl-terminated poly(amidoamine) dendrimer as a pH-sensitive nano-device.J Colloid Interface Sci. 2008;326(1):35-40. [3]Ito M, Imae T.Self-assembled monolayer of carboxyl-terminated poly(amido amine) dendrimer.J Nanosci Nanotechnol. 2006; 6(6):1667-1672. [4]安世昌,孙健,李亚莉,等.复合壳聚糖纳米微球聚乳酸-羟基乙酸/纳米羟基磷灰石缓释载体系统对蛋白的缓释作用[J].中国组织工程研究与临床康复,2011,15(25): 4615-4618. [5]刘峰,孙健,李亚莉,等.骨形态发生蛋白2壳聚糖纳米缓释载体的制备及性能测定[J].上海口腔医学,2015, 24(2) [6]高婷婷.温敏性羟丁基壳聚糖水凝胶用于胰岛素缓释载体研究[D]. 青岛:中国海洋大学,2014. [7]Zhang Y, Yu S, Bao F.Crystal structure of cyclomaltoheptaose (beta-cyclodextrin) complexes with p-aminobenzoic acid and o-aminobenzoic acid.Carbohydr Res. 2008;343(14):2504-2508. [8]约赛.羧甲基壳聚糖-β-环糊精纳米粒子作为药物缓释体系:评价反对MCF-7乳腺癌细胞[D].中南大学,2014. [9]姜升阳,赵朋,杨骏宇,等. 以羟丙基-β-环糊精及聚乙二醇为基质的硝苯地平骨架缓释片的制备及特性[J].重庆医学,2014,(17):2172-2174. [10]杨黎燕,杨威,尤静,等.茶碱β-环糊精聚合物微球的制备与缓释性能[J].中国实验方剂学杂志, 2011,17(16): 8-12. [11]叶漫文,曾曙光,高文峰,等.京尼平交联的丝素蛋白-壳聚糖缓释微球的制备与表征[J].南方医科大学学报, 2014, (6): 875-879. [12]李娟.柞蚕丝素蛋白的自组装及其在药物缓释上的应用[D].上海:东华大学,2012. [13]王娟.离子诱导柞蚕丝素蛋白微球的形成及其在药物缓释上的应用[D].苏州:苏州大学,2014. [14]Dai M, Xu X, Song J,et al.Preparation of camptothecin-loaded PCEC microspheres for the treatment of colorectal peritoneal carcinomatosis and tumor growth in mice.Cancer Lett. 2011;312(2):189-196. [15]Hamishehkar H, Emami J, Najafabadi AR,et al.Effect of carrier morphology and surface characteristics on the development of respirable PLGA microcapsules for sustained-release pulmonary delivery of insulin.Int J Pharm. 2010;389(1-2):74-85. [16]何胤,杨宗强,王骞,等.复合三联抗结核药聚乳酸-羟基乙酸缓释微球的制备及体外释药特性[J].中国脊柱脊髓杂志,2015,25(5):456-461. [17]杨桔.PLGA微球/P(NIPAAm-co-Aam)水凝胶复合体系的构建及药物缓释性能研究[D].重庆:重庆大学,2011. [18]Fukuda M, Peppas NA, McGinity JW.Properties of sustained release hot-melt extruded tablets containing chitosan and xanthan gum.Int J Pharm. 2006;310(1-2): 90-100. [19]赵志娟.双乳法制备海藻酸钙/壳聚糖微球及载BSA性能[D].大连:大连理工大学,2013. [20]张银叶,代苗苗,邱叶艳,等.一种新型蛋白类药物口服载体的海藻酸钠/巯基化果糖-壳聚糖复合水凝胶[J].生物学杂志,2013,30(1):22-26,17. [21]王旭.新型pH敏感型药物缓释系统?介孔硅掺杂的海藻酸钠/壳聚糖的制备, 难溶性药物的负载与释放研究[D].郑州:河南大学,2011. [22]宋策,张阳德,于丽,等.乳糖化修饰海藻酸钠-多聚赖氨酸纳米粒的制备及其肝靶向性研究[J].中国现代医学杂志, 2008,18(22):3269-3272. [23]Zhang Y, Wei W, Lv P,et al.Preparation and evaluation of alginate-chitosan microspheres for oral delivery of insulin.Eur J Pharm Biopharm. 2011;77(1):11-19. [24]Nagarwal RC, Kumar R, Pandit JK.Chitosan coated sodium alginate-chitosan nanoparticles loaded with 5-FU for ocular delivery: in vitro characterization and in vivo study in rabbit eye.Eur J Pharm Sci. 2012;47(4): 678-685. [25]王素军.新型药物控释材料——端羟基聚(丙交酯-co-对二氧环己酮)及其微球制备的研究[D].重庆:重庆大学, 2008. [26]王孝娟.(PUA/PSS)4层层自组装微胶囊的可逆温度响应性药物释放及形貌控制[D].郑州:郑州大学,2014. [27]Tomita S, Sato K, Anzai J.Layer-by-layer assembled thin films composed of carboxyl-terminated poly (amidoamine) dendrimer as a pH-sensitive nano-device. J Colloid Interface Sci. 2008;326(1):35-40. [28]Satarkar NS, Zach Hilt J.Hydrogel nanocomposites as remote-controlled biomaterials.Acta Biomater. 2008; 4(1):11-16. [29]Mandal BB, Mann JK, Kundu SC.Silk fibroin/gelatin multilayered films as a model system for controlled drug release.Eur J Pharm Sci. 2009;37(2):160-171. [30]Zhuang PY, Li YL, Fan L,et al.Modification of chitosan membrane with poly(vinyl alcohol) and biocompatibility evaluation.Int J Biol Macromol. 2012;50(3):658-663. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [11] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [12] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [13] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [14] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| [15] | Liu Liyong, Zhou Lei. Research and development status and development trend of hydrogel in tissue engineering based on patent information [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3527-3533. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||