Chinese Journal of Tissue Engineering Research ›› 2013, Vol. 17 ›› Issue (19): 3581-3588.doi: 10.3969/j.issn.2095-4344.2013.19.025
Previous Articles Next Articles
Clinical progress in olfactory ensheathing cell transplantation for treatment of chronic spinal cord injury
Wen Jian1, Wang Yan-song1, Wei Li2, Li Jie3
- 1 Department of Spine Surgery, Second Hospital of Harbin Medical University, Harbin 150086, Heilongjiang Province, China
2 Department of Emergency and Trauma, Second Hospital of Harbin Medical University, Harbin 150086, Heilongjiang Province, China
3 Department of Neurology, Second Hospital of Harbin Medical University, Harbin 150086, Heilongjiang Province, China
-
Received:2012-09-10Revised:2012-09-19Online:2013-05-07Published:2013-05-07 -
Contact:Wang Yan-song, M.D., Chief physician, Department of Spine Surgery, Second Hospital of Harbin Medical University, Harbin 150086, Heilongjiang Province, China wys1975@163.com -
About author:Wen Jian★, Studying for master’s degree, Physician, Department of Spine Surgery, Second Hospital of Harbin Medical University, Harbin 150086, Heilongjiang Province, China finerain120@163.com -
Supported by:the National Natural Science Foundation of China, No. 30800260*
CLC Number:
Cite this article
Wen Jian, Wang Yan-song, Wei Li, Li Jie. Clinical progress in olfactory ensheathing cell transplantation for treatment of chronic spinal cord injury[J]. Chinese Journal of Tissue Engineering Research, 2013, 17(19): 3581-3588.
share this article
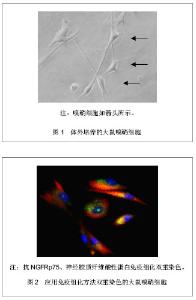
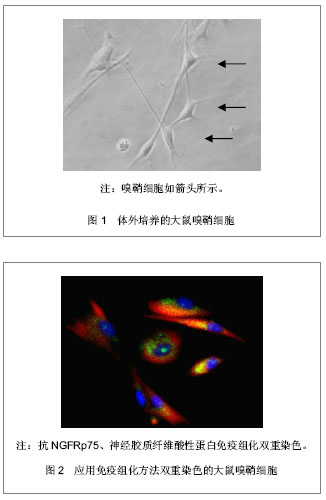
2.1 嗅鞘细胞修复脊髓损伤的亚临床研究概况 2.1.1 脊髓损伤修复的理论研究 脊髓损伤后神经传导通路受损,损伤平面以下的肢体缺乏脑等上级神经元的支配,导致运动感觉功能受损甚至完全丧失。而要想恢复损伤平面以下的感觉运动功能,就需要重新建立神经传导通路。在自然情况下,受损的神经功能难以恢复,大部分几乎无任何恢复。医学上至今也无有效疗法,主要原因就是无法充分促进损伤神经轴突的再生,以重新建立断端有效的神经联系。目前,大量的动物实验和临床研究都表明成年哺乳动物的神经纤维轴突在脊髓损伤后有一定的再生能力。进一步研究表明,神经轴突的再生需要一个适当的、稳定的微环境:①充分而有效的神经营养因子。②无明显阻碍轴突生长的胶质瘢痕,及由于外伤所致局部及全身细胞分泌的一些轴突生长抑制因子,阻碍轴突生长。③继发性细胞凋亡,局部炎症反应及神经脱髓鞘作用,使轴突无法攀附,诱导延伸,建立正确的神经联系。因此如何解决上述问题成为了治疗脊髓损伤所致神经功能缺损的关键所在。 2.1.2 关于嗅鞘细胞 自从1979年Graziadei等发现成年的哺乳动物的嗅神经具有不断的更新的能力后,利用嗅鞘细胞移植修复中枢神经系统损伤被认为是最有潜力的疗法之一。同时也能最大程度上建立一个稳定适宜的局部微环境,从而满足神经轴突再生的条件,促进轴突生长延伸,重建神经传导通路,促进神经功能的恢复。 嗅鞘细胞是一类特殊类型的神经胶质细胞,既存在于周围神经系统,又存在于中枢神经系统,能够促使哺乳动物的嗅神经不断的更新,见图1,2。"
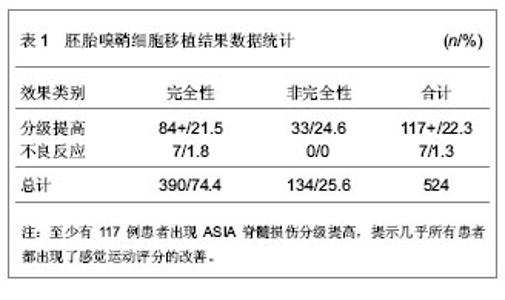
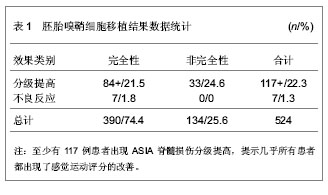
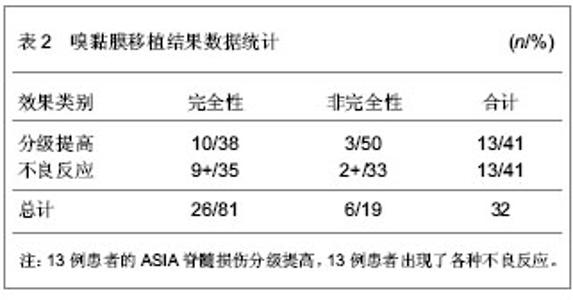
而嗅鞘细胞能够成为修复脊髓损伤的种子细胞,主要有以下几点:①改变脊髓损伤局部的微环境,使得局部微环境适合轴突的再生和修复,减少抑制因子产生。同时,嗅鞘细胞能够覆盖在轴突上,从而将损伤的轴突与损伤局部周围不适合轴突再生的微环境相隔离,并且嗅鞘细胞还可以分泌一系列的神经营养因子,促进轴突和髓鞘再生,引导轴突向远端生长,有利于形成有效的神经联系,促进神经功能恢复。②嗅鞘细胞能够抑制损伤局部反应性神经胶质细胞再生,从而减少神经胶质瘢痕的形成,使得轴突能够穿过受损局部到达远端,而且嗅鞘细胞具有良好的穿透性,能够穿越再生轴突无法通过的胶质瘢痕,建立神经胶质桥,恢复神经传导通路。③嗅鞘细胞能够诱导局部血管的再生,从而为损伤局部血液再灌注提供先决条件,减少损伤局部组织坏死和二次损伤。 2.1.3 嗅鞘细胞修复脊髓损伤的动物实验研究基础 体外细胞培养表明,嗅鞘细胞具有能够促进神经轴突再生的潜质,其特性能够作为修复脊髓损伤的种子细胞。因此,必须首先通过动物实验,来验证嗅鞘细胞是否能够具有促进脊髓损伤后神经功能的修复。早在1994年Ramon-Cueto等[8]就首次利用嗅鞘细胞修复修复截断的成年大鼠的背根神经,成功的验证了嗅鞘细胞具有促进损伤的神经轴突再生的能力。并且他们在2000年,又进一步通过将嗅鞘细胞移植入被完全横断的成年大鼠的脊髓内的实验,证明了嗅鞘细胞能够促进脊髓损伤后损伤平面以下神经功能的恢复。同年,Mie等[9]首次证明了的嗅鞘细胞能够使已经脱髓鞘的脊髓背侧柱轴突重新发生髓鞘化,即能够促进神经细胞的存活,轴突的再生,防止神经细胞凋亡。2004年Ramer等[10]通过对大鼠背侧脊髓损伤处进行自体嗅鞘细胞移植,发现嗅鞘细胞不仅能够减少瘢痕组织和空洞的形成,同时也能够促进神经轴突的再生。因此,通过上述动物实验研究,可以认为嗅鞘细胞具有促进脊髓损伤后损伤神经轴突的再生,脱髓鞘的神经轴突重新髓鞘化,并且可以减少瘢痕和空洞的形成,最终能过促进损伤平面以下神经功能的恢复。 2.2 嗅鞘细胞修复慢性脊髓损伤的临床研究进展 利用嗅鞘细胞移植治疗脊髓损伤,在体外试验和动物模型中获得良好的效果之后,临床试验开始显得有必要了。因此,有的学者开始进行了嗅鞘细胞移植治疗慢性脊髓损伤的临床试验研究。到目前为止,嗅鞘细胞病灶直接移植治疗慢性脊髓损伤按嗅鞘细胞来源分主要集中在以下几个方面:①胚胎嗅鞘细胞移植。②嗅黏膜移植。③嗅黏膜源性嗅鞘细胞移植。 2.2.1 胚胎嗅鞘细胞移植 胚胎嗅鞘细胞移植方法主要见于国内研究者的报道。在国内外都没有统一移植标准的前提下,国内移植标准主要参照黄红云等或郑遵成等的移植方法。二者在嗅鞘细胞的取材、培养纯化,髓内移植及评价方法等方面大同小异:都是将流产或者堕胎的胎儿嗅球胚胎嗅鞘细胞纯化培养后,在全麻下采用区域性多靶点注射方法进行髓内移植,并运用ASIA脊髓损伤分级和感觉运动功能评分进行随访评价。而二者的主要区别就在于病例的入选标准方面。黄红云等强调入选患者必须是受损脊髓压迫解除后无任何功能恢复或功能稳定至少3个月者,以避免伤后神经功能自发性恢复的干扰。而郑遵成等移植方法无此方面的定义。 早在2006年黄红云等[11-12]就报道了他们对300例完全(222例)和非完全(78例)性慢性脊髓损伤的患者进行胚胎嗅鞘细胞移植后,随访2-8周的结果。随访期间,他们未发现长期发热,脊髓感染,功能恶化等不良反应,亦无与手术有关的死亡病例报告。而几乎所有患者的ASIA感觉运动评分都增加了;117例患者的ASIA脊髓损伤分级提高了,其中84例为原完全性脊髓损伤患者。2012年他们又报道了对其中108例完全性慢性脊髓损伤的患者术后平均(3.47±1.12)年的随访结果[13]。32例患者的ASIA脊髓损伤分级提高。9例患者术后改善了行走功能或者甚至能够重新站立行走(扶拐或者不扶拐)。12/84的男性性功能有改善。亦未见任何不良反应报道。 孙天胜等[14-15]根据黄红云等的方法对11例完全性慢性脊髓损伤的患者进行了胚胎嗅鞘细胞移植和1-1.5年的随访。结果显示,所有患者的感觉功能(触觉和针刺痛觉)有明显的改善,感觉平面下降了3-10个脊髓节段,感觉评分明显增加。5例下颈椎损伤的患者中有3例ASIA运动评分有所改善。4例痉挛性瘫的患者手后痉挛程度均有改善。除了7例患者术后3个月内有明显的损伤平面以下的疼痛外,未见其他不良反应。 郑遵成等[16-17]对213例伤后2个月-21年的完全(157例)和非完全性脊髓损伤患者进行了胚胎嗅鞘细胞移植及3周以上随访评价。结果显示,术后3周后,所有患者的脊髓神经功能均有不同程度的改善,ASIA感觉运动评分明显提高,且有随时间延长不断改善趋势。但是有多少例患者ASIA脊髓损伤分级发生变化未见数据。在最长达5年的随访中,未见已恢复的神经功能减退及移植不良反应报道。 综合上述资料,总共524例慢性脊髓损伤患者(是否有重复及遗漏计算患者未知)中至少有117例(22.3%)出现ASIA脊髓损伤分级提高,而390例完全性慢性脊髓损伤的患者中至少有84例(21.5%)患者出现ASIA脊髓损伤分级提高。只有7例(1.3%)患者出现了不良反应。而上述所有资料都显示几乎所有患者都出现了感觉运动评分的改善,见表1。因此,在上述资料完全可信的,以及忽略重复、遗漏统计的基础上,可以认为胚胎嗅鞘细胞移植治疗慢性脊髓损伤是安全和有效的。"
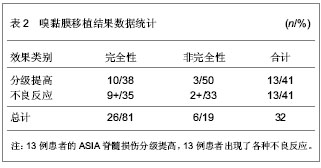
然而Dobkin等[18]通过对接受黄红云嗅鞘细胞移植疗法的7例患者进行的1项独立的检查发现,7例患者中5例患者出现严重的并发症,包括无菌性脑膜炎、脑膜脑炎、消化道出血、肺炎。7例患者中没有任何患者出现ASIA运动感觉功能恢复或者是功能性能力的恢复。与黄红云等报道的不相符。并且提出黄红云等在患者移植术后两三天就报道了ASIA运动感觉评分和脊髓损伤分级的改善;术后所有同种异体移植的患者未给予任何免疫抑制治疗;在试验方法上拒绝参加随机临床实验。另外,有的患者术前就有良好的运动功能,可以行走;进而认为实际上进入入选标准的患者比他们公开报道的要广泛得多。因此对于胚胎嗅鞘细胞移植治疗脊髓损伤的安全性和有效性尚存在争议,包括胚胎嗅鞘细胞移植的伦理道德问题,移植标准问题(移植的细胞数量、部位、时机等),恢复平台期的判定问题,以及其他许多不确定的安全因素等,在这些方面还需要更多的数据和事实依据。因此暂时不主张患者进行这种手术。 2.2.2 嗅黏膜移植 Lima等[19]在2006年首先报道了他们对7例伤后6个月-6.5年的完全性脊髓损伤患者,通过移除受伤部位的瘢痕组织并将自体嗅黏膜(细胞成分主要为神经干细胞和嗅鞘细胞)移植入该部位的自体嗅黏膜移病例。并对这7例患者进行18个月的随访评估。结果显示,18个月后,2例患者ASIA脊髓损伤分级从A改善到了C。除了1例患者之外的所有患者的ASIA感觉和运动评分都有改善。3例患者有可自主控制新的肌肉的迹象。2例患者的尿便功能或者感觉有改善。因取嗅黏膜后出现的暂时性嗅觉散失,术后都也能完全恢复。所有患者术后MRI可见:受损部位的缺损减少。而不良反应只有:1例患者的ASIA感觉评分降低;2例患者术后有两三个月的躯干疼痛。 2010年Lima等[20]又报道了对20例伤后18个月以上的完全性(15例)和非完全性(5例)脊髓损伤的患者进行嗅黏膜移植,平均27.7个月随访的结果。20例患者中有11例患者ASIA脊髓损伤分级提高了,其中3例为非完全性损伤患者;仅有1例患者从ASIA B降至A。术后MRI可见受损部位被移植物填充,5例患者排尿反应有改善,15例患者可检测到新的自主肌电信号反应,4例患者可记录到新的体感诱发电位。而只有1例患者因无菌性脑膜炎重新住院,以及4例其他患者出现轻微不良反应。 Chhabra等[21]运用Lima的方法对5例伤后29~99个月的脊髓损伤患者进行了嗅黏膜移植及18个月的随访。随访期间,所有患者在神经学,电生理学和尿动力学等方面未见任何改善。相反,术后1例患者神经痛加重,2例患者的ASIA感觉评分较术前降低,4例患者脊髓软化加重,1例患者出现1个瘘管,1例患者手术部位不愈合,需要二次手术关闭创口。5例患者均出现不同程度的不良反应。由此可见,Chhabra等的这次试验并未达到Lima等的报道的那样预期的良好结果,所有患者的ASIA感觉运动评分都无明显提高,同时可见较多的不良反应。 因此,综上所述,总共32例完全性(26例)和非完全性(6例)慢性脊髓损伤患者中,13例(40.6%)患者的ASIA脊髓损伤分级提高,其中3例为非完全性脊髓损伤患者,只有1例(3.1%)患者ASIA分级下降,见表2。然而,同时也发现,2例(6%)患者在术后需二次住院治疗,5例(16%)患者有脊髓空洞或者软化,共有13例(41%)出现了各种不良反应。因此,嗅黏膜移植治疗脊髓慢性损伤的安全性还有待进一步验证,同时由于缺乏大样本统计和对照组,其有效性无法验证。"

利用嗅黏膜移植修复脊髓损伤,虽然在在动物试验中已经取得了良好的效果,但是在临床试验中却未得到预期的结果。原因除了物种差异导致结果不一致外,如下几点可能影响结果[22-23]:①入选标准。在Lima等的试验中作者注意到康复锻炼疗法和好的结果之间有着潜在的联系。因此入选患者术前术后接受了康复锻炼的疗程长短和强度,是否已经完全达到了功能恢复的平台期直接影响移植结果。②作者注意到Lima等的试验方法中需要去除损伤处的神经瘢痕组织,然而此操作到目前为止仍然存在争议,因为可能存在的潜在的存活的神经通路。③移植细胞的组成没有明确的标准和定义,虽然主要成分是嗅鞘细胞和神经干细胞。同时移植的细胞数量、位置、时机等移植技术中涉及的问题也缺乏相应标准。④缺乏有效的评估方法,评估者主观意见对结果影响很大,而且没有任何措施来降低这种误差。因此,如何不断完善移植相关方法、程序,制定统一标准,以增加试验的稳定性、可靠性和重复性,还有相当长的路要走。 2.2.3 嗅黏膜源性嗅鞘细胞移植 Mackay-Sim 等[24-25]于2005年首先报道了应用自体嗅黏膜嗅鞘细胞移植治疗慢性脊髓损伤的患者的临床试验。他们把6例达到“恢复稳定期”(伤后6个月-3.5年) 的完全性胸椎截瘫的患者平均分为细胞移植组和假手术组。并将取自患者本人嗅黏膜嗅鞘细胞体外培养纯化后,移植到3例细胞移植组患者受损的脊髓周围。同时采用盲评的方法对6例患者进行了3年的随访评估。评估内容包括医学、社会心理、放射线、神经学的临床评价、神经和功能缺陷方面专门测试(ASIA和FIM)以及损伤平面以下感觉和运动功能的神经生理试验。到随访1年时,Feron等[26]对试验进行了总结和评估,未发现任何不良反应,MRI也未见任何改变。到随访结束时,Mackay-Sim等[25]又对随访结果进行了全面总结和评估:3年的随访中,所有3例自体嗅鞘细胞移植者未见任何不良反应(安全率100%),例如神经痛、瘘管、瘤样新生物、脊髓软化等。同时,对照研究也未发现任何明显的功能改善。只有1例细胞移植组患者出现双侧3个节段的浅触觉和针刺痛觉的部分恢复。因此,他们认为本移植术是安全的。 但是有的学者提出此移植患者的样本数量太少,而且未见其他类似的报道,在统计学上无法有效的说明此移植的安全性和有效性。同时,Mickay-Sim等[24-25]也承认,目前为止,很多此类移植试验设计所共同面对的一个问题是:纵向试验和临床结果评价如何保证评价者的评价的客观性,从而使结果更加接近真实,减少人为因素造成的干扰。因此,现有的实验数据只能说明此移植方法是相对安全的,还需要更多的数据来进一步证明和完善此移植方法的安全性和有效性。"

| [1] Ramón-Cueto A, Muñoz-Quiles C. Clinical application of adult olfactory bulb ensheathing glia for nervous system repair. Exp Neurol. 2011;229(1):181-194. [2] Li Y, Field PM, Raisman G. Regeneration of adult rat corticospinal axons induced by transplanted olfactory ensheathing cells. J Neurosci.1998;18:10514-10524. [3] Lu J, Feron F, Ho SM,et al.Transplantation of nasal olfactory tissue promotes partial recovery in paraplegic adult rats. Brain. 2001;889:344-357. [4] Ito D, Fujita N,Ibanez C,et al. Serum-free medium provides a clinically relevant method to increase olfactory ensheathing cell numbers in olfactory mucosa cell culture.Cell Transplant. 2008;16(10):1021-1027. [5] Wu M,Fan D,Tadmori I,et al.Death of axotomized retinal ganglion cells delayed after intraoptisc nerve transplantation of olfactory ensheathing cells in adult rats. Cell Transplant. 2010;19(2):159-166. [6] Shen Y,Qian Y,Zhang H,et al. Guidance of olfactory ensheathing cell growth and migration on electrospun silkfibroin scaffolds. Cell Transplant. 2010; 19:147-157.[7] Ma Y,Zhang Y,Cao L,et al.Effect of neurotrophin-3 genetically modifiedolfactory ensheathing cells transplantation on spinal cord injury. Cell Transplant. 2010;19:167-177. [8] Ramón-Cueto A, Nieto Sampedro M. Regeneration into the spinal cord of transected dorsal root axons is promoted by ensheathing glia transplants. Exp Neurol.1994;127(2): 232-244.[9] Mie M,Ohgushi H,Yanaqida Y,et al.Osteogenesis coordinated in C3H10T1/2 cells by adipogenesis-dependent BMP-2 expression system.Tissue Enq.2000;6(1):9-18.[10] Ramer LM, Au E, Richter MW, et al. Peripheral olfactory ensheathing cells reduce scar and cavity formation and promote regeneration after spinal cord injury. J Comp Neurol. 2004;473(1):1-15.[11] Huang H,Chen L,Wang H,et al.Influence of patients’ age on functional recovery after transplantation of olfactory ensheathing cells into injured spinal cord injury. Chin Med J (Engl). 2003;116:1488-1491. [12] Huang H, Wang H, Chen L, et al. Influence factors for functional improvement after olfactory ensheathing cell transplantation for chronic spinal cord injury. Zhongguo Xiu Fu Chong Jian Wai Ke Za Zhi. 2006;20:434-438. [13] Huang H,Chen L,Xi H,et al. Long-Term Outcome of Olfactory Ensheathing Cell Therapyfor Patients With Complete Chronic Spinal Cord Injury. Cell Transplantation.2012;21:S23–S31. [14] 孙天胜,任继鑫,吴军,等.嗅鞘细胞移植促进脊髓损伤修复的长期实验和临床观察[J].中国临床康复.2005;9(2):122-124.[15] Wu J,Sun T,Ye C,et al.Clinical Observation of Fetal Olfactory Ensheathing Glia Transplantation(OEGT) in Patients With Complete Chronic Spinal Cord Injury.Cell Transplantation. 2012;21: S33-S37. [16] 郑遵成,刘超,张振兴,等.嗅鞘细胞移植治疗陈旧性脊髓损伤48例[J].中国临床康复,2006,10(9):170-172.[17] 郑遵成,魏开斌,刘峰,等. 嗅鞘细胞移植治疗脊髓损伤的临床验证[J].中国组织工程研究与临床康复,2010,14(27):5119-5122.[18] Dobkin BH, Curt A, Guest J. Cellular Transplants in China:Observational Study from the Largest Human Experiment in Chronic Spinal Cord Injury. Neurorehabil Neural Repair.2006;20(1):5-13.[19] Lima C,Pratas-Vital J, Escada P,et al.Olfactory mucosa autografts in human spinal cord injury: a pilot clinical study.Spinal Cord Med. 2006;29: 191-203. discussion 204-206.[20] Lima C, Escada P, Pratas-Vital J, et al.Olfactory mucosal autografts and rehabilitation for chronic traumatic spinal cord injury. Neurorehabil. Neural Repair.2010; 24:10-22.[21] Chhabra HS, Lima C, Sachdeva S, et al.Autologous olfactory [corrected] mucosal transplant in chronic spinal cord injury:an Indian Pilot Study. Spinal Cord. 2009;47: 887-895. [22] Mackay-Sim A, St John JA. Olfactory ensheathing cells from the nose: Clinical application in human spinal cord injuries. Exp Neurol.2011;229: 174-180.[23] Dobkin BH. Recommendations for publishing case studies of cell transplantation for spinal cord injury. Neurorehabil Neural Repair. 2010;24(8):687-691. [24] Mackay-Sim A. An olfactory ensheathing cells and spinal cord repair. Keio J Med. 2005;54(1):8-14. [25] Mackay-Sim A, Féron F, Cochrane J, et al. Autologous olfactory ensheathing cell transplantation in human paraplegia: a 3 year clinical trial. Brain.2008;131(Pt 9): 2376-2386. [26] Feron F, Perry C, Cochrane J, et al.Autologous olfactory ensheathing cell transplantation in human spinal cord injury. Brain.2005;128:2951-2960.[27] Lu J,Feron F,Ho SM,et al.Transplantation of nasal olfactory tissue promotes partial recovery in paraplegic adult rats.Brain Res.2001;889(1-2):344-357.[28] Lu J,Feron F,Mackay-Sim A,et al.Olfactory ensheathing cells promote locomotor recovery after delayed transplantation into transected spinal cord.Brain.2002;125(Pt 1):14-21.[29] Bohbot A. Olfactory ensheathing glia transplantation combined with LASERPONCTURE in human spinal cord injury: Results measured by electromyography monitoring. Cell Transplantation. 2010;19:179-184.[30] Chen L, Chen D, Xi H,et al.Olfactory ensheathing cell neurorestorotherapy for amyotrophic lateral sclerosis patients: Benefits from multiple transplantations.Cell Transplant.2012; 21Suppl 1:S65-77. [31] Zhang SX,Huang F,Gates M,et al.Tail nerve electrical stimulation combined with scar ablation and neural transplantation promotes locomotor recovery in rats with chronically contused spinal cord.Brain Res. 2012;1456:22-35.[32] Li BC,Xu C,Zhang JY,et al.Differing Schwann Cells and Olfactory Ensheathing Cells Behaviors, from Interacting with Astrocyte, Produce Similar Improvements in Contused Rat Spinal Cord's Motor Function.J Mol Neurosci.2012; 48(1): 35-44.[33] Silva NA, Sousa RA, Pires AO,et al.Interactions between Schwann and olfactory ensheathing cells with a starch/polycaprolactone scaffold aimed at spinal cord injury repair. J Biomed Mater Res A.2012; 100A:470-476.[34] Liu X,Sun J,Cui X,et al.Protective effect of olfactory ensheathing cells in combination with intrathecal injection of vascular endothelial growth factor on injured spinal cord in rats.Zhongguo Xiu Fu Chong Jian Wai Ke Za Zhi.2011; 25(6): 699-704. |
| [1] | Wang Jian-ji, Yang Long, Li Jing, Sun Qi, Zuo Wei-min, Ren Qi-feng, Sun Yu, Wu Zhan-yu, Zou Qiang, Ma Min-xian, Ye Chuan. Development and application of special-purpose grafter by femoral head decompression combined with bone marrow mesenchymal stem cells transplantation based on three-dimensional printing technology [J]. Chinese Journal of Tissue Engineering Research, 2016, 20(44): 6636-6642. |
| [2] | Zhou Chang-yan, Zhou Qing-huan, Bian Jing, Chen Ke, Chen Wen. Bone marrow mesenchymal stem cells combined with calcium phosphate cement to repair articular cartilage defects in rabbits [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(8): 1195-1199. |
| [3] | Ma Fa-ku, Wang Huan, Liu Bin, Yang Yan-li, Su Qin-jun, Qian Zhen, Dong Liang. Expression of CD44+/C-myc+ cancer stem cells and its relationship with the prognosis of patients in colorectal tumors [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2161-2166. |
| [4] |
Chen Ping, Wang Jian.
Enrichment of lung cancer stem cells and expression of related markers
[J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2167-2171.
|
| [5] | Fan Zhi-gang, Fan Hong-liang. Oxidative stress response in diabetic nephropathy rats following injection of embryonic stem cells via the tail vein [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2199-2204. |
| [6] | Wang Yong, Zhao Wei, Feng Jian-zhou, Chen Xiao-chun. Nerve growth factor-modified adipose derived stem cells for repair of spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2224-2229. |
| [7] | Sha Wen-qiong, She Rui-lian, Wang Zi-neng, Ke Ru. Ultrastructure and phagocytotic function of human placental mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2230-2235. |
| [8] | Du Qing-hua, Cao Jun-kai, Dong Xi-xi, E Ling-ling, Wei Li-jun. Osteogenic differentiation of pluripotent stem cells induced by akermanite extracts [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2236-2242. |
| [9] | Wu Yan, Huang Lan . Bone morphogenetic protein 9-induced osteogenic differentiation of dental follicle cells in vitro [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2255-2260. |
| [10] | Rao Li-jia, Li Qi-meng, Li Jin-ling, Xu Qiong. Expression pattern of ten-eleven translocation family during differentiation of human dental pulp cells [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2261-2266. |
| [11] | Gao Zhuo-yue, Liu Yong-qi, He Jian-xin, Wu Zhi-wei, Luo Ya-li, Su Yun, Zhang Li-ying, Zhang Qi, Wu You-ming, Zhou Ni-na. Regulatory effects of warming yang and invigorating qi treatment on the inflammatory balance and genetic stability of bone marrow mesenchymal stem cells under tumor microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2267-2272. |
| [12] | Wang Fang, Chen Shao-wei. In vitro culture of embryos and establishment of embryonic stem cell lines [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2273-2277. |
| [13] |
Du Wei-bin, Quan Ren-fu, Zheng Xuan, Wang Tuo.
Hair follicle stem cells promote the healing of skin wound
|
| [14] | Du Hua, Shi Ying-xu . Bone marrow microenvironment controls the “fate” of hematopoietic stem cells [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2283-2290. |
| [15] | Xu Xiang, Yin He-ping. Platelet-rich plasma accelerates the proliferation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(14): 2144-2148. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||