Chinese Journal of Tissue Engineering Research ›› 2013, Vol. 17 ›› Issue (16): 3010-3017.doi: 10.3969/j.issn.2095-4344.2013.16.023
Previous Articles Next Articles
Synthetic nerve conduit versus autogenous nerve transplantation for repair of peripheral nerve defects
Luo Peng1, Peng Qiu-liang2, Xiang Jian-ping3, Qi Jian3
- 1 First Department of Orthopedics, Shenzhen Sixth People’s Hospital, Shenzhen 518054, Guangdong Province, China
2 Department of Medicine, Guangzhou Zhongda Medical Device Company, Guangzhou 510275, Guangdong Province, China
3 Department of Microscopy Traumatic Surgery, the First Affiliated Hospital of Sun Yat-sen University, Guangzhou 510080, Guangdong Province, China
-
Received:2012-12-29Revised:2013-02-19Online:2013-04-16Published:2013-04-16 -
Contact:Qi Jian, Doctor, Associate professor, Department of Microscopy Traumatic Surgery, the First Affiliated Hospital of Sun Yat-sen University, Guangzhou 510080, Guangdong Province, China speedsnow@126.com -
About author:Luo Peng☆, Doctor, Physician, First Department of Orthopedics, Shenzhen Sixth People’s Hospital, Shenzhen 518054, Guangdong Province, China gaidihu0308@sina.com -
Supported by:National Natural Science Foundation of China, No. 30571913*
CLC Number:
Cite this article
Luo Peng, Peng Qiu-liang, Xiang Jian-ping, Qi Jian. Synthetic nerve conduit versus autogenous nerve transplantation for repair of peripheral nerve defects[J]. Chinese Journal of Tissue Engineering Research, 2013, 17(16): 3010-3017.
share this article
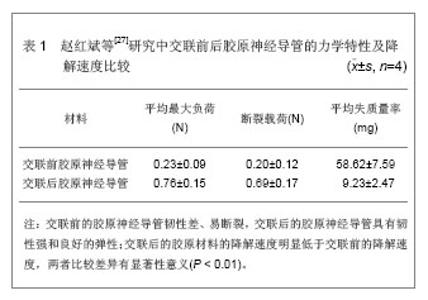
2 自体神经移植修复周围神经缺损的特点 自体神经移植是切取功能相对次要的周围神经,通过端端吻合的方法来移植修复周围神经缺损。有学者报道一种单束神经移植方法,动物实验显示,使用此方法后移植物中再生神经纤维数量和髓鞘化程度均较常规方法显著升高[14] 。在众多的神经移植体中,有学者认为采用同侧耳大神经移植手术在同一切口,取材方便,并且具有移植神经直径相近等优点。目前,神经移植的方法有以下几种,可根据情况选用[15-16] : 单股神经游离移植法:用于移植的神经与修复的神经应粗细相仿,如利用皮神经或废弃指的神经修复指神经,可采用神经外膜缝合法,将移植的神经与需修复神经作外膜吻合。移植神经的长度应稍长于需修复神经缺损的距离,使神经修复后缝合处无张力。 电缆式神经游离移植法:如用于移植的神经较细,则须将数股合并以修复缺损的神经。先将移植的神经切成多段,缝合神经外膜,形成一较大神经,再与待修复的神经缝合,此法因神经束对合不够准确,效果不肯定。 神经束间游离移植法:在手术显微镜下操作。操作技术与神经束膜缝合术相同,即先将神经两断端的外膜切除1 cm,分离出相应的神经束,切除神经束断端的瘢痕至正常部分,然后将移植的神经束置于相对应的神经束间作束膜缝合。 神经带蒂移植法:较细的神经移植后,一般不致发生坏死。取用粗大的神经作移植时,往往由于神经的游离段缺血,发生神经中心性坏死,导致束间瘢痕化,影响移植效果。带蒂法移植可避免上述情况发生。如将正中神经及尺神经近段假性神经瘤切除并作对端吻合,再将尺神经近侧神经干切断而尽量保留其血管,6周后将尺神经近端切断缝合于正中神经远段。 带血管蒂神经游离移植法:多用带小隐静脉的腓肠神经作游离移植,将小隐静脉与受区一知名动脉吻合。以使移植段神经获得血液供应。然而,这种采用挖肉补疮式的自体神经移植进行修复,目前既是临床通用手段,同时也是无奈的选择。这种无奈来源于使用自体神经移植,除供体来源有限,会造成供体部位神经部分功能丧失,有供区神经瘤形成和运动、感觉障碍等并发症,还受可修复长度、瘢痕等问题的限制,所以不是最理想的桥接移植方法[17-18] 。除此之外,还有神经导管及细胞因子的应用、细胞移植等治疗方法。这些治疗方法已经在动物实验或临床上取得了可喜的效果,但若用于修复长距离缺损的神经,效果均不满意。因此,世界各国的医学家、材料学家尝试用其他方法,选用合成材料来修复神经的缺损。 周围神经损伤后再生的过程十分复杂,包括以下条件[19-20] :①必须保证神经元的存活,并能启动神经再生所需的代谢反应。②在远离周围神经损伤的部位,即神经再生的局部环境能提供良好的营养。③再生后的神经能支配相应组织,并能恢复原有功能。许多研究者发现在导管内加入神经生长因子,可以促进神经细胞的再生,进而有利于受损神经的修复[21] 。神经生长因子的作用主要是对交感神经元和感觉神经元生长、发育、分化、存活及功能特性的表达具有调节作用,促进神经轴突延伸和髓鞘化,这类生长因子以神经营养因子为代表。正常生长的神经元必须从靶组织器官、远端胶质细胞获得足够的神经营养因子,周围神经损伤后切断了营养来源,导致细胞营养不良甚至死亡。但如果有外源性神经营养因子供给,即使无内源性营养因子,神经元仍可能得以生存和再生[22] 。除神经营养因子促进神经元的存活和再生外其他促进神经再生的因素[23] 。 3 合成神经导管材料的选择 神经导管可为神经的修复提供一个合适的微环境,使得神经纤维能够再生并顺利到达远端。已被用于制备神经导管材料的可生物降解材料的研制和开发始终在进行中[24] 。随着研究的深入,不仅要求神经导管材料有良好的安全性、生物相容性,还希望能具备利于手术、促进神经生长等特性[25] 。 3.1 胶原神经导管的特点 胶原蛋白作为细胞外基质的主要组成部分,被广泛应用于周围神经缺损的修复[26] 。胶原蛋白在体内可完全降解,但其缺点是降解速度快、力学性能较差,需要使用交联剂改善其机械性能。赵红斌等[27]通过胶原神经导管对外周周围神经缺损修复的实验研究,对交联前后的胶原神经导管进行拉伸实验并评价其力学特性。力学实验和常规降解实验结果见表1。 实验结果表明通过交联后的胶原神经导管,其力学性能明显增强达到了实验设计的要求。交联后的神经导管降解速度显著降低,克服了胶原蛋白降解快的缺点,可以使它的降解-吸收速率与组织再生速率大体相当,有利于神经组织的生长[28] 。"

3.2 DL-乳酸-ε-己内酯神经导管的特点 在神经导管材料的应用中,天然材料存在许多不足之处,比如,胶原蛋白会在产品的各个批次之间存有差异,例如分子量和分子量分布的差异等。这就需要通过不同的合成途径和方法合成一些具有特殊物理性质和特殊降解时间的大分子聚合物[29] 。作为生物可降解的聚合物,聚乳酸和聚己内酯表现出很好的生物相容性,因此,许多研究者期望能使用它们的共聚物合成出优秀的神经导管材料[30-31] 。 Meek等[32]使用聚乳酸和聚己内酯共聚物制成的DL-乳酸-ε-己内酯神经导管修复大鼠15 mm周围神经损伤,3周后在远端组织中观察到有髓鞘的神经纤维,12周后无髓鞘纤维明显增多,肌电图等测试数据显示达到了自体移植的效果。目前,除了DL-乳酸-ε-己内酯神经导管外,还有许多其它的合成共聚物,如聚丙三醇癸二酸酯、聚乙交酯-丙交酯共聚物等[33-34] 。 3.3 聚乙醇酸神经导管的特点 聚乙醇酸具有良好的生物相容性和生物降解性能且降解速度可控,在生物医学工程领域有广泛的用途,目前已被制作为神经导管。这种导管可替代自体和异体神经移植,促进周围神经再生,达到神经快速生长、功能完全恢复的效果,是近几年来被证明的周围神经缺损修复的最有效方法之一,并具有最好的产业化发展前景[35] 。为进一步改善聚乙醇酸神经再生导管的降解性能,提高损伤神经的再生速度和质量,人们对影响聚乙醇酸神经导管降解的因素进行了深入研究[36] 。影响聚乙醇酸神经导管降解的材料自身因素,见表2。"

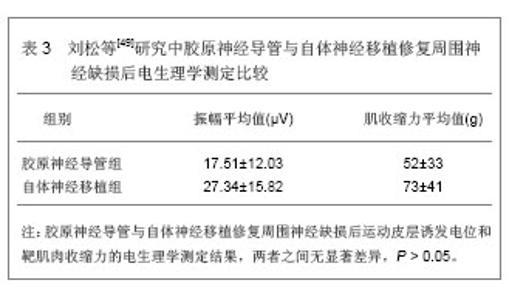
4 三维重建对周围神经导管材料修复周围神经损伤的评估价值 周围神经损伤后神经功能是否恢复是判断神经再生效果的关键。神经的传导性是周围神经的基本功能,周围神经离断后,神经传导性消失,因此神经传导功能可作为判断周围神经损伤和修复的一项可靠指标[40] 。理想的神经导管首先要满足神经细胞生长所需的基本要求[41-42] :①导管降解能够和神经恢复同步,并且能完全降解。②具有光滑的内表面,避免影响再生神经的生长,并且易于细胞生长和黏附。③良好的物理机械性能和柔韧性。④良好的组织相容性和无毒性[43]。⑤管壁具有选择透过性,能够从外界组织中吸取营养物质。⑥易于加工成型。在满足以上要求前提下,通过动物体内移植实验,观察、测定再生神经功能恢复的程度和神经再生的数目等。目前,周围神经内部显微解剖的三维重建已经逐渐深入,三维重建对于临床医生理解神经内部结构,对周围神经损伤的精细诊断与准确定位、神经导管的设计等有积极的作用。 4.1 三维重建为周围神经导管修复周围神经损伤提供解剖依据 近年来,随着对周围神经损伤的深入研究,周围神经导管材料不断改进,相对于自体神经移植,合成材料神经导管有着明显的优点。但是合成材料神经导管研制的重要前提条件是首先要明确周围神经内部神经束的复杂交叉重组关系,因为解剖结构的完整性和连续性是周围神经发挥正常神经传导功能的基础,三维重建技术能够准确的显示正中神经内部解剖结果及其相互关系,因此,对周围神经导管修复周围神经损伤有着重要的指导意义,并为临床上采取的神经损伤修复方式的选择提供一定的解剖参考意义,提供了一种周围神经系统内部显微结构三维可视化的有效方法。 陈增淦等[44]于2004年首先进行了人体臂丛神经的三维重建研究,为人体坐骨神经连续组织切片三维重建研究的顺利进行打下了良好的基础,研究通过连续组织切片的方法,成功的重建了人体坐骨神经内部神经束的三维结构,能够准确显示坐骨神经内部神经束的三维结构,为临床神经修复提供有益的三维解剖参考,同时对周围神经导管的修复重建也具有指导意义。 目前,定位标志点的获取是连续组织切片三维重建必须解决的首要问题和关键性技术难题[45] ,影响后续的三维建模进程及效果,难以对四肢周围神经进行大批量精确研究[46] 。张毅等[47]对周围神经三维重建前期的全景二维图像上完整标志点获取的关键技术路线进行了研究,利用二次成像Photoshop图像处理软件基于神经连续组织切片,实现了上臂长段尺神经外轮廓和内部功能束的三维重建,合成图像获得的标志点定位精确,并验证了此三维重建技术的可行性。 4.2 三维重建为周围神经导管材料内部空间构型提供可行性依据 理想的周围神经导管材料应保证神经修复所需的三维空间,即神经导管既具有适宜的强度、硬度和弹性,使之可以保证神经再生的通道,又具有理想的双层结构,外层为大孔结构,大的表面积有利于细胞的附着和伸张,而大的孔体积有利于传递足够多的细胞供组织修复,较好的通透性还有利于代谢产物的交换和神经营养物质的输送,内侧则为紧密结构,可以起到防止结缔组织长入的屏障作用,神经导管的表面最小孔径往往由细胞来决定,因此随细胞不同而变化。目前,周围神经内部显微解剖的三维重建已经逐渐深入,只有按照人体周围神经内部天然精确结构构件人工神经,才能获得最佳的效果。周围神经三维重建是深入了解周围神经内部结构和功能的重要途径之一,可为临床上周围神经损伤修复方式的选择以及组织工程神经的构建提供有益帮助,对病损组织进行形态、结构和功能的重建并达到永久性替代。三维重建是目前开发出能方便应用的周围神经修复辅助软件,为周围神经导管修复周围神经缺损的精度提供了有效的辅助引导方法。 Hadlock等[48]用聚乳酸、聚乙醇酸按85:1的比例聚合成周围神经导管,直径2.3mm,其中5条纵行排列的小管腔,小管腔直径500 µm,管腔经粘连蛋白溶液表面修饰后,引入浓度为5×108 L-1的许旺细胞,移植入大鼠坐骨神经7mm的缺损区,6周后神经组织通过移植的切面平均面积优于自体神经移植组,其神经纤维的直径也比自体神经移植组粗。另外,Rutkowski等[49]研究表明,周围神经导管孔隙率在75%左右时,神经生长因子和氧的供应能达到周围神经修复的最大需求。因此,有适当的孔径和孔隙率,利于导管内外物质交换,周围神经导管材料应是一种特定的三维结构支架的神经导管。 5 胶原、DL-乳酸-ε-己内酯、聚乙醇酸3种合成神经导管与自体神经移植修复周围神经缺损的比较 5.1 胶原神经导管与自体神经移植修复周围神经缺损的效果比较 刘松等[49]为探讨用胶原神经导管修复周围神经缺损的可行性,将15只成年雄性大白鼠使用胶原神经导管修补周围神经缺损作为实验组,用一段移植的5 mm自体神经段修补周围神经缺损作为对照组。术后9个月,采用电生理学监测修复后肌肉的电生理活动及收缩功能,通过病理学及组化学,观察脊髓和神经元的轴突再生状况并作了移植物的形态学分析,以评价神经肌肉功能恢复的情况。运动皮质诱发电位和靶肌肉收缩力的电生理学测定,见表3。 实验证明大量的新生神经纤维经过移植物进入到被修复的神经根及其周围神经,并使神经组织和肌肉重 新形成了运动终板,从而恢复了一定的肌肉收缩功能。胶原神经导管可允许细胞迁移及生存并能接收保存神经营养因子于其管内及壁内,因而能有效的促进轴突再生。并且,术后9个月内未发现其它病理反应,说明了胶原神经导管无毒,因此表明胶原神经导管是修复周围神经缺损的良好生物材料。 5.2 DL-乳酸-ε-己内酯神经导管与自体神经移植修复周围神经缺损的效果比较 Huang等[50]对犬胫神经 30 mm缺损,分别进行DL-乳酸-ε-己内酯神经导管与自体神经移植进行修复,9个月后进行神经传导速度、有髓神经纤维密度、轴突的平均直径和平均年龄髓鞘厚度的检测,结论认为DL-乳酸-ε-己内酯神经导管可作为替代自体神经移植治疗大直径周围神经缺损,弥补了自体神经移植的缺陷。 Xu等[51]对DL-乳酸-ε-己内酯神经导管降解性能进行了实验研究,将DL-乳酸-ε-己内酯神经导管植入3个月的周围神经缺损的大鼠体内,检测发现,DL-乳酸-ε-己内酯神经导管发生明显降解,而且再生神经进行整合,残端成功的从近端到远端生长。这些结果表明,DL-乳酸-ε-己内酯神经导管的降解率可适应神经再生,无过敏反应,可作为一种新的生物降解材料修复周围神经缺损。Dong等[52]DL-乳酸-ε-己内酯神经导管与自体神经移植修复周围神经缺损的形态学进行了研究。建立一个DL-乳酸-ε-己内酯修复坐骨周围神经缺损的动物模型,并以自体神经移植作为对照组。术后3个月,根据组织学观察,DL-乳酸-ε-己内酯神经导管与周围组织之间导管部分降解,但仍保持完整的轮廓和近端神经再生通过导管腔,并且神经纤维直径没有显著差异。因此,认为DL-乳酸-ε-己内酯神经导管能够有效修复大鼠坐骨周围神经损伤,促进再生,DL-乳酸-ε-己内酯神经导管修复周围神经缺损的观察指标接近自体神经移植。"
| [1]张勇杰,金岩,聂鑫,等.组织工程周围神经修复坐骨周围神经缺损应用研究[J].中华神经外科疾病研究杂志,2004,3(2):141-144.[2]游华,矫树生,陈建梅,等.组织工程人工神经对大鼠坐骨周围神经缺损后神经再生速度的影响[J].成都医学院学报,2010,5(3): 193-195.[3]游华,矫树生,冯帅南,等.OEC-SC-ECM-PLGA桥接体对大鼠坐骨周围神经缺损的解剖学修复作用[J].第三军医大学学报,2008, 30(21):2015-2019.[4]吴志伟,陈峥嵘,汪洋,等.人胚雪旺细胞组织工程神修复坐骨周围神经缺损的实验研究[J].中国临床医学,2006,13(5):810-813.[5]Barcelos AS,Rodrigues AC,Silva MD,et al.Inside-out vein graft and inside-out artery graft in rat sciatic nerve repair. Microsurgery.2003;23(1):66-71.[6]Mohammad JA,Warnke PH,Pan YC,et al.Increased axonal regeneration through a biodegradable amnionic tube nerve conduit: effect of local delivery and incorporation of nerve growth factor/hyaluronic acid media.Ann Plast Surg.2000; 44(1):59-64.[7]Bini TB,Gao S,Xu X,et al.Peripheral nerve regeneration by microbraided poly(L-lactide-co-glycolide) biodegradable polymer fibers.J Biomed Mater Res A.2004;68(2):286-295.[8]Weiss p,The technology of nerve regeneration:sutureless tubulation and related methods of repair.Neurosury.1944; 1:400.[9]蒋良福,劳杰,何继银,等.几丁糖胶原复合膜及激活态雪旺细胞修复周围神经缺损的实验研究[J].中华手外科杂志,2005,21(3): 172-174.[10]刘俊建,王建广,魏延云,等.同轴共纺复合神经生长因子导管修复大鼠坐骨周围神经缺损的实验研究[J].中华创伤骨科杂志,2009, 11(4):351-356.[11]董红让,徐达传,徐永年,等.外消旋聚乳酸复合神经生长因子缓释导管促周围神经再生的形态学研究[J].中国修复重建外科杂志, 2006,20(8):787-790.[12]中国知网.中国学术期刊总库[DB/OL].2012-08-10. https://www.cnki.net[13]SCI数据库.Web of Sciencevia ISI Web of Knowledge[DB/OL]. 2012-08-10.http://ip-science.thomsonreuters.com/mjl[14]Mohammad J,Shenaq J,Rabinovsky E,et al.Modulation of peripheral nerve regeneration: a tissue-engineering approach. The role of amnion tube nerve conduit across a 1-centimeter nerve gap.Plast Reconstr Surg.2000;105(2): 660-666.[15]洪光祥,陈振兵.周围神经端侧吻合的研究进展[J].实用手外科杂志,2006,20(2):67-69.[16]Wang X,Hu W,Cao Y,et al.Dog sciatic nerve regeneration across a 30-mm defect bridged by a chitosan/PGA artificial nerve graft.Brain.2005;128(8):1897-1910.[17]戴传昌,商庆新,王炜.用组织工程方法桥接周围神经缺损的实验研究[J].中华外科杂志,2000,13(5):388.[18]冯世庆,李崴,陈家,等.壳聚糖-胶原生物膜介导雪旺细胞联合神经干细胞桥接周围神经缺损[J].中华实验外科杂志,2008, 25(12): 1630-1632.[19]Stang F,Fansa H,Wolf G,et al.Structural parameters of collagen nerve grafts influence peripheral nerve regeneration.Biomaterials.2005;26(16):3083-3091.[20]卢凤琦,庄昭霞,曹晶,等.可降解性壳聚糖复合膜的研制与生物学评价[J].生物医学工程学杂,2003,20(2):277-280.[21]刘新,郑启新,吴永超,等.三种人工可降解材料上雪旺细胞培养的体外活性研究[J].医药论坛杂志,2008,29(14):4-8.[22]崔树森,徐莘香,尹维田,等.组织工程人工周围神经的研制[J].白求恩医科大学学报,2000,26(1):20-22.[23]医师网.组织工程:神经修复的一把利器[DB/OL].2010-8-23. http://www.mdweekly.com.cn/article.asp?id=27781[24]Tos P,Battiston B,Geuna S,et al.Tissue specificity in rat peripheral nerve regeneration through combined skeletal muscle and vein conduit grafts.Microsurgery.2000; 20(2): 65-71.[25]Dezawa M,Takahashi I,Esaki M,et al.Sciatic nerve regeneration in rats induced by transplantation of in vitro differentiated bone-marrow stromal cells.Eur J Neurosci. 2001;14(11):1771-1776.[26]Cuevas P,Carceller F,Dujovny M,et al.Peripheral nerve regeneration by bone marrow stromal cells.Neurol Res. 2002;24(7):634-638.[27]赵红斌,马敬,杨银书,等.胶原神经导管对外周周围神经缺损修复的实验研究[J].生物医学工程与临床,2010,14(2):100-104.[28]Maquet V,Martin D,Malgrange B,et al.Peripheral nerve regeneration using bioresorbable macroporous polylactide scaffolds.J Biomed Mater Res.2000;52(4):639-651.[29]Hadlock T,Elisseeff J,Langer R,et al.A tissue-engineered conduit for peripheral nerve repair.Arch Otolaryngol Head Neck Surg.1998;124(10):1081-1086.[30]Federoff HJ,Geschwind MD,Geller AI,et al.Expression of nerve growth factor in vivo from a defective herpes simplex virus 1 vector prevents effects of axotomy on sympathetic ganglia.Proc Natl Acad Sci U S A.1992;89(5):1636-1640.[31]Baumgartner BJ,Shine HD.Targeted transduction of CNS neurons with adenoviral vectors carrying neurotrophic factor genes confers neuroprotection that exceeds the transduced population.J Neurosci.1997;17(17):6504-6511.[32]Meek MF,Van Der Werff JF,Nicolai JP,et al.Biodegradable p(DLLA-epsilon-CL) nerve guides versus autologous nerve grafts: electromyographic and video analysis.Muscle Nerve. 2001;24(6):753-759.[33]Zhang Y,Dijkhuizen PA,Anderson PN,et al.NT-3 delivered by an adenoviral vector induces injured dorsal root axons to regenerate into the spinal cord of adult rats.J Neurosci Res.1998;54(4):554-562.[34]Baumgartner BJ,Shine HD.Permanent rescue of lesioned neonatal motoneurons and enhanced axonal regeneration by adenovirus-mediated expression of glial cell-line-derived neurotrophic factor.J Neurosci Res.1998;54(6):766-777.[35]Giménez y Ribotta M,Revah F,Pradier L,et al.Prevention of motoneuron death by adenovirus-mediated neurotrophic factors.J Neurosci Res.1997;48(3):281-285.[36]沈华,沈尊理,张佩华,等.甲壳素涂层并预置引导纤维神经导管的实验研究[J].中国修复重建外科杂志,2005,19(11):860-863.[37]Nuo Wang,Xue Shen Wu,et al.A novel approach to stabilization of protein drugs in poly(lactic-co-glycolic acid)microspheres using agarose hydrogel.International Journal of Pharmaceutics.1998;1(166):1-14.[38]Youxin Li,Christian Volland,Thomas Kissel.Biodegradable brush-like graft polymers from poly(D,L-lactide)or poly(D,L-lactide-coglycolide)and controlled releases of hydrophilic macromolecules.Polymer.1998;14(39):3087-3097.[39]罗丙红,全大萍,廖凯荣,等.低热-高压法制备PLGA多孔支架及其体外降解研究[J].功能高分子学报,2003,19(2):149-154.[40]Fakoya FA,Caxton-Martins EA.Neocortical neurodegeneration in young adult Wistar rats prenatally exposed to ethanol.Neurotoxicol Teratol.2006;28(2):229-237.[41]Tabakoff B,Hoffman PL.Animal models in alcohol research.Alcohol Res Health.2000;24(2):77-84.[42]Raimondo S,Nicolino S,Tos P,et al.Schwann cell behavior after nerve repair by means of tissue-engineered muscle-vein combined guides.J Comp Neurol.2005;489(2):249-259.[43]Origlia N,Capsoni S,Domenici L,et al.Time window in cholinomimetic ability to rescue long-term potentiation in neurodegenerating anti-nerve growth factor mice.Alzheimers Dis.2006;9(1):59-68.[44]顾玉东.周围神经缺损的基本概念与治疗原则[J].中华手外科杂志,2002,18(3):129-130.[45]Rosales-Cortés M,Peregrina-Sandoval J,Bañuelos-Pineda J,et al.Immunological study of a chitosan prosthesis in the sciatic nerve regeneration of the axotomized dog.J Biomater Appl.2003;18(1):15-23.[46]Williams LR.Rat aorta isografts possess nerve regeneration-promoting properties in silicone Y chambers. Exp Neurol.1987;97(3):555-563.[47]张毅,李小林,钟映春,等.基于二次成像技术标志点获取和自动配准的长段周围神经功能束三维可视化关键技术研究[J].中国修复重建外科杂志,2010,24[48]Hadlock T,Sundback C,Hunter D,et al.A polymer foam conduit seeded with Schwann cells promotes guided peripheral nerve regeneration.Tissue Eng.2000;6(2):119-127.[49]刘松,刘宗惠,G.Said.通过胶原管架桥使轴突从脊髓到神经根再生长的研究[J].中华神经外科杂志,2000,16(5):324.[50]Huang J,Xiang J,Yan Q,et al.Dog tibial nerve regeneration across a 30-mm defect bridged by a PRGD/PDLLA/β-TCP/NGF sustained-release conduit.Reconstr Microsurg.2013;29(2):77-87.[51]Xu H,Yan Y,Wan T,et al.Degradation properties of the electrostatic assembly PDLLA/CS/CHS nerve conduit.Biomed Mater.2009;4(4):45-60.[52]Dong H,Xu D,Xu Y.Morphologic research on PDLLA/NGF-controlled release conduit promoting peripheral nerve regeneratio.Zhongguo Xiu Fu Chong Jian Wai Ke Za Zhi.2006;20(8):787-790.[53]医药卫生.传统神经移植治疗短周围神经缺损的替代疗法[DB/OL].2012-11-15.http://www.doc88.com/p-338768269608.html |
| [1] | Shen Jinbo, Zhang Lin. Micro-injury of the Achilles tendon caused by acute exhaustive exercise in rats: ultrastructural changes and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1190-1195. |
| [2] | Liang Xueqi, Guo Lijiao, Chen Hejie, Wu Jie, Sun Yaqi, Xing Zhikun, Zou Hailiang, Chen Xueling, Wu Xiangwei. Alveolar echinococcosis protoscolices inhibits the differentiation of bone marrow mesenchymal stem cells into fibroblasts [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 996-1001. |
| [3] | Duan Liyun, Cao Xiaocang. Human placenta mesenchymal stem cells-derived extracellular vesicles regulate collagen deposition in intestinal mucosa of mice with colitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1026-1031. |
| [4] | Luo Xuanxiang, Jing Li, Pan Bin, Feng Hu. Effect of mecobalamine combined with mouse nerve growth factor on nerve function recovery after cervical spondylotic myelopathy surgery [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 719-722. |
| [5] | Li Li, Ma Li. Immobilization of lactase on magnetic chitosan microspheres and its effect on enzymatic properties [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 576-581. |
| [6] | Liu Liu, Zhou Qingzhu, Gong Zhuo, Liu Boyan, Yang Bin, Zhao Xian. Characteristics and manufacturing techniques of collagen/inorganic materials for constructing tissue-engineered bone [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 607-613. |
| [7] | Song Kaikai, Zhang Kai, Jia Long. Microenvironment and repair methods of peripheral nervous system injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 651-656. |
| [8] | Chen Lei, Zheng Rui, Jie Yongsheng, Qi Hui, Sun Lei, Shu Xiong. In vitro evaluation of adipose-derived stromal vascular fraction combined with osteochondral integrated scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3487-3492. |
| [9] | Zhou Anqi, Tang Yufei, Wu Bingfeng, Xiang Lin. Designing of periosteum tissue engineering: combination of generality and individuality [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3551-3557. |
| [10] | Lang Limin, He Sheng, Jiang Zengyu, Hu Yiyi, Zhang Zhixing, Liang Minqian. Application progress of conductive composite materials in the field of tissue engineering treatment of myocardial infarction [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3584-3590. |
| [11] | Chen Jie, Liao Chengcheng, Zhao Hongbo, Zhao Wei, Chen Zhiwei, Wang Yan. Application of tissue engineering urethral stent and its preparation technology in urethral reconstruction [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3591-3596. |
| [12] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [13] | Yang Li, Li Xueli, Song Jinghui, Yu Huiqian, Wang Weixia. Effect of cryptotanshinone on hypertrophic scar of rabbit ear and its related mechanism [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3150-3155. |
| [14] | Lu Yi, Deng Wenchong. Regulation and difference of different exercise styles on brain structure and cognitive function [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3252-3258. |
| [15] | Liu Zhendong, Wang Rui, Li Xiaolei, Wang Jingcheng. Review of interferon alpha-2b inhibiting scar formation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(2): 317-321. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||

