Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (2): 317-321.doi: 10.3969/j.issn.2095-4344.2984
Previous Articles Next Articles
Review of interferon alpha-2b inhibiting scar formation
Liu Zhendong1, Wang Rui2, Li Xiaolei1, Wang Jingcheng1
- 1Clinical Medical College of Yangzhou University, Yangzhou 225001, Jiangsu Province, China; 2Department of Dermatology, Dezhou People's Hospital, Dezhou 253000, Shandong Province, China
-
Received:2020-02-13Revised:2020-02-22Accepted:2020-03-18Online:2021-01-18Published:2020-11-14 -
Contact:Wang Jingcheng, MD, Professor, Doctoral supervisor, Clinical Medical College of Yangzhou University, Yangzhou 225001, Jiangsu Province, China -
About author:Liu Zhendong, MD candidate, Attending physician, Clinical Medical College of Yangzhou University, Yangzhou 225001, Jiangsu Province, China -
Supported by:the National Natural Science Foundation of China, No. 81772332
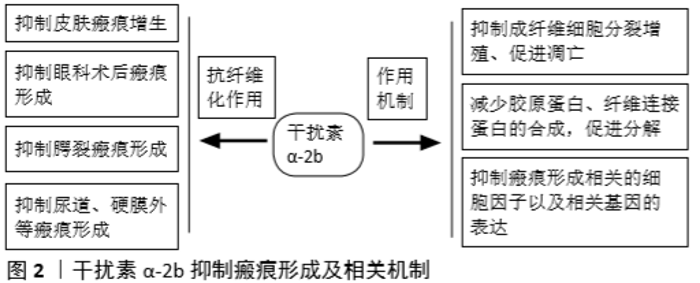
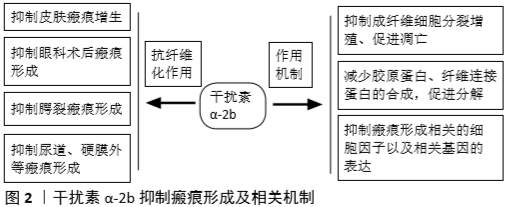
2.1 抑制皮肤瘢痕增生 皮肤是人体最大的器官,作为身体与外部环境的屏障来保护身体免受害刺激。在皮肤重塑功能受损后,导致皮肤病理性瘢痕的产生,这其中主要包括萎缩性瘢痕、增生性瘢痕和瘢痕疙瘩[6]。IFNα-2b作为一种生物制品,最早在1989年由BERMAN等[7]报道了1例患者通过局部注射IFNα-2b治疗瘢痕疙瘩,并取得了良好的治疗效果。而后LEE等[8]给予瘢痕疙瘩患者局部病灶内注射IFNα-2b联合曲安奈德,报道中大多数病例的改善率超过了80%。既往文献研究中,IFNα-2b抑制皮肤瘢痕的机制主要包括以下几方面,见图2。 2.1.1 抑制成纤维细胞增殖,降低胶原蛋白生成 WANG等[9]报道指出通过系统给予IFNα-2b药物治疗后,烧伤瘢痕患者的增生性瘢痕内的成纤维细胞数目明显减少,且通过体外实验证实,IFNα-2b呈剂量依赖性阻止外周血单核细胞分化为纤维细胞。另外,IFNα-2b可以抑制纤维细胞的增殖,降低转化生长因子β介导的α-平滑肌肌动蛋白在纤维细胞中的表达。最终结论认为IFNα-2b抑制增生性瘢痕与纤维细胞数量和活性下降有关。TELASKY等[10]体外培养人皮肤成纤维细胞,然后给予2 000 U/mL的 IFNα-2b进行干预,结果显示,IFNα-2b可以抑制真皮成纤维细胞的增殖,降低细胞中Ⅰ型前胶原mRNA的水平,降低了条件培养基中胶原的生成。同时,这种干预还增加了细胞中的胶原酶mRNA水平和培养基中的胶原酶活性。实验结论认为IFNα-2b可以用作治疗纤维增殖性疾病,如烧伤后增生性瘢痕等。 2.1.2 抑制瘢痕形成相关的细胞因子 TREDGET等[11]针对烧伤瘢痕患者每周3次局部注射IFNα-2b药物,经过系统的干预治疗,可以明显改善严重烧伤患者肥厚性瘢痕的外观和烧伤瘢痕评分,通过检测结果显示瘢痕组织内转化生长因子β含量和胶原合成显著多于正常皮肤成纤维细胞,给予IFNα-2b干预刺激可显著抑制细胞的增殖,并且能够抑制两种细胞内转化生长因子β1的分泌,而转化生长因子β1则被一直认为是致纤维化因子。陆兴安等[12]给予不同浓度(100,10 000 U/mL)的IFNα-2b处理瘢痕成纤维细胞,通过PCR技术检测细胞因子分泌情况,结果显示,IFNα-2b对增生性瘢痕的抑制作用与转化生长因子β1、基质金属蛋白酶1、血小板衍化生长因子BB以及糖基转移酶(ppGalNAc-T2)表达均有关联,其作用可能是直接或间接通过它们来调节细胞增殖、分化、胶原沉积等,并且具有浓度依赖性。 2.1.3 抑制瘢痕形成相关基因的表达 GHAHARY等[13]的实验报道IFNα-2b可显著降低真皮成纤维细胞内Ⅰ型胶原的表达,此外,通过2 000 U/mL的浓度干预 96 h,IFNα-2b还可显著增加真皮成纤维细胞中胶原酶mRNA的表达,其研究机制认为可能是通过刺激胶原酶启动子的-127/-91区域作为IFNα-2b的响应元件。黄勇等[14]分别取瘢痕疙瘩与正常皮肤组织提取成纤维细胞,选用10 000 IU/mL作为实验干预浓度,通过MTT法测定药物作用不同时间对成纤维细胞生长增殖的影响,流式细胞仪观察细胞凋亡情况,PCR法检测端粒酶活性,结果表明,IFNα-2b作用48 h后对两类成纤维细胞有较明显的生长抑制作用,实验结论认为降低成纤维细胞端粒酶活性是其作用机制之一。徐少骏等[15]通过地塞米松和IFNα-2b (1 000U/mL) 对病理性瘢痕成纤维细胞进行干预,探讨其实验机制,结果研究发现IFNα-2b可抑制增殖瘢痕的ERK1/2通路,而对JNK通路无影响,且不引起正常皮肤成纤维细胞ERK1/2和JNK通路的变化。刘传君等[16]的实验针对增生性瘢痕患者进行对比干预治疗,之后手术切取标本组织进行免疫组化检测分析以及基因表达的检测,实验结果认为:①药物IFNα-2b通过抑制血小板衍化生长因子基因表达,减少成纤维细胞的有丝分裂,使瘢痕的成纤维细胞受到抑制;②IFNα-2b通过抑制Ⅰ,Ⅲ型前胶原的转录,使mRNA减少,从而抑制Ⅰ,Ⅲ型前胶原的蛋白翻译抑制胶原合成;③抑制c-myc基因表达并上调p53基因表达。 2.2 抑制眼科术后瘢痕形成 青光眼滤过性手术是目前治疗青光眼的主要办法。经典的小梁切除术通过对青光眼患者施行滤过性手术,建立人工房水引流路径,可达到降低眼压、控制青光眼的作用,但术后滤过通道的过度纤维化仍有可能降低房水引流的效率,导致患眼术后眼压再次升高。成纤维细胞的过度增殖和细胞外基质的过度产生导致组织过度瘢痕化,从而导致手术效果不佳,成为一直困扰临床医师的主要原因[17]。因此,国内外学者围绕着如何解决滤道瘢痕化问题进行了一系列研究[18-19]。 近年来的实验研究发现,IFNα-2b在体外可抑制人眼Tenon囊的成纤维细胞增殖和胶原的产生,从而抑制眼科滤过术后瘢痕纤维化的发生。GILLIES等[20]体外培养人眼tenon囊成纤维细胞,同时选用不同浓度的IFNα-2b干预刺激,结果显示在10-10 000 U/mL的范围内呈浓度依赖性抑制人眼Tenon囊成纤维细胞增殖。其抑制周期作用在有丝分裂前,因此认为其可应用于青光眼术后防瘢痕粘连治疗。WANG 等[21]体外细胞实验培养丝裂霉素c耐药的人Tenon成纤维细胞株,用IFNα-2b和IFN-γ预处理48 h,然后再用Fas抗体激动剂(CH11)刺激2 d,流式细胞术和Western blot检测凋亡相关蛋白的变化;结果显示IFNα-2b或IFN-γ预处理 48 h可使Fas、Fas相关死亡蛋白和caspase-8的表达增加,联合刺激可进一步增加表达;其作用机制可能涉及通过上调Fas、与死亡结构域相关的fas相关蛋白和caspase-8表达来增加死亡诱导信号复合物的形成。陈君毅等[22]取青光眼患者滤过术中剪下的Tenon囊组织,在体外培养成纤维细胞,采用不同浓度的IFNα-2b干预处理,检测转化生长因子β1、转化生长因子β2、Ⅰ型胶原蛋白、纤维连接蛋白表达的影响;结果显示IFNα-2b对上述蛋白及细胞因子均有抑制作用,结论认为IFNα-2b可作为一种比较理想的青光眼滤过术后抗瘢痕形成的药物。 张秀兰等[23]取新西兰兔行巩膜切除术,同时在滤过区旁结膜下注射IFNα-2b,然后术后于不同时间段取标本进行免疫组化检测,结果同不用药的对照组比较发现,IFNα-2b可在体内环境下拮抗碱性成纤维细胞生长因子、转化生长因子β1的作用。熊新春等[24]的动物实验证实,IFNα-2b可减少青光眼滤过术后瘢痕组织中的胶原含量,且能够显著降低小梁切除术后的房水蛋白浓度,而体外细胞实验则显示,IFNα-2b可抑制结膜下成纤维细胞表皮生长因子受体的表达。 IFNα-2b在眼科应用中,除上述青光眼滤过术后抑制瘢痕形成作用外,还在翼状胬肉术后防复发中起到一定的积极作用。孙亚杰等[25]收集临床复发性翼状胬肉组织标本,而后分离提取出成纤维细胞进行实验,通过对比几种临床药物对细胞的干预作用进行分析验证,实验结果证实IFNα-2b可抑制复发性翼状胬肉成纤维细胞的增殖并促进细胞凋亡。YIN等[26]在一项临床前瞻性研究中,将初发翼状胬肉患者于手术治疗后进行分组,干预组在术后3个月内采用IFNα-2b滴眼液每天滴眼4次,然后对所有患者随访18个月进行对比分析,结果证明干扰素干预组的术后复发率远远低于对照组,因此研究认为应用IFNα-2b滴眼液对术后减少翼状胬肉复发安全有效。 根据文献报道及实验研究,IFNα-2b作用于眼科术后减少瘢痕粘连的具体机制可归结为以下几点:①抑制成纤维细胞分裂增殖,并促进凋亡;②减少胶原蛋白(主要为Ⅰ、Ⅲ型胶原)、纤维连接蛋白的合成表达;③通过干预与瘢痕形成相关的细胞因子或相关基因,来达到抗纤维化作用。其中涉及到的分子生物学尚需进一步探索。 2.3 抑制腭裂瘢痕形成 先天性腭裂的发生严重影响了患者口腔颌面部形态与功能,对患者心理造成极大伤害。如今随着外科学技术的进步,已经实现了对腭部裂隙的整形修复,对于语音功能和吞咽要求基本恢复,但随着术后患者上颌骨的生长发育,仍有部分患者出现继发性畸形。究其原因多为腭裂术后遗留在上颌骨硬腭的裸露骨面瘢痕挛缩所 致[27-29],因此,如何防治腭裂术后裸露骨面瘢痕形成是目前此领域急待解决的问题之一。CORNELISSEN等[30]从出生8 d的大鼠腭部黏膜伤口和正常大鼠腭部组织中获得肉芽组织成纤维细胞,用IFNα-2b干预细胞19 h之后检测细胞增殖能力,结果显示IFNα-2b可使肉芽和正常成纤维细胞的增殖减少,但是差异不显著,分析其原因或许是作用时间太短导致。胡超等[31]通过动物实验制作兔腭裂术后裸露骨面瘢痕的动物模型,术后4周取腭部裸露骨面上的瘢痕组织分离培养成纤维细胞,采用不同浓度IFNα-2b干预细胞并观察其生物学特征改变,结果与对照组比较,实验组加入IFNα-2b作用48 h后,瘢痕成纤维细胞的生长趋势及增殖活性被明显抑制,G1期细胞百分数明显增高,结论认为IFNα-2b在防治腭裂术后裸露骨面瘢痕形成中有一定的应用价值。随后陶明等[32]进行了同样的实验研究,通过不同浓度的IFNα-2b作用不同时间,采用MTT法、流式细胞术等方法观察、分析其效果,结果显示实验组作用24 h变化不明显,但是作用48 h后腭裂术后瘢痕成纤维细胞的生长趋势及增殖活性被明显抑制。而这两个实验或许可以解释CORNELISSEN等[30]实验中的结果差异,也印证了其分析的原因所在。 2.4 其他 孟凡伟等[33]利用男性尿道成形术中切除的尿道瘢痕组织,提取分离出成纤维细胞,之后给予不同浓度的IFNα-2b干预刺激,观察细胞形态,分析细胞周期,并测定胶原的含量。结果显示药物作用72 h后,随着加入IFNα-2b浓度的增加,S-G2-M期细胞百分比降低,尿道瘢痕成纤维细胞的胶原含量显著降低;最后结论认为IFNα-2b是成纤维细胞负性调节因子,降低胶原合成,可有效抑制尿道瘢痕形成。而FIRAT等[34]与GOKCE等[35]的大鼠动物实验模型研究结果也认为,IFNα-2b可以在泌尿系瘢痕形成中起到一定的防治作用。除上述之外,苏云等[36]通过动物实验研究证实,IFNα-2b/聚乳酸-羟基乙酸共聚物复合膜可以抑制硬膜外瘢痕形成。"
| [1] ISAACS A, LINDENMANN J. Virus interference .I. the interferon. Proc R Soc Lond B Biol Sci. 1957;147(927):258-267. [2] 李晨,李洁.重组人干扰素的研究进展及相关专利申请[J].中国发明与专利,2018,15(2):15-19. [3] HU JH, CHANG ML, HUANG TJ, et al. Comparison of Compliance and Efficacy of Pegylated Interferon α-2a and α-2b in Adults with Chronic Hepatitis C. J Interferon Cytokine Res. 2019;39(4):205-213. [4] NINGRUM RA. Human interferon alpha-2b: a therapeutic protein for cancer treatment. Scientifica (Cairo). 2014;970315:1-8. [5] KALIKI S, BEJJANKI KM, DESAI A, et al. Interferon Alfa 2b for ocular surface squamous neoplasia: factors influencing the treatment response. Semin Ophthalmol. 2019,34(8):465-472. [6] COENTRO JQ , PUGLIESE E, HANLEY G , et al. Current and upcoming therapies to modulate skin scarring and fibrosis. Adv Drug Deliv Rev. 2019;146:37-59. [7] BERMAN B, DUNCAN MR. Short-term keloid treatment in vivo with human interferon alfa-2b results in a selective and persistent normalization of keloidal fibroblast collagen, glycosaminoglycan, and collagenase production in vitro. J Am Acad Dermatol. 1989;21(4): 694-702. [8] LEE JH, KIM SE, LEE AY. Effects of interferon-α2b on keloid treatment with triamcinolone acetonide intralesional injection. Int J Dermatol. 2008;47(2):183-186. [9] WANG J, JIAO H, STEWART TL, et al. Improvement in postburn hypertrophic scar after treatment with IFN-α2b is associated with decreased fibrocytes. J Interferon Cytokine Res. 2007; 27(11): 921-930 [10] TELASKY C , TREDGET EE, SHEN Q, et al. IFN-α2b Suppresses the Fibrogenic Effects of Insulin-Like Growth Factor-1 in Dermal Fibroblasts. J Interferon Cytokine Res. 1998;18(8):571-577. [11] TREDGET EE , WANG R, SHEN Q,et al. Transforming Growth Factor-βmRNA and Protein in Hypertrophic Scar Tissues and Fibroblasts: Antagonism by IFN-αand IFN-γ In Vitro and In Vivo. J Interferon Cytokine Res. 2000; 20(2):143-151. [12] 陆兴安,许明,沈国良,等.干扰素治疗增生性瘢痕机理的研究[J]. 苏州大学学报(医学版),2005,25(6):1091-1103 [13] GHAHARY A, TREDGET EE, SHEN Q. Induction of Collagenase mRNA Expression in Dermal Fibroblasts by IFN-a2b and Determination of the IFN-a2b Responsive Element on 5’-Flanking Regions of Collagenase Promoter. J Interferon Cytokine Res. 2001; 21(8):611-620 . [14] 黄勇,邢新.干扰素α-2b对瘢痕疙瘩成纤维细胞凋亡及端粒酶活性的影响[J].中华实验外科杂志,2007,24(4):432-434. [15] 徐少骏,滕建英,谢菁,等.细胞信号传导在激素和干扰素诱导的增殖瘢痕成纤维细胞凋亡中的作用[J].中华整形外科杂志, 2008, 24(1):46-49. [16] 刘传君,陈东明,徐少骏,等.干扰素治疗增生性瘢痕的机制[J].中华医学美学美容杂志,2002,8(1):33-34. [17] SCHLUNCK G, MEYER-TER-VEHN T, KLINK T, et al. Conjunctival fibrosis following filtering glaucoma surgery. Exp Eye Res. 2016;142: 76-82. [18] ANDREW NH, AKKACH S, CASSON RJ. A review of aqueous outflow resistance and its relevance to microinvasive glaucoma surgery .Surv Ophthalmol. 2020;65(1): 18-31. [19] 沙倩,乔喜珍,聂庆珠,等.不同高分子生物材料抑制小梁切除后瘢痕的形成[J].中国组织工程研究与临床康复,2009,13(8): 1513-1516. [20] GILLIES M, SU T, SAROSSY M, et al. Interferon-alpha 2b inhibits proliferation of human Tenon’s capsule fibroblasts. Graefes Arch Clin Exp Ophthalmol. 1993;231(2) : 118-121. [21] WANG XY, CROWSTON GJ, WHITE AJ, et al. Interferon-alpha and interferon-gamma modulate Fas-mediated apoptosis in mitomycin-C-resistant human Tenon’sfibroblasts. Clin Exp Ophthalmol.2014; 42(6): 529-538. [22] 陈君毅,孙兴怀,笪翠弟,等.干扰素α-2b对人眼Tenon囊成纤维细胞纤维化作用的影响[J].中国眼耳鼻喉科杂志,2011,11(5): 277-280. [23] 张秀兰,梁凌毅,彭大伟,等.青光眼术后滤过区生长因子的表达及干扰素拮抗生长因子作用的初步研究[J].眼科学报, 2001, 17(2):106-110. [24] 熊新春,杜蜀华,吕源淑,等.干扰素α-2b作为青光眼滤过术后辅助用药的实验研究[J]. 中华眼科杂志,1999,35(1):52-54. [25] 孙亚杰,林婷婷,何彦津,等.临床常用药物对体外培养的复发性翼状胬肉成纤维细胞的抑制效果比较[J]. 中华实验眼科杂志, 2017,35(6):512-519. [26] YIN MY, LI H, ZHANG YN, et al. Interferon Alpha-2b eye drops prevent recurrence of pterygium after the bare sclera technique : a single-center, sequential, and controlled study. Cornea. 2019; 38(10): 1239-1244. [27] Salgado KR, Wendt AR, Fernandes Fagundes NC, et al. Early or delayed palatoplasty in complete unilateral cleft lip and palate patients? A systematic review of the effects on maxillary growth. J Craniomaxillofac Surg.2019;47(11): 1690-1698. [28] SCHEUERMANN M , VANREUSEL I , CASTEELE EV, et al. Spontaneous bone regeneration after closure of the hard palate cleft: a literature review. J Oral Maxillofac Surg. 2019;77(5): 1074. [29] 胡广伟,廖天安,王涛,等.明胶海绵与生物蛋白胶在腭裂修复术中松弛切口处理的疗效观察[J].中国美容医学, 2017,26(2): 84-86. [30] CORNELISSEN AM, VONDEN HOFF IW, MALTHA JC, et al. Effects of interferons on proliferation and collagen synthesis of rat palatal wound fibroblasts. Arch Oral Biol.1999;44(7): 541-547. [31] 胡超,丁丁,刘安东,等.重组人干扰素α-2b对腭裂术后瘢痕成纤维细胞影响的实验研究[J] 安徽医科大学学报, 2008,43(5):520-523. [32] 陶明,胡超,丁丁,等.干扰素对腭裂术后裸露骨面瘢痕成纤维细胞生物学影响的实验研究[J]. 中国美容医学,2011,20(6):926-928. [33] 孟凡伟,刘玉强,史本康,等.干扰素-α2b对尿道瘢痕成纤维细胞生物学的影响[J]. 山东大学学报(医学版),2011,49(12):92-94. [34] FIRAT F, ULUOCAK N, ERDEMIR F, et al. Evaluation of the effects of omega-3 & interferon alpha-2b administration on partial bladder outlet obstruction in a rat model. Indian J Med Res. 2016;144: 572-579. [35] GOKCE A, ABDELMAGEED ZY, LASKER GF, et al. Intratunical injection of genetically modified adipose tissue-derived stem cells with human interferon α-2b for treatment of erectile dysfunction in a rat model of tunica albuginealfibrosis. J Sex Med. 2015;12(7): 1533-1544. [36] 苏云,孟祥俊,于小光,等.干扰素/聚乳酸-羟基乙酸共聚物及壳聚糖/聚乳酸-羟基乙酸共聚物复合膜防止椎板切除术后硬膜外瘢痕粘连的实验[J].中国组织工程研究与临床康复,2008,12(23): 4427-4430. [37] 孔亚男,陆宏,陈颖,等.青光眼滤过术后瘢痕形成机制及抗瘢痕化研究进展[J].国际眼科杂志,2019,19(10):1688-1691. [38] 张思敏,亓发芝. 巨噬细胞极化在增生性瘢痕和瘢痕疙瘩中的作用[J].中国免疫学杂志,2019,35(5):639-642. [39] JIN Q, GUI L, NIU F, et al. Macrophages in keloid are potent at promoting the differentiation and function of regulatory T cells. Exp Cell Res. 2018;362(2):472-476. [40] VERMA SK, GARIKIPATI VNS, KRISHNAMURTHY P, et al. Interleukin-10 inhibits bone marrow fibroblast progenitor cell-mediated cardiac fibrosis in pressure-overloaded myocardium. Circulation. 2017; 136(10): 940-953. [41] OGAWA R. Keloid and hypertrophic scars are the result of chronic inflammation in the reticular dermis. Int J Mol Sci. 2017;18(3): E606. [42] GONG YF, ZHANG XM, LIU F, et al. Inhibitory effect of recombinant human endostatin on the proliferation of hypertrophic scar fibroblasts in a rabbit ear model. Eur J Pharmacol. 2016;791:647-654. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Yu, Tian Shaoqi, Zeng Guobo, Hu Chuan. Risk factors for myocardial infarction following primary total joint arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1340-1345. |
| [3] | Xiao Guoqing, Liu Xuanze, Yan Yuhao, Zhong Xihong. Influencing factors of knee flexion limitation after total knee arthroplasty with posterior stabilized prostheses [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1362-1367. |
| [4] | Wang Haiying, Lü Bing, Li Hui, Wang Shunyi. Posterior lumbar interbody fusion for degenerative lumbar spondylolisthesis: prediction of functional prognosis of patients based on spinopelvic parameters [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1393-1397. |
| [5] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [6] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [7] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [8] | Gu Xia, Zhao Min, Wang Pingyi, Li Yimei, Li Wenhua. Relationship between hypoxia inducible factor 1 alpha and hypoxia signaling pathway [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1284-1289. |
| [9] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [10] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [11] | Wu Xun, Meng Juanhong, Zhang Jianyun, Wang Liang. Concentrated growth factors in the repair of a full-thickness condylar cartilage defect in a rabbit [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1166-1171. |
| [12] | Shen Jinbo, Zhang Lin. Micro-injury of the Achilles tendon caused by acute exhaustive exercise in rats: ultrastructural changes and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1190-1195. |
| [13] | Li Jing, Xie Jianshan, Cui Huilin, Cao Ximei, Yang Yanping, Li Hairong. Expression and localization of diacylglycerol kinase zeta and protein kinase C beta II in mouse back skin with different coat colors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1196-1200. |
| [14] | Chai Le, Lü Jianlan, Hu Jintao, Hu Huahui, Xu Qingjun, Yu Jinwei, Quan Renfu. Signal pathway variation after induction of inflammatory response in rats with acute spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1218-1223. |
| [15] | Liu Cong, Liu Su. Molecular mechanism of miR-17-5p regulation of hypoxia inducible factor-1α mediated adipocyte differentiation and angiogenesis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1069-1074. |
| Viewed | ||||||||||||||||||||||||||||||||||||||||||||||||||
|
Full text 140
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
Abstract 520
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||