Chinese Journal of Tissue Engineering Research ›› 2013, Vol. 17 ›› Issue (1): 131-136.doi: 10.3969/j.issn.2095-4344.2013.01.021
Previous Articles Next Articles
Hematopoietic stem cells transplantation for the treatment of refractory multiple myeloma
Chen Yi ,Yang Ze-song, Chen Jian-bin
- Department of Hematology, the First Affiliated Hospital of Chongqing Medical University, Chongqing 400016, China
-
Received:2012-05-06Revised:2012-07-20Online:2013-01-01Published:2013-01-01 -
Contact:Chen Jian-bin, M.D., Department of Hematology, the First Affiliated Hospital of Chongqing Medical University, Chongqing 400016, China Cqchenjianbin2007@126.com -
About author:Chen Yi★, Studying for master’s degree, Department of Hematology, the First Affiliated Hospital of Chongqing Medical University, Chongqing 400016, China marangel@126.com
CLC Number:
Cite this article
Chen Yi,Yang Ze-song, Chen Jian-bin. Hematopoietic stem cells transplantation for the treatment of refractory multiple myeloma[J]. Chinese Journal of Tissue Engineering Research, 2013, 17(1): 131-136.
share this article
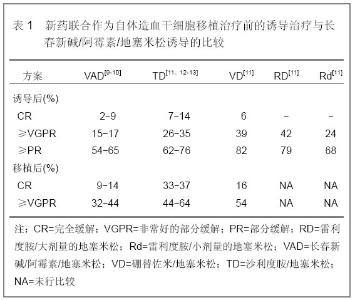
2.1 纳入文献基本情况 初检得到152篇文献,中文99篇,英文53篇。阅读标题和摘 要进行初筛,排除因研究目的与此文无关102篇,内容重复性的研究22篇,共保存22篇中英文文献做进一步分析。文献[1-2]阐述多发性骨髓瘤的临床现状,文献[3-5]篇主要包括了自体移植对多发性骨髓瘤的影响,文献[6-17]篇研究了造血干细胞移植及新药联用的不同方案的疗效比较,文献[18-22]研究了双次移植及异基因造血干细胞移植的优缺点。 2.2 结果描述 2.2.1 造血干细胞移植概述 难治性多发性骨髓瘤是指经多次常规化疗或大剂量化疗未缓解,或化疗甚至造血干细胞移植治疗缓解后60 d内疾病出现进展者[2]。难治性多发性骨髓瘤患者总体生存时间短,生活质量差,目前已成为血液专业的医务工作者关注的重点。造血干细胞移植是通过大剂量放化疗、免疫抑制剂预处理,清除患者体内的肿瘤或异常细胞,再将正常的自体或异体造血干细胞经血管输注给患者,重建骨髓正常造血及免疫功能。根据选用造血干细胞供者的不同可分为:同基因造血干细胞移植、异基因造血干细胞移植、自体造血干细胞移植。由于同基因供者的机会极少,临床上常见的是自体造血干细胞移植和异基因造血干细胞移植。 2.2.2 自体造血干细胞移植及新药联合 自体造血干细胞移植:自体造血干细胞移植是指干细胞供者是患者本人,一般年龄小于65岁,无严重心、肺、肝、肾脏器功能减退且能耐受预处理方案放化疗者,通常选择体内肿瘤负荷最小时进行自体造血干细胞移植,血液系统肿瘤患者宜在第一次完全缓解后在巩固三四个疗程进行。近十多年来,常规化疗治疗多发性骨髓瘤完全缓解率很低,复发率高,多次化疗后肿瘤细胞产生耐药,成为难治性多发性骨髓瘤,欧美等诸多国家组织了多项关于自体造血干细胞移植治疗多发性骨髓瘤的多中心临床协作研究,结果证明自体造血干细胞移植治疗多发性骨髓瘤后可以显著提高多发性骨髓瘤患者的完全缓解和非常好的部分缓解率,延长无进展生存期及总生存期[3]。Fermand等[4]对190例多发性骨髓瘤患者进行长达10年的随访,结果提示移植组患者与化疗组患者的完全缓解率分别为48%和8%(P < 0.01),移植组无进展生存期为25个月,优于化疗组19个月。总的来说,自体造血干细胞移植与传统化疗相比有较好的反应率,无进展生存期延长。Raikumar等[5]回顾大量文献并在其文章中推荐有条件的多发性骨髓瘤患者均要考虑行自体造血干细胞移植,对药物治疗反应好的标危患者可以在第1次复发时进行移植,但是干细胞的采集需在疾病早期阶段进行。所以近期国内外关于多发性骨髓瘤的指南均推荐自体造血干细胞移植+高剂量化疗可成为年轻患者(年龄<65岁)的标准一线治疗手段。 自体造血干细胞移植联合免疫调节剂:目前广泛应用于多发性骨髓瘤治疗的免疫调节剂主要有沙利度胺和其衍生物雷利度胺,他们均有抗肿瘤血管生成、调节各种免疫因子、促进T淋巴细胞增殖等抗肿瘤效应,而雷利度胺在体外的抗肿瘤效应比沙利度胺强数百倍。早在1999年,Singhal等[6]报道了每天口服200- 800 mg沙利度胺治疗多发性骨髓瘤,在大量临床患者中总体有效率为25%。近年来大量的临床随机试验发现雷利度胺联合地塞米松治疗第1次复发的多发性骨髓瘤患者,总体有效率67%,完全缓解/非常好的部分缓解率40%,明显优于单用地塞米松[7]。因为没有移植物抗骨髓瘤效应,所以自体造血干细胞移植复发率较异基因造血干细胞移植复发率高,而免疫调节剂的免疫调节抗肿瘤效应有望能弥补其不足,随后大量临床医生将沙利度胺或雷利度胺用于移植前的诱导治疗和移植后的维持治疗。在新型诱导方案出现之前常采用长春新碱/阿霉素/地塞米松方案或美法仑/泼尼松方案等,但是长春新碱/阿霉素/地塞米松方案化疗三四个疗程后的完全缓解/非常好的部分缓解率仍然很低,完全缓解<10%,完全缓解+非常好的部分缓解<20%,见表1[8],而沙利度胺联合地塞米松的诱导方案比长春新碱/阿霉素/地塞米松方案获益更多。 该表还显示雷利度胺与大剂量的地塞米松联用比与小剂量地塞米松联用有较好的完全缓解+非常好的部分缓解率,雷利度胺与地塞米松联用到现在还没有与其他诱导方案相比较。 沙利度胺主要的毒性是疲劳、困倦、便秘及周围神经病,主要和日使用剂量及持续使用时间相关。雷利度胺的毒性与沙利度胺完全不同,其最常见的不良反应大多是用药28 d后骨髓抑制[14]。沙利度胺和雷利度胺与地塞米松联用时都可以增加其深静脉血栓的风险。尤其是在诱导治疗时,肿瘤负担高,血液处于高凝状态。因此在高风险患者中应用阿司匹林或低分子肝素抗凝[15]。 在2000年以前,即使行造血干细胞移植术,几乎所有的患者最终也都复发,维持治疗显得十分重要。Lokhorst等[16]对556例移植前缓解率无明显差异的多发性骨髓瘤患者移植后的维持治疗进行研究,A组采用α-干扰素,B组采用沙利度胺进行维持治疗,结果A、B两组治疗总有效率分别为79%和88%(P =0.005),完全缓解+非常好的部分缓解分别为54%和66% (P =0.005),完全缓解率分别为23%和31%(P =0.04)。沙利度胺将平均无事件生存期从22个月提高到34个月(P < 0.001,差异有显著性意义),将平均无进展生存期从25个月提高到34个月(P < 0.001,差异有显著性意义)。中位生存期也延长13个月(73-60个月)该研究表明沙利度胺维持治疗在完全缓解(或者完全缓解+非常好的部分缓解)率和无进展生存期方面有明显的获益,可以延长中位生存期。因此沙利度胺在难治性多发性骨髓瘤治疗中占据重要地位,与干细胞移植的联用也是大大改善了难治性多发性骨髓瘤患者的预后。 自体造血干细胞移植联合蛋白酶体抑制剂:硼替佐米是首个发现的蛋白酶体抑制剂,已有大量研究证实硼替佐米单药或与传统化疗药物、免疫抑制剂联合治疗能显著改善治疗的反应率,延长无进展生存期及提高总体生存率。目前包含硼替佐米的治疗方案已成为复发、难治性多发性骨髓瘤患者优先考虑的治疗方案。硼替佐米在干细胞移植前诱导治疗和移植后的维持治疗也显示出它的优越性,在上述表1的对比中可以得出硼替佐米和地塞米松联用作为移植前的诱导治疗,与用长春新碱/阿霉素/地塞米松方案相比,无论在自体造血干细胞移植前或后,完全缓解与非常好的部分缓解率均有明显的增加,相应的无进展生存期与总体生存期均有可能得到提高[8]。而且Cavo等[17]最新随机3期临床研究,对474例多发性骨髓瘤患者随机分为硼替佐米/沙利度胺/地塞米松方案组和沙利度胺/地塞米松方案组,硼替佐米/沙利度胺/地塞米松方案组双次自体造血干细胞移植前的诱导方案及移植后的巩固治疗均为硼替佐米/沙利度胺/地塞米松方案,而沙利度胺/地塞米松方案组双次自体造血干细胞移植的诱导方案及移植后的巩固治疗均为沙利度胺/地塞米松方案,研究结果显示巩固治疗前两组的完全缓解和接近完全缓解率分别为63.1%和54.7%差异无显著性意义,巩固治疗后硼替佐米/沙利度胺/地塞米松组与沙利度胺/地塞米松组完全缓解率分别为60.6% 和 46.6%(P=0.012), 完全缓解/接近完全缓解率分别为73.1% 和60.9%(P=0.020) 差异均有显著性意义,巩固治疗后硼替佐米/沙利度胺/地塞米松组与沙利度胺/地塞米松组3年无进展生存率分别为60%和48%(P=0.042),该研究向医生们提供一个信息硼替佐米/沙利度胺/地塞米松方案作为移植后巩固的治疗方案可以提高患者完全缓解和非常好的部分缓解率,在延长无进展生存时间方面明显获益。但是硼替佐米/沙利度胺/地塞米松方案治疗时出现两三级周围神经病变较沙利度胺/地塞米松方案明显(8.1% vs. 2.4%),虽不影响总体治疗方案,但在治疗中也应注意观察患者周围神经病变的症状及体征,及早发现并予以处理。 双次移植:双次移植是指进行第1次自体造血干细胞移植后再有计划的进行自体或异体移植。两次自体造血干细胞移植治疗多发性骨髓瘤是否可以获得更大的临床效果在争论中不断地研究。在法国IFM 94研究中,399例初治患者被随机分配接受单次自体造血干细胞移植治疗或双次移植[18]。结果显示,完成2次自体造血干细胞移植者总完全缓解率较接受单次自体造血干细胞移植者高(63%对49%),双次移植使患者无进展生存期和总生存期提高1倍。另外Cavo 等[19]结果显示,单次自体造血干细胞移植移植与双次自体造血干细胞移植的完全缓解/接近完全缓解率分别为 33% 和 47%(P =0.008,差异有显著性意义),双次自体造血干细胞移植显著延长无复发生存期(24 vs. 42个月,P < 0.001),且单次移植与双次移植相关死亡率为3% vs. 4%(P=0.70)。双次自体造血干细胞移植对那些对一线治疗无效和(或)在第2次移植后未达到完全缓解或接近完全缓解者有特别的好处。所以双次自体造血干细胞移植能更好的治疗多发性骨髓瘤,特别是难治性多发性骨髓瘤。目前的临床试验中,双次自体造血干细胞移植与1次相比其可以改善患者的无进展生存期,但是对总体生存没有改善。而且,只有当患者在第1次自体造血干细胞移植至少没有达到非常好的部分缓解率在行第2次自体造血干细胞移植则可获益。但是有细胞遗传性异常的差预后患者即使行两次自体造血干细胞移植治疗其预后也是差的。因此仍应继续寻找更好更合理的治疗手段。 当了解双次自体造血干细胞移植比单次自体造血干细胞移植有较好的疗效时,临床医生考虑自体移植后再次进行异体移植会不会有更好的疗效。Bruno等[20]为了研究多发性骨髓瘤患者选择双次自体移植或自体+异体序贯移植疗效。对162例年龄小于65岁且至少有1个同胞的多发性骨髓瘤患者进行前瞻性研究。所有患者在最初接受长春新碱/阿霉素/地塞米松方案后均进行大剂量美法仑+自体造血干细胞移植,其后有80例多发性骨髓瘤患者接受异基因造血干细胞移植,另82例无同胞人类白细胞抗原供体者再次行自体造血干细胞移植治疗。结果显示中位随访45个月(21-90个月)时,中位0S率及EFS率在自体造血干细胞移植+异基因造血干细胞移植及双次自体造血干细胞移植组分别为80个月对54个月(P=0.04)及35个月对29个月(P=0.02)。在完成预定治疗目标患者中,自体造血干细胞移植+异基因造血干细胞移植组58例,双次自体造血干细胞移植组46例,治疗相关死亡率比较,差异无显著性意义(P=0.09),但骨髓瘤原发病相关死亡率在双次自体造血干细胞移植组中显著增高。自体造血干细胞移植+异基因造血干细胞移植组中位随访期为38个月(10-72个月)时,58例中有21例(36名)仍处于完全缓解期,而双次自体造血干细胞移植组46例患者中有25例(54%)死亡。由此得出结论,对于年龄<65岁的新诊断多发性骨髓瘤患者,如果有人类白细胞抗原完全相合的同胞供者,在自体移植后行异体干细胞移植,其生存期优于双次自体移植。 2.2.3 异基因造血干细胞移植 异基因造血干细胞移植是指供、受者为同一种族,但要求供受者主要组织相容性抗原一致,是目前应用最广泛,疗效最好的造血干细胞移植技术,在理论上可以完全治愈血液系统的恶性疾病,恢复健康造血。通常按供者来源不同又分为同胞兄妹供者和无血缘关系供者的异基因造血干细胞移植。 异基因造血干细胞移植能治愈多发性骨髓瘤,是基于供体移植物中不含骨髓瘤细胞,且移植物抗骨髓瘤效应。随着时代的前进,非清髓异基因造血干细胞移植显著降低移植相关死亡率但复发率稍高一些。移植后增加供体淋巴细胞输注,免疫调节剂、蛋白酶体抑制剂等联合使用可以进一步延长患者无进展生存期和总体生存期[21]。Kröger等[22]对经异基因造血干细胞移植后获得部分缓解的32例多发性骨髓瘤患者进行供体淋巴细胞输注,8例患者获得完全的血液学缓解,8例患者中有7例获得分子生物学缓解,对于剩下未缓解的患者加用沙利度胺、雷利度胺或硼替佐米等治疗,32例患者中共19例患者获得完全的血液学缓解,15例患者中有7例获得分子生物学缓解,这些患者的无进展生存率及总体生存率得到了很大提高。随着近年来免疫调节剂及蛋白酶体抑制剂的发展,异基因造血干细胞移植逐渐的不受到临床医师的青睐。所以异基因造血干细胞移植也是一种拥有相同的人类白细胞抗原捐献者的年轻难治性患者的选择,结合免疫调节剂、蛋白酶体抑制剂、供者淋巴细胞输注等综合治疗手段,可以从根本上治愈疾病,提高生活质量。"
| [1] 陈灏珠,林果为,徐建民.多发性骨髓瘤.实用内科学[M].人民卫生出版社,2009:2554-2560.[2] Siegel DS, Vij R, Jakubowiak AJ. Jakubowiak, Clinical roundtable monograph. Emerging treatment options for relapsed and refractory multiple myeloma. Clin Adv Hematol Oncol.2011;9(4):1-15. [3] Harousseau JL, Attal M, Avet-Loiseau H. The role of complete response in multiple myeloma. Blood. 2009;114(15): 3139-3146.[4] Fermand JP, Katsahian S, Divine M, et al. High-dose therapy and autologous blood stem-cell transplantation compared with conventional treatment in myeloma patients aged 55 to 65 years: long-term results of a randomized control trial from the Group Myelome-Autogreffe. J Clin Oncol. 2005;23(36): 9227-9233. [5] Rajkumar SV. Multiple myeloma: 2012 update on diagnosis, risk-stratification, and management. Am J Hematol. 2012; 87(1):78-88.[6] Singhal S, Mehta J, Desikan R, et al. Antitumor activity of thalidomide in refractory multiple myeloma. N Engl J Med. 1999;341(21): 1565-1571. [7] Stadtmauer EA, Weber DM, Niesvizky R, et al. Lenalidomide in combination with dexamethasone at first relapse in comparison with its use as later salvage therapy in relapsed or refractory multiple myeloma. Eur J Haematol. 2009; 82(6): 426-432. [8] Harousseau JL. Ten years of improvement in the management of multiple myeloma: 2000-2010. Clin Lymphoma Myeloma Leuk. 2010;10(6):424-442.[9] Cavo M, Zamagni E, Tosi P, et al., Superiority of thalidomide and dexamethasone over vincristine- doxorubicindexamethasone (VAD) as primary therapy in preparation for autologous transplantation for multiple myeloma. Blood. 2005;106(1):35-39. [10] Macro M, Divine M, Uzunban Y, et al. Dexamethasone plus Thalidomide (Dex/Thal) compared to VAD as a pre-transplant treatment in newly diagnosed multiple myeloma (MM): A randomized trial. Blood. 2006.108(11 Pt 1):1a-1062a. [11] Rajkumar SV, Jacobus S, Callander NS, et al. Lenalidomide plus high-dose dexaethasone versus lenalidomide plus low-dose dexamethasone as initial therapy for newly diagnosed multiple myeloma:an open-label randomized controlled trial. Lancet Oncol.2010;11(1):29-37.[12] Einsele H, Liebisch P, Langer C, et al. Velcade, intravenous cyclophosphamide and dexamethasone induction for previously untreated multiple myeloma (German DSMM Xia trial). Blood. 2009;114(22):59-60 (abstract 130). [13] Patriarca F, Einsele H, Spina F, et al. Allogeneic stem cell transplantation in multiple myeloma relapsed after autograft: a multicenter retrospective study based on donor availability. Biol Blood Marrow Transplant. 2012;18(4): 617-626.[14] Richardson P, Jagannath S, Hussein M, et al. Safety and efficacy of single-agent lenalidomide in patients with relapsed and refractory multiple myeloma. Blood, 2009;114(4): 772-778.[15] Palumbo A, Facon T, Sonnevevld P, et al. Thalidomide for treatment of multiple myeloma: 10 years later. Blood. 2008; 111(8): 3968-3977.[16] Lokhorst HM, van der Holt B, Zweegman S, et al. A randomized phase III study on the effect of thalidomide combined with adriamycin, dexamethasone (TAD) and high-dose melphalan followed by thalidomide maintenance in patients with multiple myeloma. Blood. 2010;115(6):1113- 1120. [17] Cavo M, Tacchetti P, Patriarca F, et al. A phase III study of double autotransplantation incorporating bortezomib- thalidomide- dexamethasone (VTD) or thalidomide dexamethasone (TD) for multiple myeloma:superior clinical outcomes with VTD compared to TD. Blood. 2009;114(22): 148-149 (abstract 351).[18] Harousseau JL, Attal M, Avet-Loiseau H, et al. Bortezomib plus dexamethasone is superior to vincristine plus doxorubicin plus dexamethasone as induction treatment prior to autologous stem-cell transplantation in newly diagnosed multiple myeloma: results of the IFM 2005-01 phase III trial. J Clin Oncol. 2010;28(30): 4621-4629.[19] Cavo M, Tosi P, Zamagni E, et al. Prospective, randomized study of single compared with double autologous stem-cell transplantation for multiple myeloma: Bologna 96 clinical study. J Clin Oncol. 2007;25(17): 2434-2441. [20] Bruno B,Rotta M,Patriarca F, et al. A comparison of allografting with autografting for newly diagnosed myeloma. N Engl J Med. 2007;356(11): 1110-1120. [21] Gahrton G. Progress in allogeneic transplantation for multiple myeloma. Eur J Haematol. 2010;85(4):279-289. [22] Kröger N, Badbaran A, Lioznov M, et al. Post-transplant immunotherapy with donor-lymphocyte infusion and novel agents to upgrade partial into complete and molecular remission in allografted patients with multiple myeloma. Exp Hematol. 2009;37(7): 791-798. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Xiumei, Zhai Yunkai, Zhao Jie, Zhao Meng. Research hotspots of organoid models in recent 10 years: a search in domestic and foreign databases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1249-1255. |
| [3] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [4] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [5] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [6] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [7] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [8] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| [9] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [10] | Kong Desheng, He Jingjing, Feng Baofeng, Guo Ruiyun, Asiamah Ernest Amponsah, Lü Fei, Zhang Shuhan, Zhang Xiaolin, Ma Jun, Cui Huixian. Efficacy of mesenchymal stem cells in the spinal cord injury of large animal models: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1142-1148. |
| [11] | Hou Jingying, Yu Menglei, Guo Tianzhu, Long Huibao, Wu Hao. Hypoxia preconditioning promotes bone marrow mesenchymal stem cells survival and vascularization through the activation of HIF-1α/MALAT1/VEGFA pathway [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 985-990. |
| [12] | Shi Yangyang, Qin Yingfei, Wu Fuling, He Xiao, Zhang Xuejing. Pretreatment of placental mesenchymal stem cells to prevent bronchiolitis in mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 991-995. |
| [13] | Liang Xueqi, Guo Lijiao, Chen Hejie, Wu Jie, Sun Yaqi, Xing Zhikun, Zou Hailiang, Chen Xueling, Wu Xiangwei. Alveolar echinococcosis protoscolices inhibits the differentiation of bone marrow mesenchymal stem cells into fibroblasts [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 996-1001. |
| [14] | Fan Quanbao, Luo Huina, Wang Bingyun, Chen Shengfeng, Cui Lianxu, Jiang Wenkang, Zhao Mingming, Wang Jingjing, Luo Dongzhang, Chen Zhisheng, Bai Yinshan, Liu Canying, Zhang Hui. Biological characteristics of canine adipose-derived mesenchymal stem cells cultured in hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1002-1007. |
| [15] | Geng Yao, Yin Zhiliang, Li Xingping, Xiao Dongqin, Hou Weiguang. Role of hsa-miRNA-223-3p in regulating osteogenic differentiation of human bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1008-1013. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||