Chinese Journal of Tissue Engineering Research
Previous Articles Next Articles
Membrane biomaterials in tissue engineering: an outlook on guided membrane regeneration theory
Li Li1, Zhang Heng2, Tang Li-bo1
- 1School of Basic Medicine and Life Sciences, Hainan Medical University, Haikou 571199, Hainan Province, China; 2Panjin Municipal Library, Panjin 124000, Liaoning Province, China
-
Received:2018-01-18Online:2018-08-08Published:2018-08-08 -
Contact:Tang Li-bo, Master, Professor, School of Basic Medicine and Life Sciences, Hainan Medical University, Haikou 571199, Hainan Province, China -
About author:Li Li, M.D., Associate professor, School of Basic Medicine and Life Sciences, Hainan Medical University, Haikou 571199, Hainan Province, China -
Supported by:the Natural Science Foundation of Hainan, No. 813190
CLC Number:
Cite this article
Li Li1, Zhang Heng2, Tang Li-bo1 . Membrane biomaterials in tissue engineering: an outlook on guided membrane regeneration theory[J]. Chinese Journal of Tissue Engineering Research, doi: 10.3969/j.issn.2095-4344.0777.
share this article

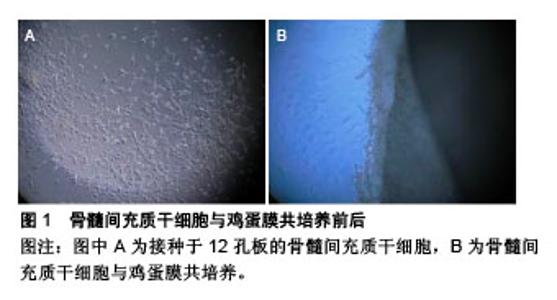
按膜生物材料的来源,可分为天然脱细胞基质膜、有机高分子膜及人工合成大分子膜。 2.1 天然脱细胞基质膜 天然脱细胞基质膜是一类来源于动物组织或尸体来源材料,包括猪小肠黏膜下层、小牛真皮脱细胞基质、人羊膜脱细胞基质、动物角膜脱细胞基质等。一般采用酸碱或酶的方法溶解基质材料上的细胞,仅保留细胞外基质。脱细胞基质的主要成分是胶原蛋白、层粘连蛋白、弹性蛋白、纤维粘连蛋白、硫酸肝素及蛋白多糖,另外在脱细胞处理过程中保留了部分细胞因子,能促进后续种子细胞与膜材料的复合。天然脱细胞基质膜常用于膜引导材料诱导组织再生,由于属于天然材料,具有合适的孔隙度和吸附性,适合细胞的黏附和生长,具有良好的生物相容性,常用于制作人工血管和人工皮肤的替代品。其缺陷在于力学性能较差,体内降解速率的不可控性。可通过再生膜或使用交联剂改良天然脱细胞基质膜的力学特性,控制其体内降解速率。 2.2 天然有机高分子膜 天然有机高分子膜利用天然有机高分子材料经化学或物理处理后形成膜,包括蛋白质类、多糖类。 2.2.1 蛋白质类膜生物材料 胶原:胶原作为细胞外基质成分,具有良好的生物相容性和成膜性。其缺陷在于抗张力强度不够,膜材料移植后降解速率难以控制。根据来源不同组织,可分为Ⅰ-Ⅺ型胶原,其中成膜性最佳的是Ⅱ型胶原(表1)。 研究表明,胶原膜既可为组织再生提供一个空间屏障,防止细胞迁移出缺损区域,还可以引导血管再生。许繁等[3]利用骨髓间充质干细胞与胶原膜复合培养,结果表明由于胶原膜独特的网状结构,对细胞具有锚定和支持作用。另外,在引导骨组织再生技术中,胶原膜常被用作骨组织再生的引导膜,促进骨组织的再生修 复[4-5]。制作胶原膜的原材料有许多种,如动物的肌腱组织、软骨组织、大鼠鼠尾胶原的提取等。除了天然的动物来源的胶原以外,常常用市面可采购的胶原水解 物——明胶制作胶原膜,并用人工合成的有机大分子进行混合,根据组织修复的需要,设计成不同拉伸强度和降解速率的复合膜材料。 鸡蛋膜:俗称“凤凰衣”,民间常用于创伤、压疮的敷贴,是一种性状优异,具有应用开发价值的天然膜生物材料。鸡蛋膜的主要成分是Ⅰ型胶原,另有特殊的Ⅹ型胶原,具有可剥离的内外双层膜结构,类似于哺乳动物的羊膜。鸡蛋壳膜在其形成过程中,不断有钙离子渗入到胶原膜的孔隙中,蛋白分子之间有大量的二硫键。故天然的鸡蛋膜具有质脆、强度差,在组织工程实践中难以直接应用。目前,对于鸡蛋膜材料研究主要集中在鸡蛋膜的改性,其关键技术点在于鸡蛋膜的溶解方法和成膜化研究。鸡蛋壳膜的溶解方法包括碱溶解法、酶溶解法。李吕梁[6]采用氢氧化钠-乙醇溶解法得到10%-15%的蛋膜素溶液。Yi等[7-8]报道了一种打开鸡蛋膜分子中的二硫键,使鸡蛋膜液态化的一种方法,他们采用β-硫代丙酸还原溶解法,在鸡蛋膜中加入一定浓度的β-硫代丙酸和乙酸溶液,80-90 ℃溶解,而后通过添加壳聚糖或羟基磷灰石和聚乳酸,进行成膜化处理,获得了具有良好生物相容性和拉伸强度的共混膜。液态化的鸡蛋膜除了可与其他膜生物材料形成共混膜以外,还可以对一些生物支架材料表面进行改性,如利用低温等离子法成功将聚乙烯支架材料表面用蛋壳膜水溶液进行固化处理,洗脱实验表明,采用蛋壳膜溶剂对固化的聚乙烯表面进行长时间洗涤,其固定是牢固的。同时,也使聚乙烯支架材料具备了良好的生物相容性。作者所在课题组曾用鸡蛋膜为原料,通过酶的消化作用成功液化鸡蛋膜,经流延法自然成膜,用大鼠骨髓间充质干细胞进行复合培养,结果表明鸡蛋膜改性成膜后的材料具有良好的生物相容性(图1)。 羊膜:除了上述两种蛋白质类膜生物材料外,在组织工程生物材料的研究中羊膜也备受关注。一般从生物相容性考虑,首选人羊膜,其次也选自猪或者其他哺乳动物的羊膜。 人羊膜是一种天然的高分子复合膜生物材料,含有胶原、糖蛋白、蛋白多糖、整合素和细胞因子等多种成分,人羊膜及羊膜脱细胞基质可作为构建周围神经组织工程、皮肤组织工程、角膜组织工程、血管组织工程、肌腱组织工程及骨组织工程的修复材料。Mligiliche等[9]将人羊膜脱细胞基质制成管状诱导周围神经再生,以修复大鼠坐骨神经缺损。研究发现修复效果与人羊膜管径大小相关,同时证明了人羊膜脱细胞基质与许旺细胞复合重构的膜管对于大鼠周围神经的修复具有牵引作用。刘德伍等[10]利用SD大鼠表皮干细胞与人羊膜脱细胞基质复合构建组织工程皮肤,在糖尿病大鼠模型上进行覆盖实验,结果表明人工复合羊膜能有效促进糖尿病创面的愈合。王振显等[11]将人脱细胞羊膜与大鼠骨髓间充质干细胞复合培养,体外用膀胱匀浆液诱导7 d获得组织工程膀胱,体内移植2周后,人脱细胞羊膜被吸收降解,体内自身的膀胱移行细胞和平滑肌细胞开始附着形成,结果表明人脱细胞羊膜基质是理想的膀胱替代修补材料。近年来,将内皮细胞种植在人羊膜脱细胞基质上构建组织工程血管成为一种有效的方法[12]。此外,在肌腱修复组织工程实践中,丁宝志等[13]应用光化学组织粘合技术联合人羊膜包裹修复鸡第三趾伸屈肌腱断裂,在抗粘连程度、抗炎症细胞浸润及抗张力强度指标方面都取得了良好效果。 玉米醇溶蛋白质膜:主要是由玉米种子中经醇溶提取的蛋白质,经纯化而成的膜。该膜是一种可生物降解的膜,常用于绿色可降解的包装膜,具有良好的阻气性、阻油性、保香性和防湿性。原料采用玉米种子,使用有机溶剂提取醇溶蛋白,流延法浇注成膜。李萍等[14]介绍了一种醇溶蛋白质膜的制作工艺,采用体积分数75%乙醇浸泡萃取粉碎的玉米种子(液固比6∶1),离心分离,回收乙醇,湿产品冷冻干燥成膜。采用有机溶剂萃取制备的玉米醇溶蛋白质膜的抗拉伸强度、延展性和吸湿性指标均不理想,膜脆而硬,故在生物支架材料制备上常常针对其缺陷及支架的用途进行必要的改性,如添加一定比例的壳聚糖、聚乙醇酸和硬脂酸形成复合膜,增加材料的可塑性和抗拉伸强度。并用于膜诱导再生修复支架材料。李敏等[15]利用玉米醇溶蛋白为原料,采用溶剂浇注/粒子沥滤法制备玉米醇溶蛋白质膜,在Beagle犬上作为膜诱导材料,促进了牙周缺损的修复。 2.2.2 多糖类膜生物材料 壳聚糖是经典的多糖类成膜材料,可利用蟹、虾和昆虫的甲壳中提取的甲壳素经脱乙酰化处理而成,微溶于水。壳聚糖易成膜,制备工艺简单。从分子结构来看,壳聚糖分子由于提取处理工艺差异,其表面带有不同比例的活性基团,一般带有反应活性较强的羟基、羧基和氨基,可根据膜生物材料的用途进行必要的化学修饰,如酰基化、硫酸酯化、羟乙基化等,同时,壳聚糖也可以与其他膜生物材料混合,形成复合膜材料。因此壳聚糖属于用途最为广泛的膜生物材料,如与胶原、丝素蛋白的复合制作软骨修复材 料,与羟基磷灰石复合制作骨修复材料[16],此外,与聚乙烯醇、聚乳酸、聚羟基乙酸等人工合成大分子复合形成膜材料。一般而言,由于活性基团的交联作用,壳聚糖的加入可增强膜的抗拉伸张力与孔隙度,有利于细胞的吸附和黏着作用。此外,由于壳聚糖本身具有良好的生物相容性,常与其他无机支架材料复合,改善无机材料的生物相容性和体内降解性。郎明媚等[17]利用壳聚糖膜包裹鸡曲指肌腱缝合处,预防肌腱粘连,实验表明缝合后的肌腱愈合良好,缝合处表面光滑,肌腱与周围组织有明显的界限,腱鞘缺损处有假鞘形成,说明壳聚糖膜具有良好的隔离作用。壳聚糖膜具有良好的可塑性,可利用模具塑造成各种组织外形,在3D器官打印、水凝胶材料制备方面都具有无可比拟的优势。李雅勋等[18]将壳聚糖膜卷曲成管状支架,以代替硅胶支架和金属支架用于食管缺损的修补,为食管重建提供了一种可降解的生物支架。利用成膜方法用模具制成管状,而后用氢氧化钠处理,制成中空的壳聚糖导管,消毒后植入大鼠体内,观察生物相容性和体内降解性,结果表明管状壳聚糖支架表面光滑洁净,柔韧性好,组织相容性好,无炎症免疫反应,随时间可被组织吸收降解。 纤维素是地球上现存的最广泛的多糖类分子,可来源于植物和真菌、纤维素及其衍生物,是一大类可再生的天然高分子材料,与人工合成的大分子材料相比,纤维素具有无毒、无环境污染、来源广泛、易成膜等特点[19],在食品、化工和生物材料等方面有着广泛应用,在生物材料方面主要制成丝、膜、水凝胶、气凝胶和智能材料等形态而在实践中应用。纤维素难溶于水,因此若将纤维素用于膜生物材料,一般需要对其进行化学修饰或对其进行改性处理形成再生纤维素。有学者偶然发现在7%NaOH/12%尿素水溶液或4.6%LiOH/15%尿素水溶液(均为质量分数)中加入纤维素,在预冷至-12 ℃后可在2 min内迅速溶解纤维素,且该溶液在0-5 ℃可长时间保持稳定的溶液状态[20]。溶液化是成膜的关键步骤,也是与其他膜生物材料复合形成复合膜的前提条件,在液化状态下,采用流延法,蒸发出溶液中的水分子,加入交联剂即可成膜。目前临床上常用的纤维素膜生物材料主要包括纤维素膜、改性纤维素膜及纤维素与其他膜生物材料形成的复合膜3大类。而纤维素膜又可分为再生纤维素膜和纤维素膜衍生物,临床上常用于透析膜。再生纤维素膜的特点是具有很强的亲水性,通透性好,抗拉伸强度大。纤维素膜衍生物是利用C2、C3、C6三个位置上羟基的活性经化学修饰方法产生的衍生物,具有成膜性、孔隙率加大的特性,能有效滤过小分子物质(如肌酐、尿素和磷),而带电离子和蛋白质不能通过。醋酸纤维素膜和临床使用较多的血仿膜就属于纤维素衍生膜。改性的纤维素膜主要着眼于改变膜的物理特性,如水溶性、吸水性、抗拉伸强度、孔隙度及生物相容性。王立靖[21]通过比较不同材料的纤维素膜在血液透析中的生物相容性及宿主炎症反应,证实血液透析膜与血液接触后主要引起补体激活,以及细胞因子、C-反应蛋白、β2-微球蛋白的变化,其中以纤维素衍生物为材料制作的血仿膜对血磷的降幅最大,引起氧化应激反应最小。曹静洁等[22]以细菌纤维素膜为支架,体内培养兔角膜上皮细胞,观察角膜细胞与纤维素膜的复合情况,实验结果表明,细菌纤维素膜具有良好的生物相容性。纤维素膜具有廉价、易得、再生性好的特点,但其缺陷也是显而易见的,纤维素膜脆性大,抗拉伸强度弱,故常与其他高分子材料复合,用于复混膜的材料包括壳聚糖、聚乳酸、聚乙醇酸、褐藻酸钠等。刘格莎等[23]利用壳聚糖和褐藻酸钠不同的配比关系与纤维素复合制备组织工程皮肤,其柔软度、抗拉伸性及生物相容性都达到了理想状态。近年来,也有一些研究者将一些纳米颗粒复合到纤维素膜中,用于改善膜的强度[24]。王碧等[25]利用胶原蛋白、褐藻酸钠及羧甲基纤维素制备共混膜,这3类大分子之间有较强的交联作用。通过钙离子的交联,氢键和范德华力的相互作用,使共混膜(复合膜)的力学性能有了明显改善,当胶原蛋白质量分数为18.1%、海藻酸钠为45.5%、羧甲基纤维素为36.4%时三元共混膜的抗拉张强度最大,达到102 MPa。 除上述外,其他成膜的多糖类材料包括海藻酸盐、琼脂糖、卡拉胶、聚合淀粉等。这类多糖类物质由于具有良好的水合性,常与其他膜生物材料混合使用,成膜方式也是多种多样。向翠丽等[26]利用琼脂糖与壳聚糖混合溶液,采用电沉积法在电极上沉积形成复合膜,同时用电化学方法在膜上组装了免疫大分子,体外构建了免疫分子分析体系。刘格莎等[23]利用海藻酸盐吸水性能好的特点,将其添加到纤维素中构建组织工程皮肤,其柔软度及抗张性都达到了人体皮肤的相应指标。崔菁等[27]利用聚乙烯醇与卡拉胶复合制膜,在膜上种植血管内皮细胞,通过调节卡拉胶的浓度可调节细胞的生长速度。研究表明,当卡拉胶质量分数为20%-30%的膜材料最适合细胞的生长,复合膜有利于诱导内皮细胞的黏附生长。除了制作组织工程再生诱导膜材料以外,多糖类物质常被设计成药物缓释系统包被材料及外源细胞包被材料,作为分子传感器或者消除外源细胞的免疫原,即微囊化人工细胞。其技术原理就是将异源细胞包被于具有免疫隔离功能的膜内,使细胞发挥正常的生理功能。同时避免宿主的免疫排斥反应。此技术在人工肝、人工胰的制作方面有着广泛应用。王健等[28]系统地比较了海藻酸盐、卡拉胶、壳聚糖等多种多糖膜生物材料在微囊化异源细胞中的作用,结果表明壳聚糖结合纤维素膜形成的包被材料在免疫隔离、小分子传递等方面具有优异的性能。 2.3 人工合成有机大分子材料膜 人工合成的有机大分子种类繁多,是组织工程膜材料的基础,早期采用诸如硅胶、聚酯类膜材料,植入体内易引发炎症反应,同时由于无法降解,需要二次手术取出。随着新材料的发现,在膜生物材料方面也有所突破。归纳起来,有以下几种人工合成的大分子膜材料。 2.3.1 聚乳酸和聚乙醇酸及两者共聚物PLGA 聚乳酸是由乳酸的环状二聚体即丙交酯聚合而成,在体内易降解为乳酸而进入代谢循环,聚乙醇酸是由乙交酯开环聚合而得,在体内降解为羟基乙酸并参与体内循环。这两种人工合成的大分子材料可以一定比例混合形成共聚物,常用于制备可生物降解的膜,其柔韧度、降解时间等指标可通过改变两种分子的比例调控。 PLGA膜材料具有可控的降解性、合适的抗拉伸性和机械强度,材料成膜条件易于控制,在组织修复领域得到广泛应用。但其缺陷也是显而易见的,表现为:聚乳酸、聚乙醇酸和PLGA液化步骤需要有机溶剂溶解,成膜后有机溶剂的残留易导致机体的炎症反应;膜材料吸水性较差;与细胞的生物相容性较差。有鉴于此,PLGA膜在实际应用中常需改性或与其他生物膜材料形成复混膜。 PLGA膜具有膜诱导作用,Zhang等[29]评价了不同比例聚乳酸与聚乙醇酸静电纺丝膜的诱导作用,在1∶1的比例下能有效诱导组织再生。此外,PLGA膜也可作为隔离膜使用。赵哲珊等[30-31]就采用有机溶剂-氯仿溶解PLGA,制备口腔修复中的根管桩膜。 2.3.2 聚乙烯醇 聚乙烯醇是由聚醋酸乙烯酯水解而成的水溶性聚合物,由于其分子结构中含有大量的羟基,该材料具有良好的吸水性和柔韧性。在组织修复中,常用于制作水凝胶,以替代受损的关节软骨,用于骨损伤修复。聚乙烯醇单独成膜存在膜降解速率太快,生物相容性差等缺陷,在实际应用中,常与胶原或壳聚糖复合成膜。改良后的聚乙烯醇具有弹性好、化学结构稳定,易于成型,无毒,生物相容性较佳,在生物医学各个领域得到广泛的使用。崔菁等[27]的研究表明,利用20%- 30%卡拉胶改良聚乙烯醇的生物相容性,效果最佳。 2.3.3 聚己内酯 聚己内酯是一类疏水性人工合成的大分子膜材料,成膜后具有较强的抗拉伸性,在生物体内可缓慢降解。其缺陷在于需要有机溶剂溶解,利用溶剂挥发成膜,而有机溶剂的残留可能诱发机体的炎症反应。胡星友等[32]利用静电纺丝技术将聚己内酯制成小口径人造血管,用于替换因静脉曲张或血栓而导致的功能障碍小口径血管,由于改变了成膜工艺,使其生物相容性得到改良。动物体内实验表明,植入体未诱发炎症反应。此外,也有通过对聚己内酯进行改性,与其他膜材料混合,以改善其柔韧性和生物相容性。吴巍等[33]将明胶与聚己内酯纳米纤维共混经电纺丝技术成膜,制作人工皮肤。采用Hacat细胞测试电纺膜的生物相容性,并对接种细胞前后机械性能进行评价,应用CCK-8法检测细胞增殖情况,实验表明复合了Hacat细胞的混纺膜具有与人皮肤类似的抗张力,生物相容性良好,可用于皮肤组织工程修复。 2.3.4 聚羟基丁酸 聚羟基丁酸为聚酯类降解产物,单独成膜抗拉伸力较弱,脆性大,常与羟基戊酸形成共聚酯膜。共聚酯膜膜具有引导骨再生能力[34],与羟基磷灰石功能相似,具有良好的骨传导性和骨形成能力,在骨组织损伤修复中有着广泛应用。 2.3.5 类金刚石膜(DLC) 类金刚石膜膜是一种类金刚石材料经化学气相沉积或物理沉积作用形成的膜;早期在口腔修复中应用,用于镍和钛等金属材料表面改性作用。Sui等[35]使用类金刚石膜镀膜镍钛合金,结果表明类金刚石膜膜能显著提高血液相容性和耐腐蚀性。近些年,由于类金刚石膜膜良好的血液相容性和生物相容性,常被用于心血管材料的表面改性[36],在心血管介入治疗和心脏病治疗领域得到了广泛应用。Salahas等[37]对245例植入带有类金刚石膜膜涂层的phytis支架患者进行术后临床跟踪观察,结果显示这种支架植入成功率高,安全有效。虽然这种观察缺乏对照,难以下肯定结论,但说明类金刚石膜膜对人体是安全有效的。 2.3.6 羟基磷灰石膜 严格意义上说,羟基磷灰石本身不能形成膜,但由于羟基磷灰石属于骨组织成分,是天然生物材料,故常与其他膜材料混合使用,改善共混膜的物理和生物特性。与之混合的膜材料包括聚乳酸、聚酰胺、聚乙烯醇,用于改善羟基磷灰石本身力学性能不足的缺陷。近些年来,采用羟基磷灰石-壳聚糖复合膜在组织再生中受到广泛关注[38-39]。传统工艺中,羟基磷灰石很难在有机相中分散均匀,而通过超声和其他物理化学处理方法可使羟基磷灰石均匀分散,将该复合液制成膜,则使羟基磷灰石与有机高分子结合牢固并体现出良好的力学性能。羟基磷灰石-壳聚糖复合膜在骨骼再生、骨移植得到了广泛应用。"

| [1] 曲晓娟,朱建华.应用引导组织再生膜与人工骨、bFGF等生物材料治疗牙周骨缺损[J].中国组织工程研究与临床康复, 2009, 13(12):2291-2294. [2] Cao CS,Yao Y,Yao QQ,et al.Preparation and preliminary in vitro evaluation of a bFGF-releasing heparin-conjugated poly(epsilon-caprolactone) membrane for guided bone regeneration.J Biomater Sci Polym Ed.2015;26(10):600-616. [3] 许繁,杨德圣.Bio-Gide胶原膜对兔骨髓间充质细胞增殖和成骨分化的影响[J].中国组织工程研究,2014,18(30):4787-4803.[4] Behring J,Walboomers XF.Toward guided tissue and bone regeneration:morphology, attchm ent, proliferation,and migration of cells culture done collagen barrier membranes.A systematic review.Odontology.2008;96(1):l-11.[5] Taguchi Y,Amizuka N,Nakadate M,et al.A histological evaluation for guided bone regeneration induced by a collagenous membrane.Biomaterials.2005;26(31):248-253.[6] 李吕粱.中国专利,1111514A,1995-11-l5.[7] Yi F,Guo ZX,Zhang LX,et al.Soluble eggshell membrane protein: preparation, characterization and biocompatibility. Biomaterials.2004;25(19):4591-4599.[8] 熊曦,李强,弋峰,等.鸡蛋壳膜蛋白在生物相容性材料中的应用研究[J].高分子通报,2011,24(4):25-33.[9] Mligiliche N,Endo K,Okamoto K,et al.Extracellular matrix of human amnion manufactured into tubes as conduits for peripheral nerve regeneration.Biom Mater Res. 2002;63(5): 591-600.[10] 刘德伍,钟清玲,刘繁荣.表皮干细胞复合羊膜构建组织工程皮肤修复糖尿病难愈创面[J].透析与人工器, 2010,21(3):12-14.[11] 王振显,蔡文清,庞国勋,等.人脱细胞羊膜负载大鼠骨髓间充质干细胞构建组织工程膀胱的研究[J].中国老年学杂志, 2010,30(2): 207-210.[12] Tsai SH,Liu YW,Tang WC,et al.Characterization of porcine arterial endothelial cells cultured on amniotic membrane, a potential matrix for vascular tissue engineering.Biochem Biophys Res Commun. 2007;357:984-990.[13] 丁宝志,姚敏.光化学组织粘合技术联合羊膜修复手部肌腱损伤的研究[J].现代医学,2017,54(3):406-412.[14] 李萍,李登新.一种新型的生物降解材料玉米醇溶蛋白质膜[J].化学工程与装备,2011,40(1):136-140.[15] 李敏,王瑶,王双双.玉米醇溶蛋白支架生物相容性及其在牙周缺损修复中的应用[J].中国组织工程研究, 2016,20(25): 3726-3731.[16] 袁秋华,张自强,巫剑波,等.羟基磷灰石-壳聚糖复合膜的制备及研究进展[J].广东化工,2016,43(14):75-78.[17] 郎明媚,何玉龙,吴淼.生物材料防黏连膜修复运动性肌腱断裂的特点及性能评价[J].中国组织工程研究与临床修复,2010,14(34) 6393-6398.[18] 李雅勋,陈刚,石文君.壳聚糖管状支架的制备及生物降解性[J].中国组织工程研究与临床康复,2010,14(29):5360-5362.[19] Davood G,Salavati-Niasari M,Farshad B,et al.Electro-spinning of cellulose acetate nanofibers: Microwave synthesize of calcium ferrite nanoparticies and CA-Ag-CaFe204 nanocomposites.Mater Sci. 2015;26(11):8358.[20] Parra CJDL,Zambrano JR,Bermejo MD,et al.Influence of water concentration in the viscosities and densities of cellulose dissolving ionic liquids.Correlation of viscosity data.J Chem Thermodyn.2015;91:8-16.[21] 王立婧.不同透析膜材料清除血磷效果及其生物相容性[J].中国组织工程研究与临床康复,2008,12(45): 913-916.[22] 曹静洁,张琛,赵少贞.细菌纤维素膜作为生物支架构建组织工程角膜上皮的可行性研究[J].中华实验眼科杂志, 2016,34(2): 121-124.[23] 刘格莎,杨砜,李娜梅.纤维素-壳聚糖-海藻酸钠复合膜组织工程皮肤的制备与表征[J].医学分子生物学杂志, 2014,37(3): 165-168.[24] Shah N,UI-Islam M,Khattak WA,et al.Overview of bacterial cellulose composites: A multipurpose advanced material. Carbohydr Polym.2013;98(2):1585-1589.[25] 王碧,廖立敏,李建凤,等.胶原蛋白/海藻酸/羧甲基纤维素共混膜的结构与性能[J].化学世界,2013,54(3):155-160,164.[26] 向翠丽,邱树君,孙立贤,等.壳聚糖复合膜的制备及其界面的生物功能化[J].功能材料,2012,43(B08):125-128.[27] 崔菁,张亚彬,熊艳杰.卡拉胶/聚乙烯醇复合材料的制备及生物相容性评价[J].中国组织工程研究, 2017,21(2):215-220.[28] 王健,王常勇,奚廷斐.海藻酸盐微囊化人工细胞研究面临的挑战与进展[J].药物分析杂志,2010,30(7): 1373-1379.[29] Zhang E,Zhu C,Yang J,et al.Electrospun PDLLA/PLGA composite membranes for potential application in guided tissue regeneration.Mater Sci Eng C Mater Biol Appl. 2016; 58:278-285. [30] 赵哲珊,黄华,邱荣敏.聚乳酸可吸收根管桩膜生物相容性试验[J].华西口腔医学杂志,2016,34(5):122-124.[31] 黄华,陈爱华,周永明.用于增强乳牙可吸收根管桩密闭的可吸收聚乳酸薄膜[P].中国:CN103349797, 2015-04-01.[32] 胡星友,赵新哲,高晶.静电纺材料结构对细胞生长的影响[J].产业用纺织品,2013,31(5):1-5.[33] 吴巍,段惠川,曹谊林.明胶/聚己内酯纳米纤维电纺膜在表皮组织工程的应用[J].组织工程与重建外科, 2014,10(2):61-68.[34] 唐倩,陈建洪,黄南楠.聚羟基丁酸-羟基戊酸共聚酯膜与聚羟基丁酸-羟基戊酸共聚酯-溶胶-凝胶生物活性玻璃复合材料修复骨缺损的研究[J].中华生物医学工程杂志,2010,16(3):201-205.[35] Sui JH,Gao ZY,Cai W,et al. DLC films fabricated by plasma immersion ion implantation and deposition on the NiTi alloys for improving their corrosion resistance and biocompatibility. Mater Sci Eng. 2007;454:472-476.[36] Liao TT,Zhang TF,Li SS,et al.Biological responses of diamond-like carbon (DLC) films with different structures in biomedical application.Mater Sci Eng C Mater Biol Appl. 2016;69:751-759.[37] Salahas A,Vrahatis A,Karabinos I,et al.Success,safely and efficacy of implantation of diamond-like carbon-coated stents.Angiology.2007;58(2):203-210.[38] Cheng Y,Li Y,Zuo Y,et al.Propertics and in vitro biological evalution of nano-hdroxyapatite/chitosan membranes for bone guide regeneration.Mater Sci Eng C. 2009;(29): 299-335.[39] 杨俊,陈治清,胡常红.壳聚糖/多壁碳纳米管复合膜诱导羟基磷灰石仿生合成的研究[J].第三军医大学学报, 2013,35(14): 1480-1484.[40] 李瑞欣,张西正,郝庆新.微米级煅烧羟基磷灰石/壳聚糖复合膜的制备与性能[J].复合材料学报,2013, 30(1):103-111.[41] 汤辉,陈汉邦,徐阳.Lbl法制备磁性纳米复合纤维膜生物相容性的研究[J].口腔医学,2015,35(5):321-325.[42] Nowogrodzki A.The cell seeker.Nature. 2017;547(1038): 24-26.[43] Danesh-Sani SA,Tarnow D,Yip JK,et al.The influence of cortical bone perforation on guided bone regeneration in humans.Int J Oral Maxillofac Surg. 2017;46(2):261-266.[44] 汤玉斐,谢高伟,赵康,等.静电纺丝法制备多层复合骨引导再生微纳米纤维膜[J].材料导报,2014,27(24): 82-87.[45] Rakhmatia YD,Ayukawa Y,Furuhashi A,et al.Current barrier membranes: titanium mesh and other membranes for guided bone regeneration in dental applications.J Prosthodont Res. 2013;57(1):3-14. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Shen Jinbo, Zhang Lin. Micro-injury of the Achilles tendon caused by acute exhaustive exercise in rats: ultrastructural changes and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1190-1195. |
| [3] | Liang Xueqi, Guo Lijiao, Chen Hejie, Wu Jie, Sun Yaqi, Xing Zhikun, Zou Hailiang, Chen Xueling, Wu Xiangwei. Alveolar echinococcosis protoscolices inhibits the differentiation of bone marrow mesenchymal stem cells into fibroblasts [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 996-1001. |
| [4] | Duan Liyun, Cao Xiaocang. Human placenta mesenchymal stem cells-derived extracellular vesicles regulate collagen deposition in intestinal mucosa of mice with colitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1026-1031. |
| [5] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [6] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [7] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [8] | Li Li, Ma Li. Immobilization of lactase on magnetic chitosan microspheres and its effect on enzymatic properties [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 576-581. |
| [9] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [10] | Liu Liu, Zhou Qingzhu, Gong Zhuo, Liu Boyan, Yang Bin, Zhao Xian. Characteristics and manufacturing techniques of collagen/inorganic materials for constructing tissue-engineered bone [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 607-613. |
| [11] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [12] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [13] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [14] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [15] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||