Chinese Journal of Tissue Engineering Research
Previous Articles Next Articles
Physical and chemical properties of 3D extrusive bioprinting cell-encapsulated hydrogel
Gu Ya-wei, Li Mu, Fan Zi-wen, Wang Long, Li Ze-yao, Chen Chang
- Department of Thoracic Surgery, Shanghai Pulmonary Hospital, Tongji University School of Medicine, Shanghai 200433, China
-
Received:2017-12-03Online:2018-08-08Published:2018-08-08 -
Contact:Chen Chang, Professor, Department of Thoracic Surgery, Shanghai Pulmonary Hospital, Tongji University School of Medicine, Shanghai 200433, China -
About author:Gu Ya-wei, Master, Department of Thoracic Surgery, Shanghai Pulmonary Hospital, Tongji University School of Medicine, Shanghai 200433, China -
Supported by:the Scientific Plan Program of Shanghai Science and Technology Committee, No. 15JC1490900
CLC Number:
Cite this article
Gu Ya-wei, Li Mu, Fan Zi-wen, Wang Long, Li Ze-yao, Chen Chang. Physical and chemical properties of 3D extrusive bioprinting cell-encapsulated hydrogel[J]. Chinese Journal of Tissue Engineering Research, doi: 10.3969/j.issn.2095-4344.0746.
share this article

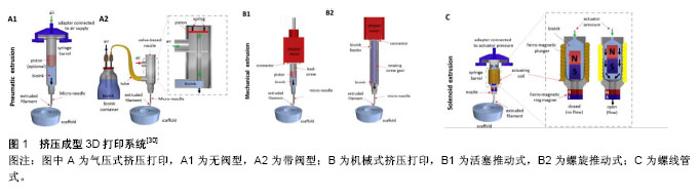
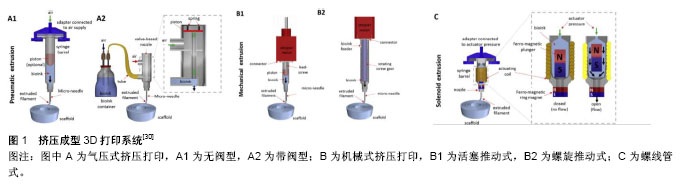
2.1 生物墨水 所有被打印的物料统称为生物墨水,包括以下几个方面:支架材料,通常是由天然聚合物或合成聚合物形成的水凝胶;细胞及生物、化学因子;交联剂。在挤压成型式打印中,由于生物墨水是通过打印机的喷头被挤压出来的,所以生物墨水的可打印性是首先需要被考虑的因素。生物墨水应该满足以下的条件:类流体的形态,可通过很小口径的打印喷头;在打印过程中不会堵塞喷头。衡量这2个条件的是生物墨水的黏度。首先需要确定能打印成型的生物墨水的黏度,其次还需要对内在细胞兼容性的平衡,才能确定最佳的墨水配 比[12]。其他影响生物墨水配制的因素包括合理的机械性能、生物墨水微环境等。 2.1.1 水凝胶 水凝胶是在水溶性高分子中引入一部分疏水基团和亲水基团,亲水残基与水分子结合,将水分子连接在网状内部,而疏水残基遇水膨胀的交联聚合物。由于这种特性,水凝胶被用于3D生物打印的支架材料,其主要作用是维持三维空间结构及组成细胞外基质。作为生物墨水中的主要组成部分,水凝胶很大程度上影响了生物墨水的生物和机械性能。选择一种合适的水凝胶是3D生物制造的基础和关键。理想的水凝胶应当具备以下几个特征:可快速、可控的交联,交联后能维持形状,避免形变;含有细胞结合序列,增强细胞的结合和分化;在内在细胞产生自己的细胞外基质,形成组织前能够稳定地维持支架结构[13];允许营养物质和氧气进入,同时可让代谢产物排出[14]。 在选择水凝胶时,亲水的、吸水性强的聚合物比较受青睐[15-17],吸水的聚合物在交联后形成有微小孔隙、透水的水凝胶,允许培养液的渗入及代谢产物的排出。不同的聚合物交联后形成的孔隙和透水性各有差异。聚合物分为天然来源的聚合物和人工合成聚合物。天然来源聚合物形成的水凝胶,由于和细胞外基质存在一定的相似性,再通过适量加入其他成分,可一定程度地复制细胞外基质,给细胞提供结构、物理和生物学行为上的支持,成为近年来研究的热点材料[14,18]。但天然来源聚合物常见的不足是形成溶液的黏度低,机械强度弱,因此组成的生物墨水打印性较差,交联后的水凝胶柔韧性不足。相较之下,人工合成聚合物的机械性能都更加可控[19]。与天然来源聚合物不同的是,这类合成聚合物大多缺乏细胞结合域[20],所以在生物制造中的应用受限。各类水凝胶性能的比较见表1[21]。 2.1.2 新型水凝胶与混合配方策略 上述提到,无论是天然聚合物还是人工合成聚合物形成的水凝胶,都有各自的优缺点。如何利用好两种材料的优点,弥补各自的不足也成为很多研究的主题。一方面可通过对聚合物的改性实现更好的性能,例如对于明胶的改性。明胶是天然胶原部分降解的产物,其含有细胞结合域RGD (Arg-Gly-Asp)序列及基质金属蛋白酶作用部位[22]。明胶是一种对温度敏感的材料,当其溶液温度低于上临界溶解温度时,明胶分子相互交联形成凝胶;而当温度上升超过上临界溶解温度时,分子简单交联作用失效,复成水溶液。这种交联方式受温度影响大,且难以控制。甲基丙烯酸酯明胶(gelatin methacrylate,GelMA)是通过在明胶的RGD序列上引入甲基丙烯酸酯分子侧基。在加入光引发剂后,经过紫外光照射,光引发剂释放活性碎片,进而引发溶液中单体明胶分子上的甲基丙烯酸酯侧基相互交联,形成水凝胶[22]。该交联过程受到溶质浓度、引发剂的浓度及光照时间影响,因此更容易控制。另外像硫醇化的壳聚糖[23],最早应用于药物递释,相比于未改性的壳聚糖,其有很好的黏膜黏附性、促进渗透作用,因此也被应用于3D生物打印中作为支架材料。其他用于改性的功能基团还有如丙烯酸酯、酪酸等[24-25]。另一方面,可通过材料的混合各取所长,尽可能实现多样的生物功能和物理性质。在这种策略中,仍然以天然聚合物为主要成分,合成的聚合物为辅助材料;或作为牺牲材料起临时作用而在后期被移除。Kang等[26]的研究中使用甲基丙烯酸酯明胶/聚乙二醇二丙烯酸酯/海藻酸钠打印心脏瓣膜细胞,其中聚乙二醇二丙烯酸酯作用是获得可调的机械性能,而海藻酸钠是用于增加黏度。Schuurmann等[27]用透明质酸增加黏度。透明质酸广泛存在于人类和动物组织中,目前在美容和再生医学上已得到较多应用。在3D生物打印中也被视为可模拟细胞外基质的一种理想材料。此外,胶原/海藻酸钠、琼脂/聚乙二醇、海藻酸钠/聚丙烯酰胺、海藻酸钠/甲基纤维素等配方也都被用于3D生物打印的研究。 除了对一些传统材料进行改进外,也有一些研究致力于新材料的开发。Cheng等[28]的研究展示了一种对pH值敏感的全DNA水凝胶。这种水凝胶是通过单一类型的DNA“Y”型结构在一定pH值下相互交联形成,当pH值改变时,水凝胶又可快速转化成水溶液。此后一种通过DNA交联的多肽-DNA结合物被用于原位多层3D生物打印[29]。这种DNA水凝胶不仅具有不溶胀、不收缩、可降解等优势,还可协同纳米粒子、蛋白、多聚物发挥更多元的生物功能。 2.2 打印与交联对水凝胶内部细胞的影响 2.2.1 可打印性和打印损伤 挤压式3D生物打印机通常由生物墨水分配系统、全自动打印系统及打印平台组成。打印时,由电脑控制墨水分配系统根据设计的结构精确地将墨水仓中的生物墨水通过压力被挤出成型。一般打印的形状和结构可通过计算机辅助设计(Computer Aided Design,CAD)来完成,也可直接采用CT或MRI影像中的数据,这也是3D生物打印高度个性化和精确化的因素之一。 生物墨水分配系统中的压力可通过气体、机械或螺线管等方式实现[30](图1)。其中气压式分为阀门式和无阀门式。无阀门式原理简单,应用更加广泛,而在打印精度上则略逊于阀门式。机械式可通过活塞或螺旋来施加压力。在控制方面,活塞式更加直接简单,而螺旋式则在空间上有更好地把控,并且适合打印一些黏度较高的生物墨水。螺线管式通过电磁场的产生,抬起墨水仓中的磁铁,生物墨水填充于间隙中时,电磁场消失,磁铁被下方的磁铁吸引落下将间隙中的生物墨水挤出成型。 虽然挤压的原理不同,但打印的大致流程较为类似。生物墨水从墨水仓被挤压至喷嘴,最后被挤出至平台。相比于其他打印类型,比如喷墨式生物打印,挤压生物可打印更高黏度的生物墨水,这也使打印高密度细胞生物墨水成为可能。与此同时,流体通过管道时,管道内壁会对流体产生摩擦力,即剪切力。剪切力的存在会作用于生物墨水内部的细胞,产生相应的损伤,这也是打印过程中影响细胞存活及其生物学性能的主要因素。在一般情况下,剪切力与距管道内壁的距离呈负相关。而在打印过程中生物墨水的黏度、挤压力大小、喷嘴内径也都会影响剪切力。因此如何减小剪切力避免造成细胞的损伤同时,又不降低生物墨水的打印性[27],也是3D生物打印中值得研究的一部分。 Blaeser等[31]对于剪切力的研究发现,随着剪切力的增加,打印后的细胞存活率下降,不仅如此,在后期培育中,受到高剪切力的细胞生长和数量也明显低于对照组。当打印过程中剪切力小于5 kPa时,其对细胞几乎不产生短期和长期损伤。该研究采用的材料为海藻酸钠,打印对象为小鼠成纤维细胞和骨髓间充质干细胞,结果虽然存在一定的局限性,但对其他种类的生物墨水和细胞仍有参考价值。此外,对于一些温度敏感性材料,如明胶,在打印的时候受到温度的影响较大。Zhao等[12] 对不同浓度的明胶、明胶海藻酸钠混合物在不同温度下及不同料持仓时间进行流变性能测试,通过此方法可找到最合适的打印温度,并且确保在一定时间内打印能够维持细胞高存活率。 2.2.2 交联过程 水凝胶前体在打印后需要经过交联固化,成型后维持结构外形。根据原理交联一般分为物理交联和化学交联两大类,具体的交联方式因聚合物的种类各有不同。通常交联剂的浓度、交联时间影响了最终打印后水凝胶的硬度和机械强度。打印的水凝胶在不变形的基础上也必须确保内部细胞的存活,因此交联的强度不宜过大。选择一种对细胞损伤最小的交联剂和交联方式是生物制造前期构建中的关键。Kang等[26]的研究对比了两种光引发剂,即Irgacure2959和VA086对于细胞存活率的影响。相比于VA086,Irgacure2959在提高水凝胶硬度的情况下降低了对细胞的损伤。另外该研究还证明了过氧化氢酶可减少紫外光对细胞的损伤。 此外,也有学者研究交联方式对于打印的改善。天然聚合物海藻酸钠可被钙离子交联,然而纯海藻酸钠的浓度会影响内部细胞的存活,4%的浓度是一个分水岭,当海藻酸钠浓度低于4%时,打印后细胞存活率在90%左右,但4%浓度以下的海藻酸钠溶液由于流动性较大,因此成型性不很理想;而当海藻酸钠浓度高于4%时,细胞存活率随浓度升高明显下降。基于此,Tabriz等[32]使用多次交联方法打印海藻酸钠细胞混合液。将海藻酸钠预先与浓度较低的钙离子溶液混合,形成部分交联海藻酸钠溶液,打印时再逐层用较高浓度钙离子溶液交联,待打印结束,整个结构浸没于钡离子溶液中加强交联。此方法解决了低浓度海藻酸钠打印性差的问题同时,保证了细胞的存活率。类似的方法也用于其他材料的打印中,比如Bertassoni等[33]用紫外短时间交联GelMA溶液形成部分交联状态,而后挤压成型。 2.3 水凝胶模拟细胞微环境 传统的贴壁细胞培养为2D单层培养,无法提供类似细胞在体内立体的微环境。在3D结构中,细胞在空间上分布于水凝胶中,水凝胶不仅起到了支撑作用,也起到类似于细胞外基质的作用。一方面3D生物打印可构建具有一定孔隙的结构,另一方面,水凝胶本身也具有更微小的孔隙,二者都能使营养物质能够渗入到立体结构内部。除此之外,细胞在水凝胶内还可感受到能够决定细胞命运的生物和机械信号[4],这两种信号来自于细胞和细胞之间及细胞与细胞外基质之间的交互作用。细胞通过对这些信号的反应产生相应的下游生物学活动。因此,在这种立体结构中,细胞在汲取营养物质、生长、繁殖、分化和分泌上都区别于传统单层培养[4]。 2.3.1 机械信号 细胞在水凝胶中能够感受到的机械信号分为两种,即水凝胶的硬度和结构中的应力及表面张力。 通常正常人类组织的硬度在0.1-40 kPa之间。Discher等[34]的研究表明,细胞外基质的硬度能够调控细胞的生长、形态和分化,对干细胞的影响尤其明显。Engler等[35]用不同硬度覆盖胶原的聚丙烯酰胺水凝胶培养人类间充质干细胞,发现当水凝胶硬度接近某种天然组织时,间充质干细胞会往该种组织中的细胞分化。 此外,细胞在正常组织中也受到不同的应力,如张力(韧带)、压力(软骨)、剪切力(血管内皮)等。细胞在感受到这些应力后,内部的机械信号通路被激活,从而改变某些基因的表达,最终影响细胞的行为。例如在胶原中被周期拉伸的心肌细胞倾向于形成沿长轴排列的相互连接的心肌束[36]。平滑肌细胞在胶原中展现出沿着拉伸方向的排列方式和定向的迁移行为,成骨相关的基因表达及钙沉着也沿此方向有所下降[37]。 通常水凝胶的硬度由多聚物的浓度和交联剂密度决定[38]。对于一些微小的组织补片,均质的水凝胶可满足制造要求,其中的聚合作用可广泛单一地进行,无需太多选择性。比如用离子溶液交联时,仅一种离子浓度或者在光固化过程中,紫外线的剂量和照射时间固定[39]。然而一些天然组织并非机械性能均质的,如肌腱、心脏瓣膜等[40-41]。这种情况下,单一的交联方法无法最大程度地复制天然组织的机械性能,导致无法真实地获取细胞在真实情况下的生物学行为。因此研究者开发了一些模式化的、有梯度变化的水凝胶系统,用于研究机械性能不均质性对细胞行为的影响。这些由水凝胶系统通过可变的交联过程或多重交联实现。一些研究结果也表明,相比于单一交联的水凝胶,选择化交联的水凝胶或者逐步交联的水凝胶更有利于细胞的生长或控制细胞的铺展[24]。 2.3.2 生物信号 细胞外微环境的另一重要因素为生物学因素。为了能够最大程度地保持打印后的细胞生物学功能,仿生细胞外生物环境是一种解决方案,也被称为材料仿生学。水凝胶系统本身即是一种很有前景的细胞传递系统,原因如下:其亲水表面与体液接触时有较低的界面张力,可减少蛋白的吸收和多余的细胞黏附[42];具有高度渗透性,可提高营养物质和代谢产物的转运[43]。在天然的细胞外基质中,有至少30种分子组成其多态的结构(例如胶原、糖蛋白、弹力蛋白、蛋白多醣等),形成了支撑细胞和维持组织形态的网络。基于此前对于细胞学的研究和知识,确定每种细胞对应细胞外基质中的成分并不困难,为仿制提供了依据。一般而言,蛋白质和细胞因子是两个用于提升细胞性能的重要成分[34]。 Jones等[44]用添加了粘连蛋白聚乙二醇水凝胶培养人类牙髓干细胞,相比于没有添加粘连蛋白的水凝胶,其存活率和铺展能力都更佳。在Cui等[45]的研究中,软骨细胞在成纤维因子2和转化生长因子β1的作用下具有最好的成软骨特性,因为两种的协同刺激促进软骨细胞的增殖和成软骨表型的形成。该研究还指出,生长和分化因子应当配伍低密度的细胞,效果更好。为了能够高度模拟细胞外基质,Skardal等[46]对组织内的细胞外基质进行脱细胞处理,混合于生物墨水中,可给每种细胞提供特定的细胞外基质成分。 在模拟细胞外基质和细胞关系的过程中,同样存在失真和平衡问题。一方面,在生物体内的细胞外基质是一个动态过程,无论是组织的机械性能还是生物成分,都会随着发育、衰老和病理过程而变化,这给水凝胶仿生细胞外基质带来了很大挑战;另一方面,水凝胶和细胞的组合也是一个动态过程,细胞在分泌细胞外基质、细胞因子等的同时,原来作为细胞外基质的水凝胶也在不断降解,如何确保两者速率保持一致,保证制作的组织结构维持形状不塌陷,一直以来也是难以控制的因素。目前大多研究注意到了细胞和水凝胶在体外培育和体内培育的动态变化,但还不能十分精确地掌控这一动态变化的发生。 "

| [1] Langer R,Vacanti JP.Tissue engineering.Science.1993;260(5110):920-926.[2] Hutmacher DW.Scaffold design and fabrication technologies for engineering tissues--state of the art and future perspectives.J Biomater Sci Polym Ed.2001;12(1):107-124.[3] Hutmacher DW,Schantz T,Zein I,et al.Mechanical properties and cell cultural response of polycaprolactone scaffolds designed and fabricated via fused deposition modeling.J Biomed Mater Res.2001; 55(2):203-216.[4] Colacino JA.3D human tissue culture: modeling environmental effects on the stem cell epigenome.Epigenomics.2016;8(11):1453-1457.[5] Caiazzo M,Okawa Y,Ranga A,et al.Defined three-dimensional microenvironments boost induction of pluripotency.Nat Mater.2016; 15(3):344-352.[6] Nakamura M,Iwanaga S,Henmi C,et al.Biomatrices and biomaterials for future developments of bioprinting and biofabrication. Biofabrication. 2010;2(1):014110.[7] Fedorovich NE,Schuurman W,Wijnberg HM,et al.Biofabrication of osteochondral tissue equivalents by printing topologically defined, cell-laden hydrogel scaffolds.Tissue Eng Part C Methods. 2012;18(1): 33-44.[8] Derby B.Printing and prototyping of tissues and scaffolds.Science. 2012; 338(6109):921-926.[9] Nakamura M,Nishiyama Y,Henmi C,et al.Inkjet bioprinting as an effective tool for tissue fabrication[C].proceedings of the NIP & Digital Fabrication Conference, F,2006.[10] Kirchmajer DM,Iii RG,Panhuis MIH.An overview of the suitability of hydrogel-forming polymers for extrusion-based 3D-printing.J Mater Chem B.2015;3(20):4105-4117.[11] Kilpatrick JI,Revenko I,Rodriguez BJ.Nanomechanics of Cells and Biomaterials Studied by Atomic Force Microscopy.Adv Healthc Mater. 2015;4(16):2456-2474.[12] Zhao Y,Li Y,Mao S,et al.The influence of printing parameters on cell survival rate and printability in microextrusion-based 3D cell printing technology.Biofabrication.2015;7(4): 045002.[13] Poveda-Reyes S,Moulisova V,Sanmartin-Masia E,et al. Gelatin-Hyaluronic Acid Hydrogels with Tuned Stiffness to Counterbalance Cellular Forces and Promote Cell Differentiation. Macromol Biosci.2016;16(9):1311-1324.[14] Slaughter BV,Khurshid SS,Fisher OZ,et al.Hydrogels in regenerative medicine. Adv Mater.2009; 21(32-33):3307-3329.[15] Jungst T,Smolan W,Schacht K,et al.Strategies and Molecular Design Criteria for 3D Printable Hydrogels.Chem Rev.2016;116(3):1496-1539.[16] Kang HW,Lee SJ,Ko IK,et al.A 3D bioprinting system to produce human-scale tissue constructs with structural integrity.Nat Biotechnol. 2016;34(3):312-319.[17] Pescosolido L,Vermonden T,Malda J,et al.In situ forming IPN hydrogels of calcium alginate and dextran-HEMA for biomedical applications.Acta Biomater.2011;7(4):1627-1633.[18] Seliktar D.Designing cell-compatible hydrogels for biomedical applications. Science.2012;336(6085):1124-1128.[19] Gasperini L,Mano JF,Reis RL.Natural polymers for the microencapsulation of cells.J R Soc Interface.2014;11(100): 20140817.[20] Wolf MT,Daly KA,Brennan-Pierce EP,et al.A hydrogel derived from decellularized dermal extracellular matrix.Biomaterials. 2012;33(29): 7028-7038.[21] Panwar A,Tan LP.Current Status of Bioinks for Micro-Extrusion-Based 3D Bioprinting. Molecules(Basel,Switzerland).2016;21(6).pii: E685.doi: 10.3390/molecules21060685.[22] Nichol JW,Koshy ST,Bae H,et al.Cell-laden microengineered gelatin methacrylate hydrogels.Biomaterials.2010;31(21):5536-5544.[23] Sakloetsakun D,Bernkop-Schnürch A.Thiolated chitosans.J Drug Deliv Sci Technol.2010;20(1):63-69.[24] Khetan S,Burdick JA.Patterning network structure to spatially control cellular remodeling and stem cell fate within 3-dimensional hydrogels. Biomaterials.2010;31(32):8228-8234.[25] Toh WS,Lim TC,Kurisawa M,et al.Modulation of mesenchymal stem cell chondrogenesis in a tunable hyaluronic acid hydrogel microenvironment.Biomaterials.2012;33(15):3835-3845.[26] Kang LH,Armstrong PA,Lee LJ,et al.Optimizing Photo-Encapsulation Viability of Heart Valve Cell Types in 3D Printable Composite Hydrogels. Ann Biomed Eng.2017;45(2):360-377.[27] Schuurman W,Levett PA,Pot MW,et al.Gelatin-methacrylamide hydrogels as potential biomaterials for fabrication of tissue-engineered cartilage constructs.Macromol Biosci.2013; 13(5):551-561.[28] Cheng E,Xing Y,Chen P,et al.A pH-triggered, fast-responding DNA hydrogel.Angew Chem Int Ed Engl.2009;48(41):7660-7663.[29] Li C,Faulkner-Jones A,Dun AR,et al.Rapid formation of a supramolecular polypeptide-DNA hydrogel for in situ three-dimensional multilayer bioprinting.Angew Chem Int Ed Engl. 2015;54(13): 3957-3961.[30] Ozbolat IT,Hospodiuk M.Current advances and future perspectives in extrusion-based bioprinting.Biomaterials.2016;76:321-343.[31] Blaeser A,Duarte Campos DF,Puster U,et al.Controlling Shear Stress in 3D Bioprinting is a Key Factor to Balance Printing Resolution and Stem Cell Integrity.Adv Healthc Mater.2016;5(3): 326-333.[32] Tabriz AG,Hermida MA,Leslie NR,et al.Three-dimensional bioprinting of complex cell laden alginate hydrogel structures.Biofabrication. 2015;7(4):045012.[33] Bertassoni LE,Cardoso JC,Manoharan V,et al.Direct-write bioprinting of cell-laden methacrylated gelatin hydrogels.Biofabrication. 2014;6(2): 024105.[34] Discher DE,Mooney DJ,Zandstra PW.Growth factors, matrices, and forces combine and control stem cells.Science. 2009;324(5935):1673-1677.[35] Engler AJ,Caragkrieger C,Johnson CP,et al.Embryonic cardiomyocytes beat best on a matrix with heart-like elasticity: scar-like rigidity inhibits beating.J Cell Sci.2008;121(22): 3794-3802.[36] Zimmermann WH,Schneiderbanger K,Schubert P,et al.Tissue Engineering of a Differentiated Cardiac Muscle Construct.Circ Res. 2002;90(2):223-230.[37] Pang Y,Wang X,Lee D,et al.Dynamic quantitative visualization of single cell alignment and migration and matrix remodeling in 3-D collagen hydrogels under mechanical force. Biomaterials. 2011;32(15): 3776-3783.[38] Diederich VE,Studer P,Kern A,et al.Bioactive polyacrylamide hydrogels with gradients in mechanical stiffness.Biotechnol Bioeng. 2013;110(5): 1508-1519.[39] Hockaday LA,Kang KH,Colangelo NW,et al.Rapid 3D printing of anatomically accurate and mechanically heterogeneous aortic valve hydrogel scaffolds.Biofabrication.2012;4(3):035005.[40] Patwari P,Lee RT.Mechanical Control of Tissue Morphogenesis.Circ Res.2008;103(3): 234-243.[41] Ulrich TA,De Juan Pardo EM,Kumar S.The mechanical rigidity of the extracellular matrix regulates the structure, motility, and proliferation of glioma cells.Cancer Res.2009;69(10):4167-4174.[42] Abraham S,Brahim S,Ishihara K,et al.Molecularly engineered p(HEMA)-based hydrogels for implant biochip biocompatibility. Biomaterials. 2005;26(23):4767-4778.[43] Tse M,Uludag H,Sefton MV,et al.Secretion of recombinant proteins from hydroxyethyl methacrylate-methyl methacrylate capsules. Biotechnol Bioeng.996;51(3):271-280.[44] Jones TD,Kefi A,Sun S,et al.An Optimized Injectable Hydrogel Scaffold Supports Human Dental Pulp Stem Cell Viability and Spreading.Adv Med.2016;2016:7363579.[45] Cui X,Breitenkamp K,Lotz M,et al.Synergistic action of fibroblast growth factor-2 and transforming growth factor-beta1 enhances bioprinted human neocartilage formation. Biotechnol Bioeng.2012; 109(9):2357-2368.[46] Skardal A,Devarasetty M,Kang HW,et al.A hydrogel bioink toolkit for mimicking native tissue biochemical and mechanical properties in bioprinted tissue constructs.Acta Biomater.2015; 25:24-34. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [11] | Shu Qihang, Liao Yijia, Xue Jingbo, Yan Yiguo, Wang Cheng. Three-dimensional finite element analysis of a new three-dimensional printed porous fusion cage for cervical vertebra [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(24): 3810-3815. |
| [12] | Zuo Zhenkui, Han Jiarui, Ji Shuling, He Lulu. Pretreatment with ginkgo biloba extract 50 alleviates radiation-induced acute intestinal injury in mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3666-3671. |
| [13] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [14] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [15] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||