Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (20): 3256-3262.doi: 10.3969/j.issn.2095-4344.0742
Previous Articles Next Articles
Notch signaling pathway and the nucleus pulposus cells in degenerative intervertebral disc: roles in the repair and reconstruction
Zhong Yuan-ming1, Liang Zi-yang2, He Jia2, Xu Wei2, Mo Ri-yang2
- 1the First Affiliated Hospital of Guangxi University of Chinese Medicine, Nanning 530023, Guangxi Zhuang Autonomous Region, China; 2Guangxi University of Chinese Medicine, Nanning 530001, Guangxi Zhuang Autonomous Region, China
-
Received:2017-12-25Online:2018-07-18Published:2018-07-18 -
About author:Zhong Yuan-ming, Master, Chief physician, Professor, Master’s supervisor, the First Affiliated Hospital of Guangxi University of Chinese Medicine, Nanning 530023, Guangxi Zhuang Autonomous Region, China -
Supported by:the Natural Science Foundation of Guangxi Zhuang Autonomous Region of China, No. 2014GXNSFAA118210
CLC Number:
Cite this article
Zhong Yuan-ming1, Liang Zi-yang2, He Jia2, Xu Wei2, Mo Ri-yang2. Notch signaling pathway and the nucleus pulposus cells in degenerative intervertebral disc: roles in the repair and reconstruction[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(20): 3256-3262.
share this article
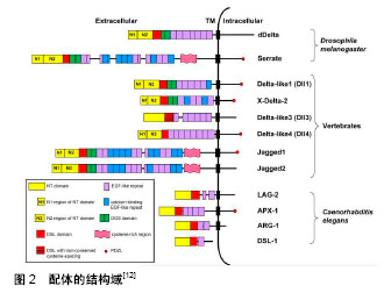
2.1 Notch信号通路的组成和激活 2.1.1 Notch受体 在哺乳动物中Notch信号通路的核心要素包括:Notch受体、Delta-like(DLL)、Jagged配体(JAG)和转录因子CBF1-SU(H)-LAG1(CSL)DNA结合蛋白(如CBF1)。由于存在几个旁系同源基因和多个调控相关因子,使哺乳动物的Notch信号传导更为复杂。目前在脊柱动物中已经鉴定了4个Notch家族成员,分别为Notch1,2,3,4和5个Notch配体(即JAG1 JAG2, DLL1,DLL3和DLL4)[8-9]。Notch受体是单道Ⅰ型跨膜蛋白,其结合配体,引发一系列导致Notch信号受体细胞中基因调控的事件[10]。其参与了响应配体结合向细胞核转移的特异性细胞外信号,从单个mRNA转录物翻译后,未加工的Notch蛋白质通过分支途径转运到高尔基复合体中通过furin蛋白酶样转化酶在位点S1被蛋白水解切割,将原始多肽转化成通过非共价相互作用连接的亚单位——异二聚体蛋白,其是存在于细胞表面的跨膜受体[9]。最终生成的Notch信号分子由胞外区域、跨膜区域和胞内区域组成。Notch受体的胞外域都含有介导配体相互作用的29-36串联的表皮生长因子重复序列和3个富含半胱氨酸的家族特异性重复序列Notch/LIN-12 repeat (LNR),可以起到阻止与配体无关的过度表达。同时,LNR的疏水性介导了Notch受体的细胞外和跨膜加细胞内亚基之间的异源二聚作用。细胞内区域包含多个保守的功能元件,包括核定位序列;RAM(RBP-J结合模块)结构域,其可参与结合下游转录因子CSL;涉及对下游信号的调节、对Notch通路起修饰作用的锚蛋白重复序列;具有反式激活作用的结构域和C末端PEST(脯氨酸/谷氨酸/丝氨酸/苏氨酸)结构域,其是Notch蛋白泛素化和降解所必需的蛋白质,确保Notch信号通路作用的持续时间[11]。 2.1.2 Notch配体 Notch信号通路的大部分是由DSL (Delta,Serrate和Lag2)配体家族诱导激发的,然而,越来越多的非规范配体也被证明可以激活Notch信号。基于与果蝇等Notch信号通路配体Delta和Serrate的同源性,哺乳动物的DSL配体被分类为Delta样(DLL1,DLL3和DLL4)或Jagged(JAG1和JAG2)。DSL配体是Ⅰ型跨膜蛋白,胞外域由N末端结构域、DSL结构域、钙结合蛋白、多个串联排列的表皮生长因子重复序列和一"


个富含半胱氨酸的结构域构成(图2)[12]。其在进化中高度保守,是激活Notch信号通路所必需的。Jagged1和Jagged2的表皮生长因子重复序列数量是Delta样配体数量的两倍,其中一些含有未知功能的保守插入[13]。有国外学者认为Jagged1和Jagged2在Delta样配体中未发现富含半胱氨酸的区域[14],与血管性血友病因子C型结构域具有部分同源性。Notch信号通路的正反馈调节机制由Notch信号配体Delta和Serrate表达实现,如果Serrate或Delta存在于一个细胞的外部,则它们可以在相邻细胞中激活Notch信号,触发细胞膜表面Notch分子的活化,然而,Delta和Serrate的表达在反式激活期间能控制Notch活性,Serrate或Delta配体存在于与Notch相同细胞的表面上,它们会将受体转移而不是激活它。这种机制决定了细胞的不同分化情况与方向[15-16]。 2.1.3 Notch信号通路的激活及主要途径 Notch信号通路的引发需通过Notch受体的胞外区域与相邻细胞上的Notch配体的结合。经典的Notch信号通常被认为是两个相邻细胞之间的短距离信号:在细胞表面表达的Notch受体的信号接收细胞和表达配体的信号发送细胞。未加工的Notch蛋白质通过分支途径转运到高尔基复合体中通过furin蛋白酶样转化酶在位点S1被蛋白水解切割产生异二聚体蛋白,后将该受体转移到细胞表面。Notch受体通过与其配体连接导致一系列蛋白水解事件。首先由去整合素金属蛋白酶(ADAM)在位点S2处切割受体以释放胞外域,其随后被配体表达细胞内吞[17]。在这种切割之后,Notch受体成为γ-分泌酶复合物的底物,并被含有早老素1/2、Nicastrin、Pen-2和Aph-1构成的γ-分泌酶复合物在S3位点切割[18],其作为一个多蛋白复合物介导多个跨膜蛋白包括淀粉样蛋白前体蛋白的切割,S3处的切割允许释放Notch的胞内域(NICD),NICD是Notch受体的活性形式,其迁移到细胞核以改变转录。在细胞核中,其RAM结构域及ANK重复序列与与下流转录因子CSL(CBF1,Su(H),LAG-1)结合,取代由RBP-J结合的共抑制因子复合物,并募集辅激活物Mastermind-Like(MAML)等相互作用,形成转录复合物,进而诱导靶基因的转录[19-20]。在哺乳动物中,最佳描述的典型的Notch靶基因是属于碱性-螺旋-环-螺旋转录因子家族的成员(YRPW基序家族的促进分支Hey和Hes),包括Hes1、Hes5和Hes7以及Hey1、Hey2和HeyL[11]。 因此,Notch信号通路被认为是“简单”的核心信号通路,原因在于没有第二信使用来参与信号转导,直接将相邻细胞接收的信号传递到细胞核,与转录因子结合激活靶细胞。与其他信号系统不同,经典的Notch信号通路激活(CSL依赖途径)不会导致信号的放大,受体在转导过程中的切割,解离和破坏是不可逆的。同时,Notch信号“等比传输”的特点,也使受调控的细胞对Notch信号的活性敏感。少数经典的Notch靶基因,如HES或HEY家族,其调控大多数的生物过程,并且部分成为了不同Notch受体旁系同源物的靶特异性的基础。然而,其他基因也可以调控这些Notch信号的直接靶基因,这可能是Notch信号通路成分与其他信号通路(Wnt/β-catenin、缺氧诱导因子1α、PI3K/AKT、核转录因子kappa B等)的直接或间接的相互作用串联实现[21]。 2.2 Notch信号通路与髓核细胞的联系 2.2.1 盘内的缺氧环境介导髓核中的Notch信号传导活性,并且该途径对于控制髓核细胞增殖至关重要 椎间盘中纤维环到髓核之间的过渡区以及髓核细胞中,缺氧诱导因子1α和缺氧诱导因子2α均具有稳定和组成型基因表达,确认内部的纤维环和髓核细胞驻存在一个缺氧的环境[22-23]。有研究提示,髓核细胞已经适应于在缺氧诱导因子1α的稳定表达中存活,这是一种对局部氧气分压起反应的转录因子。当缺氧诱导因子1α缺失时,髓核中存在大量凋亡细胞,可能是由于糖酵解减少引起的能量衰竭,而当椎间盘内氧气分压低于5%时,椎间盘内拥有最大的细胞存活率[24]。 目前国内外业界有相关报道讨论髓核细胞核如何响应低氧敏感蛋白和缺氧对椎间隙细胞退行性细胞的影响,但尚未见太多文献椎间盘内缺氧对髓核细胞再生的影响。纤维环和髓核中的细胞数量由于细胞凋亡和衰老而降低,与大多数类型的结缔组织的特征一致,椎间盘内的细胞更新缓慢,其更新取决于祖细胞进入纤维环或髓核细胞中进行终末分化的能力。实际上,在椎间盘以及软骨中,克隆增殖反应是退化的标志,而髓核祖细胞的增殖受缺氧敏感的Notch信号通路的调控。 Hiyama等[25]测量成熟大鼠和人体椎间盘组织中Notch信号表达,发现人椎间盘组织分析显示,抑制Notch信号可阻断椎间盘细胞增殖,在退化的椎间盘中Notch信号蛋白的表达增加,其中Notch-2受体的表达高于其他Notch受体的表达。然而,其表达不足以维持髓核细胞数量并保持细胞的分化状态,这可能导致随着年龄的增大,髓核细胞修复反应的能力下降,出现细胞的老化和凋亡。此外,在两种组织中,椎间盘内的缺氧状态增加了Notch1和Notch4受体的mRNA表达,Notch配体Jagged1、Jagged2的mRNA表达对两组织中的缺氧状态高度敏感,缺氧亦诱导了Notch靶基因Hes1的表达,并与NICD联合表达增加Hes1启动子活性。 国内韩小博等[26]模拟髓核低氧微环境和培养方式诱导黄韧带干细胞向髓核分化,发现通过抑制Notch通路的下游基因Twist-1的表达可促进了黄韧带干细胞向髓核样细胞分化。他们认为,缺氧激活了Notch通路,使椎间盘内祖细胞数量保持恒定。因此,从某种意义说,盘内的缺氧或者低氧环境介导调节Notch信号通路活性,从而达到增殖髓核细胞的分化条件之一。 有研究认为,缺氧激活的Notch信号涉及缺氧诱导因子1α缺氧因子和NICD之间的相互作用[27],导致抑制肌源性细胞和神经元细胞的分化。Hirose等[28]发现髓核细胞中抑制缺氧诱导因子1因子FIH-1不表达会抑制涉及参与细胞间控制和信息交互的大量分泌细胞外基质蛋白,导致几种已知的Notch信号传导途径基因的诱导,包括HES/HEY样转录因子,JAG1信号传导的激活因子等。国内尚未发现有关Notch信号通路在缺氧状态下对髓核细胞的作用及机制方面的研究,但有Notch信号通路在缺氧下对神经星形胶质细胞、小胶质细胞表达增强,介导细胞中炎症相关因子的释放,影响细胞增殖与迁移的类似报道[29-30]。 2.2.2 髓核促炎细胞因子介导Notch信号通路的表达和活化 Wang等[31]亦在人类退化的椎间盘中发现Notch信号蛋白的表达增加,其中,在退化的椎间盘中发现了Notch受体和靶基因的表达。无独有偶,他们将退化的椎间盘与非退行性的椎间盘样本相比,发现中年段退化椎间盘的髓核组织Notch2受体的表达水平升高。此外,他们在研究中发现调节髓核细胞增殖、分化和细胞命运决定有关的Notch信号通路受髓核细胞中的炎性细胞因子白细胞介素1β和肿瘤坏死因子α上调实现。当椎间盘被破坏后,疾病状态的特征之一是髓核细胞在分子水平上发生一系列分解代谢的级联事件,导致促炎细胞因子的上调,降解酶的增加,同时减少细胞外基质的合成。这种分解代谢过程被认为是由许多细胞因子介导的,包括白细胞介素1β和肿瘤坏死因子α。前者被证明是直接参与基质合成减少和使增加基质的降解,而后者则被认为与髓核凋亡、髓核组织突出和神经刺激有关[32]。 国外有研究表明,人类退化髓核中存在白细胞介素1β和肿瘤坏死因子αmRNA的表达增加[33-34]。Wang等[31]的报告认为肿瘤坏死因子α和白细胞介素1β诱导髓核细胞增加Notch1、Notch2受体、配体Jagged-2之外,髓核细胞中的细胞因子增加了下流转录因子CBF1和靶基因启动子HES1、HEY1和HEY2的活性。此外,当具有CSL结合位点的CBF1报告基因突变时,髓核细胞中的细胞因子依赖性诱导能力将被消除。Ottaviani等[35]研究白细胞介素1β治疗对Notch1/Hes1通路的影响,亦支持增加的Notch信号传导表达受细胞因子影响这一观点。 总之,这些研究说明了细胞因子增加Notch途径基因的表达,导致Notch信号传导的激活,因此,Notch信号传导可能是由于退行性椎间盘炎症细胞因子的反应而引起,并且能通过增殖恢复髓核内源细胞的机制来补偿丧失的细胞数量,Notch2受体在中年段退化髓核组织比老年段退化髓核组织表达水平提高亦提示着该信号系统的活性可能尝试进行细胞和组织上的修复。有研究认为肿瘤坏死因子α抑制剂和白细胞介素1受体拮抗剂的药物具有对椎间盘疾病的治疗作用的潜力[3],但是迄今为止相对不成功。 2.2.3 髓核细胞内的Notch通路的表达和活化可能与MAPK和核转录因子kappa B信号通路存在交互作用 此外,除了缺氧的作用,髓核细胞内细胞因子介导的Notch信号通路的表达和活化可能依赖于MAPK和核转录因子kappa B等信号的共同交互作用。Vo等[36]认为核转录因子kappa B信号通路也涉及年龄相关性椎间盘退变的机制,与无症状椎间盘相比,有症状的椎间盘具有更高水平的促炎细胞因子,其被认为是典型的核转录因子kappa B靶基因,例如肿瘤坏死因子α,白细胞介素1β,6,8等。 核转录因子kappa B的p50亚基是免疫和炎症反应的重要抑制因子[37],有研究认为p50同源二聚体的形成及其与κB基序的结合可能促进转录抑制因子HDAC1等募集到Notch2受体启动子[38],从而抑制RelA反应,目前被认为其是控制炎症中起主要作用的经典核转录因子kappa B通路的一部分。但核转录因子kappa B信号通 路如何调节Notch2受体启动子的功能仍有待进一步研究。丝裂原活化蛋白激酶(MAPK)也被认为与退行性腰椎间盘病息息相关,髓核细胞内的主要促炎细胞因子(肿瘤坏死因子α和白细胞介素1β)能激活ERK1/2或p38 MAPK信号通路,从而激活分解代谢产物如ADAMT-4,基质金属蛋白酶3或者SDC4,Mavrogonatou等[39]通过氨基葡萄糖等抑制了MAPK激活防止了分解代谢产物的产生,表明MAPK信号通路的调节机制可能会减慢椎间盘退变和衰老的进程。Wang等[31]学者的研究也提出了MAPK调节细胞因子介导大鼠髓核细胞中Notch2启动子活性的诱导。这可能是Notch信号通路与其他信号通路在髓核组织中间接的交互作用的体现。 2.3 调节Notch信号通路的传导活性进行修复退变髓核的再生治疗前景 在关节软骨细胞中,Notch信号传导通路能够调控软骨细胞增殖、分化,维持软骨细胞表型,维持软骨的基质代谢平衡,是近来被确定为软骨发育的关键调节因子[40]。曹光彪等[41]检测了Notch信号在小鼠椎间盘中的表达水平及差异,筛选出Dll-1、Jag-1这2个表达变化最显著的信号分子,而Dll-1、Jag-1对软骨细胞分化起负性调节作用。提示Notch信号通路亦能在脊柱软骨终板中通过调控软骨细胞增殖、分化的机制来营养修复退变的椎间盘。但国内仍未有报道Notch信号通路能直接修复髓核细胞的研究。 髓核是一种以松散网状结构的方式构建而成的Ⅱ型胶原蛋白和蛋白多糖的复合体,和软骨细胞之间存在一定的表型相似性,但目前已有研究指出两者之间仍然存在明显的表型差异[42]。近年来对间质充干细胞的研究广泛开展,认为间质充干细胞相对容易培养,将间质充干细胞移植到退变的椎间盘中能向类髓核细胞分化,但目前仍未有十分确凿的报道其能最终分化成髓核细胞。同时,将间质充干细胞移植到人体退变的椎间盘中,盘内营养支持移植细胞的问题仍是下一步需要继续考虑和研究的问题。营养物质的剥夺是椎间盘退变的重要因素,因此,在移植间质充干细胞的同时,增加生长因子的补充移植可以通过改善髓核细胞的营养,补充退化椎间盘已经很低的营养水平。考虑到这一点,间质充干细胞移植可能更适合作为椎间盘退变的早期介入治疗[27]。 然而,对于椎间盘内源性祖细胞的研究也在同步的进行中。祖细胞的存在已经得到验证,其与间质充干细胞的表型非常相似[43]。祖细胞进入纤维环或髓核细胞中进行终末分化的能力使这类细胞在未来很可能成为椎间盘退变生物学治疗的重要种子细胞。由髓核祖细胞表达或用于确定这些细胞在椎间盘中的定位的表面标志物包括CD24,CD29,CD44,CD49a/e/f,CD51,CD56,CD63,CD73,CD133/1,CD166,CD184,OCT3/4,Notch受体和配体,C-KIT,KI67,STRO-1,Tie2和GD2[27]。Notch信号通路对于各种组织中的祖细胞活性、增殖和命运决定是必需的,因此其相关分子用作干祖细胞标记。从上文中得知抑制Notch信号通路可阻断椎间盘细胞增殖,提示抑制了Notch通路的活性,也降低了祖细胞的含量。 因此,在对退变的椎间盘进行髓核细胞再生治疗的策略方面,可以通过操作Notch信号传导途径的特异性配体和受体以重新激活存活的内源髓核祖细胞以促进其增殖和分化。同时,Notch信号传导通路对椎体退变软骨板软骨细胞的有一定的增殖和分化作用,能促进椎间盘内细胞修复的营养支持。但是对于这类的研究,目前国外只局限于动物试验,国内亦未有相应的报道。此外,椎间盘退变是一个渐进过程,进行干预的时机仍需进一步的商榷,对髓核细胞的表型、祖细胞的表面标记物以及分化诱导的条件等认识亦需更深入的探索,但对于利用Notch信号通路的传导活性来进行退变髓核的内源性干细胞修复治疗的发展前景是较为广阔的。Notch信号通路与退变髓核细胞的研究见表1。"

| [1] Feng Y,Egan B,Wang J.Genetic Factors in Intervertebral Disc Degeneration.Genes & diseases.2016;3(3):178-185. [2] Feng C,Liu H,Yang M,et al.Disc cell senescence in intervertebral disc degeneration:Causes and molecular pathways.Cell Cycle.2016;15(13): 1674-1684.[3] Kadow T, Sowa G, Vo N,et al. Molecular Basis of Intervertebral Disc Degeneration and Herniations: What Are the Important Translational Questions?.Clin Orthop Relat Res. 2015;473(6):1903-1912.[4] Engin F, Lee B. Notching the bone: Insights into multi-functionality. Bone.2010;46(2):274-280. [5] Liu P, Ping Y, Ma M, et al. Anabolic actions of Notch on mature bone.Proc Natl Acad Sci U S A. 2016;113(15): E2152-E2161.[6] Mead TJ, Yutzey KE. Notch pathway regulation of chondrocyte differentiation and proliferation during appendicular and axial skeleton development. Proc Natl Acad of Sci U S A.2009;106(34):14420-14425.[7] Risbud MV, Schipani E, Shapiro IM. Hypoxic regulation of nucleus pulposus cell survival: from niche to Notch.Am J Pathol.2010;176(4):1577-1583.[8] Bray SJ. Notch signalling: a simple pathway becomes complex. Nature Rev Mol Cell Biol.2006;7:678-689.[9] Kopan R, Ilagan MX.The canonical Notch signaling pathway: unfolding the activation mechanism. Cell. 2009;137: 216-233.[10] Zanotti S,Smerdel-Ramoya A,Stadmeyer L,et al. Notch Inhibits Osteoblast Differentiation and Causes Osteopenia. Endocrinol.2008;149(8):3890-3899. [11] Shang Y,Smith S, Hu X. Role of Notch signaling in regulating innate immunity and inflammation in health and disease. Protein Cell.2016;7(3):159-174.[12] D’Souza B, Meloty-Kapella L, Weinmaster G. Canonical and non-canonical Notch ligands. Curr Top Dev Biol. 2010;92: 73-129 [13] D’souza B,Miyamoto A,Weinmaster G.The many facets of Notch ligands. Oncogene.2008;27(38):5148-5167. [14] Vitt UA, Hsu SY, Hsueh AJ. Evolution and classification of cystine knot-containing hormones and related extracellular signaling molecules. Mol Endocrinol.2001;15:681–694.[15] Palmer WH, Jia D, Deng WM. Cis-interactions between Notch and its ligands block ligand-independent Notch activity. Elife, 2014,3:e04415.[16] Fleming RJ, Hori K, Sen A, et al. An extracellular region of Serrate is essential for ligand-induced cis-inhibition of Notch signaling.Development.2013;140(9):2039-2049.[17] Cheng P, Gabrilovich D. Notch signaling in differentiation and function of dendritic cells.Immunol Res.2008;41(1):1-14. [18] Chen S,Lee BH,Bae Y. Notch signaling in Skeletal Stem Cells. Calcif Tissue Int.2014;94(1):68-77. [19] Wang MM. Notch signaling and Notch signaling modifiers.Int J Biochem Cell Biol. 2011;43(11):1550-1562. [20] Contreras-Cornejo H,Saucedo-Correa G,Oviedo-Boyso J,et al.The CSL proteins, versatile transcription factors and context dependent corepressors of the Notch signaling pathway.Cell Div.2016;11(1):12. [21] Geisler F,Strazzabosco M.Emerging roles of Notch signaling in liver disease. Hepatology.2015;61(1):382-392. [22] Chen S, Fang XQ, Wang Q, et al.PHD/HIF-1 upregulates CA12 to protect against degenerative disc disease: a human sample, in vitro and ex vivo study.Lab Invest. 2016;96(5): 561-569. [23] Yang SH, Hu MH, Sun YH, et al. Differential phenotypic behaviors of human degenerative nucleus pulposus cells under normoxic and hypoxic conditions:influence of oxygen concentration during isolation, expansion, and cultivation. Spine J.2013;13(11):1590-1596. [24] Risbud MV, Schipani E, Shapiro IM. Hypoxic Regulation of Nucleus Pulposus Cell Survival: From Niche to Notch.Am J Pathol.2010;176(4):1577-1583.[25] Hiyama A,Skubutyte R,Markova D,et al.Hypoxia Activates the Notch Signaling Pathway in Cells of the Intervertebral Disc: Implications in Degenerative Disc Disease.Arthritis and rheum. 2011;63(5):1355-1364. [26] Han XB,Zhang YL,Li HY, et al.Differentiation of human ligamentum flavum stem cells toward nucleus pulposus-like cells induced by coculture system and hypoxia.Spine. 2015; 40(12):E665.[27] Choi H, Johnson ZI, Risbud MV. Understanding nucleus pulposus cell phenotype: A prerequisite for stem cell based therapies to treat intervertebral disc degeneration.Curr stem cell res ther.2015;10(4):307-316.[28] Hirose Y,Johnson ZI,Schoepflin ZR,et al. FIH-1-Mint3 Axis Does Not Control HIF-1α Transcriptional Activity in Nucleus Pulposus Cells.J Biol Chem.2014;289(30):20594-20605.[29] 何坤. Notch-1信号通路在缺氧下对星形胶质细胞增殖和活化的影响及作用机制[D].济南:山东大学,2016.[30] 姚琳丽. Notch信号通路对小胶质细胞激活的作用及机制研究[D].济南:山东大学,2016.[31] Wang H, Tian Y, Wang J, et al.Inflammatory Cytokines Induce Notch Signaling in Nucleus Pulposus Cells: IMPLICATIONS IN INTERVERTEBRAL DISC DEGENERATION.J Biol Chem. 2013;288(23):16761-16774. [32] Risbud MV,Shapiro IM.Role of Cytokines in Intervertebral Disc Degeneration: Pain and Disc-content.Nat Rev Rheumatol. 2014;10(1):44-56.[33] Molinos M,Almeida CR,Caldeira J,et al.Inflammation in intervertebral disc degeneration and regeneration.J R Soc Interface.2015;12(104):20141191.[34] Johnson ZI,Schoepflin ZR,Choi H,et al. Disc in Flames: Roles of TNF-α and IL-1β in Intervertebral Disc Degeneration.Eur Cell Mater.2015;30:104-117.[35] Ottaviani S, Tahiri K, Frazier A, et al. Hes1, a new target for interleukin 1beta in chondrocytes. Ann Rheum Dis. 2010; 69(8):1488-1494. [36] Vo NV,Hartman RA, Patil PR, et al. Molecular Mechanisms of Biological Aging in Intervertebral Discs. J orthop res. 2016; 34(8):1289-1306.[37] Quan M,Park SE,Lin Z,et al.Steroid treatment can inhibit nuclear localization of members of the NF-κB pathway in human disc cells stimulated with TNF-α.Eur J Orthop Surg Traumatol. 2015;25(1):S43-51.[38] Elsharkawy AM, Oakley F, Lin F, et al.The NF-κB p50:p50:HDAC-1 repressor complex orchestrates transcriptional inhibition of multiple pro-inflammatory genes.J Hepatol.2010;53(3-2):519-527.[39] Mavrogonatou E,Angelopoulou MT,Kletsas D.The catabolic effect of TNF-α on bovine nucleus pulposus intervertebral disc cells and the restraining role of glucosamine sulfate in the TNF-α-mediated up-regulation of MMP-3.J Orthop Res. 2014;32(12):1701-1707. [40] Mirando AJ,Liu Z,Moore T,et al.RBPjκ-dependent Notch signaling is required for articular cartilage and joint maintenance.Arthritis Rheum.2013;65(10):2623-2633. [41] 曹光彪,李明,何通川,等. Notch信号通路相关分子在脊椎生长过程中的差异表达及其对软骨细胞分化的调控作用[J].中国生物制品学杂志,2013,(08):1094-1099.[42] Pattappa G,Li Z,Peroglio M,et al. Diversity of intervertebral disc cells: phenotype and function. J Anat. 2012;221(6): 480-496. [43] Blanco JF,Graciani IF,Sanchez-Guijo FM,et al.Isolation and characterization of mesenchymal stromal cells from human degenerated nucleus pulposus: comparison with bone marrow mesenchymal stromal cells from the same subjects. Spine.2010;35(26):2259-2265.[44] Risbud MV, Shapiro IM. Notochordal Cells in the Adult Intervertebral Disc: New Perspective on an Old Question. Crit Rev Eukaryot Gene Expr. 2011;21(1):29-41. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [11] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [12] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [13] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [14] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| [15] | Liu Liyong, Zhou Lei. Research and development status and development trend of hydrogel in tissue engineering based on patent information [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3527-3533. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||