Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (5): 793-800.doi: 10.3969/j.issn.2095-4344.0453
Previous Articles Next Articles
Human Wharton’s Jelly-derived mesenchymal stem cells: advances and prospects in directional differentiation
Shi Qin, Yang Xiao-qing, Zhang Yu-quan
- Department of Obstetrics and Gynecology, Affiliated Hospital of Nantong University, Nantong 226001, Jiangsu Province, China
-
Revised:2017-09-12Online:2018-02-18Published:2018-02-18 -
Contact:Zhang Yu-quan, Ph.D., Chief physician, Department of Obstetrics and Gynecology, Affiliated Hospital of Nantong University, Nantong 226001, Jiangsu Province, China -
About author:Shi Qin, Studying for master’s degree, Department of Obstetrics and Gynecology, Affiliated Hospital of Nantong University, Nantong 226001, Jiangsu Province, China -
Supported by:the National Natural Science Foundation of China, No. 81370677
CLC Number:
Cite this article
Shi Qin, Yang Xiao-qing, Zhang Yu-quan. Human Wharton’s Jelly-derived mesenchymal stem cells: advances and prospects in directional differentiation[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(5): 793-800.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
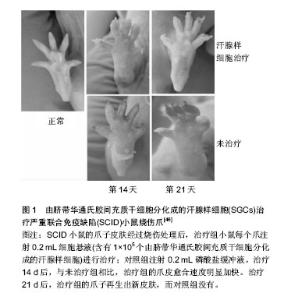
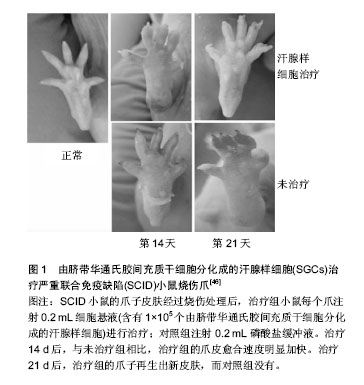
2.1 WJ-MSCs分化为成骨细胞 早在2003年,Romanov等就首次从脐带华通氏胶中分离出间充质干细胞,并验证了其具有成骨分化能力。在这之后的10多年来,许多学者对于诱导分化的方法进行了改进。在WJ-MSCs成骨分化的研究中,越来越多的实验证明,利用特定的成骨诱导培养基(含体积分数为10%胎牛血清,10 nmol/L地塞米松,10 mmol/L β-甘油磷酸钠以及50 mg/L抗坏血酸的DMEM/F12培养基)能够诱导WJ-MSCs向成骨细胞分化。碱性磷酸酶是目前较为肯定的参与钙化的酶类,它与骨钙素基因一起,被认为是鉴定细胞成骨分化能力的可靠指标。Li等[5]于2016年取第3代WJ-MSCs种于培养板内,并加入上述成骨诱导培养基,持续诱导21 d后发现,与未诱导的对照组相比,诱导组干细胞的碱性磷酸酶活性从第5天开始升高,诱导第9天达到高峰,之后一直维持在较高水平,同时,在诱导过程中,骨钙素基因的表达也持续升高,当使用抑制剂阻断WJ-MSCs中的ERK信号通路后,上述成骨分化指标明显降低。研究结果提示WJ-MSCs在一定的诱导条件下具有定向分化为成骨细胞的能力,且ERK信号通路在WJ-MSCs的成骨分化过程中发挥了重要作用。该结果加强了人们对WJ-MSCs成骨分化特性的理解。通过激活上述信号通路诱导WJ-MSCs分化,将为组织工程骨的生产创造有利条件。 2014年,曾庆慧等[6]采用高浓度胶原的液晶态制备出一种表面具有类液晶有序结构的胶原膜。将WJ-MSCs种植于上述胶原膜表面,辅以成骨诱导培养基培养,能够促进干细胞的成骨分化。在同一年,Chang等[7]发现了一种高效且高产出的WJ-MSCs培养方法,他们用特制的放有重复培养架的培养皿可以实现华通氏胶的重复利用,所获得的细胞相较于用传统分离方法多15-20倍,且细胞的成骨能力不受影响。这在一定程度上解决了干细胞用于批量生产组织工程骨时数量不足的问题。需要注意的是,虽然用上述方法培养得到的不同批次的干细胞具有一致的成骨分化潜能,但其成脂及成软骨能力是否稳定尚未得到充分验证,需要进一步的实验观察。 周建等[8]在2015年的研究发现,在使用成骨诱导培养基的基础上,如果提前采用频率为50 Hz、强度为1.8 mT的正弦交变电磁场处理干细胞2.5 h,能够显著增强WJ-MSCs成骨分化的效率。 2.2 WJ-MSCs分化为软骨细胞 2012年,De等[9]首次将WJ-MSCs诱导分化为软骨细胞。他们首先将WJ-MSCs接种于96孔板内,然后加入含有体积分数为10%胎牛血清、1%青霉素和链霉素、1.5×10-4 mol/L单硫代甘油、5g/L抗坏血酸和6 mg/L转铁蛋白的DMEM培养基培养,以促进干细胞自发呈球状排列,接着更换成软骨基质培养基(在DMEM中加入体积分数为15% knockout血清、5 g/L抗坏血酸、6 mg/L转铁蛋白、10 μmol/L地塞米松、1×10-7 mol/L视黄酸和1 μg/L重组人转化生长因子β3),持续诱导46 d,隔3 d换液,分别在诱导的第0,4,7,14,28,46天检测干细胞表达的软骨相关蛋白量。结果显示,干细胞能够通过上述方法被诱导为分泌软骨细胞外基质蛋白的软骨样细胞。通过这种方法,有望实现体外构建各种基于细胞移植和组织工程研究的软骨生成模型,这对于许多风湿性疾病的体外研究具有重要价值。 2014年,国内学者罗二梅等[10]探索了另一种诱导方法,他们利用孔径≤3.0 μm的Transwell膜和Transwell小室将WJ-MSCs与兔膝关节软骨细胞共培养21 d,结果发现共培养组WJ-MSCs分泌的软骨细胞外基质蛋白GAG和COL2A1及相应的mRNA表达明显增多,且当WJ-MSCs与兔膝关节软骨细胞的共培养比例为1∶4时分化效果最佳。这说明WJ-MSCs在该种共培养体系中能够分化为软骨细胞,但其具体的机制还有待进一步研究。 2.3 WJ-MSCs分化为脂肪细胞 近5年来,国内外有多篇在体外成功将WJ-MSCs诱导分化为脂肪细胞的报道,但这些研究中所采用的诱导液却不尽相同。杨雯等[11]采用的诱导液为含有1 μmol/L地塞米松、5 μmol/L胰岛素、0.5 μmol/L吲哚美辛、0.5 μmol/L IBMX、体积分数为15%胎牛血清的α-MEM培养液;Mennan等[12]采用的诱导液为含有体积分数为10%胎牛血清、1%胰岛素、0.5 μmol/L IBMX、1 μmol/L地塞米松和100 μmol/L吲哚美辛的DMEM/F12培养基;余永春等[13]采用的诱导液为含有1 μmol/L地塞米松、0.5 mmol/L IBMX、5 mg/L胰岛素和0.2 mmol/L吲哚美辛的混合液。 2014年,Saben等[14]比较了3种成脂培养液诱导WJ-MSCs成脂分化的效果:分别在含有体积分数为10%胎牛血清、1%抗生素和抗真菌剂、1 μmol/L地塞米松、500 μmol/L IBMX的DMEM中加入1 μmol/L胰岛素(MDI);60 μmol/L吲哚美辛(MDI-I);10 μmol/L罗格列酮(MDI-R)。然后用这3种培养基持续诱导干细胞35 d,隔3 d换液。结果发现,加入吲哚美辛(MDI-I)的培养基诱导干细胞成脂分化的作用最强。同时也指出,用上述培养基长时间培养(5周以上)会使干细胞出现胰岛素抵抗,其成脂分化能力随之降低。 2.4 WJ-MSCs分化为神经细胞 2.4.1 WJ-MSCs分化为神经元细胞 早在2003年,Mitchell等就首次成功地诱导WJ-MSCs分化为神经元细胞。在这之后的14年间,有关WJ-MSCs向神经系统细胞分化的研究一直是干细胞研究领域的热点[15]。起初,人们采用诱导骨髓间充质干细胞的方法诱导WJ-MSCs,结果显示含有二甲基硫氧化物(DMSO)的诱导液也能够诱导WJ-MSCs分化为神经元细胞。由于DMSO具有较高的细胞毒性,人们尝试探索了许多新的诱导方法,在近5年内,也不乏有许多新成果。2012年,Cho等[16]采用亚音速振动刺激诱导WJ-MSCs,使其形态发生类似于神经元细胞的改变。同时,神经元特异性标记物(包括MAP-2,NF-L和NeuroD1)以及其他神经细胞标志物,如GFAP和O4的表达均有所增加。他们的研究表明亚音速振动能够非选择性诱导WJ-MSCs分化成神经元样细胞,并且这一过程与ERK信号通路存在密切联系。有学者发现,WJ-MSCs在一定时间内分化为神经元样细胞时高度依赖视黄酸的浓度[17]。在其他条件不变的情况下,当应用10-4 mol/L浓度的视黄酸时,超过一半的细胞分化,但是在10-6 mol/L浓度下分化的细胞相对减少。2015年,Nan等[18]采用单睾酮己糖神经节苷脂(GM1)诱导WJ-MSCs,通过免疫组织化学方法检测神经细胞标志物:微管相关蛋白2(MAP-2)、神经丝蛋白(NF-H)和胶质纤维酸性蛋白(GFAP)的表达水平。结果发现,用单睾酮己糖神经节苷脂处理6 h后,WJ-MSCs出现了类似神经元样细胞的椭圆形细胞体和神经突,并且表达神经细胞标志物MAP-2和NF-H,不表达GFAP。该研究表明单睾酮己糖神经节苷脂能够有效地在体外诱导WJ-MSCs分化成神经元样细胞,但是单睾酮己糖神经节苷脂是否可以在体内发挥相同作用,需要进一步研究。 在国内,还有多位学者发现了能够促进WJ-MSCs分化为神经元细胞的物质,其中包括虎杖苷联合生长因子[19]、抗脑衰胶囊含药血清[20]、整合素连接激酶等[21]。2015年,祝加学等[22]尝试了诱导分化的新方法:将WJ-MSCs通过Transwell小室与SD乳鼠许旺细胞共培养2周,部分间充质干细胞出现类似神经元的形态,并表达nestin、NF-200、β-Ⅲ-tubulin等神经元特异性标记物,不表达许旺细胞特异性表记物S100和胶质细胞特异性标记物MAB1580。 2.4.2 WJ-MSCs分化为具有特定功能的神经细胞 2013年,Li等[23]研究首次发现,将表达HGF的腺病毒载体(Ad-HGF)转导到体外培养的WJ-MSCs中,WJ-MSCs可分化为分泌多巴胺、酪氨酸羟化酶和多巴胺转运蛋白的多巴胺能神经元样细胞。为了提高诱导的成功率,2015年,Ko等[24]探索了他们认为更加有效的方法:利用音猬因子、成纤维细胞生长因子8和神经元条件培养基诱导过表达Nurr1的WJ-MSCs,分化成功率约71%。将这种细胞移植到帕金森病大鼠纹状体中,能够改善其行为缺陷,且移植后的细胞能够存活3个月以上。这为基于WJ-MSCs的帕金森病治疗打下了基础。 2012年,Zhang等[25]研究首次发现,由脑源性神经营养因子和低血清培养基组成的神经元诱导培养基(NIM),辅以海马胆碱能神经刺激肽(HCNP)或大鼠去神经化的海马提取物(rDHE),能够诱导WJ-MSCs分化为胆碱乙酰转移酶阳性细胞,并通过实验证实分化后的细胞能够分泌乙酰胆碱。这些结果表明WJ-MSCs有望用于细胞移植以治疗阿尔茨海默病。 2016年,Bagher等[26]研究发现,利用聚己内酯(PCL)/胶原支架能为WJ-MSCs分化为运动神经元样细胞提供合适的三维环境。他们分别在mRNA和蛋白质水平检测干细胞表面运动神经元样细胞标志物的表达,结果证明该纳米结构支架有利于WJ-MSCs向运动神经元样细胞分化,对于神经再生具有潜在应用价值。 2.5 WJ-MSCs分化为肝细胞样细胞 从2008年,Campard等首次发现WJ-MSCs能够分化为肝细胞样细胞以来,相关的诱导方法逐渐成熟。目前的研究表明,利用小鼠胚胎肝条件性培养基(mouse fetal liver-conditioned medium,FLCM)能够诱导WJ-MSCs分化成肝细胞样细胞[27]。具体诱导方法为:取妊娠13.5 d小鼠的胚胎肝脏,在PBS中切成小于1 mm3的小块,用3 g/L Ⅰ型胶原酶在37 ℃下消化40-60 min后,在培养皿中加入6 mL含有体积分数为10%胎牛血清的DMEM,并在37 ℃、体积分数为5%CO2下培养48 h。收集上清液并使用0.25 mm过滤器过滤,得到的滤液即为小鼠胚胎肝条件性培养基。取第3代WJ-MSCs,接种于培养板内,加入小鼠胚胎肝条件性培养基诱导,可成功将WJ-MSCs诱导分化成肝细胞样细胞。同样,Yan等[28]在利用上述方法诱导干细胞后也发现,当小鼠胚胎肝条件性培养基处理后,间充质干细胞特异性标志物的表达降低,而肝细胞特异性基因表达增加,尿素生成、白蛋白分泌、糖原贮积均增多,细胞色素P450 3A4(CYP3A4)活性显著增强,此外,ERK1/2的磷酸化过程通过Raf/MEK/ERK途径随着时间进行性增加,在诱导过程中维持在高水平,而通过U0126(ERK1/2抑制剂)和K71R(ERK1的阴性突变体)抑制ERK1/2信号通路激活后,能够阻碍WJ-MSCs中肝特异性基因的表达,并显著影响细胞的相关功能。这些结果进一步阐明了WJ-MSCs分化为肝细胞过程中的相关分子机制。2015年,国内学者闫成等[29]、钟艳等[30]研究发现,肝纤维化大鼠肝组织匀浆上清液和肝衰竭大鼠血清均能够使WJ-MSCs向肝样细胞分化,具体机制有待进一步研究。 2.6 WJ-MSCs分化为胰岛素生成细胞 2013年,Qu等[31]研究首次发现,层粘连蛋白411通过Pdx1和Ngn3信号通路能有效诱导WJ-MSCs分化为胰岛素生成细胞。此外,通过体内实验证实,层粘连蛋白411诱导的胰岛素生成细胞能明显改善1型糖尿病大鼠的症状和存活率。这些新发现提示了层粘连蛋白411诱导的胰岛素生成细胞在1型糖尿病治疗中的潜在临床应用价值,相关机制有待进一步研究。具体诱导方法如下:取第4代WJ-MSCs置于培养板内,加入含有5 mg/L层粘连蛋白411和25 mmol/L葡萄糖的完全培养基培养。随后换成含有胰岛素转运蛋白硒的DMEM/F12培养基培养4 d。接着在上述培养基中加入10 mmol/L烟酰胺,持续培养3 d。最后再加入N2和B27补充剂继续培养4 d,得到成熟的胰岛素生成细胞。 2014年,陈燕等[32]、柴树宏等[33]也成功地在体外微环境下将WJ-MSCs诱导分化为胰岛素分泌细胞。前者先后予以1 mmol/L 2-巯基乙醇培养2 d,10 μg/L表皮生长因子、10 μg/L碱性成纤维细胞生长因子及2% B27培养7 d,之后添加20 mmol/L尼克酰胺及艾塞那肽培养7 d对WJ-MSCs进行诱导分化。后者在无血清培养液中添加尼克酰胺、活化素A、肠促胰岛素类似物4、肝脏生长因子、胃泌素对WJ-MSCs进行诱导分化,结果显示分化后的细胞能够分泌胰岛素,并且具有良好的增殖活性,是通过细胞移植治疗糖尿病的良好细胞来源。 2.7 WJ-MSCs分化为心肌细胞 2009年,Wu等研究首次发现WJ-MSCs能够在体外和体内分化为心肌细胞样细胞。近年来人们对于WJ-MSCs分化为心肌细胞的相关分子机制进行了探索。2012年,Qian等[34]将第2代WJ-MSCs加入含有体积分数为10%胎牛血清和10 mmol/L 5-氮杂胞苷的LG-DMEM培养基,诱导24 h后,撤除5-氮杂胞苷,更换为含有体积分数为10%胎牛血清的新鲜LG-DMEM培养基继续培养2周后,WJ-MSCs可表现出心肌细胞表型。并且,ERK通路的特异性抑制剂U0126可以抑制5-氮杂胞苷诱导的WJ-MSCs心脏特异性基因和蛋白质的表达。2015年,Zhu等[35]继续对其诱导分化的信号通路进行了探讨,结果发现,DLL4-Notch信号通路也可能参与了5-氮杂胞苷诱导干细胞分化的过程。2016年,Ruan等[36]研究表明,过表达Nkx2.5基因能明显增加干细胞心脏相关基因cTnI、Desmin、GATA-4的表达,促进WJ-MSCs分化为心肌细胞,相关机制有待进一步研究。同年,Jiang等[37]改进了之前的诱导方法,他们利用生物活性脂质鞘氨醇-1-磷酸(S1P)及5-氮杂胞苷组成的条件培养基诱导WJ-MSCs。结果显示合适的分化时间为14 d,并且S1P的最佳浓度为0.5 μmol/L,此外,S1P和心肌细胞培养基联合作用,能够使干细胞产生钙瞬变,而钙瞬变是这些分化后的细胞在体内起作用的特异性电生理特性之一,S1P不仅能够促进WJ-MSCs在心肌细胞培养基中分化为功能性心肌细胞,而且能与5-氮杂胞苷产生协同作用。如何使这两者达到最佳的组合,相关条件还需要进一步摸索。国内学者何万里等[38]研究发现,WJ-MSCs经缬沙坦诱导后培养1-3周,细胞明显变小呈短梭形且不规则排列,免疫细胞化学和免疫荧光结果显示,有心肌特异蛋白cTnI和心肌相关转录因子GATA4蛋白表达。RT-PCR结果显示,WJ-MSCs自发的、持续性表达心肌相关转录因子Tbx5、GATA4和Nkx2.5的mRNA,经缬沙坦诱导1周时其mRNA表达水平略有上升,随后逐渐下降。cTnI的mRNA在诱导第3周时出现,未见心肌发育相关基因心房利钠肽(ANP)和β-心肌肌球蛋白重链(β-MHC)的mRNA表达,结果表明,WJ-MSCs具有心肌分化潜能但无法自发分化;缬沙坦具有诱导WJ-MSCs向心肌样细胞分化的能力。 2.8 WJ-MSCs分化为上皮样细胞 近年来,出现了WJ-MSCs向前列腺上皮样细胞[39]、口腔黏膜和皮肤上皮样细胞[40]、角膜上皮样细胞[41]、视网膜色素上皮样细胞分化的研究[42],开拓了WJ-MSCs定向分化的新领域。 Li等[39]将WJ-MSCs与大鼠泌尿生殖器窦基质细胞(rUGSS)共同移植到裸鼠肾小囊内,移植2个月后,WJ-MSCs能够表达前列腺特异性抗原(PSA),在裸鼠体内形成半透明上皮样腺体结构,与正常的前列腺上皮腺泡类似,这些发现证明了WJ-MSCs具有分化为通常源自内胚层的上皮样细胞的能力,表明其在组织修复和许多内胚层衍生的内脏器官的再生中具有的潜在应用价值。Garzón等[40]发明了三维生物活性系统,配合特定的上皮细胞培养基,先后将WJ-MSCs诱导分化为多层口腔黏膜和皮肤上皮细胞[40]、角膜上皮样细胞[41]。这些成果为口腔皮肤黏膜和角膜组织再生提供了新的细胞来源。国内王丽等[42]采用慢病毒包装系统获得分别含有11个转录因子Sox2、Pax6、Rax、Six6、Nr2e1、Otx2、Lhx2、Crx、Mitf-A、Klf4和c-Myc的病毒,并通过感染WJ-MSCs来诱导WJ-MSCs向视网膜色素上皮细胞样细胞分化。结果显示视网膜及视网膜色素上皮细胞发育相关的关键转录因子能够将WJ-MSCs直接转分化为视网膜色素上皮细胞样细胞,并表达ZO-1、RPE65、Bestrophin-1(Best-1)、CK8/18、Cralbp、Mertk、Tyrosinase(Tyr)、PEDF等视网膜色素上皮细胞的特征分子,从而为细胞移植治疗视网膜变性疾病带来了新的希望。 2.9 其他 2013年,Li等[43]研究首次发现,由取自SD大鼠下臼齿的牙胚细胞制成的条件培养基(TGC-CM)诱导第3代WJ-MSCs,其碱性磷酸酶水平显著增高,并伴有矿化结节的生成。反转录聚合酶链式反应结果表明诱导后的干细胞高表达牙本质唾液酸蛋白(DSPP)和牙本质基质蛋白1(DMP1)基因。此外,在免疫荧光分析中,检测出高水平的牙本质涎蛋白(DSP)和牙本质基质蛋白1(DMP1)。这些结果表明TGC-CM可以使WJ-MSCs向成牙质细胞样细胞分化,为牙齿再生提供了一种新的策略。对于其分化过程中涉及的分子机制还有待进一步研究。在同一年,Yuan等[44]收集第1-5代膀胱平滑肌细胞培养液上清,与完全培养基以1︰1比例混合,配制成条件培养液可诱导WJ-MSCs定向分化为膀胱平滑肌细胞。据此,WJ-MSCs有望成为修复和重建泌尿系统的种子细胞。Devarajan等[45]将含有Atoh1基因的腺病毒转染到WJ-MSCs中,使干细胞诱导分化为与内耳毛细胞形态和免疫细胞化学特征类似的细胞。这项研究首次证实了WJ-MSCs作为再生内耳毛细胞来源的潜力,为利用组织工程和细胞移植治疗听力损伤提供了新方法。 2016年,Xu等[46]利用含有重组人角质形成细胞生长因子的条件培养基(DMEM中加入体积分数为10%胎牛血清、100 U/mL青霉素、100 g/L链霉素、2 mmol/L L-谷氨酰胺、10 mL/L胰岛素转移亚硒酸钠溶液、2 μmol/L三碘甲腺原氨酸T3、0.4 g/L半琥珀酸氢化可的松、10 μg/L重组人表皮生长因子、40 μg/L重组人角质形成细胞生长因子),诱导WJ-MSCs 3周后可分化成汗腺样细胞,并证明了WJ-MSCs分化的汗腺样细胞可以在小鼠烧伤模型中再生出功能性的汗腺。该研究表明,WJ-MSCs能够通过再生被破坏的汗腺以治疗皮肤损伤,见图1。"
| [1] de Girolamo L, Lucarelli E, Alessandri G, et al. Mesenchymal stem/stromal cells: a new ''cells as drugs'' paradigm. Efficacy and critical aspects in cell therapy. Curr Pharm Des. 2013; 19(13):2459-2473.[2] Castro-Manrreza ME, Montesinos JJ. Immunoregulation by mesenchymal stem cells: biological aspects and clinical applications. J Immunol Res. 2015;2015:394917.[3] Roson-Burgo B, Sanchez-Guijo F, Del Cañizo C, et al. Insights into the human mesenchymal stromal/stem cell identity through integrative transcriptomic profiling. BMC Genomics. 2016;17(1):944.[4] Watson N, Divers R, Kedar R, et al. Discarded Wharton jelly of the human umbilical cord: a viable source for mesenchymal stromal cells. Cytotherapy. 2015;17(1):18-24.[5] Li CS, Zheng Z, Su XX, et al. Activation of the Extracellular Signal-Regulated Kinase Signaling Is Critical for Human Umbilical Cord Mesenchymal Stem Cell Osteogenic Differentiation. Biomed Res Int. 2016;2016:3764372.[6] 曾庆慧,李娜,田冶,等.Ⅰ型胶原膜的类液晶结构对人脐带间充质干细胞黏附、增殖和分化性能的影响[J].高等学校化学学报, 2014, 35(8):1658-1664.[7] Chang Z, Hou T, Xing J, et al. Umbilical cord Wharton's jelly repeated culture system: a new device and method for obtaining abundant mesenchymal stem cells for bone tissue engineering. PLoS One. 2014;9(10):e110764.[8] 周建,马小妮,陈克明,等.电磁场不同处理时间对人脐带间充质干细胞增殖与分化的影响[J].解放军医药杂志, 2015,27(3): 11-15.[9] De la Fuente A, Mateos J, Lesende-Rodríguez I, et al. Proteome analysis during chondrocyte differentiation in a new chondrogenesis model using human umbilical cord stroma mesenchymal stem cells. Mol Cell Proteomics. 2012;11(2): M111.010496.[10] 罗二梅,张家文,胡笑轲,等.共培养人脐带间充质干细胞(hUC-MSCs)和兔关节软骨细胞诱导hUC-MSCs分化成软骨细胞[J].基础医学与临床, 2014, 34(1):82-87.[11] 杨雯,惠玲,吕同德,等.人脐带间充质干细胞的成脂诱导分化及其相关基因鉴定[J].现代生物医学进展, 2014, 14(11):2043-2046.[12] Mennan C, Wright K, Bhattacharjee A, et al. Isolation and characterisation of mesenchymal stem cells from different regions of the human umbilical cord. Biomed Res Int. 2013; 2013:916136.[13] 余永春,孙洁,王伟新,等.脐带间充质干细胞成脂分化的研究[J]. 现代生物医学进展, 2015,15(24):4624-4626.[14] Saben J, Thakali KM, Lindsey FE, et al. Distinct adipogenic differentiation phenotypes of human umbilical cord mesenchymal cells dependent on adipogenic conditions. Exp Biol Med (Maywood). 2014;239(10):1340-1351. [15] Frausin S, Viventi S, Verga Falzacappa L, et al. Wharton's jelly derived mesenchymal stromal cells: Biological properties, induction of neuronal phenotype and current applications in neurodegeneration research.Acta Histochem. 2015;117(4-5): 329-338.[16] Cho H, Seo YK, Jeon S, et al. Neural differentiation of umbilical cord mesenchymal stem cells by sub-sonic vibration. Life Sci. 2012;90(15-16):591-599.[17] Eftekhar-Vaghefi SH, Zahmatkesh L, Salehinejad P, et al. Evaluation of neurogenic potential of human umbilical cord mesenchymal cells; a time- and concentration-dependent manner. Iran Biomed J. 2015;19(2):82-90.[18] Nan C, Shi Y, Zhao Z, et al. Monosialoteterahexosyl ganglioside induces the differentiation of human umbilical cord-derived mesenchymal stem cells into neuron-like cells. Int J Mol Med. 2015;36(4):1057-1062.[19] 阮玲娟,崔戈,顾旭东,等.虎杖苷联合生长因子诱导人脐带间充质干细胞向神经元样细胞分化的研究[J].中华中医药杂志, 2015, 30(1):284-287.[20] 王宪英,王梅.抗脑衰胶囊含药血清诱导人脐带间充质干细胞分化为神经元样细胞的作用[J].临床合理用药杂志, 2015,8(32): 45-46.[21] 周剑云,孙炜,张新,等.整合素连接激酶对脐带间充质干细胞向神经干细胞样细胞分化的作用[J].中国康复理论与实践, 2014, 20(11):1022-1027.[22] 祝加学,陶海荣,沈尊理.人脐带间充质干细胞与乳鼠许旺细胞共培养向类神经元样细胞的分化[J].中国组织工程研究, 2014, 18(45):7250-7254.[23] Li JF, Yin HL, Shuboy A, et al. Differentiation of hUC-MSC into dopaminergic-like cells after transduction with hepatocyte growth factor. Mol Cell Biochem. 2013;381(1-2): 183-190.[24] Ko TL, Fu YY, Shih YH, et al. A high-efficiency induction of dopaminergic cells from human umbilical mesenchymal stem cells for the treatment of hemiparkinsonian rats. Cell Transplant. 2015;24(11):2251-2262.[25] Zhang L, Tan X, Dong C, et al. In vitro differentiation of human umbilical cord mesenchymal stem cells (hUCMSCs), derived from Wharton's jelly, into choline acetyltransferase (ChAT)-positive cells. Int J Dev Neurosci. 2012;30(6):471- 477.[26] Bagher Z, Azami M, Ebrahimi-Barough S, et al. Differentiation of Wharton's Jelly-Derived Mesenchymal Stem Cells into Motor Neuron-Like Cells on Three-Dimensional Collagen-Grafted Nanofibers. Mol Neurobiol. 2016;53(4): 2397-2408.[27] Pan RL, Chen Y, Xiang LX, et al. Fetal liver-conditioned medium induces hepatic specification from mouse bone marrow mesenchymal stromal cells: a novel strategy for hepatic transdifferentiation. Cytotherapy. 2008;10(7): 668-675.[28] Yan Y, Zhu Y, Sun F, et al. Extracellular regulated protein kinases 1/2 phosphorylation is required for hepatic differentiation of human umbilical cord-derived mesenchymal stem cells. Exp Biol Med (Maywood). 2015;240(4):534-545.[29] 闫成,薛改,吴丽颖,等.两种肝组织匀浆上清液诱导人脐带间充质干细胞向肝细胞分化的比较[J].中国组织工程研究, 2015, 19(19):2993-2998.[30] 钟艳,唐晓鹏.肝损伤大鼠血清诱导培养脐带间充质干细胞向肝样细胞的分化[J].中国组织工程研究, 2015,19(23):3644- 3651.[31] Qu H, Liu X, Ni Y, et al. Laminin 411 acts as a potent inducer of umbilical cord mesenchymal stem cell differentiation into insulin-producing cells. J Transl Med. 2014;12:135.[32] 陈燕,汪珊珊,刘尚全,等.体外诱导人脐带间充质干细胞向胰岛素分泌细胞分化[J].安徽医药, 2014, 18(1):63-66.[33] 柴树宏,鲍艳春.人脐带间充质干细胞向胰岛素分泌细胞分化的研究[J].实用医学杂志, 2014,30(23):3752-3754.[34] Qian Q, Qian H, Zhang X, et al. 5-Azacytidine induces cardiac differentiation of human umbilical cord-derived mesenchymal stem cells by activating extracellular regulated kinase. Stem Cells Dev. 2012;21(1):67-75.[35] Zhu L, Ruan Z, Yin Y, et al. Expression and significance of DLL4--Notch signaling pathway in the differentiation of human umbilical cord derived mesenchymal stem cells into cardiomyocytes induced by 5-azacytidine. Cell Biochem Biophys. 2015;71(1):249-253.[36] Ruan Z, Zhu L, Yin Y, et al. Overexpressing NKx2.5 increases the differentiation of human umbilical cord drived mesenchymal stem cells into cardiomyocyte-like cells. Biomed Pharmacother. 2016;78:110-115.[37] Jiang L, Wang Y, Pan F, et al. Synergistic effect of bioactive lipid and condition medium on cardiac differentiation of human mesenchymal stem cells from different tissues. Cell Biochem Funct. 2016;34(3):163-172.[38] 何万里,李永海,杨军政,等.缬沙坦诱导人脐带间充质干细胞向心肌样细胞分化[J].解剖学报, 2014,45(6):841-846.[39] Li W, Ye B, Cai XY, et al. Differentiation of human umbilical cord mesenchymal stem cells into prostate-like epithelial cells in vivo. PLoS One. 2014;9(7):e102657.[40] Garzón I, Miyake J, González-Andrades M, et al. Wharton's jelly stem cells: a novel cell source for oral mucosa and skin epithelia regeneration. Stem Cells Transl Med. 2013;2(8): 625-632.[41] Garzón I, Martín-Piedra MA, Alfonso-Rodríguez C, et al. Generation of a biomimetic human artificial cornea model using Wharton's jelly mesenchymal stem cells. Invest Ophthalmol Vis Sci. 2014;55(7):4073-4083.[42] 王丽,范文斌,吕立夏,等.转录因子诱导人脐带间充质干细胞转分化为视网膜色素上皮样细胞的研究[J].同济大学学报:医学版, 2015,36(5):1-7.[43] Li TX, Yuan J, Chen Y, et al. Differentiation of mesenchymal stem cells from human umbilical cord tissue into odontoblast-like cells using the conditioned medium of tooth germ cells in vitro. Biomed Res Int. 2013;2013:218543.[44] Yuan H, Liu L, Zheng S, et al. Experimental study of differentiation of umbilical cord mesenchymal stem cells into smooth muscle cells induced by bladder smooth muscle cells conditioned medium. Zhongguo Xiu Fu Chong Jian Wai Ke Za Zhi. 2013;27(12):1506-1511.[45] Devarajan K, Forrest ML, Detamore MS, et al. Adenovector- mediated gene delivery to human umbilical cord mesenchymal stromal cells induces inner ear cell phenotype. Cell Reprogram. 2013;15(1):43-54.[46] Xu Y, Hong Y, Xu M, et al. Role of Keratinocyte Growth Factor in the Differentiation of Sweat Gland-Like Cells From Human Umbilical Cord-Derived Mesenchymal Stem Cells. Stem Cells Transl Med. 2016;5(1):106-116. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Lin Qingfan, Xie Yixin, Chen Wanqing, Ye Zhenzhong, Chen Youfang. Human placenta-derived mesenchymal stem cell conditioned medium can upregulate BeWo cell viability and zonula occludens expression under hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 4970-4975. |
| [3] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [4] | Hou Jingying, Yu Menglei, Guo Tianzhu, Long Huibao, Wu Hao. Hypoxia preconditioning promotes bone marrow mesenchymal stem cells survival and vascularization through the activation of HIF-1α/MALAT1/VEGFA pathway [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 985-990. |
| [5] | Shi Yangyang, Qin Yingfei, Wu Fuling, He Xiao, Zhang Xuejing. Pretreatment of placental mesenchymal stem cells to prevent bronchiolitis in mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 991-995. |
| [6] | Liang Xueqi, Guo Lijiao, Chen Hejie, Wu Jie, Sun Yaqi, Xing Zhikun, Zou Hailiang, Chen Xueling, Wu Xiangwei. Alveolar echinococcosis protoscolices inhibits the differentiation of bone marrow mesenchymal stem cells into fibroblasts [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 996-1001. |
| [7] | Fan Quanbao, Luo Huina, Wang Bingyun, Chen Shengfeng, Cui Lianxu, Jiang Wenkang, Zhao Mingming, Wang Jingjing, Luo Dongzhang, Chen Zhisheng, Bai Yinshan, Liu Canying, Zhang Hui. Biological characteristics of canine adipose-derived mesenchymal stem cells cultured in hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1002-1007. |
| [8] | Geng Yao, Yin Zhiliang, Li Xingping, Xiao Dongqin, Hou Weiguang. Role of hsa-miRNA-223-3p in regulating osteogenic differentiation of human bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1008-1013. |
| [9] | Lun Zhigang, Jin Jing, Wang Tianyan, Li Aimin. Effect of peroxiredoxin 6 on proliferation and differentiation of bone marrow mesenchymal stem cells into neural lineage in vitro [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1014-1018. |
| [10] | Zhu Xuefen, Huang Cheng, Ding Jian, Dai Yongping, Liu Yuanbing, Le Lixiang, Wang Liangliang, Yang Jiandong. Mechanism of bone marrow mesenchymal stem cells differentiation into functional neurons induced by glial cell line derived neurotrophic factor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1019-1025. |
| [11] | Duan Liyun, Cao Xiaocang. Human placenta mesenchymal stem cells-derived extracellular vesicles regulate collagen deposition in intestinal mucosa of mice with colitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1026-1031. |
| [12] | Pei Lili, Sun Guicai, Wang Di. Salvianolic acid B inhibits oxidative damage of bone marrow mesenchymal stem cells and promotes differentiation into cardiomyocytes [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1032-1036. |
| [13] | Li Cai, Zhao Ting, Tan Ge, Zheng Yulin, Zhang Ruonan, Wu Yan, Tang Junming. Platelet-derived growth factor-BB promotes proliferation, differentiation and migration of skeletal muscle myoblast [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1050-1055. |
| [14] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [15] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||