Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (5): 787-792.doi: 10.3969/j.issn.2095-4344.0452
Previous Articles Next Articles
Stem cell repair of intrauterine adhesions: preliminary achievements and clinical translation
Zhan Xin-lu, Zhou Meng-ni, Tan Bu-zhen
- Department of Obstetrics and Gynecology, the Second Affiliated Hospital of Nanchang University, Nanchang 330000, Jiangxi Province, China
-
Revised:2017-09-24Online:2018-02-18Published:2018-02-18 -
Contact:Tan Bu-zhen, Master, Professor, Doctoral supervisor, Chief physician, Department of Obstetrics and Gynecology, the Second Affiliated Hospital of Nanchang University, Nanchang 330000, Jiangxi Province, China -
About author:Zhan Xin-lu, Studying for master’s degree, Physician, Department of Obstetrics and Gynecology, the Second Affiliated Hospital of Nanchang University, Nanchang 330000, Jiangxi Province, China -
Supported by:the Social Development Project of Jiangxi Province, No. 2106BBG70218; the Innovative Foundation for Postgraduates in Nanchang University, No. cx2016338
CLC Number:
Cite this article
Zhan Xin-lu, Zhou Meng-ni, Tan Bu-zhen. Stem cell repair of intrauterine adhesions: preliminary achievements and clinical translation[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(5): 787-792.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
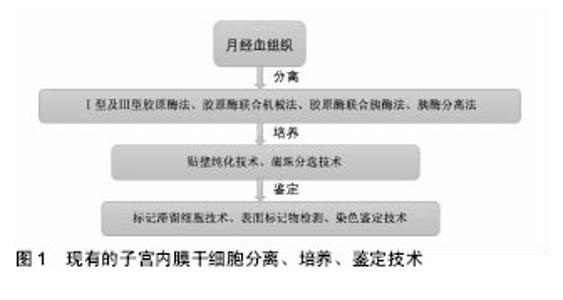
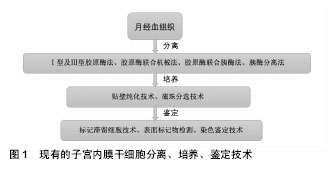
2.1 宫腔粘连 2.1.1 宫腔粘连的病理及病因 1894年由Fritsch最先描述,Asherman等首次详细报道定义为:由于子宫内膜损伤导致宫腔部分或全部闭塞从而导致月经异常、不孕与反复流产[2]。多次人工流产、术后感染及术后卵巢功能低下者易引起宫腔粘连,临床出现闭经、月经过少和不育。通常在子宫内膜受损后,上皮细胞可迅速再生,一般可使子宫内膜达到完全无痕修复。1992年,有学者总结出了宫腔粘连的病理表现:宫腔粘连患者子宫内膜被无活性的单层柱状上皮和间质纤维结缔组织所替代,腺体稀少,呈无活性形态或囊样扩张,不能分辨其功能层和基底层,上皮受到激素刺激呈无反应型,缺乏新生血管,宫腔内纤维性粘连形成。Schenker等[3]首次提出人工流产和妊娠后4周内实行清宫术是发生宫腔粘连的主要危险因素。Hooker等[4]认为患者多次实行清宫术是宫腔粘连的危险因素,而手术治疗、药物治疗本身对患者的生育影响无明显差异。Rein等[5]研究发现,宫腔镜手术的患者与清宫手术的患者相比较,宫腔镜组不仅妊娠率更高,术后再次妊娠间隔时间更短,术后宫腔粘连发生率也低于清宫术组。这提示妊娠后清宫术为宫腔粘连的高危因素之一,清宫术是妇产科医生常见的一种诊疗手段,有可能给子宫内膜带来不可逆的损伤,教育患者做好避孕措施,减少不必要的宫腔操作,可以有效预防宫腔粘连的发生。 2.1.2 宫腔粘连的诊断和分级 目前国际上已有宫腔粘连诊断系统:1978年March评分法、1988年AFS评分标准、1995年ESGE评分标准、2000年NasrAL宫腔镜评分,但这些系统诊断无统一标准。2015年,由中华医学妇产科学分会提出了宫腔粘连临床诊疗中国专家共识[6],专家观点提示:宫腔镜检查能全面评估宫腔形态、子宫内膜分布及损伤程度,是诊断宫腔粘连的准确方法;子宫输卵管造影和宫腔声学造影检查,可在无宫腔镜检查条件时选择;超声及MRI检查的益处尚不明显。宫腔粘连患者的分级在一定程度上指导着后续的治疗,重度宫腔粘连严重影响患者的月经生理与生殖预后,对其进行分级评分有必要性。由于现有的文献报道采用多种分级评分标准,使得不同研究之间诊断标准不尽统一,缺乏可比性。目前尚无任何一种分级评分标准得到国际范围内的采纳,反映出每种评分标准均存在自身缺陷。参照美国生育学会(AFS)与欧洲妇科内镜学会(ESGE)提出的评分量表,结合宫腔粘连治疗效果及影响因素,同时纳入与治疗结局密切相关的临床指标,专家提出了中国宫腔粘连分级评分标准,临床价值尚待观察。 2.1.3 宫腔粘连的治疗现状 近年来,宫腔粘连患病率有上升的趋势,多种治疗方法已被用于治疗子宫内膜损伤[7-8],包括:宫腔镜下粘连松解术;大剂量激素治疗如雌激素和促性腺激素释放激素激动剂;血管活性药物如阿司匹林、维生素E、己酮可可碱,L-精氨酸或西地那;生长因子如粒细胞集落刺激因子;再生医学的最新应用。大多数只能轻微改变子宫内膜的厚度和随后的妊娠率[9],疗效并不理想。在临床中,即使加以多种辅助治疗,国际上仍然有3%-23%的复发率,甚至有些病例复发率可高达20%-62%[10]。因此,在宫腔形态恢复后,不仅需要一些辅助措施来隔离宫腔手术创面以免形成新的粘连,而且需要促进内膜化的进程,使得基底层细胞完全覆盖创面,才可以起到自然隔离创面防止再粘连的作用。 2.2 子宫内膜干细胞 2.2.1 子宫内膜干细胞概述 干细胞是一类具有自我复制能力的多潜能细胞,在一定条件下,能够分化为多种功能细胞,具有多分化潜能;干细胞还具有自我更新能力,能够产生高度分化的功能细胞。根据干细胞所处的发育阶段可分为胚胎干细胞和成体干细胞。有学者推测,子宫内膜干细胞可能来源于胚胎期残留细胞和骨髓间充质干细胞。2012年,Cervello ?等[11]在接受了骨髓移植的女性受者子宫内膜中发现了1.7%-2.62%的男性XY供体细胞的存在。在此试验中,骨髓干细胞被认为是一个诱导子宫内膜细胞再生的有限来源,而不是子宫内膜干细胞的循环来源。子宫内膜的高度增殖活性、周期性更新,提示子宫内膜中可能存在子宫内膜干细胞,驱动子宫内膜进行快速的增生和重建,成体干细胞的多向分化潜能和无限增殖能力证明了它应用于临床的潜能[12-14]。 2.2.2 子宫内膜干细胞的分离、培养和鉴定 人子宫内膜干细胞可由刮宫术或从月经中获得,是来源最广的成体干细胞。现在国内外对子宫内膜干细胞分离培养有许多方法[15-17],但没有一种统一的方法,且实验的重复性差。目前对原代子宫内膜细胞的分离方法有:Ⅰ型及Ⅲ型胶原酶法、胶原酶联合应用机械法、胶原酶联合应用胰酶法、仅用胰酶法。郭玉琪等[18]研究发现使用Ⅲ型胶原酶分离子宫内膜干细胞具有一定的优势,可能是由于胶原酶是从溶组织梭状细胞芽孢菌中提取制备的,主要水解结缔组织中胶原蛋白成分,可使上皮细胞和胶原成分分离而不受伤害。毕玉虎等[19]研究发现相对于胰蛋白酶法和胰蛋白酶联合胶原酶Ⅰ法而言,胶原酶Ⅰ法分离培养所得的子宫内膜基质干细胞数量较多,生长速度较快。马颖等[20]采用混合法(机械和酶消化相结合)和胶原酶Ⅰ法对子宫内膜组织进行消化,混合法获得的活细胞数多于胶原酶Ⅰ法,其差异有显著性意义(P < 0.01)。 常用的两种培养人子宫内膜干细胞的方法是贴壁纯化技术和磁珠分选技术,有学者发现磁珠分选培养干细胞的方法比较复杂,但与贴壁纯化技术比较可获得大量干细胞[21]。干细胞进行培养时,多用含体积分数为5%-10%胎牛血清的合成培养基,这给培养产物的分离、纯化和检测带来一定的不便,在细胞的使用上也会带来病毒和免疫的隐患。并且血清的成分是未知的,已被报道可能影响再生能力。康康等[22]证明无血清培养基也可培养出子宫内膜间充质干细胞,且分化能力并未受到影响,无血清培养基代替传统的动物血清培养子宫内膜干细胞是可行的。周云帆等[23]从健康女性的月经血标本中成功分离出子宫内膜干细胞,并进行单个核细胞培养,传代纯化后的细胞具有间充质干细胞的典型形态,实验中发现即使有部分细胞贴壁,也并非每份样品都能获得间充质干细胞,其中的个体差异机制不明。对提取出的内膜干细胞进行免疫组化检测,nestin阳性细胞表达高达(10.35±0.51)%,说明其有分化为神经元样细胞的潜能。 现已有学者在体外成功使子宫内膜干细胞定向分化为平滑肌细胞、脂肪细胞、软骨细胞、成纤维细胞和成骨细胞[24]。子宫内膜干细胞的定向分化方法:分离提纯后在体外培养条件下,加入成脂诱导剂(地塞米松、胰岛素、吲哚美辛和IBMX)或成骨诱导剂(地塞米松、甘油磷酸钠、抗坏血酸),可诱导成脂、成骨等分化[25]。陈波[26]从人早孕蜕膜组织中分离得到子宫内膜间质干细胞,使用含有重组人转化生长因子β1、表皮生长因子以及重组人血小板源性生长因子BB的诱导液成功诱导分化为子宫内膜上皮细胞。 迄今为止,如何鉴定子宫内膜干细胞在国际上仍没有公认的标准,2006年,Chan等[12]采用标记滞留细胞(label-retaining cell,LRC)技术,成功确定了小鼠子宫内膜中干细胞的存在和定位。绝大多数学者的共识是干细胞用于移植前,需进行形态学观察、增殖能力检测、表面标记物检测等。目前并未发现特异性的子宫内膜干细胞的标记物,国内外学者们仍在不断探索新的鉴定方法[27]。已有多种干细胞表面标志物被用于鉴定子宫内膜干细胞,如CD73、CD90、CD29、CD44、CD117、HLA-ABC,但各位学者使用的标志物并未统一[19-20,23,26],不能特异性区分子宫内膜干细胞和其他类型干细胞。镜下观察子宫内膜干细胞可见[28]:细胞多呈梭形、不规则三角形,核为卵圆形,位于靠近细胞质的中央,细胞排列成漩涡状、放射状或似栅栏状生长;Vimentin染色阳性。已分化的干细胞可以通过染色鉴定,分别是油红O染色(鉴定脂滴)、茜素红染色(鉴定成骨细胞)、von Kossa染色(鉴定钙化的细胞外基质)、阿利新蓝染色(鉴定硫酸蛋白多糖)。虽然现在子宫内膜干细胞的提取、分离、培养、鉴定并没有一个标准化的流程,但这些实验结果可为更深层次的子宫内膜干细胞研究提供依据(图1)。"
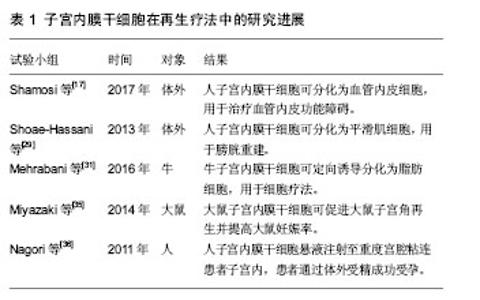
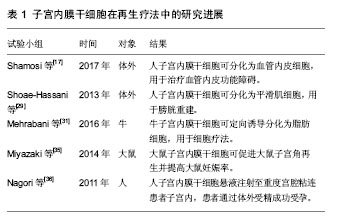
2.3 子宫内膜干细胞在宫腔粘连修复治疗中的应用 子宫内膜干细胞可以通过简单的刮宫术、宫腔镜手术,甚至月经血中获得,近年来备受关注。大量的实验和临床研究已经评估了不同来源子宫内膜干细胞用于细胞治疗的潜力。子宫内膜干细胞作为一种成体干细胞具有容易分离和扩增的特性,有更强的集落形成能力和更少的提取技术问题,拥有巨大的自体治疗潜力。Shamosi等[17]提出子宫内膜干细胞可作为治疗血管内皮功能障碍的新方向,为冠心病、高血压和动脉粥样硬化提供了一个新的选择。Shoae-Hassani等[29]使用水凝胶作为支架,成功的使人子宫内膜干细胞分化为平滑肌细胞,用于膀胱重建。Khademi等[30]研究证明了子宫内膜干细胞用于细胞移植的可行性,也有研究证明其可分化为平滑肌细胞、脂肪细胞、软骨细胞、成纤维细胞和成骨细胞[12]。Mehrabani等[31]从健康母牛的子宫中提取出子宫内膜干细胞,诱导分化为脂肪细胞用于细胞疗法。 子宫结构或功能完全丧失的患者,只能通过代孕或子宫移植来实现妊娠愿望,但这种治疗手段一直有着伦理学上的争议[32-34]。2014年,Miyazaki等[35]提出了生成人工子宫的想法。为获取细胞外基质和脱落的子宫基质细胞(主要为子宫内膜干细胞),他们使用洗涤剂灌注大鼠子宫主动脉,并对获取的细胞悬液进行免疫组化染色来检测Ⅰ型胶原和层粘连蛋白的表达。先进行体外试验,将脱落的子宫基质细胞和骨髓间充质干细胞,注射到离体的大鼠子宫壁,将其移植到一个特殊的体外培养灌注腔。经3 d灌注培养,发现子宫细胞部分分布在基质中,形成子宫内膜样组织;免疫荧光检测显示波形蛋白阳性(基质细胞)与角蛋白阳性(上皮细胞)。再进一步探索其是否有促进体内子宫角再生的潜力。实验分为3组:空白对照组、大鼠子宫角切除/再生组、大鼠子宫角切除组。大鼠子宫角切除/再生组将大鼠子宫基质细胞、大鼠骨髓干细胞与胶原支架移植于大鼠受损子宫角处,90 d后处死大鼠,分析再生子宫角的组织学类型。组织切片显示再生的子宫角组织几乎与正常子宫角组织相同。切除/再生组与切除组相比较,单宫角妊娠率和胎儿平均体质量的差异均有显著性意义。结果表明:子宫基质细胞可用于子宫再生,并治疗子宫因素导致的不孕不育。 迄今为止,子宫内膜干细胞已经应用于多种临床试验以及一些小动物研究,虽然关于子宫内膜干细胞促进内膜再生的报道极少,同属成体干细胞的骨髓干细胞和胚胎干细胞的成功应用提示了子宫内膜干细胞促进内膜再生的巨大潜能。国内外鲜有相关的临床报道,2011年,印度学者Nagori等[36]率先将自体子宫内膜干细胞悬液注射至1例重度宫腔粘连患者的子宫内,术后予抗炎治疗及激素治疗,患者通过体外受精成功受孕。因此,使用子宫内膜干细胞移植治疗重度宫腔粘连患者的再生疗法在临床上有着很好的前景。但子宫内膜干细胞促进内膜修复的具体机制需要进一步研究。见表1。"
| [1] Yamamoto N, Izuchi D, Yuge N, et al. Hysteroscopic adhesiolysis for patients with Asherman’s syndrome: menstrual and fertility outcomes. Reproductive Medicine & Biology. 2013; 12(4):159-166.[2] Yu D, Wong YM, Cheong Y, et al. Asherman syndrome--one century later. Fertil Steril. 2008;89(4):759779.[3] Schenker JG, Margalioth EJ. Intrauterine adhesions: an updated appraisal. Fertil Steril. 1982;37(5):593-610.[4] Hooker AB, Lemmers M, Thurkow AL, et al. Systematic review and meta-analysis of intrauterine adhesions after miscarriage: prevalence, risk factors and long-term reproductive outcome. Hum Reprod Update. 2014;20(2):262-278.[5] Rein DT, Schmidt T, Hess AP, et al. Hysteroscopic management of residual trophoblastic tissue is superior to ultrasound-guided curettage. J Minim Invasive Gynecol. 2011; 18(6):774-778.[6] 中华医学会妇产科学分会. 宫腔粘连临床诊疗中国专家共识[J]. 中华妇产科杂志,2015,50(12):881-887.[7] Zhao J, Chen Q, Cai D, et al. Dominant factors affecting reproductive outcomes of fertility-desiring young women with intrauterine adhesions. Arch Gynecol Obstet. 2017;295(4): 923-927.[8] He Y, Ji F, Zhou X, et al. Short-term clinical effects of 68 cases of transcervical resection of adhesions. Biomedical Research. 2017;28(5):2267-2271.[9] Lebovitz O, Orvieto R.Treating patients with "thin" endometrium - an ongoing challenge. Gynecol Endocrinol. 2014;30(6):409-414.[10] Tu CH, Yang XL, Qin XY, et al. Management of intrauterine adhesions: a novel intrauterine device. Med Hypotheses. 2013;81(3):394-396.[11] Cervelló I, Gil-Sanchis C, Mas A, et al. Bone marrow-derived cells from male donors do not contribute to the endometrial side population of the recipient. PLoS One. 2012;7(1): e30260.[12] Chan RW, Gargett CE. Identification of label-retaining cells in mouse endometrium. Stem Cells. 2006;24(6):1529-1538.[13] Gargett CE, Schwab KE, Deane JA. Endometrial stem/progenitor cells: the first 10 years. Hum Reprod Update. 2016;22(2):137-163.[14] Singh N, Mohanty S, Seth T, et al. Autologous stem cell transplantation in refractory Asherman's syndrome: A novel cell based therapy. J Hum Reprod Sci. 2014;7(2):93-98.[15] De Cesaris V, Grolli S, Bresciani C, et al. Isolation, proliferation and characterization of endometrial canine stem cells. Reprod Domest Anim. 2017;52(2):235-242.[16] Tabatabaei FS, Torshabi M. In vitro proliferation and osteogenic differentiation of endometrial stem cells and dental pulp stem cells. Cell Tissue Bank. 2017;18(2):239-247.[17] Shamosi A, Mehrabani D, Azami M, et al. Differentiation of human endometrial stem cells into endothelial-like cells on gelatin/chitosan/bioglass nanofibrous scaffolds. Artif Cells Nanomed Biotechnol. 2017;45(1):163-173.[18] 郭玉琪,赵潇丹,路平,等. 体外分离子宫内膜干细胞3种方法的比较[J]. 郑州大学学报:医学版,2012,47(1):20-23.[19] 毕玉虎,滕君儒. 子宫内膜基质干细胞的体外分离培养及生物学特性[J]. 中国组织工程研究,2017,21(5):760-765.[20] 马颖,何援利. 人子宫内膜中存在一群具有克隆增殖能力的细胞[J]. 中国组织工程研究,2012,16(45):8496-8500.[21] 杨新园,陈葳,李旭. 子宫内膜基质干细胞培养方法的比较研究[J]. 山西医科大学学报,2011,42(8):624-628.[22] 康康,王蔼明,尹善德,等. 评估无血清培养子宫内膜间充质干细胞的可行性[J]. 解放军医学院学报, 2015,36(6):563-567.[23] 周云帆,杨波,胡祥,等. 经血源性子宫内膜间充质干细胞的分离、培养与鉴定[J].中国组织工程研究与临床康复,2010,14(32): 5952-5956.[24] Gargett CE, Schwab KE, Zillwood RM, et al. Isolation and culture of epithelial progenitors and mesenchymal stem cells from human endometrium. Biol Reprod. 2009;80(6): 1136-1145.[25] 杨新园,李旭,陈葳. 子宫内膜基质干细胞的体外成骨诱导和成脂诱导分化[J]. 西安交通大学学报:医学版, 2012,33(1):95-98.[26] 陈波. 人早孕蜕膜组织子宫内膜间质干细胞向子宫内膜上皮细胞的分化[J]. 中国组织工程研究,2016,20(14):2098-2103.[27] Miyazaki K, Maruyama T, Masuda H, et al. Stem cell-like differentiation potentials of endometrial side population cells as revealed by a newly developed in vivo endometrial stem cell assay. PLoS One. 2012;7(12):e50749.[28] Schwab KE, Chan RW, Gargett CE. Putative stem cell activity of human endometrial epithelial and stromal cells during the menstrual cycle. Fertil Steril. 2005;84 Suppl 2:1124-1130.[29] Shoae-Hassani A, Sharif S, Seifalian AM, et al. Endometrial stem cell differentiation into smooth muscle cell: a novel approach for bladder tissue engineering in women. BJU Int. 2013;112(6):854-863.[30] Khademi F, Soleimani M, Verdi J, et al. Human endometrial stem cells differentiation into functional hepatocyte-like cells. Cell Biol Int. 2014;38(7):825-834.[31] Mehrabani D, Nazarabadi RB, Kasraeian M, et al. Growth Kinetics, Characterization, and Plasticity of Human Menstrual Blood Stem Cells. Iran J Med Sci. 2016;41(2):132-139.[32] Hooker A, Fraenk D, Brölmann H, et al. Prevalence of intrauterine adhesions after termination of pregnancy: a systematic review. Eur J Contracept Reprod Health Care. 2016;21(4):329-335.[33] Wang X, Duan H. Clinical evaluation of amniontic products after transcervical resection of intensive degree of intrauterine adhesions. Zhonghua Fu Chan Ke Za Zhi. 2016;51(1):27-30.[34] Chen Y, Liu L, Luo Y, et al. Prevalence and Impact of Chronic Endometritis in Patients With Intrauterine Adhesions: A Prospective Cohort Study. J Minim Invasive Gynecol. 2017; 24(1):74-79.[35] Miyazaki K, Maruyama T. Partial regeneration and reconstruction of the rat uterus through recellularization of a decellularized uterine matrix. Biomaterials. 2014;35(31): 8791-8800.[36] Nagori CB, Panchal SY, Patel H. Endometrial regeneration using autologous adult stem cells followed by conception by in vitro fertilization in a patient of severe Asherman's syndrome. J Hum Reprod Sci. 2011;4(1):43-48.[37] Mints M, Jansson M, Sadeghi B, et al. Endometrial endothelial cells are derived from donor stem cells in a bone marrow transplant recipient. Hum Reprod. 2008;23(1): 139-143.[38] Alawadhi F, Du H, Cakmak H, et al. Bone Marrow-Derived Stem Cell (BMDSC) transplantation improves fertility in a murine model of Asherman's syndrome. PLoS One. 2014; 9(5):e96662.[39] Kilic S, Yuksel B, Pinarli F, et al. Effect of stem cell application on Asherman syndrome, an experimental rat model. J Assist Reprod Genet. 2014;31(8):975-982.[40] Ye L, Mayberry R, Lo CY, et al. Generation of human female reproductive tract epithelium from human embryonic stem cells. PLoS One. 2011;6(6):e21136.[41] 王燕华,曲军英,吕一帆,等. 胚胎干细胞移植于内膜损伤小鼠的初步研究[J]. 国际生殖健康/计划生育杂志, 2012,31(6): 434-438.[42] Song T, Zhao X, Sun H, et al. Regeneration of uterine horns in rats using collagen scaffolds loaded with human embryonic stem cell-derived endometrium-like cells. Tissue Eng Part A. 2015;21(1-2):353-361.[43] 叶明侠,俞凌,范文生,等.经γ射线辐照后的脂肪间充质干细胞对大鼠薄型子宫内膜的治疗作用[J]. 南方医科大学学报, 2017, 37(5):1673-1677. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Lin Qingfan, Xie Yixin, Chen Wanqing, Ye Zhenzhong, Chen Youfang. Human placenta-derived mesenchymal stem cell conditioned medium can upregulate BeWo cell viability and zonula occludens expression under hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 4970-4975. |
| [3] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [4] | Hou Jingying, Yu Menglei, Guo Tianzhu, Long Huibao, Wu Hao. Hypoxia preconditioning promotes bone marrow mesenchymal stem cells survival and vascularization through the activation of HIF-1α/MALAT1/VEGFA pathway [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 985-990. |
| [5] | Shi Yangyang, Qin Yingfei, Wu Fuling, He Xiao, Zhang Xuejing. Pretreatment of placental mesenchymal stem cells to prevent bronchiolitis in mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 991-995. |
| [6] | Liang Xueqi, Guo Lijiao, Chen Hejie, Wu Jie, Sun Yaqi, Xing Zhikun, Zou Hailiang, Chen Xueling, Wu Xiangwei. Alveolar echinococcosis protoscolices inhibits the differentiation of bone marrow mesenchymal stem cells into fibroblasts [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 996-1001. |
| [7] | Fan Quanbao, Luo Huina, Wang Bingyun, Chen Shengfeng, Cui Lianxu, Jiang Wenkang, Zhao Mingming, Wang Jingjing, Luo Dongzhang, Chen Zhisheng, Bai Yinshan, Liu Canying, Zhang Hui. Biological characteristics of canine adipose-derived mesenchymal stem cells cultured in hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1002-1007. |
| [8] | Geng Yao, Yin Zhiliang, Li Xingping, Xiao Dongqin, Hou Weiguang. Role of hsa-miRNA-223-3p in regulating osteogenic differentiation of human bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1008-1013. |
| [9] | Lun Zhigang, Jin Jing, Wang Tianyan, Li Aimin. Effect of peroxiredoxin 6 on proliferation and differentiation of bone marrow mesenchymal stem cells into neural lineage in vitro [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1014-1018. |
| [10] | Zhu Xuefen, Huang Cheng, Ding Jian, Dai Yongping, Liu Yuanbing, Le Lixiang, Wang Liangliang, Yang Jiandong. Mechanism of bone marrow mesenchymal stem cells differentiation into functional neurons induced by glial cell line derived neurotrophic factor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1019-1025. |
| [11] | Duan Liyun, Cao Xiaocang. Human placenta mesenchymal stem cells-derived extracellular vesicles regulate collagen deposition in intestinal mucosa of mice with colitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1026-1031. |
| [12] | Pei Lili, Sun Guicai, Wang Di. Salvianolic acid B inhibits oxidative damage of bone marrow mesenchymal stem cells and promotes differentiation into cardiomyocytes [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1032-1036. |
| [13] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [14] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| [15] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||