Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (12): 1956-1961.doi: 10.3969/j.issn.2095-4344.0213
Previous Articles Next Articles
Research progress and literature review of animal models of osteoporosis
Li Yan-hong1, 2, Dang Xiao-qian2, Gong Fu-tai1, Ban Wen-rui2, Ma Jun2, Shi Yao-wu1, Zhang Hong-lei1
- 1Xi’an Hospital of Chinese Medicine, Xi’an 710021, Shaanxi Province, China; 2the Second Affiliated Hospital of Xi’an Jiaotong University, Xi’an 710061, Shaanxi Province, China
-
Received:2017-11-14 -
Contact:Dang Xiao-qian, the Second Affiliated Hospital of Xi’an Jiaotong University, Xi’an 710061, Shaanxi Province, China -
About author:Li Yan-hong, Doctoral candidate, Attending physician, Xi’an Hospital of Chinese Medicine, Xi’an 710021, Shaanxi Province, China; the Second Affiliated Hospital of Xi’an Jiaotong University, Xi’an 710061, Shaanxi Province, China
CLC Number:
Cite this article
Li Yan-hong1, 2, Dang Xiao-qian2, Gong Fu-tai1, Ban Wen-rui2, Ma Jun2, Shi Yao-wu1, Zhang Hong-lei1. Research progress and literature review of animal models of osteoporosis[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(12): 1956-1961.
share this article

2.1.2 小鼠 小鼠的性成熟期和性周期与大鼠相似,去卵巢后骨量及骨形态的变化也与大鼠相似,去势小鼠的骨丢失同样可以被雌激素替代疗法所预防。另外,由于小鼠的基因易于控制,小鼠成为研究基因缺失对骨流失影响的最佳模型,OPG基因敲除小鼠是一种理想的原发性骨质疏松动物模型[8],成为研究峰值骨量基因控制方面的有用动物[9]。 SAMP6是一种衰老加速型小鼠,是目前唯一证实可随年龄增长出现脆性骨折的动物[10],随年龄的增加骨量丢失,并且雌雄间无明显差异[11],是研究老年性骨质疏松的最适模型[12]。同样,由于小鼠体积小,去卵巢手术难度较大,标本留取取材量少等问题,一定程度上限制了其在骨质疏松研究中的应用。 2.1.3 兔 兔是医学研究中广泛使用的动物,寿命一般为4-9年,性成熟期为5-8个月,由于兔具有明显的哈氏重建能力,可以成功的作为骨质疏松模型[13]。 兔骨质疏松造模的优点在于:①易饲养,繁殖能力强;②耳缘静脉给药和取血方便,便于长期的动态观察;③性成熟后骺板闭合,与人类相似;④具有明显的哈佛氏重建系统,适合皮质骨影响的研究,比鼠更接近人类。⑤更适合于骨植入物和骨植入界面的研究[14-15]。 2.1.4 羊 Zarrinkalam等[16]研究表明,羊是研究椎骨骨质疏松的理想模型(表2)。"


2.1.5 犬 犬作为骨质疏松造模的实验动物,其优点在于:①易于饲养;②成年犬骨代谢、骨组织形态、皮质骨与松质骨比例均与人相似,且犬的哈佛氏重建与人类接近;③犬与人类的消化系统相似,可以口服给药;④体格较大,可以多次取骨活检及血液等标本,便于长期反复观察。然而由于犬雌激素水平低,每年仅两次发情,且持续时间短,去卵巢及雌激素耗竭等均不能造成骨量低下,因此,不适合作为绝经后骨质疏松的模型动物。 2.1.6 猪 猪因其心血管系统、消化系统、营养需要、骨骼发育以及矿物质代谢等均与人颇为相似,已被用于多种疾病的研究。起初由于其躯体肥大,饲养时间长,喂养成本高,不利于实验处理和管理。20世纪中叶,实验小型猪和微型猪的培育成功解决了这些问题,使猪成为具有广泛应用前景的新型实验动物。小型猪动物模型的优缺点见表3。"

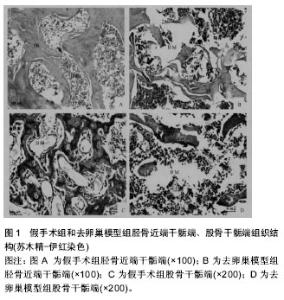
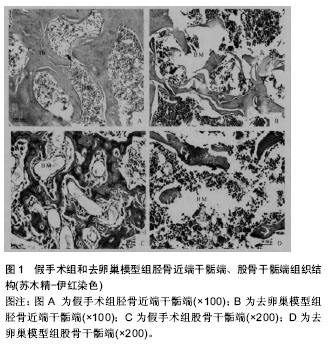
2.1.7 非人类灵长类 灵长类动物作为骨质疏松模型的实验动物,其优点是组织器官、骨生物力学特征及与年龄相关的骨代谢激素变化同人类相类似,增龄性骨量丢失与人类相似,另外,雌性动物的性周期和人类一样。然而,非人类灵长类动物资源稀缺,驯养困难,费用昂贵,且易传播动物源性疾病,制约了其应用。 2.2. 造模方法 2.2.1 去势造模法 去势法可分为手术去势和药物去势两种方法。 (1)手术去势法:是指利用外科手术的方式切除动物生殖系统使其丧失性功能以达到动物造模的方法。1969 年Saville[19]通过手术切除雌性大鼠卵巢,首次建立绝经后骨质疏松动物模型。现在去卵巢造模方法被广泛认为是绝经后骨质疏松症造模的金标准。1997年,杨霞等[20]首次成功探索了利用去势兔建立骨质疏松模型。切除雄性动物睾丸亦能用于构建骨质疏松模型,已被用于男性骨质疏松的研究。此外,老龄猕猴、小型猪也可以用去势法成功造模。需注指出的是,绵羊单纯利用去势法造模并不理想,狗亦不能用于绝经后骨质疏松的研究。 手术去势法造模因素单一、模型效果稳定、可复制性好、实验结果可信度大,能很好的模拟绝经后骨质疏松骨代谢的特点。但也有不足,卵巢切除后动物体内雌激素水平突然迅速下降,而绝经后妇女的雌激素水平下降则是一个长期缓慢的过程,二者间存在一定差异。另外,切除卵巢去势后动物体重的增加会对估量的丢失起到一定的保护作用,且手术去势创伤刺激会影响检测指标。 (2)药物去势法:是指不切除性腺,仅通过给予抑制动物雌激素分泌的药物从而造成骨量丢失的造模方法。常用药物有: 促黄体激素释放激素受体激动剂、促性腺激素释放激素激动剂、雌激素受体拮抗剂、非类固醇类雄激素拮抗剂、芳香化酶抑制剂等。药物去势虽然避免了手术创伤刺激对检测指标的干扰,但药物的不良反应以及药物与抗骨质疏松药物之间的相互作用也会在一定程度上降低实验的可信度。 2.2.2 药物致骨质疏松造模法 药物致骨质疏松造模中糖皮质激素应用最广泛,其他还有维甲酸、环磷酰胺、乙醇等。临床中,使用糖皮质激素引起的骨质疏松症,其发病率仅次于绝经后骨质疏松和老年性骨质疏松,因此,糖皮质激素诱导法建立的骨质疏松模型对研究人类骨质疏松症意义重大,最常用的糖皮质激素有地塞米松和泼尼松龙。 维甲酸可以引起骨量流失,虽然在致病机制上与人类骨质疏松存在差异,但维甲酸骨质疏松动物模型在临床表现、骨组织形态学以及对雌激素的骨反应方面与人类相似。 环磷酰胺通过抑制骨形成引起骨量减少、骨微结构退化等典型骨质疏松表现,该造模法尚处于研究阶段。 酒精可影响骨代谢,使骨吸收增强、骨形成减少、骨量降低而引发骨质疏松,任树军等[21]通过给雄性SD大鼠用红星二锅头灌胃成功构造骨质疏松模型。使用药物造模时应把握好剂量和用法,正确的用法和剂量既可以引起动物骨量丢失又不至于导致其死亡。 2.2.3 营养性骨质疏松造模法 营养是影响骨密度的众多因素之一,通过限制饮食中的钙、维生素D、蛋白质等的摄入可以成功建立营养缺乏型骨质疏松模型,该模型对研究因营养缺陷引起的骨质疏松有重要意义。但由于饲料配方复杂,且影响因素较多,普及推广困难。同时,因为单独应用营养法建模耗时长且成功率低,故常作为一种辅助方法。 2.2.4 失用性骨质疏松造模法 失用法是指由于运动受阻或者功能障碍引起骨代谢异常,骨量丢失的一种造模方法,多由失重状态、长期卧床或制动等因素导致。常用方法有:机械固定法,悬吊法,腱切除法,坐骨神经切除法等[22]。该模型对防治瘫痪、骨折、术后长期卧床的患者及航空人员出现的骨质疏松的研究有重要现实意义[23]。 2.2.5 脑源性骨质疏松动物模型 下丘脑有调节骨代谢及骨重建的功能。刘锡仪等[24]研究表明:破坏大鼠下丘脑弓状核,导致内分泌功能紊乱继而可以引起骨质疏松,被认为是一种可操作性强、稳定性高和可复制性好的大鼠骨质疏松动物模型造模法。适用于骨质疏松的发病机制及防治方面的研究。 2.2.6 基因造模法 基因造模法主要包括转基因造模法和基因突变造模法。转基因造模法是指采用基因敲除来的方式来制作骨质疏松动物模型,敲除的基因主要是α,β-雌激素受体或芳香酶,该模型具有全身骨质疏松发生情况稳定、不受外界因素干预等优点,是一种理想的原发性骨质疏松动物模型。基因突变造模法是日本学者Toshio Takeda等利用SAMP6小鼠通过近交繁殖培育的快速老化小鼠骨质疏松模型,是一种自发老年性骨质疏松模型,SAMP6小鼠遗传稳定,骨老化特点与人类老年性OP相似,是老年性OP研究较为理想的动物模型。 2.2.7 联合造模法 用去势法联合其他造模方法共同构建骨质疏松模型的方法,可以有效缩短造模时间。如去势联合糖皮质激素[25],去势联合低钙饮食[26],去势、低钙饮食、糖皮质激素三者联合等[27],且发现三联法较两联法对骨骼的影响更加明显[27]。联合造模虽能加速造模,但干扰因素较多且复杂,可能影响研究工作。 2.3 模型评价方法 骨质疏松模型是否复制成功,需要用客观的指标来评价,骨质疏松的动物模型和造模方法很多,但评价指标是一致的,主要有骨密度测定、骨组织形态计量学、生化检测分析、骨生物力学测试、体质量、性腺形态等,其中最主要的是骨量与骨组织病理学变化这两项指标(图1)[28-29]。但单一的检测指标一般存在片面性,无法对骨质疏松模型进行准确的评估,因此,通过“宏观到微观、二维到三维、定性到定量”全面立体对骨质疏松模型进行检测显得尤为重要。"
| [1] 李素萍.骨质疏松动物模型的研究现状[J].中国组织工程研究与临床康复,2011,15(20):3767-3770.[2] 祁珊珊.骨质疏松疾病动物模型的研究进展[J].黑龙江畜牧兽医, 2014,501(5):96-98.[3] Jilka RL. The relevance of mouse models for investigatingage-related bone loss in humans. J Gerontol A Biol Sci MedSci.2013;68(10):1209-1217.[4] Costa LA, Lopes BF, Lanis AB, et al. Bone demineralization inthe lumbar spine of dogs submitted to prednisone therapy. JVer Pharmacol Ther. 2010;33(6):583-586.[5] 虞惊涛,马信龙,马剑雄.骨质疏松动物模型评价方法[J].中华骨质疏松和骨矿盐疾病杂志,2014,(1):66-70.[6] Lelovas PP,Xanthos TT,Thoma SE.The laboratory ratas an animal model for osteoporosis researc.Comp Med.2008;58: 424-430.[7] Egermann M, Goldhahn J, Schneide RE,Animal modelsfor fracture treatment in osteoporosis.Osteoporos Int.2005; 16:S129-S138.[8] Priemel M, Schilling AF, Haberland M, et al Osteopenicmice: animal models of the aging skeleton.J MusculoskeletNeuron Interact.2002;2: 212-218.[9] 贾经汉,邱新建,陈志坚.常用骨质疏松动物模型特点的综述[J].广西中医学院学报, 2006,9(4):76-79.[10] 张月峰,韩景献.骨质疏松动物模型研究进展[J].动物医学进展, 2005,26(3):8-11.[11] Matsushita M,Tsuboyama T,Kasai R,et al. Agerelatedchanges in bone mass in the senescenceacceleratedmouse(SAM). SAM-R/3 and SAM-P/6as new murine models for senile osteoporosis.AmJ Pathol.1986;125(2):276-283. [12] Takada K,Inaba M,Ichioka N,et al.Treatment of senile osteoporosisin SAMP6 mice by intra-bone marrow injection of allogeneicbone marrow cells.Stem Cells.2006;24:399-405.[13] 杨晋,刘毅,王兆杰.去势加氢化可的松肌内注射兔骨质疏松模型建立的实验研究[J].中国医药指南,2013,11(19):486-487.[14] Castaneda S, Calvo E, Largo R, et al. Characterization of a newexperimental model of osteoporosis in rabbits.J Bone MinerMetab.2008;26(1):53-59.[15] Baofeng L,Zhi Y, Bei C,et al.Characterization of a rabbitosteoporosis model induced by ovariectomy and glucocorticoid.Acta Orthop.2010;81(3):396-401.[16] Zarrinkalam MR, Beard H, Schultz CG, et al.Validationof the sheep as a large animal model for the study of vertebralosteoporosis.Eur Spine J.2009;18: 244-253. [17] Turner AS. The sheep as a model for osteoporosis in humans.Vet J.2002;163: 232-239.[18] Wilke HJ, Ketter A, Claes LE. Are sheep spines a valid biomechanicalmodel for human spines?.Spine.1997; 22: 2365-2374.[19] Saville PD. Changes in skeletal mass and fragility with castrationin the rat; a model of osteoporosis.J Am Geriatr Soc.1969; 17( 2):155-166.[20] 杨霞,蔡桂英,魏玲,等.去势兔骨质疏松模型建立的初探[J].生物医学工程学杂志,1997,14( 4):353-358.[21] 任树军,邢国利,等.补肾健脾益气法对酒精性骨质疏松大鼠骨密度(BMD)、骨矿含量(BMC)影响的研究[J].中医药学报, 2013, 41(1):24-26.[22] Giangregorio L,Blimkie CJ.Skeletal adaptations to alterations inweight-bearing activity: a comparison of models of disuseosteoporosis. Sports Med. 2002;32(7):459-476.[23] 谭雄进,王前,郑磊,等.不同年龄尾吊鼠负重骨骨代谢及力学性能变化[J].中国骨质疏松杂志,2003,9(1):6-8.[24] 刘锡仪,刘浩宇.大鼠脑源性骨质疏松动物模型[J].中国骨质疏松杂志,2008,14(3):143-147.[25] 杨晋,刘毅,王兆杰.去势加氢化可的松肌内注射兔骨质疏松模型建立的实验研究[J].中国医药指南,2013,(19) :486-487.[26] Schlewitz G,Govindarajan P,Schliefke N,et al. Ovariectomyand calciumvitamin D2 /D3 deficient diet as a model of osteoporosisin the spine of Sprague-Dawley rats.Z Orthop Unfall.2013;151(1):14-19.[27] Veigel E,Moore RJ,Zarrinkalam MR,et al. Osteopenia in themaxillofacial area: a study in sheep. Osteoporos Int.2011; 22( 4):1115-1121.[28] Miller PD, Zapalowski C, Kulak CA,et al.Bone densitometry: the best way to detect osteoporosis and to monitor therapy.J Clin Endocrinol Metab.1999;84:1867-1871[29] 祁珊珊,王永吉,庞田田,等.去卵巢大鼠骨、生殖系统组织病理学与形态计量学观察[J].中国骨质疏松杂志,2015,21(7): 774-779.[30] 莫文秋,李双蕾,陈文辉.骨质疏松动物模型评价方法的研究进展[J].医学综述,2016,22(7):1330-1332.[31] 崔轶,李军,郭海,等.骨质疏松模型的评价方法研究进展[J].中国骨质疏松杂志,2013,19( 4):416-420.[32] 高克加,史青,叶智卫,等.核素99m Tc-MDP 骨显像对不同阶段骨质疏松的相关性实验探讨[J].中国骨质疏松杂志,2013,19(8): 783-787.[33] 郭劲宇,耿晟杰.骨质疏松症的流行病学趋势与防治进展探讨[J].无线互联科技,2014,(4):224-224.[34] Cawston H,Maravic M,Fardellone P,et al. Epidemiologicalburden of postmenopausal osteoporosis in France from 2010 to2020: estimations from a disease model.Arch Osteoporos.2012;7(1-2):237-246.[35] 沈彦明,孙陈静,尹彦亮.老年骨质疏松症防治研究进展[J].现代预防医学,2013,40(9):1757-1762.[36] 马少华,马勇.中药治疗原发性骨质疏松症效应机制研究进展[J].中国骨质疏松杂志,2014,20(12):1490-1494.[37] 胡军,张华.骨质疏松症的流行病学趋势与防治进展[J].临床荟萃, 2011,26( 8) :729-731.[38] Datta NS.Osteoporotic fracture and parathyroid hormone. World J Orthop.2011;2( 8):67-74.[39] 张春丽,李忠海,周颖.构建骨质疏松动物模型建模方法的改进及评价[J].中国组织工程研究,2016,20(5):754-75996-98. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Tang Hui, Yao Zhihao, Luo Daowen, Peng Shuanglin, Yang Shuanglin, Wang Lang, Xiao Jingang. High fat and high sugar diet combined with streptozotocin to establish a rat model of type 2 diabetic osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1207-1211. |
| [3] | Li Zhongfeng, Chen Minghai, Fan Yinuo, Wei Qiushi, He Wei, Chen Zhenqiu. Mechanism of Yougui Yin for steroid-induced femoral head necrosis based on network pharmacology [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1256-1263. |
| [4] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [5] | Hou Guangyuan, Zhang Jixue, Zhang Zhijun, Meng Xianghui, Duan Wen, Gao Weilu. Bone cement pedicle screw fixation and fusion in the treatment of degenerative spinal disease with osteoporosis: one-year follow-up [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 878-883. |
| [6] | Li Shibin, Lai Yu, Zhou Yi, Liao Jianzhao, Zhang Xiaoyun, Zhang Xuan. Pathogenesis of hormonal osteonecrosis of the femoral head and the target effect of related signaling pathways [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 935-941. |
| [7] | Xiao Fangjun, Chen Shudong, Luan Jiyao, Hou Yu, He Kun, Lin Dingkun. An insight into the mechanism of Salvia miltiorrhiza intervention on osteoporosis based on network pharmacology [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 772-778. |
| [8] | Liu Bo, Chen Xianghe, Yang Kang, Yu Huilin, Lu Pengcheng. Mechanism of DNA methylation in exercise intervention for osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 791-797. |
| [9] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [10] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [11] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [12] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [13] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [14] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [15] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||

