Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (10): 1593-1602.doi: 10.12307/2023.277
Previous Articles Next Articles
Protective effect of stem cells on retinal ganglion cell regeneration
Zhang Chunli1, Liu Jingchen2, Zhou Wenjie1, Yu Yongzhen1, Tang Cuicui1, Zou Xiulan1, Zou Yuping1
- 1Department of Ophthalmology, General Hospital of Southern Theatre Command, Guangzhou 510010, Guangdong Province, China; 2Department of Ophthalmology, Jiangxi Provincial Hospital of Integrated Traditional Chinese and Western Medicine, The Fourth Affiliated Hospital of Jiangxi University of Traditional Chinese Medicine, Nanchang 330003, Jiangxi Province, China
-
Received:2022-04-02Accepted:2022-05-21Online:2023-04-08Published:2022-09-09 -
Contact:Zou Yuping, MD, Professor, Chief physician, Department of Ophthalmology, General Hospital of Southern Theatre Command, Guangzhou 510010, Guangdong Province, China -
About author:Zhang Chunli, Attending physician, Department of Ophthalmology, General Hospital of Southern Theatre Command, Guangzhou 510010, Guangdong Province, China -
Supported by:Medical Scientific Research Foundation of Guangdong Province, No. A2021377 (to ZCL); Specific Fund Program for Basic and Applied Basic Research of Guangdong Province, No. 2019A1515011732 (to ZYP); Guangzhou Science and Technology Program Project, No. 202002030413 (to ZYP)
CLC Number:
Cite this article
Zhang Chunli, Liu Jingchen, Zhou Wenjie, Yu Yongzhen, Tang Cuicui, Zou Xiulan, Zou Yuping. Protective effect of stem cells on retinal ganglion cell regeneration[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(10): 1593-1602.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
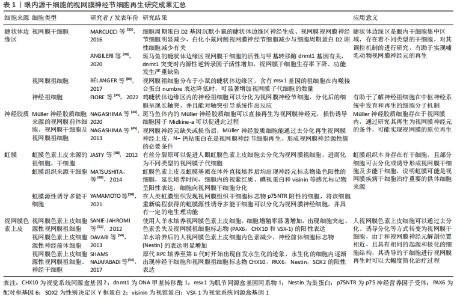
2.1 不同来源干细胞的视网膜神经节细胞再生作用 干细胞广泛存在于人和动物的组织器官中,由于组织来源的差异,不同类型的干细胞在活化状态、增殖潜能及细胞表面标志物等方面存在一定的差异。因此由其分化生成的视网膜神经节细胞的细胞表型、免疫原性及肿瘤形成风险等也存在一定的不同[8,29],将其进行分类,对细胞的再生研究具有重要意义。当前用于视网膜神经节细胞再生研究的干细胞根据其与眼部组织的关系可分为眼内源性干细胞和眼外源性干细胞。 2.1.1 眼内源性干细胞 视网膜干细胞及祖细胞:睫状体边缘区是在成熟的神经视网膜边缘发现的细胞环形区域,由视网膜干细胞和祖细胞组成[30]。在硬骨鱼和两栖动物等一些物种中,该区域能产生干细胞样特性的增殖细胞,并且能够在整个生命过程中持续分化出新的视网膜神经元[31],因而在视网膜再生领域被广泛地研究。MARCUCCI等[32]发现睫状体边缘区的视网膜神经节细胞形成与细胞周期调节因子有关,正常小鼠的该区中存在细胞周期蛋白D2的富集,而在细胞周期蛋白D2基因沉默的小鼠中,其睫状体边缘区的神经生成及视网膜神经节细胞明显减少,对白化小鼠视网膜研究也发现其同侧的视网膜神经节细胞减少与细胞周期蛋白D2阳性细胞减少有关,提示哺乳动物睫状体边缘区是产生视网膜神经节细胞的神经源性部位,其正常功能的产生依赖于细胞周期蛋白D2的活性。ANGILERI等[33]在斑马鱼视网膜研究中发现,斑马鱼眼内的睫状体边缘区内含有视网膜干细胞,当DNA甲基转移酶突变时,该区域的干细胞维持功能严重缺陷,内源性反转录因子活性增加,细胞死亡率升高,说明DNA甲基转移酶功能的缺失会导致睫状体边缘区细胞基因失调进而导致细胞死亡,在调节视网膜干细胞的增殖、基因表达和抑制内源性反转录因子活性中发挥着重要作用。BéLANGER等[34]在小鼠睫状体边缘区中发现了一组能表达msx1的祖细胞,该类细胞在分子和功能上都与传统的视网膜祖细胞存在不同,其分化的细胞表型与内噬接合蛋白numbre密切相关,numbre表达下降时Msx1祖细胞的视网膜子代细胞数量明显增加,有助于哺乳动物视网膜生成。FIORE等[35]对从鸡睫状体边缘区中获得的神经祖细胞研究发现,在适当的分化培养条件下,可以观察到神经祖细胞分化为视网膜神经节细胞,分化后的视网膜神经节细胞出现长轴突,并具有对轴突引导提示系统作出反应的能力。 有研究在与睫状体交界处的周边部视网膜组织中也发现干细胞的存在[36],JOHNSEN等[37]对成人眼部周边部视网膜标本进行研究发现,该部位视网膜存在着高密度的与祖细胞标记物共染色的细胞,对该细胞进行培养显示,增殖后的细胞生长出纤维突,其神经胶质纤维酸性蛋白和神经前体细胞标志物巢蛋白呈阳性,并且细胞中逐渐出现神经祖细胞和成熟光感受器标记物的表达,说明人周边视网膜中的细胞具有一定的祖细胞潜能,可以分化为具有关键视网膜标记物的细胞,具有神经再生的潜力。目前对于睫状体边缘区及周边部视网膜研究最为广泛,也证实了其中的干细胞能分化为视网膜神经元,但该区内的干细胞数量较少、分化能力受到限制,诱导其视网膜再生的细胞因子、组织微环境及细胞间相互作用的机制仍需探讨。 眼部组织细胞再编程:神经胶质细胞在低等脊椎动物中具有强大的再生潜力,但在哺乳动物中该功能受到明显的限制。由于其在视网膜组织的中心到外周均有分布,且部分类型的神经胶质细胞在视网膜损伤后能重新获得类似祖细胞的状态,因而在视网膜再生研究领域受到密切的关注[38-40]。人类视网膜含有3种类型的胶质细胞:小胶质细胞、星形胶质细胞和Müller细胞[41],其中Müller神经胶质细胞是视网膜中主要的神经胶质成分,它们是在发育过程中出现的最后一种视网膜细胞类型,具有维持视网膜稳态和完整性的功能[42]。研究证实在某些条件下,Müller细胞能分化为神经祖细胞,具有再生为神经元的能力[43]。NAGASHIMA等[44]研究发现斑马鱼体内Müller细胞视网膜神经元再生作用与损伤诱导的神经突生长促进因子密切相关,在其作用下Müller细胞大量增殖并再生出神经元,当该因子缺失时,细胞的再生能力则明显受到限制,另外NAGASHIMA等[45]还证实在视网膜神经元缺失或损伤时,N-钙粘蛋白介导的神经源性黏附在Müller细胞部分去分化、重新表达神经上皮标志物过程中发挥重要作用,是实现视网膜神经节细胞再生的必要条件,也是视网膜内部神经源性簇形成所必需。LENKOWSKI等[46]发现斑马鱼体的Müller细胞可以直接在内核层进行散在的、不对称的有丝分裂产生棒状的祖细胞,当视网膜神经元被破坏时,Müller细胞也可以短暂地去分化,进行神经上皮细胞特有的动力学核迁移,产生视网膜前体细胞再生出视网膜神经元。由于Müller神经胶质细胞在视网膜中广泛存在,并具有去分化为视网膜干细胞的能力,由其分化而来的神经节细胞直接定位于视网膜内,不需在视网膜中再次附着和整合,对实现神经节细胞的视网膜组织内原位再生具有重要意义,但目前Müller细胞分化为神经节细胞的精准性不高,诱导其分化的技术和细胞因子也还需进一步的研究。 虹膜色素上皮在实验室研究中显示出替代退化的光感受器的潜力[47]。JASTY等[48]发现有丝分裂原可以诱导人虹膜色素上皮细胞产生含神经球的祖细胞,并通过差异性表达基因分析观察到人虹膜色素上皮细胞来源的神经球向视网膜子代细胞分化的动态过程,表明这些细胞保持其自我更新的特性和沿着视网膜细胞谱系分化的能力,由此可见虹膜色素上皮细胞可能成为视网膜变性干细胞治疗供体细胞来源。MATSUSHITA等[49]将鸡胚胎虹膜组织中分离出的虹膜色素上皮及虹膜基质分别进行体外培养发现,两种虹膜组织都出现长突起的细长细胞,细胞中神经元标志物染色呈阳性,并逐渐出现感光细胞标记物的表达。YAMAMOTO等[50]将人类虹膜组织中表达神经营养因子受体的细胞进行重编程获得了虹膜源性多能干细胞,该干细胞能分化产生具有一定的电生理功能的视网膜神经元,证明部分虹膜组织细胞一定条件下能获得多能性,实现视网膜神经细胞的再生,由于眼部虹膜组织易于获取,并且其再生视网膜神经节细胞的已显示出具有一定的神经电生理特性,有望成为良好的细胞供体来源,但虹膜组织中的细胞类型较多,各细胞去分化的条件并不一致,需进一步研究其有效的诱导条件。 视网膜色素上皮细胞是维持光感受器功能和形成血-视网膜屏障所必需的单层细胞,在人体内,视网膜色素上皮细胞和视网膜神经元有着相同的起源和极化的细胞结构[51],因此通过一定条件诱导视网膜色素上皮细胞转分化为视网膜神经元或视网膜神经前体细胞成为可能。SANIE-JAHROMI等[52]发现经羊水处理后,视网膜色素上皮细胞的增殖率显著增加,出现细胞突起、色素丢失及视网膜祖细胞标志物的阳性表达。DAVARI等[53]发现羊水培养后的视网膜色素上皮细胞逐渐形成了包含色素细胞和非色素细胞的细胞球,检测发现这些球体中的神经前体细胞标志物明显增加,说明细胞向视网膜神经元方向分化。有研究对人眼原代视网膜色素上皮细胞进行培养发现,随着培养时间的增加,细胞开始出现自发的永生化迹象,细胞从贴壁生长逐渐转变为悬浮生长,细胞内的神经干细胞和视网膜祖细胞标志物出现阳性表达,证实了培养分化的细胞具有干细胞样特征[54]。文章总结了目前眼内源干细胞的视网膜神经节细胞再生研究成果,见表1。 "
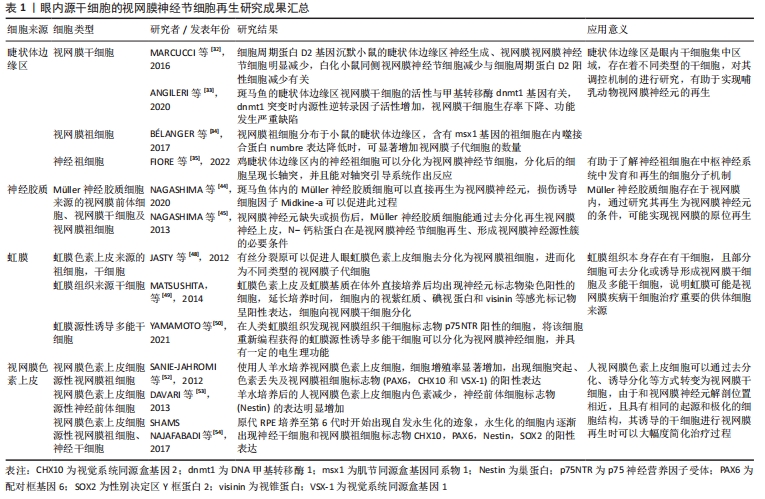

由此可见,视网膜色素上皮细胞具有转分化为视网膜干细胞及祖细胞的能力。当前人视网膜色素上皮细胞通过去分化为视网膜干细胞及祖细胞的技术尚处于初级研究阶段,多集中在对细胞标志物和电生理的分析性研究,距离临床应用还有很大的距离,但由于视网膜色素上皮和视网膜神经节细胞的解剖位置相近,且具有相同的起源和极化的细胞结构,其诱导的干细胞进行视网膜再生可以大幅度简化治疗过程。 2.1.2 眼外组织 在人体的一些组织中,由于自身增殖和组织修复需要存在着相当数量的干细胞,这些细胞根据功能和来源不同,有胚胎干细胞、诱导性多功能干细胞和成体干细胞等不同类型[55],在视网膜色素上皮的再生研究中,一些组织来源的干细胞显示出重要的应用价值[56],而对于有着相同的起源和极化的细胞结构视网膜神经节细胞,WEISS等[23-24,26-27]也开展了相关的治疗研究,报道了骨髓间充质干细胞在多种视神经相关性疾病中的临床应用,取得了一定的治疗效果,成体干细胞的开发应用,极大地扩展了视网膜神经节细胞再生的干细胞供体来源,对促进视神经疾病的研究和治疗具有重要意义,见表2。 "


胚胎相关细胞:是胚胎组织中的一类具有分化为3种原代胚层细胞的潜力[57]、来源稳定且能在体外大量扩增的细胞,广泛应用于疾病的基础与临床研究中。WANG等[58]发现视网膜分化培养基可以将人胚胎干细胞(H9-GFP)诱导分化出光学杯状结构,该结构中提取的视网膜祖细胞可以在N-甲基-d-天冬氨酸处理后的小鼠玻璃体腔中分化出含有视网膜神经节细胞特异性标记物Brn3a的细胞,并且能分布到神经节细胞层上,与宿主的视网膜神经节细胞在神经节细胞层上形成互补分布,表明从人胚胎干细胞中获得的视网膜祖细胞在体内可以整合到宿主视网膜神经节细胞层中并分化为视网膜神经节样细胞。APARICIO等[59]在体外将人胚胎干细胞培养出视网膜类器官,发现该器官中有视网膜神经节细胞标记物BRN3和RBPMS阳性的细胞存在,并在细胞分化形成过程中观察到与人类胎儿视网膜神经节细胞中结果接近的CD184和CD171差异表达,进一步证实了人胚胎干细胞具有分化为视网膜神经节细胞的潜力。在SINGH等[60]在人类胚胎干细胞衍生出的视网膜组织中发现成熟的光感受器免疫表型和发育的光感受器内段和外段的存在,将10-12周龄的人胚胎干细胞衍生视网膜组织与8-13周龄的人类胎儿视网膜对比发现,两者的基因表达谱和组织学谱有高度相关性。MCLELLAND等[61]发现人胚胎干细胞分化的视网膜移植薄片能在严重视网膜变性的大鼠模型视网膜中分化整合,产生功能性的感光器和其他视网膜细胞,通过视动测试和电生理检测发现大鼠的视觉在植入衍生的视网膜薄片后得到了改善。虽然胚胎干细胞在体外和动物实验显示出了良好的视网膜神经节细胞分化能力、并促进了视觉功能的改善,但由于人类胚胎组织在应用中存在伦理等因素的制约,取材也相对困难,其真正的临床应用还需进一步探讨。 生殖系干细胞:是一种具有分化为3个胚层能力的多能细胞,精原干细胞为成年雄性的生殖系干细胞。在生物体的整个生命周期中,精原干细胞通过自我增殖,能维持并分化成精子的细胞。在一些情况下精原干细胞也具有通过再编程转变为其他细胞的能力,研究表明精原干细胞可以在适当的条件下获得多能性,能通过再编程分化为神经前体细胞[62],预示着也具有分化为视网膜神经元的潜能。SUEN等[63]诱导精原干细胞去分化为与胚胎干细胞相似的细胞,再将该细胞向视网膜谱系分化,发现有视网膜神经节细胞特异性标记物阳性的细胞出现,该细胞表现出典型的视网膜神经节细胞基因表达模式,并且在电生理检测方面结果与真正的视网膜神经节细胞相似,移植入青光眼小鼠模型中可以存活较长时间。由此可见由精原干细胞再分化而来的细胞可能是一种替代视网膜受损视网膜神经节细胞的潜在细胞源,生殖系干细胞去分化后的干细胞与胚胎干细胞在基因表达特征和干细胞特性上类似,在一定程度上可以替代胚胎干细胞,但目前研究发现其在视网膜中存活时间虽然较长,但临床应用还有较大差距,另外其去分化和再分化的诱导条件是否影响移植后的细胞功能尚不明确。 成体干细胞:是位于人体内已分化组织中的未分化细胞群,广泛存在于血液、肠道、皮肤、肌肉、大脑和心脏等器官中,具备多能性和自我增殖的能力,能分化为所在器官的各类型细胞,对组织再生、维持体内平衡、能量代谢有重要作用[64-65]。近年来发现,成体干细胞不仅可分化为所属器官的细胞,在一定条件下也具有转化为其他组织细胞的能力,因而广泛应用于再生医学的研究中。目前研究证实包括骨髓间充质干细胞、牙周膜来源的干细胞和神经干细胞在内的多种成体干细胞具有分化为视网膜祖细胞及神经元的潜能[66]。骨髓间充质干细胞是来源于骨髓的多能干细胞,具有分化为成骨细胞、软骨细胞、脂肪细胞等多种类型细胞的能力,在视网膜神经节细胞的再生研究中也显示出良好的分化潜能,XU等[67]发现在视网膜细胞条件培养基中培养的大鼠骨髓间充质干细胞可以分化出视网膜神经节样细胞,且分化出的细胞与原代视网膜神经节细胞具有高度相似的蛋白质谱,说明在一定条件下骨髓间充质干细胞具有向视网膜神经节细胞转化的潜能。CEN等[68]将牙周膜干细胞注入视神经挤压伤大鼠模型的玻璃体腔内,发现该干细胞可以在玻璃体腔和视网膜神经节细胞层上存活,并且移植后的大鼠视网膜神经节细胞存活和再生轴突的数量显著增加,说明该干细胞具有一定的视神经保护和再生能力。成体干细胞的种类较多,细胞数量大,且在体外和动物实验中有较明确的视神经再生作用,是良好的细胞供体来源,但不同组织来源的干细胞分化而来的视网膜神经节细胞的移植成功率、分化细胞之间是否存在表型差异等尚不清楚。 诱导性多功能干细胞:是通过重编程技术从各种体细胞中诱导产生的多功能细胞[69],具有来源广泛、易获得、分化全能性及无伦理约束等诸多优点,广泛应用于疾病的细胞治疗研究中。诱导多能干细胞在眼部组织,如角膜及视网膜色素上皮等细胞的再生研究中已取得令人兴奋的结果,给疾病的治疗带来新的希望。近年来学者们也开展了这类细胞在视网膜神经节细胞再生中的研究,有研究发现人诱导多能干细胞通过培养可以形成三维的视网膜结构,其内中含有现神经元标记物和视网膜神经节细胞标志物阳性表达的细胞,该细胞可以生长出神经突,细胞间逐渐能形成类似神经突网络的结构,说明诱导多能干细胞具有分化为视网膜神经节细胞的能力,将三维的视网膜中的视网膜神经节细胞在聚乳酸-羟基乙酸共聚物支架中培养可以生长出树突结构和长的轴突,同时能在细胞中能检测到动作电位和静息膜电位的产生,将上述细胞生物工程支架植入兔眼和猴眼进行体内实验,未发现组织排斥反应和其他不良反应,可见诱导多能干细胞来源的视网膜神经节细胞具有良好的组织相容性和安全性,并具有一定的电生理功能[25]。HSU等[70]发现诱导多能干细胞分化来的视网膜神经节细胞有典型神经元形态,随着培养时间的增加,细胞的轴突分支延长并逐步分化为成熟形态,分化后的细胞内视网膜神经节细胞标志物呈阳性表达,通过膜片钳技术发现培养后期的细胞激发了高振幅动作电位,RABESANDRATANA等[1]发现在诱导多能干细胞分化的视网膜神经节细胞中,细胞表面标记物THY1阳性的细胞是可选择的细胞移植供体,这类细胞注射到患有视神经病变的小鼠玻璃体后,能有效地整合入宿主视网膜神经节细胞层中。由此可见,诱导多能干细胞可以分化为视网膜神经节细胞,能获得同质、有功能的、可供移植的视网膜神经节细胞群体,该细胞构建的生物支架也具有良好的组织相容性和安全性,但由于其是通过完全分化的成年体细胞去分化而来,再经过分化才能生成目标细胞,在该过程中使用了基因诱导及较多的转录因子,存在遗传稳定性不足、发生恶性肿瘤等潜在风险[71],其具体的临床治疗效果需后续研究进一步明确。作者总结了眼外源性干细胞的视网膜神经节细胞再生研究成果,见表3。 "


2.2 干细胞在视网膜神经节细胞保护中的作用 部分视神经发生病变的患者在去除诱发因素后,视网膜神经节细胞仍继续损伤,出现轴突退化、消失及细胞的凋亡。临床治疗中对于这类患者采取视神经保护治疗来挽救视力,但现有治疗方式的疗效欠佳,需开发新的神经保护策略。通过对既往研究结果的分析,发现干细胞有明确的视神经保护作用,可以通过表达神经营养因子、降低炎症反应、改善缺血和促进其他细胞重编程为视网膜干细胞等多种途径保护视网膜神经节细胞。 2.2.1 表达神经营养因子促进细胞的存活 神经营养因子是一类由神经支配的组织和星形胶质细胞产生的,为神经元生长与存活所必需的蛋白质分子,在神经元的发育、分化和维持中起重要作用[72-73]。研究发现神经营养因子的表达增加可以使视网膜神经节细胞在受损情况下的易于存活,并且具有促进受损细胞再生的潜力[74-75]。JI等[76]在高眼压大鼠模型中发现,人脐带间充质干细胞玻璃体腔移植后,能抑制胶质纤维酸性蛋白的产生,促进胶质源性神经营养因子及脑源性神经营养因子的表达,同时该干细胞出现轴突且数量逐渐增加,并逐渐迁移到内界膜下方及神经节细胞层中,使模型大鼠的暗视阈值反应明显增加。 色素上皮衍生因子是一种多功能分泌蛋白,通过在视网膜细胞之间相互作用,在体内和体外均能产生神经保护效应[77-78],ZHANG等[79]研究显示视神经损伤的大鼠视网膜下注射的神经干细胞具有分泌色素上皮衍生因子的功能,同时发现色素上皮衍生因子具有促进神经干细胞分化为星形胶质细胞和视网膜神经元的作用,色素上皮衍生因子与神经干细胞联合治疗,可以显著促进视神经损伤大鼠的视网膜神经节细胞存活和轴突再生。有研究发现骨髓间充质干细胞的外泌体和培养基对受伤大鼠和人干细胞来源的视网膜神经节细胞均具有显著的保护作用,加入肿瘤坏死因子α后,骨髓间充质干细胞分泌含色素上皮衍生因子和血管生长因子A的外泌体增加,使其对神经节细胞的保护作用增强,阻断肿瘤坏死因子α信号则发现其神经保护能力明显降低,说明骨髓间充质干细胞的视神经保护功能与色素上皮衍生因子和血管内皮生长因子A水平增加有关[80]。由此可见,分泌神经营养性细胞因子是干细胞促进视网膜神经节细胞存活的重要机制,但由于这类因子种类繁多,且不同来源的干细胞表达的神经营养因子并不一定相同,各神经营养因子对视网膜神经节细胞的保护效果的差异目前也并不明确,需要更多的研究来验证,以寻找出具有可靠神经营养功能的干细胞源。 2.2.2 降低细胞损伤后的炎症反应 局部炎症因子上调及免疫细胞浸润是视网膜退行性疾病的特征之一[81-82],在疾病的病理态下,眼内平衡的破坏,细胞因子失衡,血液视网膜屏障损伤和免疫细胞浸润等可以诱发眼内的炎症反应使细胞受损。受损的视网膜细胞、内源性及外源性免疫细胞产生大量促炎分子引起眼内组织的纤维化,使视网膜神经节细胞功能发生障碍、轴突变性,最终导致细胞死亡[83-86]。有研究发现骨髓间充质干细胞可以抑制玻璃体腔内注射促炎细胞因子诱导的小鼠视网膜免疫细胞浸润及炎症相关因子的表达,并且在炎症因子刺激的视网膜外植体实验中,骨髓间充质干细胞也显示出类似的免疫抑制效果[81]。JHA等[87]发现炎症细胞因子处理的脂肪干细胞浓缩条件培养基可以抑制小胶质细胞的激活、降低血管内皮通透性,进而保持视网膜屏障的完整;同时浓缩条件培养基也能减少创伤性脑损伤小鼠的视网膜神经节细胞损失及伤后胶质原纤维酸性蛋白的免疫反应性,在一定程度上减少脑损伤小鼠的视网膜形态学改变,降低视力和对比敏感度损失。在基础研究中,干细胞对视网膜炎症的抑制作用明确,但由于疾病发生后的视网膜神经节细胞的炎症反应并不一致,不同组织来源的干细胞在抗炎效果上可能也存在一定的差异,需要更多的实验数据来验证,另外伤后使用干细胞眼内注射的窗口期也需要进一步明确。 2.2.3 促进其他细胞重编程为视网膜干细胞 成年哺乳动物的视网膜干细胞可分化成视网膜的所有子代细胞类型[88],由于眼部组织中的视网膜干细胞数量相对较少、大范围的应用受限,当前研究的重点集中在干细胞数量的扩增及眼内其他类型的细胞重编程为干细胞。目前的研究证实视网膜色素上皮细胞、Müller神经胶质细胞及虹膜色素上皮细胞等多种组织细胞具有再分化为视网膜干细胞的潜能[89-92],但这些细胞由于组织微环境及解剖部位等因素的影响,导致其再编程为视网膜干细胞的功能受限,因此寻找促进这类细胞重编程为干细胞的条件及方法,对视网膜的再生研究具有重要意义。LI等[93]的研究中显示骨髓间充质干细胞可以使睫状缘色素细胞的存活率、细胞增殖指数增加,同时发现睫状缘色素细胞在体外培养情况下可以分化为视网膜干细胞相关标志物及感光器特异性基因阳性表达的细胞,这种分化作用在加入骨髓间充质干细胞后得到明显增强,说明睫状缘色素细胞具有转化为视网膜干细胞的潜能,在骨髓间充质干细胞组的作用下,可以促进睫状缘色素细胞的增殖及向视网膜干细胞方向转化。目前这类研究相对较少,虽然干细胞显示出明确的促色素上皮去分化的作用,但其机制尚不明确,对眼内其他组织细胞是否有类似作用,还需要深入研究。 2.2.4 改善视网膜缺血 视网膜缺血是多种眼病的常见病理机制[94],也是视力丧失和损害的主要原因,缺血状态下的视网膜神经节细胞的功能受到显著的影响,细胞发生凋亡并大量丢失[95],导致视神经相关疾病的发生和发展,常出现在青光眼、糖尿病视网膜病变、视网膜中央动脉阻塞等疾病中[96],到目前为止,尚未发现可用于预防和治疗视网膜神经节细胞缺血和再灌注损伤的药物[97]。近年来研究发现干细胞能够将健康和功能正常的线粒体转移到缺血性神经元及濒临灭绝的视网膜细胞中,替换受损细胞中有缺陷的线粒体,从而减少细胞死亡,使干细胞成为治疗视网膜缺血的新方法,JIANG等[98]使用绿色荧光蛋白标记人骨髓间充质干细胞,再将细胞诱导成多能干细胞后注射到线粒体功能缺陷的小鼠中,结果显示注射后的小鼠视网膜中的神经节细胞存活率显著增加,同时检测到含有荧光的线粒体进入神经节细胞中,并在小鼠视网膜中检测到人线粒体DNA的存在,说明线粒体转移在干细胞的视网膜神经节细胞保护作用密切相关。 另外干细胞对视网膜神经节细胞缺血损伤后的氧化应激水平调节也可能促进了细胞的存活,在LI等[99]的研究中发现过表达血红素加氧酶1的骨髓间充质干细胞能显著减轻过氧化氢对视网膜神经节细胞的损伤,降低细胞活性氧水平,激活抗凋亡蛋白并阻断促凋亡蛋白的表达,使细胞凋亡减少;在视网膜缺血再灌注的大鼠模型中,该干细胞处理后的大鼠视网膜厚度显著增加,细胞生存率提高,同时细胞内的抗氧化酶得到恢复,使视网膜的氧化应激水平明显降低。研究发现干细胞分泌的细胞外囊泡在视网膜神经节细胞功能保护中也发挥着重要作用,MATHEW等[96]发现骨髓间充质干细胞来源的细胞外囊泡能明显减少体外缺血模型中的视网膜神经节细胞死亡、促进细胞的增殖,将该干细胞的外囊泡注入视网膜缺血的大鼠玻璃体中,发现细胞外囊泡能被视网膜神经元、视网膜神经节细胞和小胶质细胞吸收,促进细胞功能的恢复,降低神经炎症和细胞凋亡。由此可见干细胞可以通过多种途径,对抗视网膜神经节细胞的缺血再灌注损伤,恢复神经节细胞功能,具有明显的神经保护作用。目前此类实验的观察期相对较短,干细胞在眼内维持作用的时间及其分泌体的细胞成分对眼内其他细胞的影响尚不并明确,需进行更多的研究,目前关于干细胞保护视网膜神经节细胞的作用机制研究成果见表4。 "

| [1] RABESANDRATANA O, CHAFFIOL A, MIALOT A, et al. Generation of a transplantable population of human ipsc-derived retinal ganglion cells. Front Cell Dev Biol. 2020;8:585675. [2] SLUCH VM, ZACK DJ. Stem cells, retinal ganglion cells and glaucoma. Dev Ophthalmol. 2014;53:111-121. [3] SMITH CA, VIANNA JR, CHAUHAN BC. Assessing retinal ganglion cell damage. Eye (Lond). 2017;31(2):209-217. [4] DANISZEWSKI MAO, SENABOUTH A, NGUYEN QH, et al. Single cell RNA sequencing of stem cell-derived retinal ganglion cells. Sci Data. 2018;5:180013. [5] LAHNE M, NAGASHIMA M, HYDE DR, et al. Reprogramming Müller Glia to Regenerate Retinal Neurons. Annu Rev Vis Sci. 2020;6:171-193. [6] 吴创.CNTF基因修饰骨髓间充质干细胞对碘酸钠致大鼠视网膜变性保护作用研究[D].福州:福建医科大学,2018. [7] ZAKIROVA EY, VALEEVA AN, AIMALETDINOV AM, et al. Potential therapeutic application of mesenchymal stem cells in ophthalmology. Exp Eye Res. 2019; 189:107863. [8] ACHBERGER K, HADERSPECK JC, KLEGER A, et al. Stem cell-based retina models. Adv Drug Deliv Rev. 2019;140:33-50. [9] GAZDIC M, VOLAREVIC V, HARRELL CR, et al. Stem cells therapy for spinal cord injury. Int J Mol Sci. 2018;19(4):1039. [10] ZAKRZEWSKI W, DOBRZYŃSKI M, SZYMONOWICZ M, et al. Stem cells: past, present, and future. Stem Cell Res Ther. 2019;10(1):68. [11] 张格,朱涵,张婧雯,等.诱导胚胎干细胞分化为视网膜色素上皮细胞的培养方法[J].国际眼科杂志,2020,20(12):2079-2082. [12] 贾艳妮.人胚胎干细胞诱导分化为角膜内皮样细胞的实验研究[D].青岛:青岛大学,2019. [13] MALLICK S, SHARMA M, KUMAR A, et al. Cell-based therapies for trabecular meshwork regeneration to treat glaucoma. Biomolecules. 2021;11(9):1258. [14] LAHA B, STAFFORD BK, HUBERMAN AD. Regenerating optic pathways from the eye to the brain. Science. 2017;356(6342):1031-1034. [15] SINGH MS, PARK SS, ALBINI TA, et al. Retinal stem cell transplantation: balancing safety and potential. Prog Retin Eye Res. 2020;75:100779. [16] HOLLYFIELD JG. Differential addition of cells to the retina in Rana pipiens tadpoles. Dev Biol. 1968;18(2):163-179. [17] STRAZNICKY K, GAZE RM. The growth of the retina in Xenopus laevis: an autoradiographic study. J Embryol Exp Morphol. 1971;26(1):67-79. [18] JOHNS PR. Growth of the adult goldfish eye. III. Source of the new retinal cells. J Comp Neurol. 1977;176(3):343-357. [19] FISCHER AJ, REH TA. Identification of a proliferating marginal zone of retinal progenitors in postnatal chickens. Dev Biol. 2000;220(2):197-210. [20] FISCHER AJ, REH TA. Müller glia are a potential source of neural regeneration in the postnatal chicken retina. Nat Neurosci. 2001;4(3):247-252. [21] LAWRENCE JM, SINGHAL S, BHATIA B, et al. MIO-M1 cells and similar muller glial cell lines derived from adult human retina exhibit neural stem cell characteristics. Stem Cells. 2007;25(8):2033-2043. [22] NAKANO T, ANDO S, TAKATA N, et al. Self-formation of optic cups and storable stratified neural retina from human ESCs. Cell Stem Cell. 2012; 10(6):771-785. [23] WEISS JN, LEVY S, BENES SC. Stem Cell Ophthalmology Treatment Study (SCOTS) for retinal and optic nerve diseases: a case report of improvement in relapsing auto-immune optic neuropathy. Neural Regen Res. 2015;10(9): 1507-1515. [24] WEISS JN, LEVY S, BENES SC. Stem Cell Ophthalmology Treatment Study (SCOTS): bone marrow-derived stem cells in the treatment of Leber’s hereditary optic neuropathy. Neural Regen Res. 2016;11(10):1685-1694. [25] LI K, ZHONG X, YANG S, et al. HiPSC-derived retinal ganglion cells grow dendritic arbors and functional axons on a tissue-engineered scaffold. Acta Biomater. 2017;54:117-127. [26] WEISS JN, LEVY S, BENES SC. Stem Cell Ophthalmology Treatment Study: bone marrow derived stem cells in the treatment of non-arteritic ischemic optic neuropathy (NAION). Stem Cell Investig. 2017;4:94. [27] WEISS JN, LEVY S. Stem Cell Ophthalmology Treatment Study (SCOTS): bone marrow derived stem cells in the treatment of Dominant Optic Atrophy. Stem Cell Investig. 2019;6:41. [28] BERNSTEIN SL, GUO Y, KERR C, et al. The optic nerve lamina region is a neural progenitor cell niche. Proc Natl Acad Sci U S A. 2020;117(32):19287-19298. [29] 王卓实. 视网膜祖细胞治疗视网膜变性的研究[D].沈阳:中国医科大学,2020. [30] FISCHER AJ, BOSSE JL, EL-HODIRI HM. The ciliary marginal zone (CMZ) in development and regeneration of the vertebrate eye. Exp Eye Res. 2013;116 (1096-0007 (Electronic)):199-204. [31] MILES A, TROPEPE V. Retinal stem cell ‘retirement plans’: growth, regulation and species adaptations in the retinal ciliary marginal zone. Int J Mol Sci. 2021;22(12):6528. [32] MARCUCCI F, MURCIA-BELMONTE V, WANG Q, et al. The ciliary margin zone of the mammalian retina generates retinal ganglion cells. Cell Rep. 2016;17(12):3153-3164. [33] ANGILERI KM, GROSS JM. dnmt1 function is required to maintain retinal stem cells within the ciliary marginal zone of the zebrafish eye. Sci Rep. 2020;10(1):11293. [34] BéLANGER MC, ROBERT B, CAYOUETTE M. Msx1-positive progenitors in the retinal ciliary margin give rise to both neural and non-neural progenies in mammals. Dev Cell. 2017;40(2):137-150. [35] FIORE L, OLMOS-CARREñO CL, MEDORI M, et al. Neurospheres obtained from the ciliary margin of the chicken eye possess positional values and retinal ganglion cells differentiated from them respond to EphA/ephrin-A system. Exp Eye Res. 2022;217:108965. [36] YAMADA K, MAENO T, KUSAKA S, et al. Recalcitrant macular hole closure by autologous retinal transplant using the peripheral retina. Clin Ophthalmol. 2020;14:2301-2306. [37] JOHNSEN EO, FRøEN RC, OLSTAD OK, et al. Proliferative cells isolated from the adult human peripheral retina only transiently upregulate key retinal markers upon induced differentiation. Curr Eye Res. 2018;43(3):340-349. [38] TODD L, SUAREZ L, QUINN C, et al. Retinoic acid-signaling regulates the proliferative and neurogenic capacity of müller glia-derived progenitor cells in the avian retina. Stem Cells. 2018;36(3):392-405. [39] EASTLAKE K, LAMB WDB, LUIS J, et al. Prospects for the application of Müller glia and their derivatives in retinal regenerative therapies. Prog Retin Eye Res. 2021;85:100970. [40] LANGHE R, PEARSON RA. Rebuilding the retina: prospects for müller glial-mediated self-repair. Curr Eye Res. 2020;45(3):349-360. [41] REICHENBACH A, BRINGMANN A. Glia of the human retina. Glia. 2020;68(4):768-796. [42] GOLDMAN D. Müller glial cell reprogramming and retina regeneration. Nat Rev Neurosci. 2014;15(7):431-442. [43] REICHENBACH A, BRINGMANN A. New functions of Müller cells. Glia. 2013; 61(5):651-678. [44] NAGASHIMA M, D’CRUZ TS, DANKU AE, et al. Midkine-a is required for cell cycle progression of müller glia during neuronal regeneration in the vertebrate retina. J Neurosci. 2020;40(6):1232-1247. [45] NAGASHIMA M, BARTHEL LK, RAYMOND PA. A self-renewing division of zebrafish Müller glial cells generates neuronal progenitors that require N-cadherin to regenerate retinal neurons. Development. 2013;140(22): 4510-4521. [46] LENKOWSKI JR, RAYMOND PA. Müller glia: stem cells for generation and regeneration of retinal neurons in teleost fish. Prog Retin Eye Res. 2014;40: 94-123. [47] DHAMODARAN K, SUBRAMANI M, PONNALAGU M, et al. Ocular stem cells: a status update!. Stem Cell Res Ther. 2014;5(2):56. [48] JASTY S, SRINIVASAN P, PASRICHA G, et al. Gene expression profiles and retinal potential of stem/progenitor cells derived from human iris and ciliary pigment epithelium. Stem Cell Rev Rep. 2012;8(4):1163-1177. [49] MATSUSHITA T, FUJIHARA A, ROYALL L, et al. Immediate differentiation of neuronal cells from stem/progenitor-like cells in the avian iris tissues. Exp Eye Res. 2014;123:16-26. [50] YAMAMOTO N, HIRAMATSU N, OHKUMA M, et al. Novel technique for retinal nerve cell regeneration with electrophysiological functions using human iris-derived iPS cells. Cells. 2021;10(4):743. [51] PAVAN B, DALPIAZ A. Retinal pigment epithelial cells as a therapeutic tool and target against retinopathies. Drug Discov Today. 2018;23(9):1672-1679. [52] SANIE-JAHROMI F, AHMADIEH H, SOHEILI ZS, et al. Enhanced generation of retinal progenitor cells from human retinal pigment epithelial cells induced by amniotic fluid. BMC Res Notes. 2012;5:182. [53] DAVARI M, SOHEILI Z S, AHMADIEH H, et al. Amniotic fluid promotes the appearance of neural retinal progenitors and neurons in human RPE cell cultures. Mol Vis. 2013;19:2330-2342. [54] SHAMS NAJAFABADI H, SOHEILI ZS, SAMIEI S, et al. Isolation, characterization, and establishment of spontaneously immortalized cell line HRPE-2S with stem cell properties. J Cell Physiol. 2017;232(10):2626-2640. [55] 孙颖健,郑雅娟.干细胞移植治疗视网膜神经节细胞损伤性疾病的研究进展[J]. 国际眼科杂志,2015,15(4):630-632. [56] WANG Y, TANG Z, GU P. Stem/progenitor cell-based transplantation for retinal degeneration: a review of clinical trials. Cell Death Dis. 2020;11(9): 793. [57] HUA ZQ, LIU H, WANG N, et al. Towards stem cell-based neuronal regeneration for glaucoma. Prog Brain Res. 2020;257:99-118. [58] WANG ST, CHEN LL, ZHANG P, et al. Transplantation of retinal progenitor cells from optic cup-like structures differentiated from human embryonic stem cells in vitro and in vivo generation of retinal ganglion-like cells. Stem Cells Dev. 2019;28(4):258-267. [59] APARICIO JG, HOPP H, CHOI A, et al. Temporal expression of CD184(CXCR4) and CD171(L1CAM) identifies distinct early developmental stages of human retinal ganglion cells in embryonic stem cell derived retina. Exp Eye Res. 2017;154:177-189. [60] SINGH RK, WINKLER PA, BINETTE F, et al. Comparison of developmental dynamics in human fetal retina and human pluripotent stem cell-derived retinal tissue. Stem Cells Dev. 2021;30(8):399-417. [61] MCLELLAND BT, LIN B, MATHUR A, et al. Transplanted hesc-derived retina organoid sheets differentiate, integrate, and improve visual function in retinal degenerate rats. Invest Ophthalmol Vis Sci. 2018;59(6):2586-2603. [62] KIM BJ, LEE YA, KIM KJ, et al. Effects of paracrine factors on CD24 expression and neural differentiation of male germline stem cells. Int J Mol Med. 2015; 36(1):255-262. [63] SUEN HC, QIAN Y, LIAO J, et al. Transplantation of retinal ganglion cells derived from male germline stem cell as a potential treatment to glaucoma. Stem Cells Dev. 2019;28(20):1365-1375. [64] GURUSAMY N, ALSAYARI A, RAJASINGH S, et al. Adult stem cells for regenerative therapy. Prog Mol Biol Transl Sci. 2018;160:1-22. [65] FINKEL Z, ESTEBAN F, RODRIGUEZ B, et al. Diversity of adult neural stem and progenitor cells in physiology and disease. Cells. 2021;10(8):2045. [66] 黄育强.Notch信号通路在人脂肪干细胞分化:视网膜细胞中的调控[D].汕头:汕头大学,2018. [67] XU C, LU H, LI F, et al. Protein expression profile on differentiation of bone marrow mesenchymal stem cells into retinal ganglion-like cells. J Comput Biol. 2020;27(8):1329-1336. [68] CEN LP, NG TK, LIANG JJ, et al. Human periodontal ligament-derived stem cells promote retinal ganglion cell survival and axon regeneration after optic nerve injury. Stem Cells. 2018;36(6):844-855. [69] HARVEY JP, SLADEN PE, YU-WAI-MAN P, et al. Induced pluripotent stem cells for inherited optic neuropathies-disease modeling and therapeutic development. J Neuroophthalmol. 2022;42(1):35-44. [70] HSU CC, CHIEN KH, YARMISHYN AA, et al. Modulation of osmotic stress-induced TRPV1 expression rescues human iPSC-derived retinal ganglion cells through PKA. Stem Cell Res Ther. 2019;10(1):284. [71] FENG X, CHEN P, ZHAO X, et al. Transplanted embryonic retinal stem cells have the potential to repair the injured retina in mice. BMC Ophthalmol. 2021;21(1):26. [72] 张惟,王月欣,陈松,等.玻璃体腔注射人脐带间充质干细胞诱导分化的神经干细胞对糖尿病大鼠视网膜脑源性神经营养因子表达及视网膜神经节细胞计数的影响[J].中华眼底病杂志,2016,32(6):601-604. [73] 刘保国,张龙,黄伟,等.CNTF转染人脐血干细胞复合壳聚糖支架移植对视神经损伤大鼠视网膜神经节细胞存活的影响[J].中华神经医学杂志,2015,14(11):1152-1155. [74] FUDALEJ E, JUSTYNIARSKA M, KASAREŁŁO K, et al. Neuroprotective factors of the retina and their role in promoting survival of retinal ganglion cells: a review. Ophthalmic Res. 2021;64(3):345-355. [75] CHEN DW, NARSINENI L, FOLDVARI M. Multipotent stem cell-derived retinal ganglion cells in 3D culture as tools for neurotrophic factor gene delivery system development. Nanomedicine. 2019;21:102045. [76] JI S, LIN S, CHEN J, et al. Neuroprotection of transplanting human umbilical cord mesenchymal stem cells in a microbead induced ocular hypertension rat model. Curr Eye Res. 2018;43(6):810-820. [77] BüRGER S, MENG J, ZWANZIG A, et al. Pigment epithelium-derived factor (PEDF) receptors are involved in survival of retinal neurons. Int J Mol Sci. 2020;22(1):369. [78] PAGAN-MERCADO G, BECERRA SP. Signaling mechanisms involved in PEDF-mediated retinoprotection. Adv Exp Med Biol. 2019;1185:445-449. [79] ZHANG WMM, ZHANG ZRM, ZHANG YGM, et al. Neural stem cell-based intraocular administration of pigment epithelium-derived factor promotes retinal ganglion cell survival and axon regeneration after optic nerve crush injury in rat: an experimental study. Iran J Med Sci. 2016;41(5):382-390. [80] MEAD B, CHAMLING X, ZACK DJ, et al. TNFα-mediated priming of mesenchymal stem cells enhances their neuroprotective effect on retinal ganglion cells. Invest Ophthalmol Vis Sci. 2020;61(2):6. [81] HERMANKOVA B, KOSSL J, BOHACOVA P, et al. The immunomodulatory potential of mesenchymal stem cells in a retinal inflammatory environment. Stem Cell Rev Rep. 2019;15(6):880-891. [82] BADIA A, SALAS A, DUARRI A, et al. Transcriptomics analysis of Ccl2/Cx3cr1/Crb1(rd8) deficient mice provides new insights into the pathophysiology of progressive retinal degeneration. Exp Eye Res. 2021;203:108424. [83] 张惟,陈松.间充质干细胞对糖尿病视网膜病变炎症反应调节作用的研究进展[J].中华眼底病杂志,2016,32(2):221-224. [84] GAO Y, HU S, LI Q, et al. Neonatal inflammation induces reorganization in dendritic morphology of retinal ganglion cells but not their retinogeniculate projection in mice. Neurosci Lett. 2018;676:34-40. [85] STEPP MA, MENKO AS. Immune responses to injury and their links to eye disease. Transl Res. 2021;236:52-71. [86] KRISHNAN A, KOCAB AJ, ZACKS DN, et al. A small peptide antagonist of the Fas receptor inhibits neuroinflammation and prevents axon degeneration and retinal ganglion cell death in an inducible mouse model of glaucoma. J Neuroinflammation. 2019;16(1):184. [87] JHA KA, PENTECOST M, LENIN R, et al. Concentrated conditioned media from adipose tissue derived mesenchymal stem cells mitigates visual deficits and retinal inflammation following mild traumatic brain injury. Int J Mol Sci. 2018;19(7):2016. [88] GRISé KN, BAUTISTA NX, JACQUES K, et al. Glucocorticoid agonists enhance retinal stem cell self-renewal and proliferation. Stem Cell Res Ther. 2021; 12(1):83. [89] LI B, JIANG H, LI H, et al. Direct conversion of adult human retinal pigmented epithelium cells to neurons with photoreceptor properties. Exp Biol Med (Maywood). 2021;246(2):240-248. [90] BONILLA-PONS S, NAKAGAWA S, BAHIMA EG, et al. Müller glia fused with adult stem cells undergo neural differentiation in human retinal models. EBioMedicine. 2022;77:103914. [91] TOO LK, SIMUNOVIC MP. Retinal stem/progenitor cells derived from adult Müller glia for the treatment of retinal degeneration. Front Cell Dev Biol. 2021;9:749131. [92] MATSUSHITA T, STEINFELD J, FUJIHARA A, et al. Regulation of neuronal and photoreceptor cell differentiation by Wnt signaling from iris-derived stem/progenitor cells of the chick in flat vs. Matrigel-embedding cultures. Brain Res. 2019;1704:207-218. [93] LI Y, HE X, LI J, et al. Proliferation and differentiation of direct co‑culture of bone marrow mesenchymal stem cells and pigmented cells from the ciliary margin. Mol Med Rep. 2017;15(6):3529-3534. [94] WIEMANN S, YOUSF A, JOACHIM SC, et al. Knock-out of tenascin-c ameliorates ischemia-induced rod-photoreceptor degeneration and retinal dysfunction. Front Neurosci. 2021;15:642176. [95] LIU W, XIA F, HA Y, et al. Neuroprotective effects of hsf1 in retinal ischemia-reperfusion injury. Invest Ophthalmol Vis Sci. 2019;60(4):965-977. [96] MATHEW B, RAVINDRAN S, LIU X, et al. Mesenchymal stem cell-derived extracellular vesicles and retinal ischemia-reperfusion. Biomaterials. 2019; 197:146-160. [97] YAO F, ZHANG X, YAO X, et al. Peroxisome proliferator-activated receptor α activation protects retinal ganglion cells in ischemia-reperfusion retinas. Front Med (Lausanne). 2021;8:788663. [98] JIANG D, XIONG G, FENG H, et al. Donation of mitochondria by iPSC-derived mesenchymal stem cells protects retinal ganglion cells against mitochondrial complex I defect-induced degeneration. Theranostics. 2019;9(8):2395-2410. [99] LI L, DU G, WANG D, et al. Overexpression of heme oxygenase-1 in mesenchymal stem cells augments their protection on retinal cells in vitro and attenuates retinal ischemia/reperfusion injury in vivo against oxidative stress. Stem Cells Int. 2017;2017:4985323. [100] Behtaj S, Rybachuk M. Strategies on the application of stem cells based therapies for the treatment of optic neuropathies. Neural Regen Res. 2021; 16(6):1190-1191. [101] Harrell CR, Fellabaum C, Arsenijevic A, et al. Therapeutic potential of mesenchymal stem cells and their secretome in the treatment of glaucoma. Stem Cells Int. 2019;2019:7869130. [102] GERMAN OL, VALLESE-MAURIZI H, SOTO TB, et al. Retina stem cells, hopes and obstacles. World J Stem Cells. 2021;13(10):1446-1479. |
| [1] | Dang Yi, Du Chengyan, Yao Honglin, Yuan Nenghua, Cao Jin, Xiong Shan, Zhang Dingmei, Wang Xin. Hormonal osteonecrosis and oxidative stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1469-1476. |
| [2] | Yang Zhishan, Tang Zhenglong. YAP/TAZ, a core factor of the Hippo signaling pathway, is involved in bone formation [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1264-1271. |
| [3] | Liu Xiaolin, Mu Xinyue, Ma Ziyu, Liu Shutai, Wang Wenlong, Han Xiaoqian, Dong Zhiheng. Effect of hydrogel-loaded simvastatin microspheres on osteoblast proliferation and differentiation [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 998-1003. |
| [4] | Xu Cong, Zhao He, Sun Yan. Regeneration of facial nerve injury repaired by biomaterial nerve conduits [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1089-1095. |
| [5] | Xue Ting, Zhang Xinri, Kong Xiaomei. Mesenchymal stem cell therapy for pneumoconiosis using nanomaterials combined with multi-modal molecular imaging [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1133-1140. |
| [6] | Tian Qinyu, Tian Xinggui, Tian Zhuang, Sui Xiang, Liu Shuyun, Lu Xiaobo, Guo Quanyi. Protection of manganese oxide nanoparticles for bone marrow mesenchymal stem cell spreading against oxidative stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 821-826. |
| [7] | Liu Wentao, Feng Xingchao, Yang Yi, Bai Shengbin. Effect of M2 macrophage-derived exosomes on osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 840-845. |
| [8] | Long Yanming, Xie Mengsheng, Huang Jiajie, Xue Wenli, Rong Hui, Li Xiaojie. Casein kinase 2-interaction protein-1 regulates the osteogenic ability of bone marrow mesenchymal stem cells in osteoporosis rats [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 878-882. |
| [9] | Cui Lianxu, Jiang Wenkang, Lu Dahong, Xu Junrong, Liu Xiaocui, Wang Bingyun. Clinical-grade human umbilical cord mesenchymal stem cells affect the improvement of neurological function in rats with traumatic brain injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 835-839. |
| [10] | Li Xinyue, Li Xiheng, Mao Tianjiao, Tang Liang, Li Jiang. Three-dimensional culture affects morphology, activity and osteogenic differentiation of human periodontal ligament stem cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 846-852. |
| [11] | Li Qicheng, Deng Jin, Fu Xiaoyang, Han Na. Effects of bone marrow mesenchymal stem cells-derived exosomes on hypoxia-treated myoblasts [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 853-859. |
| [12] | Wang Min, Yin Xiushan, Wang Yingxi, Zhang Yan, Zhao Long, Xia Shuyue. Inhalation of bone marrow mesenchymal stem cells-derived exosomes alleviates inflammatory injury in chronic obstructive pulmonary disease [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 827-834. |
| [13] | Yuan Wei, Liu Jingdong, Xu Guanghui, Kang Jian, Li Fuping, Wang Yingjie, Zhi Zhongzheng, Li Guanwu. Osteogenic differentiation of human perivascular stem cells and its regulation based on Wnt/beta-catenin signaling pathway [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 866-871. |
| [14] | Qiao Luhui, Ma Ziyu, Guo Haoyu, Hou Yudong. Comparison of puerarin and icariin on the biological properties of mouse preosteoblasts [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 872-877. |
| [15] | Hao Liufang, Duan Hongmei, Wang Zijue, Hao Fei, Hao Peng, Zhao Wen, Gao Yudan, Yang Zhaoyang, Li Xiaoguang. Spatiotemporal dynamic changes of ependymal cells after spinal cord injury in transgenic mice [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 883-889. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||