Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (14): 2234-2241.doi: 10.12307/2023.144
Previous Articles Next Articles
Effect of parathyroid hormone and parathyroid hormone-related peptides on tissue remodeling during orthodontics
Sun Xiaotong, Cheng Yi, Bi Lan, Wang Huida
- Department of Orthodontics, Affiliated Hospital of Binzhou Medical University, Binzhou 256600, Shandong Province, China
-
Received:2022-04-15Accepted:2022-05-24Online:2023-05-18Published:2022-09-30 -
Contact:Zhang Ronghe, Master, Chief physician, Master’s supervisor, Department of Orthodontics, Affiliated Hospital of Binzhou Medical University, Binzhou 256600, Shandong Province, China -
About author:Sun Xiaotong, Master candidate, Department of Orthodontics, Affiliated Hospital of Binzhou Medical University, Binzhou 256600, Shandong Province, China
CLC Number:
Cite this article
Sun Xiaotong, Cheng Yi, Bi Lan, Wang Huida. Effect of parathyroid hormone and parathyroid hormone-related peptides on tissue remodeling during orthodontics[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(14): 2234-2241.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
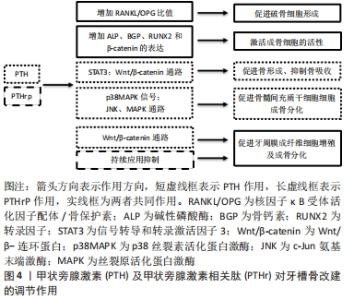
PTHrP最初是在研究成骨细胞恶性肿瘤引起高钙血症的过程中发现的一种多肽,由141个氨基酸残基组成[8]。PTHrP在结构上与甲状旁腺激素有很高的相似性。两者都能够结合PTH/PTHrP 1型受体(parathyroid hormone 1receptor,PTH1R),与其相结合后能够激活Gs/cAMP/PKA、Gq/11/PLC/PKC等信号通路[9],并具有类似的生物学特性[10],都参与调控成骨细胞的分化增殖,影响骨骼改建与代谢。与甲状旁腺激素相比,PTHrP对成骨的抑制作用和对破骨细胞的刺激作用均较小。PTHrP已知在各种类型的胚胎组织和器官中表达,如软骨、骨、皮肤、毛囊、乳腺[11]。且越来越多研究证实了甲状旁腺激素和PTHrP在牙体组织形成过程中起重要作用[12-13]。 2.2 对正畸过程中组织改建的影响 2.2.1 对牙槽骨改建的影响 牙齿移动是对施加于牙齿的机械刺激的生物反应的结果,是通过牙槽骨改建实现的,因此,牙齿移动的加速就需要加速牙槽骨的改建。如何在保证牙槽骨高度、密度的同时加快牙周膜压力侧骨组织吸收与牙周膜张力侧骨组织形成,是加快牙齿移动和维持正畸稳定的关键之一,也是正畸医生关注的焦点问题。诱导牙齿移动的手术方法从相对简单的药物治疗、物理治疗到相对复杂的外科手术治疗不一而足。牙齿移动的效率取决于正畸牙压力侧的骨吸收和骨重建,在健康的骨骼中,吸收和形成是耦合和平衡的,以维持骨量。甲状旁腺激素对骨代谢的调节作用对加速牙齿移动有着重要意义,甲状旁腺激素通过成骨细胞介导的骨形成和破骨细胞介导的骨吸收来加速骨转换[14]。间歇性服用甲状旁腺素影响骨形成并改善骨密度。甲状旁腺激素同时刺激骨形成和骨吸收,这取决于它的剂量方案[6-7]。 早前SOMA等[15]为验证甲状旁腺激素对大鼠正畸牙移动的影响,通过在大鼠背颈区持续注入甲状旁腺激素10-100 μg/(kg·d),并用正畸拉簧拉磨牙向前,使磨牙近中移动速度提高两三倍,证实了甲状旁腺激素对大鼠正畸牙移动的促进作用。TAKANO等[16]研究发现,局部注射甲状旁腺激素会导致局部骨吸收,局部注射甲状旁腺激素较全身注射更为有利。SOMA等[17]进一步证实长时间保持甲状旁腺激素局部浓度的缓释应用的开发非常有效,隔天局部应用甲状旁腺激素缓释凝胶制剂2.5 μg/kg也可以加速正畸牙齿移动。LI等[18]报道,每天皮下注射40 mg/kg甲状旁腺激素加速了大鼠上颌第一磨牙的正畸移动。SALAZAR等[19]实验得到了同样的结果,去卵巢骨质疏松大鼠皮下注射30 mg/(kg·d) 甲状旁腺激素,术后第7天正畸牙移动速度较未去卵巢骨质疏松大鼠显著增加。近年来LI等[20]发现下颌升支截骨术后通过重组人甲状旁腺激素(1-34)(recombinant human parathyroid hormone 1-34,rhPTH 1-34)间歇给药,促进了正畸牙移动,且呈剂量依赖性,高剂量甲状旁腺激素可进一步促进正畸牙受压侧核因子κB受体活化因子配体(receptor activator of nuclear factor-κB ligand,RANKL)的表达,抑制RUNX2的表达,加速下颌升支截骨后牙周骨组织改建和早期正畸牙移动。张程等[21]通过构建大鼠牙移动模型获得结论,间歇性甲状旁腺激素可能通过激活STAT3促进正畸张力侧牙槽骨的成骨活动。大量研究证实了甲状旁腺激素对正畸牙移动的促进作用。 由于骨吸收限制了正畸牙移动的速度,相关研究一直集中在促进压力侧破骨细胞的生成上,然而,当单独加强骨吸收时,牙齿在骨支持不足的情况下会变得过于可移动,进而导致牙齿松动甚至脱落。因此,一种理想的促进正畸牙移动的药物很可能具有同时促进破骨细胞生成和成骨的潜力。最新研究表明,在局部注射甲状旁腺激素或PTHrP水凝胶后加力可以促进成骨细胞分化,包括通过增加RANKL/OPG比值促进破骨细胞形成,通过增加碱性磷酸酶(ALP)、骨钙素(BGP)、RUNX2和β-catenin的表达促进成骨,使得骨改建更加活跃,从而加快正畸牙移动。机械刺激下甲状旁腺激素/PTHrP影响骨转换的确切信号通路有待进一步研究[22]。甲状旁腺激素及PTHrP对正畸治疗中牙齿移动确实能够起到加速作用,其效果取决于药物浓度、给药时间和药物释放时间,临床使用需要在药物的持续时间、剂量、方式和频率方面进行更精细的方案设计。 为了改善功能和美观,越来越多的牙周患者寻求正畸治疗,适当的正畸-牙周联合治疗可以改善牙周状况,间歇性甲状旁腺激素通过促进牙周炎大鼠牙槽骨的成骨和抑制牙槽骨的骨吸收来预防正畸牙移动过程中牙槽骨丢失。间歇性甲状旁腺激素促进成骨细胞分化,并可能以STAT3依赖的方式进一步调节Wnt/β-catenin通路,从而减少牙周炎大鼠正畸牙齿移动过程中的牙槽骨丢失[23]。甲状旁腺激素对重度牙周炎的骨组织再生有协同促进作用,WANG等[24]进一步证实甲状旁腺激素通过p38丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)信号转导促进人骨髓间充质干细胞向成骨细胞分化。QIN等[25]实验发现甲状旁腺激素通过JNK MAPK途径促进人骨髓间充质干细胞成骨分化。 复发是指正畸治疗结束后牙齿和颌骨都具有的退回到原始位置的趋势,在临床上很常见。在正畸治疗结束时,牙齿被强迫到理想的位置,而牙周组织的重塑还没有完全完成。在正畸力的作用下,牙周韧带中仍然储存着应力和应变,导致正畸矫治器移除后牙齿移位。因此为了降低复发风险,多建议患者在矫治结束后佩戴保持器至少2年。然而,这对患者来说较为困难,在经历了较长的矫治期后还要佩戴保持器,周期长且看不到明显效果使得患者容易放松懈怠,继而出现复发的情况。因此,如何在正畸治疗后促进牙周组织改建,保持牙周组织的长期稳定性,是正畸医生关注的问题。由于甲状旁腺激素治疗可以促进骨形成和提高骨密度,因此认为可以增加正畸结果的稳定性。李琴等[26]通过处理小鼠原代骨髓间充质细胞和卵巢切除致颌骨疏松的小鼠,体外和体内观察重组PTHrP1-36可促进骨髓间充质细胞的成骨分化,并促进牙槽骨骨密度和骨量的增加。LEE等[27]在动物实验中发现甲状旁腺激素对骨质疏松大鼠模型的牙齿移动没有促进作用,但确实导致复发距离和复发率的相对降低。LI等[28]研究结果也证实了这一点,通过采用体内和体外两种方法,验证了间歇性应用甲状旁腺激素在体内可通过促进牙周再生提高牙齿移动的稳定性,在体外可促进成牙本质细胞增殖和减少凋亡;并推断胰岛素样生长因子1可能在介导间歇性甲状旁腺激素的合成代谢效应中起重要作用。 骨开窗与骨开裂是比较常见的牙槽骨萎缩缺损后的症状,也是正畸治疗中发生的常见并发症,可能原因有牙齿移动速度过快、牙齿超限移动、转矩控制不良等,从而导致局部牙槽骨、牙周膜缺损,继而牙槽骨萎缩,牙龈萎缩。在一些骨修复动物模型中,甲状旁腺激素(或类似物、多肽)可以促进修复部位的骨形成。VASCONCELOS等[29]发现间歇性甲状旁腺激素可以加速大鼠骨开窗缺损处的牙周组织愈合,同对照组相比应用间歇性甲状旁腺激素组有明显的牙槽骨生成和牙周新附着,并推测这与间歇性甲状旁腺激素刺激导致牙周膜成纤维细胞的功能活化有关。甲状旁腺激素在骨折愈合和正畸治疗中能够增强机械负荷诱导的骨形成,LI等[30]经体外实验验证甲状旁腺激素通过Wnt/β-catenin通路参与了牙周膜成纤维细胞的成骨机制。WANG等[31]发现:牙周膜成纤维细胞表达较高水平的PTH1R,可以像成骨细胞一样对甲状旁腺激素做出反应。小剂量间歇性甲状旁腺激素处理后,牙周膜成纤维细胞的碱性磷酸酶活性和矿化能力升高,Runx2和Sp7基因表达显著调,有利于牙槽骨及牙骨质的再生。在此基础上,LU等[22]进行了体外实验,以进一步验证持续应用PTHrP抑制了人牙周膜成纤维细胞的成骨分化。 综上所述,甲状旁腺激素及PTHrP可以通过作用于成骨细胞、破骨细胞、人骨髓间充质干细胞及牙周膜成纤维细胞,调节其增殖和分化,进而影响牙槽骨组织改建,使得牙齿移动速度、正畸效果维持、牙周组织损伤等得到改善,但对产生的具体效应是促进还是阻碍,取决于其浓度、作用时间和作用方式,有待进一步探索,见图4,表1。 "
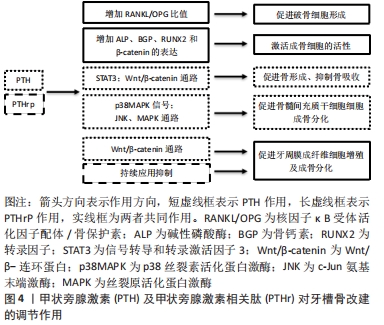

2.2.2 对颞下颌关节改建的影响 正畸治疗中功能矫治器等通过改变下颌的位置来调整咬合关系,这需要颞下颌关节的改建。同时临床中发现颞下颌关节紊乱病发病率较高,多数患者有关节弹响的症状,有疼痛症状将影响患者接受正畸治疗。错牙合畸形可能是颞下颌关节紊乱病的诱发因素之一,但颞下颌关节紊乱发展到一定程度同样会反过来导致或加重咬合关系改变及面形改变,正畸治疗中应尽量预防或改善颞下颌关节相关症状。颞下颌关节由颞骨的关节窝、下颌骨的髁状突和介于颞下窝和髁突之间的纤维软骨关节盘组成。髁突软骨与发育中的四肢软骨不同,属于次级软骨,经历软骨内骨化,表现出独特的发育和生长过程。已知PTH1R贯穿于整个软骨细胞的增殖与前肥大演变过程[32],甲状旁腺激素与PTHrP均参与调控关节软骨细胞的增殖与分化,可抑制骨关节炎软骨细胞的肥大分化及凋亡,促进其增殖,从而对骨关节炎软骨细胞起到保护作用[33]。近年来开始关注甲状旁腺激素与PTHrP对颞下颌关节的作用,为降低正畸治疗风险和颞下颌关节修复再生提供思路和研究方向。动物实验表明,功能矫治前导下颌后,髁突软骨中PTHrP的表达明显上调,该过程可能通过触发PTHrP进而促进关节软骨细胞中间充质细胞的成软骨向分化及软骨基质的形成,减缓细胞的成熟从而延长下颌骨生长周期[34],这一结果使得PTHrP有希望作为辅助手段协同促进治疗。 甲状旁腺激素对髁突软骨细胞增殖、分化的调节同样具有双向作用,效果取决于其作用方式[35]。持续性应用甲状旁腺激素促进髁突软骨细胞的增殖而抑制其分化,间歇性应用甲状旁腺激素抑制髁突软骨细胞的增殖而促进其分化。在颞下颌关节间歇或持续关节内注射甲状旁腺激素可以促进下颌髁突成骨或诱导骨吸收,可能是治疗下颌不对称的一种新方法,通过调节甲状旁腺激素的给药频率来控制下颌生长比率,以避免矫治过度,但相关机制仍需进一步研究[36]。CUI等[37]研究发现甲状旁腺激素可能通过抑制p16INK4a,减少衰老细胞在软骨下的堆积,改善骨髓微环境,促进骨重建,提示甲状旁腺激素对老年退化性颞下颌关节骨性关节炎有潜在的防治作用。DUTRA等[38]第一次证明长期间歇性应用甲状旁腺激素可促进下颌骨髁状突合成代谢和软骨下骨的矿化,同时保持关节人骨细胞未矿化部分的完整性,增加软骨的厚度。此外,在体外间歇性甲状旁腺激素处理的软骨细胞中,蛋白多糖4(Prg4)的相对基因表达显著增加。蛋白多糖4在骨和关节中高表达,对关节有保护和抗炎作用,已被确定为甲状旁腺激素促进骨骼合成代谢的新靶点。因此认为间歇性甲状旁腺激素可能通过刺激蛋白多糖4在下颌髁突起保护作用。 PTHrP是髁突软骨生长发育的关键调控蛋白,在下颌骨髁突软骨生长发育过程中通过IHH/PTHrP经典信号通路[39]、Notch信号的协同作用等多种信号发挥重要作用[40]。那些尚未发掘的甲状旁腺激素对关节然骨细胞的作用影响应该会激发未来的研究,在将其转化为患者应用之前,需要更长的观察期。关于不同信号通路在颞下颌关节正常生长发育过程中的作用以及引起骨关节炎的病理变化已经有了很大的进展,但仍有许多问题需要深入研究。未来的研究需要定义多个信号通路之间的相互作用,并确定它们之间的串联如何指导颞下颌关节的形态发生,以及更广泛的骨和软骨的分化。这些研究结果将为开发修复颞下颌关节先天畸形和后天性退行性骨关节炎损伤的新方法提供坚实的基础。见表2。 "

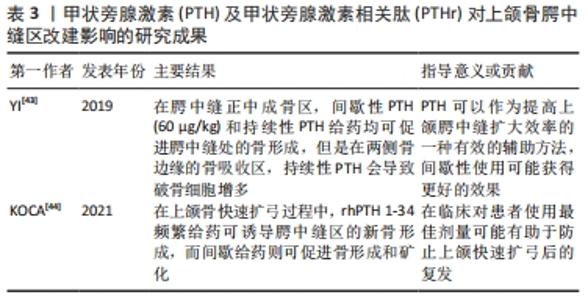
2.2.3 对上颌骨腭中缝区改建的影响 牙弓横向不调是正畸常见的错牙合畸形,需要通过正畸矫形力或外科手术方法扩大牙弓,解除牙弓横向不调。上颌扩弓的效应通常是牙效应和骨效应的结合。目前研究发现良好的腭中缝扩展对治疗的效果和稳定性有着重要的临床意义[41]。腭中缝的重建过程包括缝合中心的膜内骨形成和外侧骨缘的骨重建。腭中缝合的骨代谢速率被认为是扩弓临床疗效的瓶颈[42]。因此,控制扩张性刺激诱导骨形成和改建的关键生物学过程有望优化上颌扩弓的治疗效果。YI等[43]研究表明,在腭中缝正中成骨区,间歇性甲状旁腺激素(60 μg/kg)和持续性甲状旁腺激素给药均可以促进腭中缝处的骨形成,但是在两侧骨边缘的骨吸收区,持续性甲状旁腺激素会导致破骨细胞增多,而间歇性甲状旁腺激素给药对破骨细胞几乎无影响。同时,甲状旁腺激素可使大鼠血清钙浓度升高。因此,甲状旁腺激素可以作为提高上颌腭中缝扩大效率的一种有效的辅助方法,间歇性使用可能获得更好的效果。上颌快速扩弓后复发是临床医生面临的挑战,它可能是由多种因素引起的,但许多作者认为复发的主要原因之一可能是骨缝处的骨再生不足。KOCA等[44]研究结果表明,在上颌骨快速扩弓过程中,rhPTH 1-34频繁给药(共4 μg/kg,2次/d)可诱导腭中缝区的新骨形成,而间歇给药(4 μg/kg,1次/d)则可促进骨形成和矿化。在临床实践中,对患者使用最佳剂量可能有助于防止上颌快速扩弓后的复发。未来的研究应该确定甲状旁腺激素对腭中缝合扩张的长期影响以及潜在的不良反应,如高钙血症。见表3。"
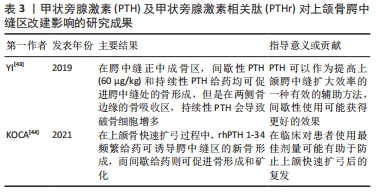
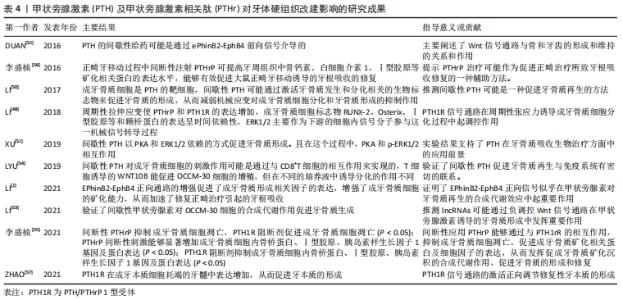
2.2.4 对牙体硬组织改建的影响 正畸治疗引起的牙根吸收是一种比较常见的病理现象,主要表现为牙根的牙骨质甚至牙本质层破坏,在根尖区通常表现为牙根变短变钝,严重情况下牙根的吸收会导致牙齿松动甚至脱落。影响牙根吸收的正畸因素分为内在与外在,与正畸治疗相关的影响因素包括拔牙、正畸力的大小、频率和持续时间、矫治器类型和牙齿移动距离等,所有这些重要因素都会影响牙根吸收。如发现正畸治疗过程中出现了中至重度的牙根吸收,应暂停治疗。正畸牙移动过程中,牙周膜部位的细胞(包括成牙骨质细胞)将感受到的机械刺激被转化为细胞内信号,在诱发牙槽骨改建的同时,也刺激分泌破骨细胞或成牙骨质细胞分子诱导牙根吸收和修复,引导破牙细胞或成牙骨质细胞分化和聚集[45]。成牙骨质细胞在正畸过程中诱导牙根吸收和修复的关键作用与其在体内和体外的牙骨质形成功能以及机械反应性有关[46]。在大多数情况下,牙周膜感受到机械应变,无论是拉伸还是压缩,都会诱导成牙骨质细胞分化,而静态压缩会抑制牙骨质的形成[47]。成牙骨质细胞的牙骨质生成活性被认为在牙根吸收/修复中起着关键作用。促进牙骨质形成仍然是牙骨质再生过程中的主要目标。 PTHrP-PTH1R系统在牙齿萌出和牙根形成的生理过程中起重要作用[48]。PTHrP功能异常突变会导致PTHrP KO小鼠的牙槽骨异常包裹生长牙胚,而牙间充质祖细胞PTH1R的缺失与牙萌出失败和由于成牙骨质细胞分化加速而缺乏牙周韧带的异常牙根有关。在临床实践中,通常采用正畸牵引来诱导埋伏牙萌出。临床报告表明,对于与PTH1R基因突变相关的原发性萌出失败患者,通常治疗较困难,即使在外科手术的辅助下,正畸牵引通常也无法取得满意的结果[49]。因此许多研究者在积极探索PTHrP在牙体发育完成后能否起到修复牙根的重要作用。 (1)促进牙骨质再生:LI等[50]验证了PTHR1在OCCM-30(小鼠成牙骨质细胞)中有内源性表达,间歇性甲状旁腺激素能进一步上调OCCM-30细胞PTHR1的表达,由此得出,成牙骨质细胞是甲状旁腺激素的靶细胞。提示间歇性甲状旁腺素可能通过激活牙骨质发生和分化相关的生物标志物[骨涎蛋白(BSP)、骨钙素(OCN)、Ⅰ型胶原(COL1)和OSX]来促进牙骨质的形成,从而减弱机械应变对成牙骨质细胞分化和牙骨质形成的抑制作用。进而推测间歇性应用甲状旁腺激素可能是一种促进牙骨质再生的方法。LI等[48]为进一步探索明确甲状旁腺激素促进牙骨质再生的作用机制,采用实时定量聚合酶链反应和Western blot检测PTHrP、PTH1R、成牙骨质细胞转录因子RUNX-2、Osterix、细胞外基质蛋白Ⅰ型胶原、骨桥蛋白的表达,通过siPTH1R转染下调PTH1R的表达,并检测成牙骨质细胞生物标志物表达的变化,得出结论:PTH1R信号通路在周期性张应力诱导成牙骨质细胞分化过程中起调控作用。XU等[51]通过体内和体外两种方法验证甲状旁腺激素对牙骨质形成的影响,最终得到结论间歇性应用甲状旁腺激素以PKA和ERK1/2依赖的方式促进牙骨质形成,且在这个过程中,PKA和p-ERK1/2相互作用。这些结果支持了甲状旁腺素在牙骨质吸收生物治疗方面中的应用前景。LI等[2]认为甲状旁腺激素的间歇性给药可能是通过ePhinB2-EphB4前向信号介导的[52],促进牙根吸收的再生和逆转的合成代谢作用,以促进牙骨质形成和促进正畸治疗引起的牙根吸收的再生;同时也证明了EPhinB2-EphB4正向信号似乎在甲状旁腺素对牙骨质再生的合成代谢效应中起重要作用,EPhinB2-EphB4正向通路的增强促进了成牙骨质形成相关因子的表达,增强了成牙骨质细胞的矿化能力,从而加速了修复正畸治疗引起的牙根吸收。LI等[53]进一步验证了间歇性应用甲状旁腺激素对OCCM-30细胞的合成代谢作用促进牙骨质生成,并发现lncRNA可能通过负调控Wnt/β-catenin信号通路在甲状旁腺牙骨质形成中发挥重要作用。LYU等[54]发现,间歇性应用甲状旁腺激素对成牙骨质细胞的刺激作用可能是通过与CD8+T细胞的相互作用来实现的,T细胞诱导的WNT10B能促进OCCM-30细胞的增殖,但在不同的培养液中诱导分化的作用不同。 同时研究发现间断性应用PTHrP也具有相似的效应,与以往持续性应用PTHrP得到的促进骨代谢分解作用不同,间断性应用PTHrP能够通过与PTH1rR的相互作用,抑制成牙骨质细胞凋亡、促进成牙骨质矿化相关蛋白及细胞因子的表达,从而发挥促成牙骨质矿化沉积的合成代谢作用,促进牙骨质的形成和修复[55]。此外也有动物实验验证正畸牙移动过程中间断性注射PTHrP可提高牙周组织中骨钙素、白细胞介素1、Ⅰ型胶原等矿化相关蛋白的表达水平,能够有效促进大鼠正畸牙移动诱导的牙根吸收的修复[56],提示 PTHrP 治疗可能作为促进正畸治疗所致牙根吸收修复的一种辅助方法。尽管目前有关甲状旁腺激素/PTHrP对促进牙骨质形成作用的证据较为普遍,但其潜在的机制仍有待阐明。 (2)促进牙本质再生:PTH1R信号通路在修复性牙本质的形成过程中也起正向调节作用。ZHAO等[57]证明了定位于细胞富集区(CZ)的Nestin-GFP阳性和Nestin-GFP阴性细胞在成牙本质细胞耗竭后增殖和分化为成牙本质细胞样细胞,再生的成牙本质细胞样细胞在修复性牙本质形成中起作用。在这个过程中,PTH1R在成牙本质细胞耗竭的牙髓中表达增加,从而促进牙本质的形成。PTH1R及其下游的磷酸化环磷酸腺苷反应元件结合蛋白(Ser133)在物理损伤牙髓中的水平升高。总的来说,成牙本质细胞死亡触发了PTH1R级联反应,这可能代表了诱导CZ介导的牙齿再生的治疗靶点。虽然该研究表明PTH1R信号通路的激活正向调节修复性牙本质的形成,但CRE/loxP介导的成牙本质细胞死亡或牙本质物理暴露损伤导致PTH1R上调的介质仍有待阐明。此外,目前还不清楚PTH1R是否也在人类受损的牙髓组织中诱导上调,同时还需要评估牙齿组织再生的年龄或性别差异。见表4。 "

| [1] 曾祥龙.现代口腔正畸学诊疗手册[M].北京:北京医科大学出版社,2000. [2] LI T, WANG H, LV C, et al. Intermittent parathyroid hormone promotes cementogenesis via ephrinB2‐EPHB4 forward signaling. J Cell Physiol. 2021;236(3):2070-2086. [3] TANG J, YAN D, CHEN L, et al. Enhancement of local bone formation on titanium implants in osteoporotic rats by biomimetic multilayered structures containing parathyroid hormone (PTH)-related protein. Biomed Mater. 2020;15(4):45011. [4] LEE PH, YEW TL, LAI YL, et al. Parathyroid hormone gene-activated matrix with DFDBA/collagen composite matrix enhances bone regeneration in rat calvarial bone defects. J Chin Med Assoc. 2018; 81(8):699-707. [5] NEER RM, ARNAYD CD, ZANCHETTA JR, et al. Effect of parathyroid hormone (1-34) on fractures and bone mineral density in postmenopausal women with osteoporosis. N Engl J Med. 2001; 344(19):1434-1441. [6] POOLE KE, REEVE J. Parathyroid hormone - a bone anabolic and catabolic agent. Curr Opin Pharmacol. 2005;5(6):612-617. [7] LOMBARDI G, DI SOMMA C, RUBINO M, et al. The roles of parathyroid hormone in bone remodeling: prospects for novel therapeutics. J Endocrinol Invest. 2011;34(7 Suppl):18-22. [8] SUVA LJ, WINSLOW GA, WETTENHALL RE, et al. A parathyroid hormone-related protein implicated in malignant hypercalcemia: cloning and expression. Science. 1987;237(4817):893-896. [9] 宋蒙胜,余霄,戎鹏泽,等.甲状旁腺激素经不同信号通路调节骨代谢的研究进展[J].中国骨伤,2021,34(6):584-588. [10] BURTIS WJ, WU T, BUNCH C, et al. Identification of a novel 17,000-dalton parathyroid hormone-like adenylate cyclase-stimulating protein from a tumor associated with humoral hypercalcemia of malignancy. J Biol Chem. 1987;262(15):7151-7156. [11] LAI NK, MARTINEZ D. Physiological roles of parathyroid hormone-related protein. Acta Biomed. 2019;90(4):510-516. [12] AZIZ S, HERMANN NV, DUNO M, et al. Primary failure of eruption of teeth in two siblings with a novel mutation in the PTH1R gene. Eur Arch Paediatr Dent. 2019;20(3):295-300. [13] NAGATA M, ONO N, ONO W. Mesenchymal Progenitor Regulation of Tooth Eruption: A View from PTHrP. J Dent Res. 2020;99(2):133-142. [14] DEMPSTER DW, COSMAN F, PARISIEN M, et al. Anabolic actions of parathyroid hormone on bone. Endocr Rev. 1993;14(6):690-709. [15] SOMA S, IWAMOTO M, HIGUCHI Y, et al. Effects of continuous infusion of PTH on experimental tooth movement in rats. J Bone Miner Res. 1999;14(4):546-554. [16] TAKANO Y, TANIZAWA T, MASHIBA T, et al. Maintaining bone mass by bisphosphonate incadronate disodium (YM175) sequential treatment after discontinuation of intermittent human parathyroid hormone (1-34) administration in ovariectomized rats. J Bone Miner Res. 1996; 11(2):169-177. [17] SOMA S, MATSUMOTO S, HIGUCHI Y, et al. Local and chronic application of PTH accelerates tooth movement in rats. J Dent Res. 2000;79(9): 1717-1724. [18] LI F, LI G, HU H, et al. Effect of parathyroid hormone on experimental tooth movement in rats. Am J Orthod Dentofacial Orthop. 2013;144(4): 523-532. [19] SALAZAR M, HERNANDES L, RAMOS A L, et al. Effect of teriparatide on induced tooth displacement in ovariectomized rats: a histomorphometric analysis. Am J Orthod Dentofacial Orthop. 2011; 139(4):e337-e344. [20] LI Y, CHEN X, TANG Z, et al. Differences in accelerated tooth movement promoted by recombinant human parathyroid hormone after mandibular ramus osteotomy. American Journal of Orthodontics and Dentofacial Orthopedics. 2019;155(5):670-680. [21] 张程,吕春晓,李天成,等.STAT3介导甲状旁腺激素调控张应力下牙槽骨塑建[J].实用口腔医学杂志,2020,36(5):736-739. [22] LU W, LI X, YANG Y, et al. PTH/PTHrP in controlled release hydrogel enhances orthodontic tooth movement by regulating periodontal bone remodaling. J Periodontal Res. 2021;56(5):885-896. [23] ZHANG C, LI T, ZHOU C, et al. Parathyroid hormone increases alveolar bone homoeostasis during orthodontic tooth movement in rats with periodontitis via crosstalk between STAT3 and beta-catenin. Int J Oral Sci. 2020;12(1):38. [24] WANG Y, HUANG L, QIN Z, et al. Parathyroid hormone ameliorates osteogenesis of human bone marrow mesenchymal stem cells against glucolipotoxicity through p38MAPK signaling. IUBMB Life. 2021;73(1): 213-222. [25] QIN Z, HUA S, CHEN H, et al. Parathyroid hormone promotes the osteogenesis of lipopolysaccharide-induced human bone marrow mesenchymal stem cells through the JNK MAPK pathway. Biosci Rep. 2021;41(8):BSR20210420. [26] 李琴,吕春华,陈玲,等. 重组甲状旁腺激素相关蛋白1-36及其在促进牙槽骨骨形成中的作用[J]. 上海口腔医学,2020,29(6):580-585. [27] LEE HS, HEO HA, PARK SH, et al. Influence of human parathyroid hormone during orthodontic tooth movement and relapse in the osteoporotic rat model: A preliminary study. Orthod Craniofac Res. 2018. doi: 10.1111/ocr.12226. [28] LI T, YAN Z, HE S, et al. Intermittent parathyroid hormone improves orthodontic retention via insulin‐like growth factor‐1. Oral Diseases. 2021;27(2):290-300. [29] VASCONCELOS DF, MARQUES MR, BENATTI BB, et al. Intermittent parathyroid hormone administration improves periodontal healing in rats. J Periodontol. 2014;85(5):721-728. [30] LI F, HE M, LI S, et al. Combination of parathyroid hormone pretreatment and mechanical stretch promotes osteogenesis of periodontal ligament fibroblasts. Am J Orthod Dentofacial Orthop. 2022;161(1):e62-e71. [31] WANG X, WANG Y, DAI X, et al. Effects of Intermittent Administration of Parathyroid Hormone (1-34) on Bone Differentiation in Stromal Precursor Antigen-1 Positive Human Periodontal Ligament Stem Cells. Stem Cells Int. 2016;2016:4027542. [32] HARRINGTON EK, RODDY GW, WEST R, et al. Parathyroid hormone/parathyroid hormone-related peptide modulates growth of avian sternal cartilage via chondrocytic proliferation. Anat Rec (Hoboken). 2007;290(2):155-167. [33] BECHTOLD TE, KURIO N, NAH H, et al. The Roles of Indian Hedgehog Signaling in TMJ Formation. Int J Mol Sci. 2019;20(24):6300. [34] RABIE AB, TANG GH, XIONG H, et al. PTHrP regulates chondrocyte maturation in condylar cartilage. J Dent Res. 2003;82(8):627-631. [35] 杨玉山,张世浩.甲状旁腺激素对髁突软骨细胞增殖、分化的影响[J].临床骨科杂志,2019,22(4):501-506. [36] WAN Q, LI Z. Intra-articular injection of parathyroid hormone in the temporomandibular joint as a novel therapy for mandibular asymmetry. Medical Hypotheses. 2010;74(4):685-687. [37] CUI C, ZHENG L, FAN Y, et al. Parathyroid hormone ameliorates temporomandibular joint osteoarthritic‐like changes related to age. Cell Prolif. 2020;53(4):e12755. [38] DUTRA EH, O BRIEN MH, CHEN P, et al. Intermittent Parathyroid Hormone [1-34] Augments Chondrogenesis of the Mandibular Condylar Cartilage of the Temporomandibular Joint. CARTILAGE. 2021;12(4): 475-483. [39] HUANG L, CAI X, LI H, et al. The effects of static pressure on chondrogenic and osteogenic differentiation in condylar chondrocytes from temporomandibular joint. Arch Oral Biol. 2015;60(4):622-630. [40] SERRANO MJ, SO S, HINTON RJ. Roles of notch signalling in mandibular condylar cartilage. Arch Oral Biol. 2014;59(7):735-740. [41] BUCCI R, D’ANTO V, RONGO R, et al. Dental and skeletal effects of palatal expansion techniques: a systematic review of the current evidence from systematic reviews and meta-analyses. J Oral Rehabil. 2016;43(7):543-564. [42] TANG GH, XU J, Chen RJ, et al. Lithium delivery enhances bone growth during midpalatal expansion. J Dent Res. 2011;90(3):336-340. [43] YI J, MEI L, LI X, et al. Effects of continuous and intermittent parathyroid hormone administration on midpalatal suture expansion in rats. Archives of Oral Biology. 2019;99:161-168. [44] KOCA CG, SADRY S, ASKER H, et al. Effects of the different administration frequencies of teriparatide (PTH [1‐34]) on new bone formation of expanded midpalatal sutures in rats: A histomorphometric and micro‐computed tomography analysis. Orthod Craniofac Res. 2021; 24(3):449-457. [45] IGLESIAS-LINARES A, HARTSFIELD JJ. Cellular and Molecular Pathways Leading to External Root Resorption. J Dent Res. 2017;96(2):145-152. [46] CHAN E, DARENDELILER MA. Physical properties of root cementum: part 7. Extent of root resorption under areas of compression and tension. Am J Orthod Dentofacial Orthop. 2006;129(4):504-510. [47] ZHANG Y, HUANG Y, ZHAO H, et al. Cementogenesis is inhibited under a mechanical static compressive force via Piezo1. Angle Orthod. 2017; 87(4):618-624. [48] LI S, LI F, ZOU S, et al. PTH1R signalling regulates the mechanotransduction process of cementoblasts under cyclic tensile stress. Eur J Orthod. 2018;40(5):537-543. [49] 高也,吕学超,王锐,等.原发性牙齿萌出障碍(PFE)的研究现状[J].口腔医学,2021,41(10):947-950. [50] LI Y, HU Z, ZHOU C, et al. Intermittent parathyroid hormone (PTH) promotes cementogenesis and alleviates the catabolic effects of mechanical strain in cementoblasts. BMC Cell Biology. 2017;18(1):19. [51] XU Y, LV C, ZHANG J, et al. Intermittent parathyroid hormone promotes cementogenesis in a PKA‐ and ERK1/2‐dependent manner. J Periodontol. 2019;90(9):1002-1013. [52] DUAN P, BONEWALD LF. The role of the wnt/beta-catenin signaling pathway in formation and maintenance of bone and teeth. Int J Biochem Cell Biol. 2016;77(Pt A):23-29. [53] LI T, WANG H, XIA K, et al. Long noncoding RNA expression profiles in intermittent parathyroid hormone induced cementogenesis. Genomics. 2021;113(1 Pt 1):217-228. [54] LYU C, ZHANG C, LI T, et al. CD8(+) T lymphocytes enhance the anabolic effect of intermittent parathyroid hormone on cementoblasts. Int Immunopharmacol. 2019;77:105927. [55] 李盛楠,李钒,管修晨,等.间断性PTHrP对成牙骨质细胞凋亡及矿化的影响[J].首都医科大学学报,2021,42(3):418-424. [56] 李盛楠,李钒,白玉兴.甲状旁腺激素相关蛋白对正畸牙移动所致牙根吸收的影响[Z].中国陕西西安:2016,3. [57] ZHAO L, ITO S, ARAI A, et al. Odontoblast death drives cell-rich zone-derived dental tissue regeneration. Bone. 2021;150:116010. |
| [1] | Li Xinyue, Li Xiheng, Mao Tianjiao, Tang Liang, Li Jiang. Three-dimensional culture affects morphology, activity and osteogenic differentiation of human periodontal ligament stem cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 846-852. |
| [2] | Wu Yujie, Wan Xiaofang, Wei Mianxing, Peng Shiyuan, Xu Xiaomei. Correlation between autophagy and the Hippo-YAP protein pathway in periodental ligament cells on the pressure side of a mouse model of orthodontic tooth movement [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(5): 683-689. |
| [3] | Jiang Haifang, Liu Rong, Hu Peng, Chen Wei, Wei Zairong, Yang Chenglan, Nie Kaiyu. Application of 3D printing technology in the precise and personalized treatment of cleft lip and palate [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 413-419. |
| [4] | Zong Mingrui, Liu Haiyan, Li Bing, Wu Xiuping. Application of carboxymethyl chitosan in tissue engineering of stomatology [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 447-452. |
| [5] | Ren Wenyan, Liu Xue, Wang Yiyu. Grophene-family nanomaterials in the treatment of periodontal disease: beneficial for osteogenic differentiation and reconstruction of periodontal support tissues [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(12): 1954-1960. |
| [6] | Zhang Haolin, Wang Yalin, Liu Yafei, Zuo Yanping, Zhang Xiaohuan. Effect of maxillary protraction on temporomandibular joint changes in skeletal class III children: a correlation analysis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(11): 1641-1646. |
| [7] | Wang Zhaoxin, Nijati•Tursun, Dai Huijuan, Wang Junxiang, Xiaheida•Yilaljiang, Li Shuhui. Effect of macrophage inflammatory protein-1 alpha on the biological behavior of human periodontal ligament stem cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(10): 1521-1527. |
| [8] | Chen Jiana, Nie Minhai, Hu Xinyue, Liu Xuqian. Platelet-derived growth factor BB promotes proliferation and osteogenic differentiation of human periodontal ligament stem cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(10): 1534-1540. |
| [9] | Zhang Min, Bai Shulin, Li Shenghong, Fan Zhibo, Xie Yijia, Xu Xiaomei. Effects of high mobility group box 1 and ERK1/2 pathway on autophagy of human periodontal ligament cells under tensile stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(10): 1560-1566. |
| [10] | Lan Qian, Gu Yangcong, Xiao Xin, Bi Xueting, Li Na. Human periodontal ligament stem cells-derived exosomes interfere with the proliferation and differentiation of MC3T3-E1 cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 54-58. |
| [11] | Liu Runyuan, Dong Ming, Han Wenqing, Dong Juhong, Niu Weidong. Application and progress of small extracellular vesicles in periodontal and pulp regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 83-90. |
| [12] | Liu Zhuoran, Jiang Ming, Li Yourui. Extracellular vesicles in chronic periodontitis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 99-104. |
| [13] | Luo Xiaoling, Zhang Li, Yang Maohua, Xu Jie, Xu Xiaomei. Effect of naringenin on osteogenic differentiation of human periodontal ligament stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1051-1056. |
| [14] | Li Maoxue, Ding Yi, Guo Shujuan. Understanding of periodontal biomaterials based on the concept of bone homeostasis control and the effects on bone formation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(34): 5562-5568. |
| [15] | Liu Chun, Jia Ying, Yang Shirong, Ding Qi, Yang Hua, Chen Bo. Characteristics of the growth, development and microarchitecture of condyle subchondral bone in rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(32): 5162-5166. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||