Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (30): 4904-4911.doi: 10.12307/2022.773
Previous Articles Next Articles
Advances focusing on strategies of promoting vascularization in dental pulp regeneration
Wang Ge1, 2, Xie Li1, 2, Tian Weidong1, 2, 3
- 1National Engineering Laboratory for Oral Regenerative Medicine, 2National Clinical Research Center for Oral Diseases, 3Department of Oral and Maxillofacial Surgery, West China Hospital of Stomatology, Sichuan University, Chengdu 610041, Sichuan Province, China
-
Received:2021-05-27Accepted:2021-10-28Online:2022-10-28Published:2022-03-29 -
Contact:Xie Li, MD, Associate researcher, National Engineering Laboratory for Oral Regenerative Medicine, and National Clinical Research Center for Oral Diseases, West China Hospital of Stomatology, Sichuan University, Chengdu 610041, Sichuan Province, China Tian Weidong, MD, Professor, National Engineering Laboratory for Oral Regenerative Medicine, and National Clinical Research Center for Oral Diseases, and Department of Oral and Maxillofacial Surgery, West China Hospital of Stomatology, Sichuan University, Chengdu 610041, Sichuan Province, China -
About author:Wang Ge, Master candidate, National Engineering Laboratory for Oral Regenerative Medicine, and National Clinical Research Center for Oral Diseases, West China Hospital of Stomatology, Sichuan University, Chengdu 610041, Sichuan Province, China -
Supported by:the National Key Research and Development Program of China, No. 2017YFA0104800 (to TWD); the National Natural Science Foundation of China, No. 81970968, No. 81600895 (to XL); the Key Research and Development Program of Science and Technology Plan of Sichuan Province, No. 2019YFS0515 (to TWD)
CLC Number:
Cite this article
Wang Ge, Xie Li, Tian Weidong. Advances focusing on strategies of promoting vascularization in dental pulp regeneration[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(30): 4904-4911.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

植入的组织块主要依靠原有的血管网络以血管出芽的方式长入到植入物,并且以一定的速度延伸,各种信号因子通过复杂的机制驱动并且影响这一过程,包括许多活化和抑制分子,如生长因子、细胞因子、基质金属蛋白酶、内源性血管生成抑制剂、转录因子以及黏附分子等[9]。常见的生长因子包括血管内皮生长因子、血小板来源生长因子、成纤维细胞生长因子、肝细胞生长因子以及血管生成素等[10]。此处简要归纳了常见的信号因子在牙髓再生血管化中的作用及其机制,并为后续讨论奠定基础。 2.1.1 血管内皮生长因子 是研究最广泛的成血管因子,血管内皮生长因子对于血管生成的速度和稳定性起着决定性作用[10]。FERRARA等[11]报道血管内皮生长因子可以促进动脉、静脉和淋巴管来源的血管内皮细胞的增殖、迁移及分化。此外,血管内皮生长因子可以诱导某些血管内皮开窗以增加渗透系数[12],这种促进血管外渗的作用在众多病理、修复过程中都发挥了重要作用。 研究证实,牙髓干细胞能大量分泌血管内皮生长因子[13-14]。ARANHA等[14]研究发现,缺氧可增强牙髓干细胞和牙髓成纤维细胞中低氧诱导因子1α和血管内皮生长因子的表达,提示血管内皮生长因子参与缺氧牙髓的血运重建。ROBERTS-CLARK等[15]发现牙本质基质是多种生长因子的储存库,在牙髓-牙本质复合体受到损伤后,包括血管内皮生长因子在内的多种因子被释放出来,以促进牙髓组织的血管生成。ZHANG等[16]研究发现血管内皮生长因子通过激活Wnt/β-catenin信号通路诱导牙髓干细胞分化形成新生血管,抑制Wnt通路会阻断这一过程,同时沉默了β-catenin通路的牙髓干细胞在体外不再分化为内皮细胞,体内血管生成减弱。Mullane等[17]将浸泡过血管内皮生长因子的牙片段植入裸鼠皮下2周,实验组的牙横切片根管内新生血管的数量和密度明显增加。 2.1.2 血小板来源生长因子 是一类二聚糖蛋白家族,最初发现于血小板。具有诱导细胞增殖的潜能[18]。其中血小板来源生长因子BB和血管内皮生长因子有显著的同源性,两者都具有促有丝分裂活性,但它们有不同的靶细胞和促血管生成活性[19]。血小板来源生长因子BB还可以通过促进血管内皮生长因子分泌间接促进血管生成[20]。血管内皮细胞会通过产生血小板来源生长因子BB来促进血管周细胞的增殖和迁移,而血管周细胞与内皮细胞的相互作用对血管的稳定至关重要[21]。 牙髓干细胞也会分泌血小板来源生长因子[13-14]。在牙本质基质中,血小板来源生长因子的总量较其他生长因子如血管内皮生长因子高[15]。ZHAJIANG等[22]应用人重组血小板来源生长因子BB治疗1例20岁患者的牙髓坏死磨牙,15个月随访结果显示该患者牙根持续发育、根尖闭合且根尖周炎愈合。 2.1.3 成纤维细胞生长因子 成纤维细胞生长因子家族及其受体调控着重要的生物学功能,通过激活血管内皮细胞上的受体促进其迁移并诱导其他细胞释放血管生成因子[23]。维持血管完整性需要保持低水平的成纤维细胞生长因子,抑制内皮细胞受体会导致血管解体[24]。 在牙髓再生过程中,成纤维细胞生长因子促血管生成的作用也有广泛的研究[13,25],大多集中在成纤维细胞因子2分子的分泌和功能上。牙髓干细胞可以在其他促血管生成因子作用下产生成纤维细胞因子2[25]。TAKEUCHI等[26]研究指出,成纤维细胞因子2类似于粒细胞集落刺激因子,在血管生成过程中对细胞增殖和迁移有广泛的影响。GORIN等[27]研究表明,与低氧诱导相比,成纤维细胞生长因子2处理过的脱落乳牙干细胞生成的血管更多;成纤维细胞生长因子2处理后增加了基质细胞抗原1(stromal cell antigen 1,STRO-1)/CD146双阳性细胞亚群比例。 2.1.4 其他调节因子 基质细胞衍生因子1α属于CXC趋化因子亚家族,在干细胞的募集、迁移和分化中起关键作用,继而增强组织血管化[28]。YANG等[29]发现经基质细胞衍生因子1α激发了牙髓干细胞的自噬作用,促进了牙髓干细胞的迁移,将含基质细胞衍生因子1α的载牙髓干细胞丝素蛋白支架置于牙片上并移植到裸鼠体内,生成了有血管结构的牙髓样组织。 辛伐他汀属于他汀类家族成员,可以促进内皮细胞的功能,并增强血管生成[30]。MIN等[30]发现在应用辛伐他汀后,牙髓干细胞会表达牙源性和血管生成标记物。KIM等[31]对牙髓细胞使用天然铁螯合剂Hinokitiol,发现牙髓细胞表达缺氧诱导因子1α和血管内皮生长因子上调,血管生成潜力提高。 细胞外囊泡是由细胞释放的由脂质双分子层包裹的颗粒,它们携带有遗传物质(信使RNA和微RNA)、生长因子等,用于细胞间信号传递。研究发现牙髓细胞来源的细胞外囊泡促进了人脐静脉内皮细胞增殖、分泌成血管因子及其成管作用,证实了牙源性外泌体应用于牙髓血管再生的潜能[32]。 2.1.5 牙髓再生中信号因子的调控研究比较总结 目前牙髓再生及血管化研究的发展历程见图3。"
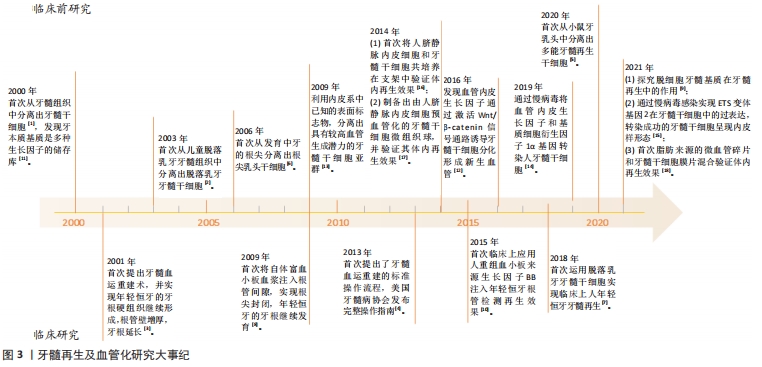
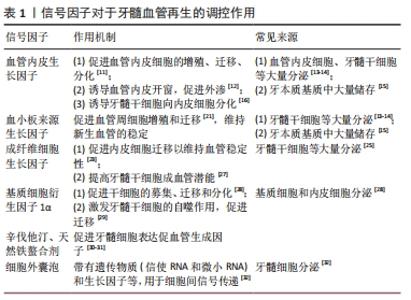
牙髓牙本质复合物受到损伤后,牙髓干细胞、牙本质基质会释放出大量信号因子,提示着炎症环境是牙髓组织修复的始发因素。血管内皮生长因子在缺氧环境中大量表达并发挥了主要作用,包括在炎症环境下促进血管外渗,促进血管内皮细胞的增殖、迁移,诱导牙髓干细胞向内皮细胞分化等,其他各类信号因子可以通过促进血管内皮生长因子的分泌间接起作用。此外,血小板来源生长因子还可以促进血管周细胞的增殖和迁移,维持血管稳定;基质细胞衍生因子1α通过募集干细胞、促进干细胞分化发挥作用;成纤维细胞生长因子通过促进内皮细胞迁移以维持血管稳定性;辛伐他汀和天然铁螯合剂则可以促进牙髓细胞表达促血管生成因子;细胞外囊泡则通过其携带的信号分子如血管内皮生长因子等发挥促血管生成作用。信号因子的存在为关键细胞的功能行使维持着适宜的微环境,提供着重要驱动力,但促血管新生信号因子易失活、半衰期短和价格昂贵,在具体应用时还有许多问题需要解答,对信号因子的分子结构、信号通路和调控机制的深入研究将进一步提高基于信号因子治疗的实用性,如通过对负载信号因子的支架材料的设计还可以维持环境中一定的分子浓度,延缓其降解,见表1。"

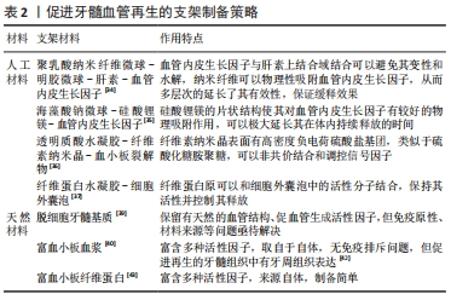
2.2.1 负载信号因子支架的设计 大多数蛋白类信号因子对高温或pH值敏感,容易被酶降解,失去作用,而如果反复揭开根管口给药会增加感染的风险、削弱患者依从性,最终降低再生的成功率。使用具有缓释能力的支架载体能维持微环境中适宜的分子浓度、保护信号因子避免其失活,并且将副反应降至最低,从而提高信号因子的利用率,最终促进再生牙髓中血管化的进程[33]。 LI等[34]将血管内皮生长因子和肝素包裹在纳米明胶球中,并进一步固定在聚乳酸纳米纤维微球里,这种多层次的微球系统不仅可以防止血管内皮生长因子的变性和降解,而且可以持续释放长达四周时间。体内结果显示新生牙髓组织占据约2/3根管全长,且有大量新生血管再生。ZHANG等[35]研制了可注射的RGD(促进细胞对生物材料的黏附的一种氨基酸序列)-海藻酸钠/硅酸锂镁水凝胶微球,并负载牙髓干细胞和血管内皮生长因子,该系统在保持其活性的同时可缓释血管内皮生长因子达28 d,体内结果显示实验组有更多牙髓组织和新生血管形成。SILVA等[36]设计了一类由纤维素纳米晶增强的透明质酸水凝胶,并加入血小板裂解物(含有多种促血管生成因子),纤维素纳米晶的掺入量越多,促血管因子保持释放的天数越多。ZHANG等[37]制备了一种细胞外囊泡-纤维蛋白凝胶复合材料,细胞外囊泡-纤维蛋白凝胶在不到7 d的时间里,通过血管内皮生长因子的持续释放,增强了体外血管样结构的形成。 2.2.2 其他支架材料的促血管生成作用 脱细胞化细胞外基质来源于人或动物组织,具有高的生物活性和组织特异性,作为理想的再生支架材料受到广泛研究,而脱细胞牙髓基质在牙髓再生方面的应用直到最近才开始研究[38]。ALGHUTAIMEL等[39]发现牛脱细胞牙髓基质保留了天然的组织结构和血管系统,并保留了血管内皮生长因子A和成纤维细胞生长因子2等成分。体外细胞培养结果显示种植在该支架上的细胞表达血管生成相关的标志物增加,此外,种植了牙髓干细胞的脱细胞牙髓基质组在体内血管生成明显增强。 富血小板血浆作为生物活性支架广泛应用于组织工程,由富含血小板的自体血浆制成。血小板在富血小板血浆中释放的重要的生长因子包括血管内皮生长因子、血小板来源生长因子、成纤维细胞生长因子和表皮生长因子等[40]。DING等[41]报道了1例16岁男性患者,其上颌左侧切牙牙髓失去活性,牙根尖部开放,将自体富血小板血浆注入根管间隙并永久性充填材料修复牙齿,3年后随访发现根尖周病变恢复,根管壁增厚,根尖持续闭合。但也有研究发现,利用富血小板血浆再生的牙髓组织,其免疫组化结果有多种牙周组织的分子标记,包括牙周韧带和骨组织等,提示富血小板血浆诱导再生的更多的是牙周组织而非牙髓组织[42]。 富血小板纤维蛋白是第2代浓缩血小板,其制备方法较富血小板血浆简单,主要成分是胶原纤维蛋白,在纤维蛋白降解重塑的过程中,嵌在纤维框架中的血小板被激活发生脱颗粒作用,以自然速率释放多种生长因子。此外,富血小板纤维蛋白含有许多血液中的白细胞,这些白细胞可以在抗炎和免疫调节活动中发挥积极作用[43]。CHEN等[44]制备一种由牙髓干细胞细胞膜片和富血小板纤维蛋白组成的新型材料,移植至裸鼠皮下和犬根根管后成功形成均匀致密的新生牙髓-牙本质样组织,且毛细血管丰富。 2.2.3 支架材料的设计研究比较总结 支架材料在组织工程中起到模拟细胞外基质的作用,其物化性质调节着血管生成的多个方面,其中对血管生成影响最大的是对信号因子的控释能力,这决定了是否能维持适宜细胞活性的微环境。作为牙髓再生血管化中信号因子传递和控释的载体,向支架上添加肝素、硅酸锂镁和纤维素纳米晶等化学材料可以溶解包裹、吸附、共价交联信号因子,可以模拟体内信号因子储存及释放机制,从而维持有效的信号分子浓度。人工合成材料最大的优势在于可以根据需要自由选择搭配信号因子的种类和剂量,虽然制备不同材料的复杂程度不同,但可以保证制备流程和产品的统一和可重复。天然材料包括脱细胞牙髓基质、富血小板血浆及富血小板纤维蛋白等的优势在于自身富含多种生物活性分子,且其自身结构可保护并控释这些信号因子,但其包含成分的种类和剂量较为固定,其促进再生的效果和方向仍需进一步验证,如富血小板血浆则可能更适用于骨组织再生,并且需要进一步完善制备方法,在保留有效成分活性的前提下降低其免疫原性,才能推动临床应用进程,见表2。"


不同的细胞类型有不同程度的成血管能力,细胞和细胞之间的相互作用会提升成血管能力,合理的细胞搭配可以显著提升成血管效果。 2.3.1 高成血管潜能的细胞 牙髓干细胞具有高度增殖活性、多向分化能力和多潜能性,其不同细胞亚群具有不同的分化潜力。研究利用内皮系中已知的表面标志物,分离出具有较高血管生成潜力的牙髓干细胞亚群[45]。研究发现基质细胞抗原1阳性或CD146阳性的牙髓干细胞表达α平滑肌肌动蛋白和血管周细胞相关抗原3G5,这提示该细胞群具有血管周细胞表型[46]。有研究分离出CD29,CD44,CD90和CD105阳性,CD34和CD45阴性的牙髓干细胞,在大鼠急性心肌梗死区域中植入该细胞后诱导了血管生成并缩小了梗死范围[47]。将包裹在胶原支架中的CD105阳性牙髓细胞和基质细胞衍生因子1α移植到去髓牙的根管内,结果形成了完整的血管结构和牙髓样组织[48]。IOHARA等[49]从牙髓中分离出表达CD31和CD146的高血管生成潜力的亚群细胞,该细胞表达CD34和血管内皮生长因子R2,表现出高度的增殖和迁移活性以及血管生成能力。在小鼠后肢缺血模型中,局部移植这一细胞形成了高密度血管网络,并提高了移植区域血流量。上述研究结论证实,分离纯化出具有高血管生成潜力的牙髓干细胞细胞亚群,并用其来促进牙髓再生中血管化的可能性。 除了高成血管潜能的细胞亚群,也有研究通过转染来促进牙髓干细胞表达成血管因子来提高其成血管能力。ZHU等[50]通过慢病毒将血管内皮生长因子和基质细胞衍生因子1α基因转染人牙髓干细胞,其血管内皮生长因子和基质细胞衍生因子1α的 mRNA及蛋白表达水平均显著增高,体内实验结果显示转染组根管内再生牙髓长度和血管密度均显著增加。LI等[51]设计了一种基于阳离子多聚物的转染系统,该载体可避免溶酶体的降解作用,最终血管内皮生长因子表达水平上调了8倍以上,显著增强了内皮细胞的迁移和血管的形成,体内结果显示转染后的牙髓干细胞加速了新血管形成,再生的牙髓组织占据了牙根管全长的大部分区域。有研究用编码肝配蛋白B2(血管内皮生长因子受体内化和信号传递所必需的)的慢病毒转染根尖乳头干细胞,低氧条件下转染后的细胞血管内皮生长因子的分泌水平上调,人脐静脉内皮细胞与转染后的细胞共培养早期即形成血管样结构,体内实验显示转染后的细胞与人脐静脉内皮细胞共移植形成更多的血管结构[52]。ZHANG等[53]以慢病毒为载体,建立血小板来源生长因子BB基因修饰的牙髓干细胞,转染后的牙髓干细胞分泌血小板来源生长因子BB和血管内皮生长因子水平升高。 2.3.2 促进干细胞向内皮细胞分化 血管内皮细胞作为血管发育的重要组成部分,构成了整个循环系统的血管内壁。研究表明,在血管损伤或缺血性疾病的治疗中,自体血管内皮细胞是理想的新生血管细胞来源,但因其供体组织稀缺且原代细胞增殖能力有限,分离后还会造成供体部位的病损,限制了其在组织工程中的广泛应用[54]。胚胎干细胞具有分化为血管内皮细胞的潜力。然而,胚胎干细胞分化效率低,临床应用时存在伦理争议,并不适合用来大规模生产血管内皮细胞[55]。也有研究利用诱导多能干细胞分化来生产血管内皮细胞。然而,多能干细胞的致瘤风险也限制其在临床上的广泛应用[56]。 牙髓干细胞有充足的自体来源、强大的增殖能力和免疫相容性,有望成为诱导分化成内皮细胞系的一种新的细胞来源[57]。有研究发现,30%表达胎肝激酶1的牙髓干细胞也表达血管生成标记,并分化为内皮细胞;该研究进一步提示胎肝激酶1阳性细胞可分化为内皮细胞,体内移植后可形成血管化的骨组织[58]。LI等[59]通过慢病毒转染实现ETS变体基因2在牙髓干细胞中的过表达,转染成功的牙髓干细胞呈现内皮样形态,内皮细胞特异性基因CD31、血管内皮生长因子R1和血管内皮生长因子R2的mRNA和蛋白表达水平均显著升高。 2.3.3 细胞共培养 在自然微环境中,组织由2种或2种以上细胞组成,不同的细胞不仅有助于结构的完整性,而且相互作用维持活性,并促进分化和其他关键的生物学活动。许多研究表明,干细胞/祖细胞与内皮/内皮祖细胞共培养可显著促进血管生成[60]。研究还发现人脐静脉内皮细胞与牙髓干细胞共培养不仅能促进血管生成,而且在体外还能调节牙髓干细胞的成牙/成骨分化[61]。此外,牙髓干细胞和其他间充质干/祖细胞在血管生成过程中分泌大量信号因子,如血管内皮生长因子和成纤维细胞生长因子2,牙髓干细胞的加入稳定了人脐静脉内皮细胞形成的血管样结构[62]。除了细胞的旁分泌效应,细胞-细胞和细胞-细胞外基质的相互作用在体内血管生成中也起重要作用[63]。研究发现在缺乏相关的血管周细胞或平滑肌细胞的情况下,新生内皮细胞变得不稳定,容易发生凋亡[64]。而许多研究证明间充质干细胞充当了周细胞或平滑肌细胞的角色,延长了新生血管的寿命[60,65]。还有研究发现牙髓干细胞通过促进人脐静脉内皮细胞的迁移来促进早期血管网络的形成,通过将人脐静脉内皮细胞和牙髓干细胞共培养在自组装多肽水凝胶支架中并注入牙片段中,然后移植到裸鼠皮下,结果显示牙片段内形成微血管网络,且与宿主血管吻合[66]。 2.3.4 组织预血管化 移植组织的血液灌注影响着细胞存活和组织再生,现有许多研究制备体外预血管化材料并植入体内,通过其与宿主血管系统融合后,可以促进结构中深部的早期血液供应,这已成为一种有效提升植入物存活率的策略[67]。有研究制备出由人脐静脉内皮细胞预血管化的牙髓干细胞微组织球,将其植入牙根切片的根管间隙并植入裸鼠皮下,4周后组织学结果显示含有微组织球体的牙根切片内形成了血管化良好的牙髓样组织,而对照组只有皮下脂肪组织填充,且人CD31免疫组织化学染色显示,人脐静脉内皮细胞在体外形成的血管结构在体内移植后与宿主血管系统成功吻合[68]。XU等[69]将脂肪来源的微血管碎片和牙髓干细胞膜片混合置于牙片段内并植入到裸鼠皮下,体外结果显示微血管碎片中有丰富的的信号因子、内皮细胞和血管周细胞,体内结果显示有完整的血管组织形成,血管显影结果显示该牙片段内血管与宿主血管吻合。 2.3.5 细胞的设计相关研究总结 在组织工程中,细胞的活性、分化潜能决定着血管再生的结果,因此精确地分选出不同成血管潜力的细胞、合理使用和搭配细胞可以最大程度地提高成血管效率。牙髓细胞中不同细胞亚群的有不同的成血管潜能,有细胞亚群承担了血管周细胞的作用,有细胞亚群对血管内皮生长因子的作用更敏感,但涉及到具体临床应用则需要开发出一套完善的细胞亚群分离、提纯、培养、储存流程。此外,通过生物、化学等载体可以转染干细胞以提高细胞分泌信号因子的能力,也可以促进干细胞向内皮细胞转化,转染后的细胞成血管能力显著提升,但目前转染技术仍不成熟,转染的效率均较低且存在异变的风险,因此转染更适用于基础研究而不是临床应用。将不同的细胞混合培养并植入可以更大程度模拟体内真实情况从而提升成血管能力,但其中的具体机制仍不明确,可能是细胞与细胞的直接接触促进了信息交流,也可能是细胞分泌的细胞因子的作用,且不同细胞所占总细胞比例不同,再生的效果也需要更进一步探索。体外预血管化是一个较新的研究的方向,在体外营养充分的情况下,将内皮细胞和干细胞以一定比例共培养可以制备出含血管结构的微组织;也可以通过酶消化脂肪组织得到微血管碎片,并依赖其管状结构和存留的血管支持细胞等发挥功能,从而植入体内后表现出快速形成新微血管网络并与宿主血管吻合的特性。相较而言,体外培养预成血管耗时且对细胞来源、培养条件要求较高,而脂肪来源微血管碎片取之于自身且制备过程较简单,或可以成为在牙髓再生中促进快速血管化最有竞争力的手段,但其制备流程仍需标准化,见表3。"

| [1] JUNG C, KIM S, SUN T, et al. Pulp-dentin regeneration: current approachs and challenges. J Tissue Eng. 2019;10:1-13. [2] ZHANG W, YELICK PC. Vital pulp therapy-current progress of dental pulp regeneration and revascularization. Int J Dent. 2010;2010:1-9. [3] CARMELIET P, JAIN RK. Angiogenesis in cancer and other diseases. Nature. 2000;407(6801):249-257. [4] POTENTE M, GERHARDT H, CARMELIET P. Basic and therapeutic aspects of angiogenesis. Cell. 2011;146(6):873-887. [5] UTZINGER U, BAGGETT B, WEISS JA, et al. Large-scale time series microscopy of neovessel growth during angiogenesis. Angiogenesis. 2015;18(3):219-232. [6] 贺露,郭俊,杨健.再血管化和牙组织工程化牙髓再生的研究进展[J].国际口腔医学杂志,2015,42(4):485-491. [7] 钟小奕,陈文霞.血管再生研究进展及其应用[J].国际口腔医学杂志,2009,36(2):183-185. [8] 韩琦,王效英.牙髓血管再生的相关研究进展[J].口腔医学,2019, 39(4):371-375. [9] SAGBIRI MA, ASATOURIAN A, SORESON CM, et al. Role of angiogenesis in endodontics: contributions of stem cells and proangiogenic and antiangiogenic factors to dental pulp regeneration. J Endod. 2015; 41(6):797-803. [10] FERRARA N, GERBER HP, LECOUTER J. The biology of VEGF and its receptors. Nat Med. 2003;9(6):669-676. [11] FERRARA N, DAVIS-SMYTH T. The biology of vascular endothelial growth factor. Endocr Rev. 1997;18(1):4-25. [12] ROBERTS WG, PALADE GE. Increased microvascular permeability and endothelial fenestration induced by vascular endothelial growth factor. 1995;108(6):2369-2379. [13] TRAN-HUNG L, MATHIEU S, ABOUT I. Role of human pulp fibroblasts in angiogenesis. J Dent Res. 2006;85(9):819-823. [14] ARANHA AMF, ZHAOCHENG Z, NEIVA KG, et al. Hypoxia enhances the angiogenic potential of human dental pulp cells. J Endod. 2010;36(10): 1633-1637. [15] ROBERTS-CLARK DJ, SMITH AJ. Angiogenic growth factors in human dentine matrix. Arch Oral Biol. 2000;45(11):1013-1016. [16] ZHANG Z, NÖR F, OH M, et al. Wnt/β‐catenin signaling determines the vasculogenic fate of postnatal mesenchymal stem cells. Stem Cells. 2016;34:1576-1587. [17] MULLANE EM, DONG Z, SEDGLEY CM, et al. Effects of VEGF and FGF2 on the revascularization of severed human dental pulps. J Dent Res. 2008;87(12):1144-1148. [18] TALLQUIST M, KAZLAUSKAS A. PDGF signaling in cells and mice. Cytokine Growth Factor Rev. 2004;15(4):205-213. [19] KECK PJ, HAUSER SD, KRIVI G, et al. Vascular permeability factor, an endothelial cell mitogen related to PDGF. Science. 1989;246(1): 1309-1312. [20] STAVRIA GT, HONG Y, ZACHARY CI, et al. Hypoxia and platelet-derived growth factor-BB synergistically upregulate the expression of vascular endothelial growth factor in vascular smooth muscle cells. FEBS Lett. 1995;358(3):311-315. [21] MATSUOKA J, GROTENDORST GR. Two peptides related to platelet-derived growth factor are present in human wound fluid. Proc Natl Acad Sci U S A. 1989;86(12):4416-4420. [22] ZHUJIANG A, KIM SG. Regenerative endodontic treatment of an immature necrotic molar with arrested root development by using recombinant human platelet-derived growth factor: a case report. J Endod. 2016;42(1):72-75. [23] BEENKEN A, MOHAMMADI M. The FGF family: biology, pathophysiology and therapy. Nat Rev Drug Discov. 2009;8(3):235-253. [24] BERGERS G, HANAHAN D. Modes of resistance to anti- angiogenic therapy. Nat Rev. 2008;8(8):592-603. [25] BRONCKAERS A, HILKENS P, YANICK F, et al. Angiogenic properties of human dental pulp stem cells. PLoS One. 2013;8(8):e71104. [26] TAKEUCHI N, HAYASHI Y, MURAKAMI M, et al. Similar in vitro effects and pulp regeneration in ectopic tooth transplantation by basic fibroblast growth factor and granulocyte‐colony stimulating factor. Oral Dis. 2015; 21(1):113-122. [27] GORIN C, ROCHEFORT GY, BASCETIN R, et al. Priming dental pulp stem cells with fibroblast growth factor-2 increases angiogenesis of implanted tissue-engineered constructs through hepatocyte growth factor and vascular endothelial growth factor secretion. Stem Cells Transl Med. 2016;5(3):392-404. [28] LIEKENS S, SCHOLS D, HATSE S. CXCL12-CXCR4 axis in angiogenesis, metastasis and stem cell mobilization. Curr Pharm Des. 2010;16(35): 3903-3920. [29] YANG JW, ZHANG YF, WAN CY, et al. Autophagy in SDF-1α-mediated DPSC migration and pulp regeneration. Biomaterials. 2015;44: 11-23. [30] MIN KS, Lee Y, HONG SO, et al. Simvastatin promotes odontoblastic differentiation and expression of angiogenic factors via heme oxygenase-1 in primary cultured human dental pulp cells. J Endod. 2010;36(3):447-452. [31] KIM MK, PARK HJ, KIM YD, et al. Hinokitiol increases the angiogenic potential of dental pulp cells through ERK and p38MAPK activation and hypoxia-inducible factor-1α (HIF-1α) upregulation. Arch Oral Biol. 2014;59(2):102-110. [32] XIAN X, GONG Q, LI C, et al. Exosomes with highly angiogenic potential for possible use in pulp regeneration. J Endod. 2018;44(5):751-758. [33] WU S, ZHOU Y, YU Y, et al. Evaluation of chitosan hydrogel for sustained delivery of VEGF for odontogenic differentiation of dental pulp stem cells. Stem Cells Int. 2019;2019:1-14. [34] LI X, MA C, XIE X, et al. Pulp regeneration in a full-length human tooth root using a hierarchical nanofibrous microsphere system. Acta Biomater. 2016;35:57-67. [35] Zhang R, Xie L, Wu H, et al. Alginate/laponite hydrogel microspheres co-encapsulating dental pulp stem cells and VEGF for endodontic regeneration. Acta Biomater. 2020;113:305-316. [36] SILVA CR, BABO PS, GULINO M, et al. Injectable and tunable hyaluronic acid hydrogels releasing chemotactic and angiogenic growth factors for endodontic regeneration. Acta Biomater. 2018;77:155-171. [37] ZHANG S, THIEBES AL, KREIMENDAHL F, et al. Extracellular vesicles-loaded fibrin gel supports rapid neovascularization for dental pulp regeneration. Int J Mol Sci. 2020;21(12):4226. [38] SONG JS, TAKIMOTO K, JEON M, et al. Decellularized human dental pulp as a scaffold for regenerative endodontics. J Dent Res. 2017;96(6): 640-646. [39] ALGHUTAIMEL H, YANG X, DRUMMOND B, et al. Investigating the vascularization capacity of a decellularized dental pulp matrix seeded with human dental pulp stem cells: in vitro and preliminary in vivo evaluations. Int Endod J. 2021. doi:10.1111/iej.13510. [40] CERVANTES J, PERPER M, WONG LL, et al. Effectiveness of platelet-rich plasma for androgenetic alopecia: a review of the literature. Skin Appendage Disord. 2018;4(1):111. [41] DING RY, CHEUNG GS, CHEN J, et al. Pulp revascularization of immature teeth with apical periodontitis: a clinical study. J Endod. 2009;35(5):745-749. [42] ZHU X, WANG Y, LIU Y, et al. Immunohistochemical and histochemical analysis of newly formed tissues in root canal space transplanted with dental pulp stem cells plus platelet-rich plasma. J Endod. 2014;40(10): 1573-1578. [43] DOHAN EHRENFEST DM, RASMUSSON L, ALBREKTSSON, T. Classification of platelet concentrates: from pure platelet-rich plasma (P-PRP) to leucocyte-and platelet-rich fibrin (L-PRF). Trends Biotechnol. 2009;27(3):158-167. [44] CHEN YJ, ZHAO YH, ZHAO YJ, et al. Potential dental pulp revascularization and odonto-/osteogenic capacity of a novel transplant combined with dental pulp stem cells and platelet-rich fibrin. Cell Tissue Res. 2015;361(2):439-455. [45] SLOAN AJ, WADDINGTON RJ. Dental pulp stem cells: what, where, how? Int J Paediatr Dent. 2009;19(1):61-70. [46] SONGTAO S, GRONTHOS S. Perivascular niche of postnatal mesenchymal stem cells in human bone marrow and dental pulp. J Bone Miner Res. 2003;18(4):696-704. [47] GANDIA C, ARMIÑAN A, GARCÍA-VERDUGO JM, et al. Human dental pulp stem cells improve left ventricular function, induce angiogenesis, and reduce infarct size in rats with acute myocardial infarction. Stem Cells. 2008;26(3):638-645. [48] IOHARA K, IMABAYASHI K, ISHIZAKA R, et al. Complete pulp regeneration after pulpectomy by transplantation of cd105 + stem cells with stromal cell-derived factor-1. Tissue Eng Part A. 2011; 17(15-16):1911-1920. [49] IOHARA K, ZHENG L, WAKE H, et al. A novel stem cell source for vasculogenesis in ischemia: subfraction of side population cells from dental pulp. Stem Cells. 2008;26:2408-2418. [50] ZHU L, DISSANAYAKA WL, ZHANG C. Dental pulp stem cells overexpressing stromal-derived factor-1α and vascular endothelial growth factor in dental pulp regeneration. Clin Oral Investig. 2019;23(5):2497-2509. [51] LI Q, HU Z, LIANG Y, XU C, et al. Multifunctional peptide-conjugated nanocarriers for pulp regeneration in a full-length human tooth root. Acta Biomater. 2021;127:252-265. [52] YUAN C, WANG P, ZHU S, et al. Overexpression of ephrinB2 in stem cells from apical papilla accelerates angiogenesis. Oral Dis. 2019;25(3):848-859. [53] ZHANG M, JIANG F, ZHANG X, et al. The effects of platelet‐derived growth factor-bb on human dental pulp stem cells mediated dentin‐pulp complex regeneration. Stem Cell Transl Med. 2017;6(12):2126-2134. [54] 罗哲文,胡竹林,徐岩泽,等.自体血管内皮细胞移植替代角膜内皮层的实验研究[J].眼科研究,2008,26(4):249-252. [55] LEBRAS A, VIJAYARAJ P, OETTGEN P. Molecular mechanisms of endothelial differentiation. Vasc Med. 2010;15(4):321-331. [56] LANNER F, SOHL M, FARNEBO F. Functional arterial and venous fate is determined by graded vegf signaling and notch status during embryonic stem cell differentiation. Arterioscler Thromb Vasc Biol. 2007;27(3):487-493. [57] YI B, DISSANAYAKA WL, ZHANG C. Growth factors and small-molecule compounds in derivation of endothelial lineages from dental stem cells. J Endod. 2020;46(9):S63-S70. [58] D’AQUINO R, GRAZIANO A, SAMPAOLESI M, et al. Human postnatal dental pulp cells co-differentiate into osteoblasts and endotheliocytes:a pivotal synergy leading to adult bone tissue formation. Cell Death Differ. 2007;14(6):1162-1171. [59] LI J, ZHU Y, LI N, et al. Upregulation of ETV2 expression promotes endothelial differentiation of human dental pulp stem cells. Cell Transplant. 2021;30:1-11. [60] DUFFY GP, AHSAN T, O’BRIEN T, et al. Bone marrow-derived mesenchymal stem cells promote angiogenic processes in a time- and dose-dependent manner in vitro. Tissue Eng Part A. 2009;15(9):2459-2470. [61] ISSANAYAKA WL, XUAN Z, CHENGFEI Z, et al. Coculture of dental pulp stem cells with endothelial cells enhances osteo-/odontogenic and angiogenic potential in vitro. J Endod. 2012;38(4):454-463. [62] AGUIRRE A, PLANELL JA, ENGEL E. Dynamics of bone marrow-derived endothelial progenitor cell/mesenchymal stem cell interaction in co-culture and its implications in angiogenesis. Biochem Biophys Res Commun. 2010;400(2):284-291. [63] NGUYEN LL, D’AMORE PA. Cellular interactions in vascular growth and differentiation. Int Rev Cytol. 2001;204:1-48. [64] DARLAND DC, D’AMORE PA. Blood vessel maturation: vascular development comes of age. J Clin Invest. 1999;103(2):157-158. [65] AU P, TAM J, FUKUMURA D, et al. Bone marrow-derived mesenchymal stem cells facilitate engineering of long-lasting functional vasculature. Blood. 2008;111(9):4551-4558. [66] DISSANAYAKA WL, HARGREAVES KM, LIJIAN J, et al. The interplay of dental pulp stem cells and endothelial cells in an injectable peptide hydrogel on angiogenesis and pulp regeneration in vivo. Tissue Eng Part A. 2015;21(3-4):550-563. [67] ATLAS Y, GORIN C, NOVAIS A, et al. Microvascular maturation by mesenchymal stem cells in vitro improves blood perfusion in implanted tissue constructs. Biomaterials. 2021;268:120594. [68] DISSANAYAKA WL, ZHU L, HARGREAVES KM, et al. Scaffold-free prevascularized microtissue spheroids for pulp regeneration. J Dent Res. 2014;93(12):1296-1303. [69] XU X, LIANG C, GAO X, et al. Adipose tissue-derived microvascular fragments as vascularization units for dental pulp regeneration. J Endod. 2021;47(7):1092-1100. |
| [1] | Kong Yamin, Yan Juntao, Ma Bingxiang, Li Huawei. Massage vibration intervenes with MyoD expression and proliferation and differentiation of muscle satellite cells in rats with sciatic nerve injury [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1160-1166. |
| [2] | Wu Cong, Jia Quanzhong, Liu Lun. Relationship between transforming growth factor beta1 expression and chondrocyte migration in adult articular cartilage after fragmentation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1167-1172. |
| [3] | Wang Baojuan, Zheng Shuguang, Zhang Qi, Li Tianyang. Miao medicine fumigation can delay extracellular matrix destruction in a rabbit model of knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1180-1186. |
| [4] | Wang Qin, Shen Cheng, Liao Jing, Yang Ye. Dapagliflozin improves renal injury in diabetic nephropathy rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1216-1222. |
| [5] | Xiao Yang, Gong Liqiong, Fei Jing, Li Leiji. Effect of electroacupuncture on nerve growth factor and its receptor expression in facial nerve nucleus after facial nerve injury in rabbits [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1253-1259. |
| [6] | Zhou Ying, Zhang Huan, Liao Song, Hu Fanqi, Yi Jing, Liu Yubin, Jin Jide. Immunomodulatory effects of deferoxamine and interferon gamma on human dental pulp stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1012-1019. |
| [7] | Liu Feng, Peng Yuhuan, Luo Liangping, Wu Benqing. Plant-derived basic fibroblast growth factor maintains the growth and differentiation of human embryonic stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1032-1037. |
| [8] | Wang Xinmin, Liu Fei, Xu Jie, Bai Yuxi, Lü Jian. Core decompression combined with dental pulp stem cells in the treatment of steroid-associated femoral head necrosis in rabbits [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1074-1079. |
| [9] | Peng Kun. Improvement of the treatment effect of osteoporotic fractures: research status and strategy analysis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 980-984. |
| [10] | Xu Jing, Yan Yongmin, Cai Mengjie . miR-373 inhibits hepatic stellate cell activation by downregulating transforming growth factor beta type II receptor [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 756-761. |
| [11] | Shen Song, Xu Bin. Diffuse distribution of bone cement in percutaneous vertebroplasty reduces the incidence of refracture of adjacent vertebral bodies [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 499-503. |
| [12] | Hou Wanxing, Li Hongwei, Zheng Xin, Zhu Xianren. Correlation between preoperative magnetic resonance imaging findings and bone cement leakage after percutaneous vertebral augmentation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 504-509. |
| [13] | Yang Sidi, Wang Qian, Xu Nuo, Wang Ronghan, Jin Chuanqi, Lu Ying, Dong Ming. Biodentine enhances the proliferation and differentiation of osteoblasts through upregulating bone morphogenetic protein-2 [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 516-520. |
| [14] | Tan Guozhong, Tu Xinran, Guo Liyang, Zhong Jialin, Zhang Yang, Jiang Qianzhou. Biosafety evaluation of three-dimensional printed gelatin/sodium alginate/58S bioactive glass scaffolds for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 521-527. |
| [15] | Le Guoping, Zhang Ming, Xi Licheng, Luo Hanwen. Preparation and in vitro evaluation of vancomycin hydrochloride@polylactic acid-glycolic acid copolymer-chitosan-hyaluronic acid composite sustained-release microspheres [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 528-534. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||