Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (10): 1588-1596.doi: 10.12307/2022.208
Previous Articles Next Articles
Molecular mechanism of bone regeneration promoted by medical metal implant materials
Zhou Hongbo1, Yu Zhengwen2, 3, Liu Jianguo1, 2, 3
- 1School of Stomatology, Zunyi Medical University, Zunyi 563099, Guizhou Province, China; 2Key Laboratory of Oral Disease Research, Guizhou Institution of Higher Education, Zunyi 563006, Guizhou Province, China; 3Key Laboratory of Oral Disease Research of Zunyi City, Zunyi 563006, Guizhou Province, China
-
Received:2021-05-10Revised:2021-05-12Accepted:2021-06-09Online:2022-04-08Published:2021-10-27 -
Contact:Liu Jianguo, MD, Professor, Chief physician, School of Stomatology, Zunyi Medical University, Zunyi 563099, Guizhou Province, China; Key Laboratory of Oral Disease Research, Guizhou Institution of Higher Education, Zunyi 563006, Guizhou Province, China; Key Laboratory of Oral Disease Research of Zunyi City, Zunyi 563006, Guizhou Province, China -
About author:Zhou Hongbo, Master candidate, School of Stomatology, Zunyi Medical University, Zunyi 563099, Guizhou Province, China -
Supported by:National Key R&D Program Project of the Ministry of Science and Technology, No. 2016YFC1102800 (to LJG and YZW); Talent Base of Medical Biomaterials Research of Guizhou Province, No. QRLF[2018]3) (to LJG and YZW); Innovative Talent Base of Medical Biomaterials Research and Development of Zunyi, No. ZW[2019]69) (to LJG and YZW); Project of Zunyi Science and Technology Bureau, No. ZSKHSZ(2018)240 (to YZW); Academic Talents and Innovation Program of Zunyi Medical University, No. QKHPTRC[2017]5733-057) (to YZW)
Cite this article
Zhou Hongbo, Yu Zhengwen, Liu Jianguo. Molecular mechanism of bone regeneration promoted by medical metal implant materials[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(10): 1588-1596.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
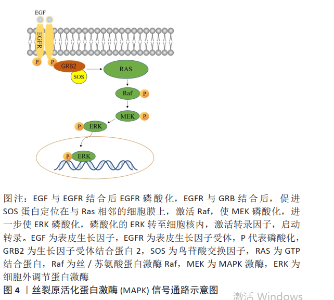
ZHOU等[10]设计了一个基于嵌合肽的生物界面,他们将可溶性PBI-BIP(peptide binding implant-bone-inducing protein)直接添加到成骨介质中,通过结合PBI-BIP来证实Wnt/β-catenin信号通路的激活。通过实时定量反转录聚合酶链反应分析,结果表明,结合的嵌合肽激活了成骨的Wnt/β-catenin信号通路,导致成骨基因表达的显著增加。人骨髓间充质干细胞的成骨潜能受医用金属植入材料释放的金属阳离子浓度影响,HONG等[11]通过反转录聚合酶链反应和蛋白质印迹分析成骨基因和蛋白表达,发现Ti6Al4V对人骨髓间充质干细胞的调控与Wnt/β-catenin信号通路有关,他们的研究表明,质量浓度5 ng/L的Ti6Al4V显著上调β-catenin和细胞周期蛋白D1的表达,而较高浓度的Ti6Al6V4显著下调骨形成中这些重要基因的表达。BERGLUND等[12]的研究表明,镁-钙-锶合金的溶解促进了骨髓间充质干细胞的增殖,一定浓度的镁离子能诱导骨髓间充质干细胞成骨分化。GU等[13]主要研究掺镁磷酸钙,并证明该材料促进骨髓间充质干细胞成骨分化,低于10 mmol的Mg2+浓度不会导致骨髓间充质干细胞死亡,掺镁磷酸三钙支架中释放的Mg2+量具有最佳的骨诱导作用。TSAO等[14]研究了细胞外高浓度镁对骨髓间充质干细胞成骨分化的影响以及镁转运蛋白SLC41A1(Solute carrier family 41 member A1)在成骨分化过程中的作用。实时定量qPCR结果显示,成骨诱导后,处于成骨早期和矿化开始前,镁浓度对野生型骨髓间充质干细胞 Wnt5a基因表达没有影响。然而,高浓度镁显著下调β-catenin表达,并且在SLC41A1基因被敲除后抑制作用减弱。 Dickkopf-1 (DKK1)是Wnt/β-catenin信号通路的分泌拮抗剂之一,其抑制矿化的作用已得到充分证实。高浓度的镁显著上调DKK1基因表达,并且在SLC41A1基因敲除后,该上调被减弱。Wnt信号可能是SLC41A1介导的骨髓间充质干细胞成骨分化的调节途径之一,其潜在机制值得进一步研究。HUNG等[15]研究了Mg2+对骨髓间充质干细胞 Wnt/β-catenin信号通路的影响,蛋白质印迹分析显示,Mg2+通过激活Wnt/β-catenin通路诱导成骨并刺激人骨髓间充质干细胞成骨分化。为了进一步了解Mg2+对Wnt/β-catenin通路的影响,他们评估了活性β-catenin的下游效应,发现在细胞质中积累后,β-catenin随后转移到细胞核中,在细胞核内β-catenin与TCF/LEF转录因子结合并取代阻遏物来调控下游基因的转录。WANG等[16]通过蛋白质印迹分析,Mg2+诱导糖原合成酶激酶3β磷酸化,阻碍了糖原合成酶激酶3β与β-catenin的结合,导致β-catenin水平升高,从而刺激了新骨的形成。SHI等[17]发现钽对成骨分化的影响是通过Wnt/β-catenin信号通路介导的,使用蛋白质印迹法定量孵育7 d后人骨髓间充质干细胞中的β-catenin来测量Wnt/β-catenin途径的激活。与钛组相比,钽组的β-catenin水平显著较高,通过定量反转录聚合酶链反应检测成骨细胞分化基因的表达,在钽组中,Sp7、Alpl、Col1a1和Smad6的表达增加了1倍,其他基因(Spp1、Runx2、Axin2、骨保护素及C-myc)的表达显著增加。Wnt/β-catenin信号通路下游成骨相关基因(Runx2、Col1a1、Axin2、Smad6、C-myc和骨保护素)的高表达证明了Wnt/β-catenin信号通路在更大程度上被激活[18]。JING等[19]系统评价了体外和体内脉冲电磁场刺激对多孔钛生物学性能的潜在影响。首先,他们研究了脉冲电磁场对体外成骨细胞活性和功能的影响及其潜在机制;此外,还研究了脉冲电磁场在体内多孔钛植入物成骨的分子信号通路机制;通过半定量反转录聚合酶链反应分析表明脉冲电磁场刺激显著促进成骨相关基因的表达,包括Runx2、Osx和Ⅰ型胶原,增加了经典Wnt信号的基因表达;还揭示了经典的Wnt/β-catenin信号与调节脉冲电磁场诱导的多孔钛种植体成骨改善骨缺损修复有关。Wnt具有上调Osx55表达的能力,此发现与体内研究保持一致,再次证明了脉冲电磁场诱导的经典Wnt信号的激活[20-21]。 2.2 医用金属植入材料促骨再生的丝裂原活化蛋白激酶 (mitogen-activated protein kinase,MAPK)信号通路机制 传统的MAPK包括3个亚家族成员:①细胞外调节蛋白激酶 (extracellular regulated protein kinases,ERK)ERK1/2、ERK5;②应激活化蛋白激酶(c-Jun N-terminal kinase,JNK)JNK1/2/3;③p38。MAPK信号通路主要参与转导胞外刺激引起细胞生长、分化和凋亡。一旦细胞接触刺激物,MAPKK激酶(MAP3K)被激活并磷酸化MAPK激酶(MAP2K),而后磷酸化激活MAPKs[22]。在MAPK家族中,ERK1/2和p38参与生物材料诱导的干细胞分化已被广泛记录[23],图4为MAPK/ERK信号通路示意图。"
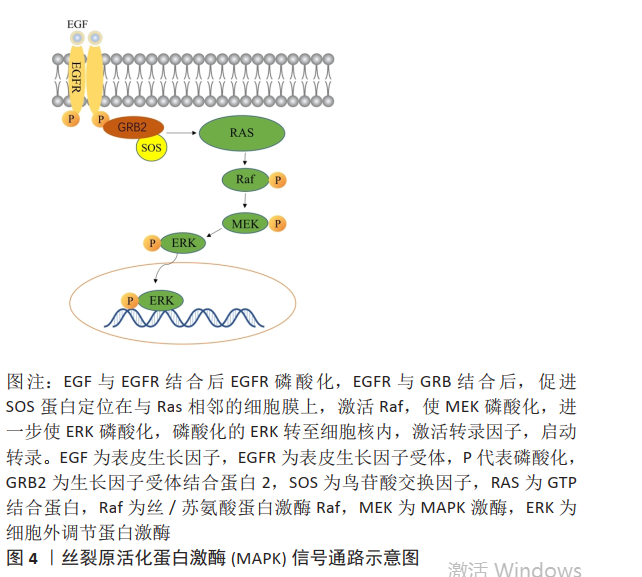
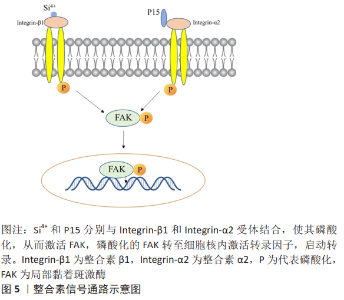
KIM等[24]介绍了一种结合茚化合物KR-34893的磷酸镁(MgP)陶瓷支架,作者发现KR-MgP支架通过诱导矿物质沉积和成骨细胞标记基因表达,促进骨髓间充质干细胞和小鼠胚胎成骨细胞前体细胞(MC3T3-E1)的成骨分化;他们发现KR-34893可能通过MAPK/ERK信号通路诱导骨形态发生蛋白7表达和Smad 1/5/8磷酸化,从而促进骨髓间充质干细胞的成骨分化。多孔钽作为一种理想的新型移植材料,具有优异的力学性能和耐腐蚀性能,因其优异的细胞相容性和诱导骨形成的能力,在生物医学领域受到越来越多的关注。DOU等[25]采用三维印刷结合化学气相沉积的方法制备了相同孔径的多孔Ti6Al4V和多孔钽,分别通过成骨活性测定、qPCR和蛋白质印迹法测定培养7,14和21 d两组的成骨活性、碱性磷酸酶、Ⅰ型胶原、骨连接蛋白和骨钙素的mRNA表达水平以及MAPK/ERK信号通路标记物p-ERK的蛋白表达水平,两组分别用MAPK/ERK特异性抑制剂U0126处理,然后分别用qPCR和蛋白质印迹法测定培养物中成骨基因的表达水平和p-ERK的蛋白表达水平,研究结果发现,与广泛使用的钛合金材料相比,多孔钽能促进骨髓间充质干细胞的黏附和增殖,多孔钽可以通过激活MAPK/ERK信号通路来调节碱性磷酸酶、Ⅰ型胶原、骨连接蛋白和骨钙素等成骨基因的表达,从而调节骨髓间充质干细胞体外成骨分化的分子机制。CAO等[26]认为钛负载的银纳米粒子通过激活MAPK/ERK信号通路促进骨髓间充质干细胞成骨分化。锌生物材料因其与骨相似的力学性能、生物相容性和与组织愈合速度更匹配的降解性,近年来引起了学者们的关注。ZHU等[27]研究了人骨髓间充质干细胞对锌的生物反应和潜在的细胞信号机制,并用典型的镁材料AZ31作对比,利用小核糖核酸干扰敲除相关的关键分子,他们的研究结果阐明了锌诱导成骨的细胞信号传导机制。瞬时受体电位离子通道蛋白7(transient receptor potential melastatin 7,TRPM7)和GPR39是促进Zn2+进入人骨髓间充质干细胞的主要细胞受体,Zn2+在细胞内激活依赖于cAMP的蛋白激酶A(cyclic-AMP dependent protein kinase A,cAMP-PKA)途径,并触发细胞内Ca2+反应,导致MAPK的激活,从而增强了人骨髓间充质干细胞生长、分化、成骨基因表达、基质产生和矿物质沉积。尽管钛及其合金已被广泛用作骨科和牙科的植入物,但如何实现钛表面优异的生物活性仍是一个挑战。研究表明,ERK1/2途径的激活广泛参与骨髓间充质干细胞的成骨分化,并被钛植入物上的纳米形貌和生物活性离子(如锶、锌和硅)激活[28-30]。ARAúJO-GOMES等[31]研究发现,硅涂层植入物可以促进骨组织的生长,并实现体内骨整合的效果,硅涂层种植体显示出良好的骨诱导性能,而无硅涂层的种植体仅显示出骨传导特性。 YAN等[32]通过电化学阳极氧化和水热处理,在钛表面制备了掺镁二氧化钛纳米管阵列,镁以钛酸镁的形式存在于纳米管中,成骨相关基因(碱性磷酸酶、Ⅰ型胶原、骨钙蛋白和Runx2)的mRNA表达在材料表面均显著上调,ERK1/2信号通路在材料表面被激活,表明镁离子通过MAPK/ERK信号通路增强钛种植体的骨诱导活性。为了提高镁合金的生物可降解性和骨诱导性,ZHAO等[33]采用电泳沉积结合磷酸盐缓冲溶液中的转化,制备了一种新型纳米石墨烯-磷酸钙-壳聚糖/AZ91D复合材料,评价了其体外生物相容性、骨诱导性和相关信号通路。他们的研究表明,从纳米石墨烯-磷酸钙-壳聚糖/AZ91D材料中释放的镁通过MAPK/ERK信号通路诱导骨髓间充质干细胞成骨分化。 WANG等[34]制备了Mg、Zn和Mg-Zn提取物,并研究了这些提取物对人骨髓间充质干细胞成骨分化和MAPK信号通路的特异性影响。Mg和Mg-Zn提取物均能显著促进人骨髓间充质干细胞的成骨分化,表现为碱性磷酸酶水平升高、钙结节形成增强,成骨标志物(包括骨形态发生蛋白、Ⅰ型胶原、Runx2和Osx)mRNA和蛋白质表达水平升高;同时,Mg培养基和Mg-Zn培养基均显著增强人骨髓间充质干细胞中MAPK信号的激活;通过在Mg-Zn培养基中添加ERK1/2信号、p38信号或JNK信号抑制剂,或在人骨髓间充质干细胞中沉默p38,他们发现该Mg-Zn合金中的Mg2+可能通过p38 MAPK信号调节的Runx2/Osx促进人骨髓间充质干细胞成骨分化。 WANG等[16]通过腐蚀试验,确定纯镁的降解能够产生碱性微环境,进一步确定Mg2+促进成骨细胞的增殖和分化。蛋白质印迹分析表明,在Mg2+处理后,ERK的磷酸化增加,阻断ERK与c-fos的结合,从而提高c-fos蛋白水平,促进细胞增殖;由于镁的腐蚀,当Mg2+形成时,溶液的碱度同时增加,释放Mg2+的成骨潜能可能与新创造的碱性微环境和通过激活MAPK/ERK信号通路促进细胞增殖和成骨分化有关。 JIANG等[35]采用碱热处理技术在Mg-3AI-1Zn合金表面包覆了多孔β-磷酸三钙,β-磷酸三钙-Mg-3AI-1Zn表面诱导SaOS-2细胞中关键细胞内信号蛋白的激活,他们的研究结果表明,β-磷酸三钙包覆的镁合金可能通过ERK1/2 MAPK信号促进镁合金表面培养的SaOS-2细胞的增殖。 锶是人体内的一种微量元素,有研究表明,在种植体表面添加锶元素或制备含锶涂层可以显著提高种植体的生物活性[36]。LI等[28]研究了Mg-1Ca-Xwt% Sr (X=0.2,0.5,1.0,2.0)合金对MC3T3-E1成骨分化和矿化的影响,结果表明,Mg-1Ca-2.0Sr合金促进成骨细胞的分化和矿化水平效果最为显著。为了进一步研究其潜在机制,采用反转录聚合酶链反应和蛋白质印迹法分别分析成骨相关基因和成骨相关细胞内信号通路的基因表达水平。反转录聚合酶链反应结果显示,Mg-1Ca-2.0Sr合金显著上调Runx2和Osx转录因子、整合素亚单位以及碱性磷酸酶、骨涎蛋白、Ⅰ型胶原、骨钙素和骨桥蛋白的表达;蛋白印迹分析结果表明,Mg-1Ca-2.0Sr合金快速诱导细胞外信号ERK激活。Mg-1Ca-2.0Sr合金具有良好的生物相容性并通过ERK/MAPK途径促进成骨,有望成为临床骨修复材料。 2.3 医用金属植入材料促骨再生的整合素信号通路机制 整合素受体通常包含α和β亚单位,这些亚单位形成22个不同的异源二聚体复合物,与整合素一起参与多种生物学过程。整合素及其受体结合参与3条主要信号通路的活化:细胞骨架重排、细胞增殖和细胞存活通路。整合素作为细胞黏附、细胞骨架蛋白和胞内信号通路的交汇点,参与多种生物学行为,这其中就包括诱导骨髓间充质干细胞成骨分化。研究表明,种植体的表面形态和化学成分在骨结合中起着重要作用,与微米或纳米尺度的表面形态相比,微/纳米复合材料形态能更好地模拟人类细胞自然生长的微环境,因此适合成骨细胞的生长。植入物表面的化学成分可以通过诱导表面成骨细胞释放生物活性元素或形成化学键来影响其行为[37]。ZHAO等[38]采用微弧氧化技术成功制备了一层由掺硅微孔钛组成的涂层,通过体内和体外实验研究了涂层的生物活性和骨结合性能。硅钛微孔涂层中的微纳米结构具有更大的表面积,可以为整合素结合提供更多的空间位点,从而影响整合素的聚集,促进成骨细胞的黏附。硅二氧化钛微孔涂层在弱碱性环境中溶解释放硅离子,从而激活整合素β1介导的信号通路,见图5。"
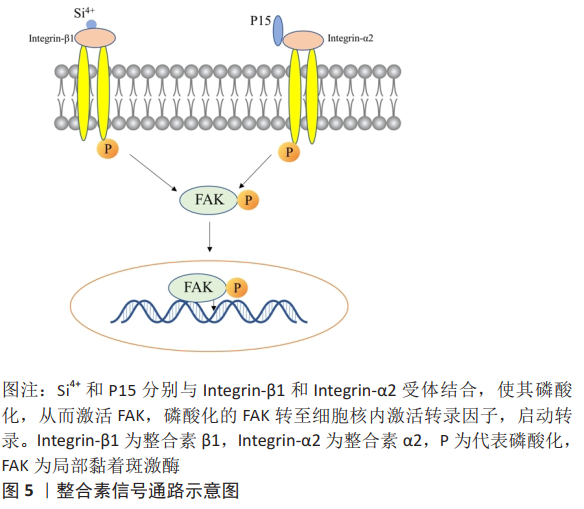
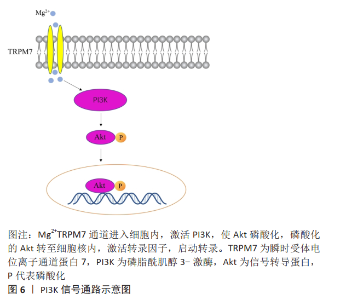
改变跨膜蛋白的结构,促进成骨细胞的增殖。GITTENS等[39]评估了成骨标记物和整合素在不同微纳米修饰的Ti6Al4V表面成骨基因的表达水平,研究结果表明微粗糙表面和微/纳米粗糙表面之间成骨标记物的基因表达水平相似,证明这些表面上有更强的成骨环境,并揭示该成骨环境可能与激活整合素信号通路有关。 P15是一种合成的15氨基酸肽,模拟人类胶原蛋白α-1链中的细胞结合结构域,LIU等[40]通过实时定量聚合酶链反应、蛋白质印迹分析和荧光免疫组织化学方法测量成骨细胞基因表达和分化,评估P15肽共价栓系到钛表面的骨整合特性。他们的研究结果表明P15表面不仅增加整合素α2的蛋白水平,而且激活局部黏着斑激酶信号,见图5,通过荧光免疫组织化学和蛋白质印迹分析观察到整合素α2表达和磷酸化局部黏着斑激酶蛋白活化的增加,表明通过P15肽结合激活整合素信号通路可增强成骨细胞分化。 2.4 医用金属植入材料促骨再生的磷脂酰肌醇3-激酶(phosphatidylinositol 3 kinase,PI3K)信号通路机制 PI3K蛋白家族参与细胞增殖、分化、凋亡等多种细胞功能的调节,近年来有学者研究发现PI3K信号通路与细胞成骨分化密切相关。QI等[6]通过下调瞬时受体电位离子通道蛋白7基因的表达发现,镁离子诱导的成骨、矿化、迁移和趋化性显著受阻,从而证实瞬时受体电位离子通道蛋白7介导了镁离子在人体内的成骨分化诱导。使用茜素红S和碱性磷酸酶检测镁离子在成骨细胞骨化和矿化中的作用,结果也表明镁离子可以通过瞬时受体电位离子通道蛋白7/PI3K信号通路上调Runx2。WANG等[41]对镁预处理的骨髓间充质干细胞应用沃特曼蛋白特异性抑制剂,发现细胞密度和活力显著降低,抑制了碱性磷酸酶活性和基质矿化,提示镁离子可引起骨代谢的一系列变化,通过激活PI3K/Akt通路[42],促进成骨细胞分化标志物(如碱性磷酸酶和骨形态发生蛋白)的表达,促进成骨细胞增殖分化[43]。 WANG等[44]通过化学沉积法在可生物降解的镁-钕-锌-锆合金(简称JDBM)表面开发了一种SrHPO4涂层。用SrHPO4包被的JDBM离子释放试验提取物处理的MC3T3-E1细胞的RNA测序显示Toll样受体4增加,随后下游PI3K/Akt信号通路激活,引起MC3T3-E1的增殖和生长。他们还探讨了影响Toll样受体4表达下游MC3T3-E1细胞生长和增殖的机制,发现虽然PI3K和p-Akt的表达在用SrHPO4包被的JDBM提取物处理的细胞中升高,但总Akt 的表达保持不变。然而,Toll样受体4信号传导抑制剂CLI-095显著降低了PI3K和p-Akt的表达,减弱了MC3T3-E1的成骨分化。表明PI3K/Akt途径受到上游Toll样受体4抑制剂的抑制,发现Toll样受体4/PI3K/Akt信号通路是控制成骨反应的潜在机制。其中,PI3K/Akt途径仅被Toll样受体4抑制剂CLI-095减弱,而不是完全失活[45]。 ZHANG等[46]检测了镁离子对人成骨细胞成骨、趋化和抗碱性应力的影响,模拟可生物降解的镁基合金植入物在体外的骨修复作用,并探讨了瞬时受体电位离子通道蛋白7/PI3K信号通路在镁离子诱导的骨修复过程中通过敲除瞬时受体电位离子通道蛋白7和拮抗PI3K活性的调节作用,见图6。"

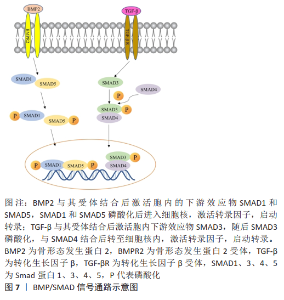
结果表明,镁离子通过瞬时受体电位离子通道蛋白7/PI3K信号通路上调Runx2和碱性磷酸酶的表达,可显著增强人成骨细胞的成骨活性。此外,基质金属蛋白酶2和血管内皮生长因子的表达水平受瞬时受体电位离子通道蛋白7/PI3K信号通路调节后增加,该信号通路通过诱导细胞迁移从低到高镁离子环境招募成骨细胞。 2.5 医用金属植入材料促骨再生的骨形态发生蛋白/Smad信号通路机制 其在成骨细胞分化的调节中起关键作用。骨形态发生蛋白可通过与膜中的丝氨酸/苏氨酸激酶受体结合并随后在丝氨酸463和S465位点磷酸化下游效应物Smad1和Smad5来发挥其功能,磷酸化的Smad1/5然后被转移到细胞核中以激活靶基因转录,见图7。"
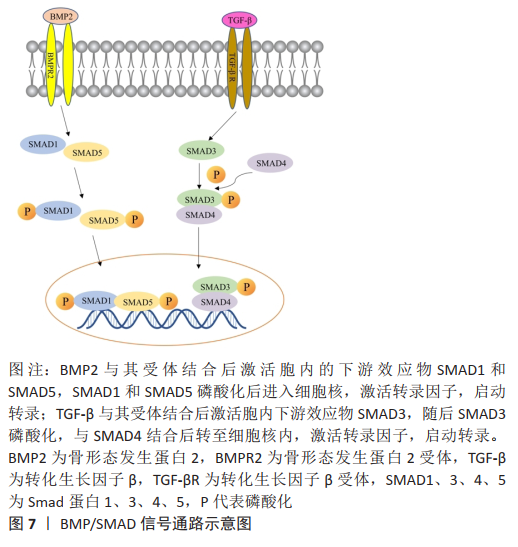
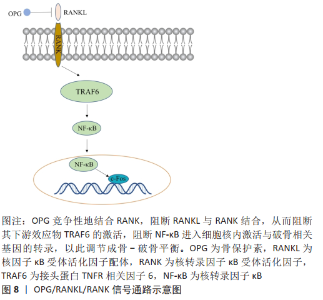
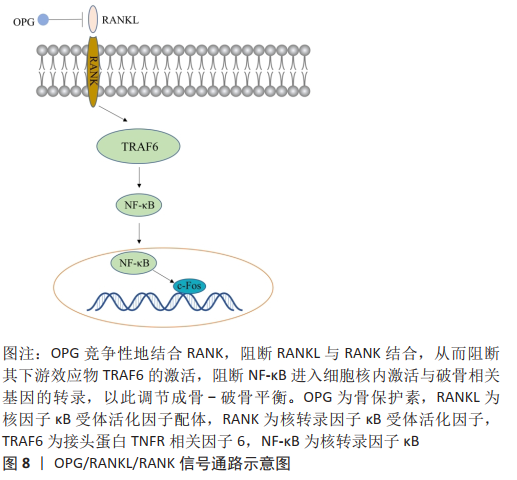
CHEN等[47]证实了这一点,他们通过将原代人成骨细胞培养在含有氯化锆或硝酸氧锆的培养基中,评估成骨细胞的增殖、分化和钙沉积。人成骨细胞培养物与锆离子的孵育增加了人成骨细胞的增殖和成骨细胞分化遗传标记的基因表达;锆离子对人成骨细胞的体外作用以前尚未研究过,此研究结果表明,锆离子能促进体外人成骨细胞的增殖和分化,这种作用与骨形态发生蛋白2表达的上调和骨形态发生蛋白信号的增加有关,并可能由其介导。由于骨形态发生蛋白2及其受体基因的表达被锆化合物上调,进一步研究了骨形态发生蛋白2蛋白的表达水平及其下游效应物Smad1和p-Smad1/5。以往的研究表明,在含锆陶瓷支架上的原代人成骨细胞的生长诱导骨形态发生蛋白2的表达[48]。与骨形态发生蛋白2信号的激活一致的是,用锆离子处理的血红蛋白细胞质和细胞核中磷酸化的Smad1/5水平显著增加。观察到的磷酸化Smad总水平的增加及其核定位的增加表明,这些转录因子通过骨形态发生蛋白配体与其受体的相互作用而激活,并具有控制成骨细胞基因表达以响应锆离子的潜在能力。在与锆离子共同处理的人类成骨细胞中,骨形态发生蛋白信号通路的抑制剂noggin对成骨基因表达的抑制提供了额外的证据,表明锆离子诱导的成骨作用与骨形态发生蛋白信号有关。 微量镁离子通过抑制Toll样受体-核转录因子κB信号通路诱导巨噬细胞M2表型改变和抗炎细胞因子的释放,同时也刺激巨噬细胞中骨诱导分子的表达,而镁离子/巨噬细胞条件培养基通过骨形态发生蛋白/Smad信号通路促进骨髓间充质干细胞的成骨。ZHANG等[49]为探讨镁离子/骨桥蛋白264.7细胞条件培养基中骨髓间充质干细胞成骨能力提高的分子机制,对骨桥蛋白/Smad信号通路进行了研究。反转录聚合酶链反应结果及蛋白印迹分析进一步证实了Smad4和骨形态发生蛋白R1A的蛋白表达。微量镁离子通过抑制Toll样受体-核转录因子κB信号通路诱导巨噬细胞的M2表型改变和抗炎细胞因子的释放,刺激巨噬细胞表达骨形态发生蛋白2,激活骨髓间充质干细胞中的骨形态发生蛋白2信号通路,从而促进成骨分化。他们的实验结果表明,控制镁离子浓度可以赋予镁支架良好的骨免疫调节性能,从而为镁基骨生物材料的开发和改性提供了基础依据。 SHI等[17]发现钽对成骨分化的影响是通过Wnt/β-catenin和转化生长因子β/Smad信号通路介导的。钽可以在更大程度上激活这些信号通路,该研究表明转化生长因子β/Smad信号通路除了减少RANKL成骨细胞分泌外,还能促进基质合成和成骨细胞分化,这可能间接促进成骨分化。体外实验证实转化生长因子β/Smad信号通路被激活。使用Smad3特异性抑制剂SIS3阻断转化生长因子β/Smad信号导致骨分化的显著抑制,再次证明钽可以激活转化生长因子β/Smad信号通路。 2.6 医用金属植入材料促骨再生的骨保护素/RANKL/RANK信号通路机制 骨保护素/RANKL/RANK信号通路也参与诱导骨髓间充质干细胞成骨分化,骨保护素可通过抑制RANK与RANKL结合,从而调节成骨细胞-破骨细胞的串扰,见图8。 LI等[50]用化学沉积法在镁锶合金上制备了一种新型双层涂层ZA-CaP。通过定量实时聚合酶链反应和蛋白质印迹法表明ZA-CaP双层包被的镁锶合金可以通过雌激素受体α和核转录因子κB信号通路调节成骨和破骨细胞生成。此外, ZA-CaP双层涂层镁锶合金可以通过骨保护素/RANKL/RANK信号通路调节成骨细胞-破骨细胞的串扰,增加共培养体系中骨保护素和RANKL的比例,促进骨重建过程的平衡。证明ZA-CaP双层包被的镁锶合金通过抑制破骨细胞中κB激酶α的激活和核转录因子κB p65亚单位的磷酸化来抑制核转录因子κB信号通路,表明ZA-CaP双层涂层镁锶合金可能代表一种新的局部辅助治疗骨缺损修复的材料。当体内镁离子浓度异常时,也可通过激活骨保护素/RANKL/RANK信号通路来调控成骨细胞的增殖和分化[51]。 "
| [1] ORYAN A, ALIDADI S. Reconstruction of radial bone defect in rat by calcium silicate biomaterials. Life Sci. 2018;201:45-53. [2] 刘建国,周宏博.医用β钛合金的性能研究现状[J].口腔医学研究, 2020,36(6):501-508. [3] ZHAO QM, LI XK, GUO S, et al. Osteogenic activity of a titanium surface modified with silicon-doped titanium dioxide. Mater Sci Eng C Mater Biol Appl. 2020;110:110682. [4] 张文毓.生物医用金属材料研究现状与应用进展[J].金属世界, 2020(1):21-27. [5] KHARE D, BASU B, DUBEY AK. Electrical stimulation and piezoelectric biomaterials for bone tissue engineering applications. Biomaterials. 2020;258:120280. [6] QI T, WENG J, YU F, et al. Insights into the role of magnesium ions in affecting osteogenic differentiation of mesenchymal stem cells. Biol Trace Elem Res. 2021;199(2):559-567. [7] Onder S, Calikoglu-Koyuncu AC, Kazmanli K, et al. Magnesium doping on TiN coatings affects mesenchymal stem cell differentiation and proliferation positively in a dose-dependent manner. Biomed Mater Eng. 2018;29(4):427-438. [8] 庞新岗,李永刚,包倪荣,等.骨代谢主要信号通路及信号分子的研究进展[J].基础医学与临床,2018,38(12):1799-1803. [9] 陈伟健,晋大祥,谢炜星,等.Runx2基因参与骨代谢相关通路的研究进展[J].中国骨质疏松杂志,2018,24(4):557-560. [10] ZHOU Y, SNEAD ML, TAMERLER C. Bio-inspired hard-to-soft interface for implant integration to bone. Nanomedicine. 2015;11(2):431-434. [11] HONG H, XU G, DENG H, et al. Concentration-dependent regulation of tial6v4 particles on the osteogenesis potential of human bone marrow mesenchymal stem cells. Biol Trace Elem Res. 2020;195(2):445-453. [12] BERGLUND IS, DIRR EW, RAMASWAMY V, et al. The effect of Mg-Ca-Sr alloy degradation products on human mesenchymal stem cells. J Biomed Mater Res B Appl Biomater. 2018;106(2):697-704. [13] GU Y, ZHANG J, ZHANG X, et al. Three-dimensional printed mg-doped β-tcp bone tissue engineering scaffolds: effects of magnesium ion concentration on osteogenesis and angiogenesis in vitro. Tissue Eng Regen Med. 2019;16(4):415-429. [14] TSAO YT, SHIH YY, LIU YA, et al. Knockdown of SLC41A1 magnesium transporter promotes mineralization and attenuates magnesium inhibition during osteogenesis of mesenchymal stromal cells. Stem Cell Res Ther. 2017;8(1):39. [15] HUNG CC, CHAYA A, LIU K, et al. The role of magnesium ions in bone regeneration involves the canonical Wnt signaling pathway. Acta Biomater. 2019;98:246-255. [16] WANG Y, GENG Z, HUANG Y, et al. Unraveling the osteogenesis of magnesium by the activity of osteoblasts in vitro. J Mater Chem B. 2018;6(41):6615-6621. [17] SHI LY, WANG A, ZANG FZ, et al. Tantalum-coated pedicle screws enhance implant integration. Colloids Surf B Biointerfaces. 2017;160: 22-32. [18] KOBAYASHI Y, UEHARA S, KOIDE M, et al. The regulation of osteoclast differentiation by Wnt signals. Bonekey Rep. 2015;4:713. [19] JING D, ZHAI M, TONG S, et al. Pulsed electromagnetic fields promote osteogenesis and osseointegration of porous titanium implants in bone defect repair through a Wnt/β-catenin signaling-associated mechanism. Sci Rep. 2016;6:32045. [20] JING D, LI F, JIANG M, et al. Pulsed electromagnetic fields improve bone microstructure and strength in ovariectomized rats through a Wnt/Lrp5/β-catenin signaling-associated mechanism. PLoS One. 2013;8(11):e79377. [21] JING D, CAI J, WU Y, et al. Pulsed electromagnetic fields partially preserve bone mass, microarchitecture, and strength by promoting bone formation in hindlimb-suspended rats. J Bone Miner Res. 2014; 29(10):2250-2261. [22] 周雷,王明海.成骨分化相关信号通路的研究进展[J].临床医学进展,2017,7(4):235-241. [23] WANG C, LIN K, CHANG J, et al. Osteogenesis and angiogenesis induced by porous β-CaSiO(3)/PDLGA composite scaffold via activation of AMPK/ERK1/2 and PI3K/Akt pathways. Biomaterials. 2013;34(1): 64-77. [24] KIM JA, YUN HS, CHOI YA, et al. Magnesium phosphate ceramics incorporating a novel indene compound promote osteoblast differentiation in vitro and bone regeneration in vivo. Biomaterials. 2018;157:51-61. [25] DOU X, WEI X, LIU G, et al. Effect of porous tantalum on promoting the osteogenic differentiation of bone marrow mesenchymal stem cells in vitro through the MAPK/ERK signal pathway. J Orthop Translat. 2019;19:81-93. [26] CAO H, ZHANG W, MENG F, et al. Osteogenesis catalyzed by titanium-supported silver nanoparticles. ACS Appl Mater Interfaces. 2017;9(6):5149-5157. [27] ZHU D, SU Y, YOUNG ML, et al. Biological responses and mechanisms of human bone marrow mesenchymal stem cells to zn and mg biomaterials. ACS Appl Mater Interfaces. 2017;9(33):27453-27461. [28] LI M, HE P, WU Y, et al. Stimulatory effects of the degradation products from Mg-Ca-Sr alloy on the osteogenesis through regulating ERK signaling pathway. Sci Rep. 2016;6:32323. [29] ZHAO L, WANG H, HUO K, et al. The osteogenic activity of strontium loaded titania nanotube arrays on titanium substrates. Biomaterials. 2013;34(1):19-29. [30] HUO K, ZHANG X, WANG H, et al. Osteogenic activity and antibacterial effects on titanium surfaces modified with Zn-incorporated nanotube arrays. Biomaterials. 2013;34(13):3467-3478. [31] ARAÚJO-GOMES N, ROMERO-GAVILÁN F, GARCÍA-ARNÁEZ I, et al. Osseointegration mechanisms: a proteomic approach. J Biol Inorg Chem. 2018;23(3):459-470. [32] YAN Y, WEI Y, YANG R, et al. Enhanced osteogenic differentiation of bone mesenchymal stem cells on magnesium-incorporated titania nanotube arrays. Colloids Surf B Biointerfaces. 2019;179:309-316. [33] ZHAO M, DAI Y, LI X, et al. Evaluation of long-term biocompatibility and osteogenic differentiation of graphene nanosheet doped calcium phosphate-chitosan AZ91D composites. Mater Sci Eng C Mater Biol Appl. 2018;90:365-378. [34] WANG Z, LIU Q, LIU C, et al. Mg2+ in β-TCP/Mg-Zn composite enhances the differentiation of human bone marrow stromal cells into osteoblasts through MAPK-regulated Runx2/Osx. J Cell Physiol. 2020;235(6):5182-5191. [35] JIANG T, GUO L, NI S, et al. Upregulation of cell proliferation via Shc and ERK1/2 MAPK signaling in SaOS-2 osteoblasts grown on magnesium alloy surface coating with tricalcium phosphate. J Mater Sci Mater Med. 2015;26(4):158. [36] ZHAO Q, YI L, JIANG L, et al. Surface functionalization of titanium with zinc/strontium-doped titanium dioxide microporous coating via microarc oxidation. Nanomedicine. 2019;16:149-161. [37] CHOUIRFA H, BOULOUSSA H, MIGONNEY V, et al. Review of titanium surface modification techniques and coatings for antibacterial applications. Acta Biomater. 2019;83:37-54. [38] ZHAO QM, LI XK, GUO S, et al. Osteogenic activity of a titanium surface modified with silicon-doped titanium dioxide. Mater Sci Eng C Mater Biol Appl. 2020;110:110682. [39] GITTENS RA, OLIVARES-NAVARRETE R, HYZY SL, et al. Superposition of nanostructures on microrough titanium-aluminum-vanadium alloy surfaces results in an altered integrin expression profile in osteoblasts. Connect Tissue Res. 2014;55 Suppl 1(1):164-168. [40] LIU Q, LIMTHONGKUL W, SIDHU G, et al. Covalent attachment of P15 peptide to titanium surfaces enhances cell attachment, spreading, and osteogenic gene expression. J Orthop Res. 2012;30(10):1626-1633. [41] WANG J, MA XY, FENG YF, et al. Magnesium ions promote the biological behaviour of rat calvarial osteoblasts by activating the PI3K/Akt signalling pathway. Biol Trace Elem Res. 2017;179(2):284-293. [42] WU SS, LIANG QH, LIU Y, et al. Omentin-1 Stimulates Human Osteoblast Proliferation through PI3K/Akt Signal Pathway. Int J Endocrinol. 2013; 2013:368970. [43] WU CM, CHEN PC, LI TM, et al. Si-Wu-tang extract stimulates bone formation through PI3K/Akt/NF-κB signaling pathways in osteoblasts. BMC Complement Altern Med. 2013;13:277. [44] WANG Z, WANG X, PEI J, et al. Degradation and osteogenic induction of a SrHPO4-coated Mg-Nd-Zn-Zr alloy intramedullary nail in a rat femoral shaft fracture model. Biomaterials. 2020;247:119962. [45] XU X, LIU X, YANG Y, et al. Resveratrol inhibits the development of obesity-related osteoarthritis via the TLR4 and PI3K/Akt signaling pathways. Connect Tissue Res. 2019;60(6):571-582. [46] ZHANG X, ZU H, ZHAO D, et al. Ion channel functional protein kinase TRPM7 regulates Mg ions to promote the osteoinduction of human osteoblast via PI3K pathway: in vitro simulation of the bone-repairing effect of Mg-based alloy implant. Acta Biomater. 2017;63:369-382. [47] CHEN Y, ROOHANI-ESFAHANI SI, LU Z, et al. Zirconium ions up-regulate the BMP/Smad signaling pathway and promote the proliferation and differentiation of human osteoblasts. PLoS One. 2015;10(1):e0113426. [48] LU Z, WANG G, ROOHANI-ESFAHANI I, et al. Baghdadite ceramics modulate the cross talk between human adipose stem cells and osteoblasts for bone regeneration. Tissue Eng Part A. 2014;20(5-6): 992-1002. [49] Zhang X, Chen Q, Mao X. Magnesium enhances osteogenesis of BMSCs by tuning osteoimmunomodulation. Biomed Res Int. 2019; 2019:7908205. [50] Li M, Wan P, Wang W, et al. Regulation of osteogenesis and osteoclastogenesis by zoledronic acid loaded on biodegradable magnesium-strontium alloy. Sci Rep. 2019;9(1):933. [51] Kulkarni RN, Bakker AD, Everts V, et al. Inhibition of osteoclastogenesis by mechanically loaded osteocytes: involvement of MEPE. Calcif Tissue Int. 2010;87(5):461-468. |
| [1] | Li Rui, Liu Zhen, Guo Zige, Lu Ruijie, Wang Chen. Aspirin-loaded chitosan nanoparticles and polydopamine modified titanium sheets improve osteogenic differentiation [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 374-379. |
| [2] | Wang Junxiang, Sun Jiangwei, Bai Bujiafu·Yellisi, Wang Zhaoxin, Nijati·Turson. Effect of three abutment materials on bone stress around maxillary angle implant under dynamic loading [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 398-405. |
| [3] | Dai Xianglin, Zhang Wenfeng, Yao Xijun, Shang Jiaqi, Huang Qiujin, Ren Yifan, Deng Jiupeng. Barium titanate/polylactic acid piezoelectric composite film affects adhesion, proliferation, and osteogenic differentiation of MC3T3-E1 cells [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 367-373. |
| [4] | Liu Wentao, Feng Xingchao, Yang Yi, Bai Shengbin. Effect of M2 macrophage-derived exosomes on osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(在线): 1-6. |
| [5] | Xue Yadong, Zhou Xinshe, Pei Lijia, Meng Fanyu, Li Jian, Wang Jinzi . Reconstruction of Paprosky III type acetabular defect by autogenous iliac bone block combined with titanium plate: providing a strong initial fixation for the prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1424-1428. |
| [6] | Xiao Hao, Liu Jing, Zhou Jun. Research progress of pulsed electromagnetic field in the treatment of postmenopausal osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1266-1271. |
| [7] | Tian Chuan, Zhu Xiangqing, Yang Zailing, Yan Donghai, Li Ye, Wang Yanying, Yang Yukun, He Jie, Lü Guanke, Cai Xuemin, Shu Liping, He Zhixu, Pan Xinghua. Bone marrow mesenchymal stem cells regulate ovarian aging in macaques [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 985-991. |
| [8] | Gao Yujin, Peng Shuanglin, Ma Zhichao, Lu Shi, Cao Huayue, Wang Lang, Xiao Jingang. Osteogenic ability of adipose stem cells in diabetic osteoporosis mice [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 999-1004. |
| [9] | Hou Jingying, Guo Tianzhu, Yu Menglei, Long Huibao, Wu Hao. Hypoxia preconditioning targets and downregulates miR-195 and promotes bone marrow mesenchymal stem cell survival and pro-angiogenic potential by activating MALAT1 [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1005-1011. |
| [10] | Liang Xuezhen, Yang Xi, Li Jiacheng, Luo Di, Xu Bo, Li Gang. Bushen Huoxue capsule regulates osteogenic and adipogenic differentiation of rat bone marrow mesenchymal stem cells via Hedgehog signaling pathway [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1020-1026. |
| [11] | Fang Xiaolei, Leng Jun, Zhang Chen, Liu Huimin, Guo Wen. Systematic evaluation of different therapeutic effects of mesenchymal stem cell transplantation in the treatment of ischemic stroke [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1085-1092. |
| [12] | Wu Weiyue, Guo Xiaodong, Bao Chongyun. Application of engineered exosomes in bone repair and regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1102-1106. |
| [13] | Wang Hailong, Li Long, Maihemuti·Yakufu, Chen Hongtao, Liu Xu, Yilihamu·Tuoheti. Finite element analysis of stress distribution of acetabular prosthesis in the Lewinnek safety zone [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 843-847. |
| [14] | Gao Wenbo, Ma Zongmin, Li Shuxian, Nie Xiuji. Finite element analysis on the effect of implant length and diameter on initial stability under different bone conditions [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 875-880. |
| [15] | Yuan Jing, Sun Xiaohu, Chen Hui, Qiao Yongjie, Wang Lixin. Digital measurement and analysis of the distal femur in adults with secondary knee valgus deformity [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 881-885. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||