1.1 设计 体外细胞实验,包括间充质干细胞的质量研究(细胞形态、表型、倍增时间、成骨成脂分化能力),功能研究(免疫调节功能及抗炎功能)及转录组学分析。
1.2 时间及地点 实验于2021年10月至2022年4月在天九再生医学(天津)科技有限公司完成。
1.3 材料
1.3.1 脐带 脐带由健康产妇分娩后自愿捐赠,由天津市第五中心医院提供。脐带采集前孕妇均进行免疫四项(HBV、HCV、HIV、梅毒标志物)检测且结果为阴性;研究内容经天津市第五中心医院伦理委员会审定通过(WZX-EC-202112),所有捐献者均签署知情同意书。
1.3.2 实验试剂 间充质干细胞培养基(友康);胰蛋白酶(Gibco);OptiVitro® 间充质干细胞成脂分化培养基(依科赛);间充质干细胞成骨分化培养基(BI);1%结晶紫乙醇溶液、CFSE、植物血凝素M(Thermo);油红O异丙醇饱和液(索莱宝);0.2%明胶溶液(Sigma);FITC抗人CD73抗体、FITC抗人CD90 (Thy1)抗体、FITC抗人CD105抗体、PE抗人CD11b抗体、PE抗人 CD19抗体、PE抗人CD34抗体、PE抗人CD45抗体、APC抗人HLA-DR抗体、PE抗人CD127(IL-7Rα)抗体、APC抗人CD4抗体、PerCP/Cyanine5.5抗人CD25抗体(Biolegend,美国);肿瘤坏死因子α ELISA试剂盒、白细胞介素10 ELISA试剂盒(依科赛,中国)。
1.3.3 实验仪器 多功能酶标仪(BioTek,德国);流式细胞仪(贝克曼,美国);倒置光学显微镜(Leica,德国);荧光细胞计数仪(Countstar,中国);生物安全柜(海尔,中国);二氧化碳培养箱(ESCO,新加坡)。
1.4 实验方法
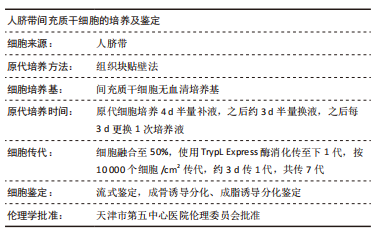
1.4.1 人脐带间充质干细胞的分离 将来源于自愿者捐献的脐带从采集瓶中取出,浸泡于体积分数为75%乙醇中两三分钟;使用DPBS清洗脐带后置于无菌平皿中,去除脐带两端后,去除羊膜层及血管,将剩余脐带华通氏胶置于50 mL离心管或玻璃烧杯中,用DPBS洗涤直至没有血迹,将其尽量剪碎并混合均匀,平铺至平皿中。将培养皿置于体积分数为5%CO2、37 ℃培养箱中培养4 h,加入适量间充质干细胞培养基刚刚覆盖皿底即可,继续培养4 d半量补液,之后约3 d半量换液,之后每3 d更换1次培养液。当上述原代细胞达到50%融合时,进行传代培养。
1.4.2 炎性因子预处理人脐带间充质干细胞 选择生长状态良好的第5代人脐带间充质干细胞,DPBS洗涤后加入适量消化酶,室温消化5 min,加入5 mL 间充质干细胞完全培养基终止消化,收集细胞并离心,弃上清液,用适量间充质干细胞培养基重悬细胞,充分混匀后计数;按照细胞密度10 000个/cm2将人脐带间充质干细胞铺至T75瓶中,体积分数为5%CO2、37 ℃培养箱中培养48 h后添加不同质量浓度(0.1,1,5,25 ng/mL)肿瘤坏死因子α预处理24 h,消化并收获细胞开展质量及功能性实验,同时以无任何因子预处理的人脐带间充质干细胞作为对照组。
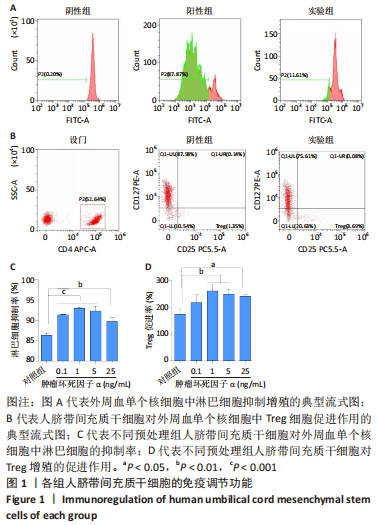
1.4.3 人脐带间充质干细胞的免疫调节能力 将外周血单个核细胞(购买于妙顺生物科技有限公司)重悬于5 μmol/L CFSE溶液中,置于37 ℃水浴锅避光孵育20 min。孵育结束后,加5倍体积含体积分数为10%胎牛血清的RPMI1640培养液,37 ℃孵育10 min以终止染色,400×g室温离心10 min,弃上清,加含体积分数为10%胎牛血清的RPMI1640培养液重悬,取6×105细胞进行流式检测确定实验处理前外周血单个核细胞群。
按照6×104个/孔的密度分别将未预处理人脐带间充质干细胞及1 ng/mL肿瘤坏死因子α预处理人脐带间充质干细胞接种于24孔板中,用间充质干细胞培养基培养过夜,弃掉孔内上清,实验组各孔加入1 mL CFSE标记的外周血单个核细胞悬液(3×108 L-1)及2 μL 0.5 mg/mL 植物凝集素M,阴性组为空白孔内加入1 mL CFSE标记的外周血单个核细胞悬液(3×108 L-1),阳性组为空白孔内加入1 mL CFSE标记的外周血单个核细胞悬液(3×108 L-1),同时每孔添加2 μL 0.5 mg/mL植物血凝素M,培养5 d后,收集各组外周血单个核细胞悬液,400×g室温离心5 min,弃上清,用300 μL DPBS重悬细胞沉淀,流式细胞仪检测CFSE阳性外周血单个核细胞占比,流式检测按照阴性组设门,统计阳性组及实验组的增殖细胞比例。淋巴细胞增殖抑制率=(阳性组增殖细胞比例-实验组增殖细胞比例)/(阳性组增殖细胞比例-阴性组增殖细胞比例)×100%。
按照6×104个/孔的密度分别将未预处理人脐带间充质干细胞及1 ng/mL肿瘤坏死因子α预处理人脐带间充质干细胞接种于24孔板中,用间充质干细胞培养基培养过夜,弃掉孔内上清,实验组各孔加入1 mL外周血单个核细胞悬液(3×108 L-1),阴性组为空白孔内加入1 mL外周血单个核细胞悬液(3×108 L-1),阳性组为空白孔内加入1 mL CFSE标记的外周血单个核细胞悬液(3×108 L-1),用含体积分数为10%胎牛血清的RPMI1640培养液培养72 h。收集孔内外周血单个核细胞悬液,400×g室温离心5 min,弃上清,每管加入100 μL的DPBS重悬细胞,对表面标志物CD127,CD4,CD25进行流式染色,流式细胞仪检测得出CD4+/CD25+/CD127-(Treg)细胞群占比,观察人脐带间充质干细胞对Treg增殖的促进作用,即促进效率=(实验组Treg百分比-阴性组Treg百分比)/阴性组Treg百分比×100%。
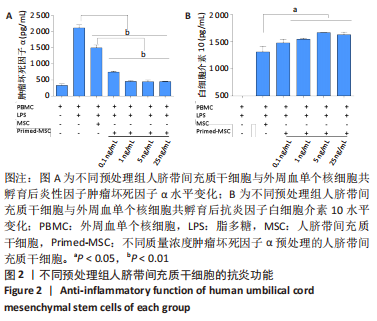
1.4.4 人脐带间充质干细胞的抗炎功能 按照5×104个/孔的密度分别将未预处理人脐带间充质干细胞及1 ng/mL肿瘤坏死因子α预处理人脐带间充质干细胞接种于24孔板中,用含体积分数为10%胎牛血清的RPMI1640培养液培养过夜。按照5×105个/孔的密度将外周血单个核细胞接种于24孔板中,同时添加1 ng/mL脂多糖刺激,用含体积分数为10%胎牛血清的RPMI1640培养液培养24 h。收集孔内培养液上清,400×g离心5 min去除沉淀。用肿瘤坏死因子α及白细胞介素10 ELISA 试剂盒检测上清中肿瘤坏死因子α和白细胞介素10水平。
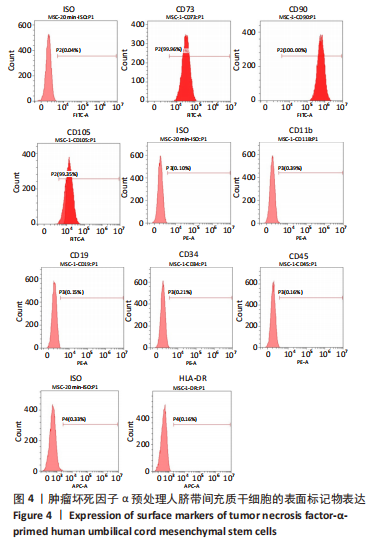
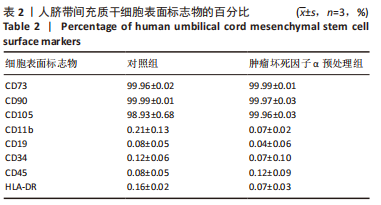
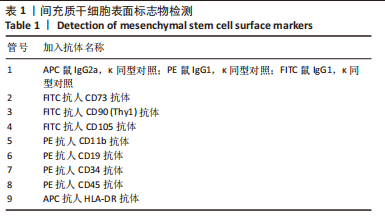
1.4.5 人脐带间充质干细胞表面标志物检测 分别消化生长状态良好的未预处理人脐带间充质干细胞及1 ng/mL肿瘤坏死因子α预处理人脐带间充质干细胞,按照计数结果移取1×106个细胞至离心管,400×g离心5 min,弃去上清液,加入0.9 mL DPBS重悬并分为9份,分别加入流式抗体或相应的同型对照抗体,充分混匀各管,避光室温孵育30 min,抗体名称见表1;待孵育结束,向各管中加入1 mL DPBS,混匀细胞,400×g离心5 min,弃去上清液,向每支管中加入300 μL DPBS重悬细胞,流式细胞仪上机分析CD73、CD90、CD105、CD11b、CD19、CD34、CD45、HLA-DR的表达。
1.4.6 人脐带间充质干细胞的增殖活性 按照细胞密度1×104个/cm2将未预处理人脐带间充质干细胞及1 ng/mL肿瘤坏死因子α预处理人脐带间充质干细胞铺至T75瓶中,体积分数为5%CO2、37 ℃培养箱中培养48 h;使用DPBS洗涤细胞后,加入TrypL Express消化酶室温消化5 min,加入5 mL 间充质干细胞完全培养基终止消化,收集细胞并离心,弃上清液,用适量间充质干细胞培养基重悬细胞,充分混匀后计数。倍增时间(TD)=t×log2/logNt-logN0,其中t:培养时间(h),N0:接种后起始细胞数;Nt:培养t小时后的细胞数。
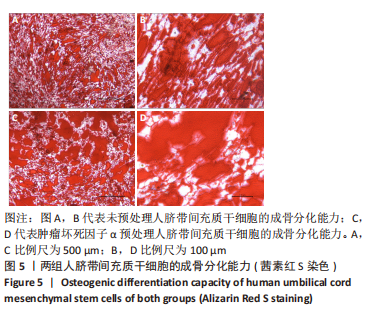
1.4.7 人脐带间充质干细胞的成骨、成脂分化能力 按照细胞密度为1.5×105个/孔分别将未预处理人脐带间充质干细胞及1 ng/mL肿瘤坏死因子α预处理人脐带间充质干细胞接种至0.2%明胶溶液预包被的12孔板中,体积分数为5%CO2、37 ℃培养箱中培养至细胞融合率90%(约2 d)以上开始成骨诱导分化,每孔加入1.5 mL成骨诱导分化培养基,每三四天换液1次,细胞诱导至21 d左右时,使用40 g/L多聚甲醛1 mL室温固定10 min,DPBS润洗1次,每孔加入1 mL 茜素红S染液,室温染色10 min,DPBS洗涤1次,加入0.5 mL DPBS,置于显微镜下观察拍照。
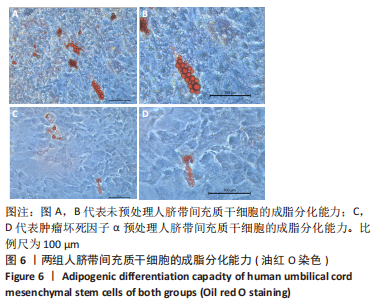
按照细胞密度为1.5×105个/孔将未预处理人脐带间充质干细胞及1 ng/mL肿瘤坏死因子α预处理人脐带间充质干细胞接种至0.2%明胶溶液预包被的12孔板中,体积分数为5%CO2、37 ℃培养箱中培养至细胞融合率90%(约2 d)以上开始成脂诱导分化,每孔加入1.5 mL成脂诱导分化培养基,每三四天换液1次,诱导至30 d左右时,使用1 mL 40 g/L多聚甲醛室温固定10 min,DPBS润洗1次,每孔加入0.9 mL油红O染色液,室温染色15 min,DPBS洗涤1次,加入0.5 mL DPBS,置于显微镜下观察拍照。
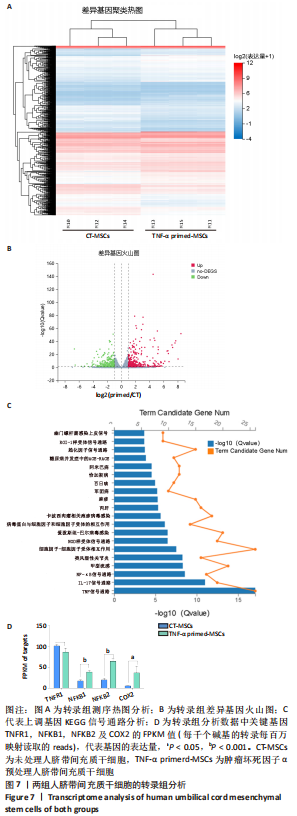
1.4.8 人脐带间充质干细胞的转录组测序 收集第7代未预处理人脐带间充质干细胞及1 ng/mL肿瘤坏死因子α预处理人脐带间充质干细胞约5×106个,DPBS洗涤后加入1 mL Trizol试剂提取RNA,并使用DNase I消化总RNA后使用Oligo(dT)磁珠进行富集,打断mRNA,使用随机引物并进行cDNA一链的合成,使用dUTP代替dTTP合成cDNA二链,末端修复后加入“A”接头连接并进行PCR反应,用UDG酶消化带U标记的第二链模板进行PCR扩增及回收,文库质量检测后进行PCR产物环化,最终上机检测。
对测序获得的数据进行对比及基因定量分析,并根据表达量进行差异表达分析,对筛选的差异表达基因进行GO功能分析、KEGG通路功能分析、聚类分析。
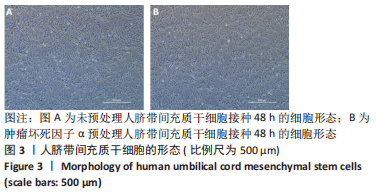
1.5 主要观察指标 ①未预处理人脐带间充质干细胞及1 ng/mL肿瘤坏死因子α预处理人脐带间充质干细胞的细胞形态及表型;②未预处理人脐带间充质干细胞及1 ng/mL肿瘤坏死因子α预处理人脐带间充质干细胞的免疫调节能力、抗炎能力和成骨、成脂分化能力;③未预处理人脐带间充质干细胞及1 ng/mL肿瘤坏死因子α预处理人脐带间充质干细胞的转录组分析。
1.6 统计学分析 采用SPSS 20.0统计软件进行分析,实验数据以x±s表示,进行t检验,P < 0.05为差异有显著性意义。