中国组织工程研究 ›› 2020, Vol. 24 ›› Issue (25): 3943-3946.doi: 10.3969/j.issn.2095-4344.2102
• 骨髓干细胞 bone marrow stem cells • 上一篇 下一篇
骨髓间充质干细胞-海螵蛸复合支架的细胞毒性评估
彭 雅1,覃 裕1,易洪城2,顾春松2,李丽莉1
1贵州省骨科医院骨内二科,贵州省贵阳市 550002;2贵阳中医学院第二附属医院骨二科,贵州省贵阳市 550002
Cytotoxicity assessment of bone marrow mesenchymal stem cells-cuttlebone composite scaffold
Peng Ya1, Qin Yu1, Yi Hongcheng2, Gu Chunsong2, Li Lili1
1Second Department of Osteopathy, Guizhou Orthopedics Hospital, Guiyang 550002, Guizhou Province, China; 2Second Department of Orthopedics, the Second Affiliated Hospital of Guizhou University of Traditional Chinese Medicine, Guiyang 550002, Guizhou Province, China
摘要:
文题释义:
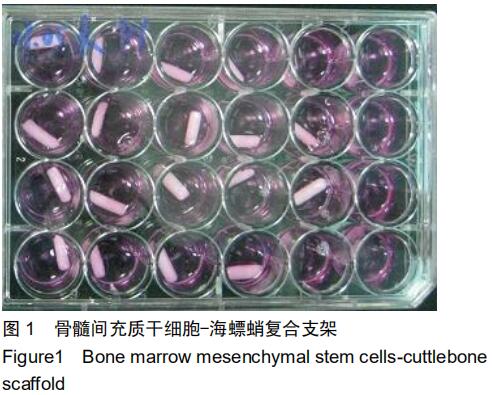
骨髓间充质干细胞复合海螵蛸支架:以中药海螵蛸为载体支架,骨髓间充质干细胞为种子细胞,二者共同培养构建复合生物支架,经过各项生物安全性测评后应用于骨缺损的治疗。制作过程为:选用第3代骨髓间充质干细胞,经0.25%胰酶消化制成细胞悬液,将细胞浓度调整为5×108 L-1,用移液枪将骨髓间充质干细胞悬液缓慢逐滴滴加于24孔板中的海螵蛸上,200 μL/孔,分2次缓慢接种,尽量不使细胞从材料上溢出,置于培养箱中培养4 h,待细胞充分黏附于海螵蛸支架材料后,缓慢逐滴加入培养液700 μL,将支架与细胞复合培养8 d,两三天换液1次。
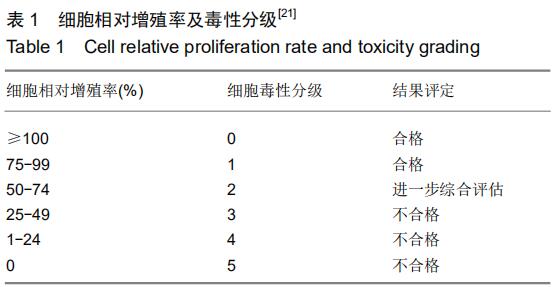
细胞毒性评估:是采用受试物与细胞共同培养的方法,对样品进行毒理学风险评估。生物材料应用于体内后,可能与体内细胞的细胞膜、细胞器、蛋白质合成、DNA合成等相互作用,产生细胞毒性。根据ISO10993-5标准,在复合支架应用于临床治疗前,需通过复合材料浸提液试验以测定其对细胞活性、功能、遗传的影响。
摘要
背景:作为骨组织工程的修复材料,应具有良好的生物相容性及降解吸收性,许多学者在此方面也做了较深入的研究,但中药复合细胞生物支架的研究较少。
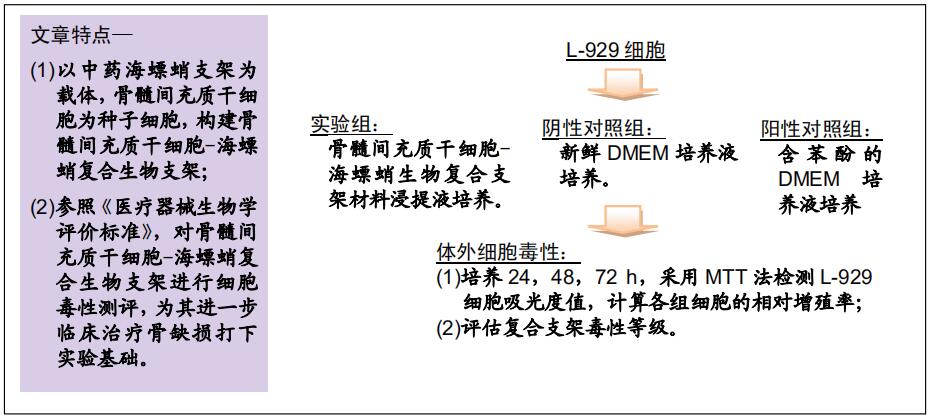
目的:参照《医疗器械生物学评价标准》,对兔骨髓间充质干细胞-海螵蛸生物复合支架进行体外细胞毒性检测,评估复合支架的毒性等级,为临床应用生物支架提供实验依据。
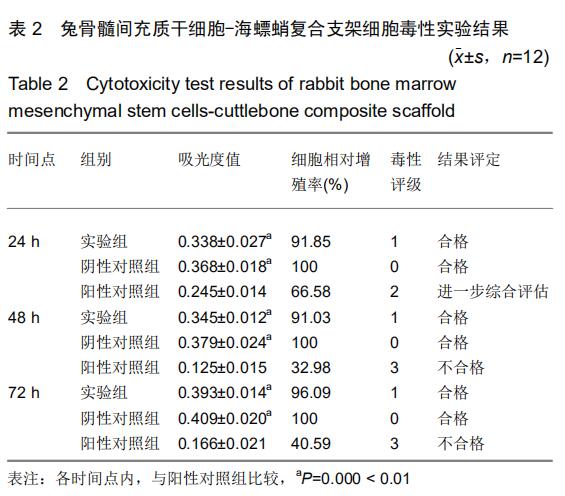
方法:依照ISO标准按“材料面积∶浸提介质体积=3-6 cm2∶1 mL”制作骨髓间充质干细胞-海螵蛸生物复合支架材料浸提液。制备L-929细胞悬液,将细胞浓度调整至1×107 L-1进行接种培养,设置阳性对照组(含苯酚的DMEM培养液)、实验组(材料浸提液)、阴性对照组(新鲜DMEM培养液)。培养24,48,72 h采用MTT法检测L-929细胞吸光度值,计算各组细胞的相对增殖率,评估复合支架毒性等级。
结果与结论:实验组、阴性对照组、阳性对照组吸光度值在不同时间点不完全相同(P=0.000 < 0.01),各时间点内比较,实验组与阴性对照组吸光度值均明显高于阳性对照组(P < 0.01);兔骨髓间充质干细胞-海螵蛸生物支架细胞毒性为1级。结果说明兔骨髓间充质干细胞-海螵蛸生物支架无明显毒性作用,符合生物材料应用要求。
ORCID: 0000-0002-0003-6228(彭雅)
中国组织工程研究杂志出版内容重点:干细胞;骨髓干细胞;造血干细胞;脂肪干细胞;肿瘤干细胞;胚胎干细胞;脐带脐血干细胞;干细胞诱导;干细胞分化;组织工程中图分类号: