中国组织工程研究 ›› 2016, Vol. 20 ›› Issue (42): 6324-6329.doi: 10.3969/j.issn.2095-4344.2016.42.014
• 神经组织构建 nerve tissue construction • 上一篇 下一篇
神经细胞分泌因子促进骨骼肌细胞生长
蔡明轩1,王美辰1,徐治成1,颜 南2,孟欣雨1,王正东3
- 沈阳医学院,1基础医学院,2康复教研室,3解剖学教研室,辽宁省沈阳市 110034
Neuron-secreted factors promote the growth of skeletal muscle cells
Cai Ming-xuan1, Wang Mei-chen1, Xu Zhi-cheng1, Yan Nan2, Meng Xin-yu1, Wang Zheng-dong3
- 1Basic Medical School, 2Department of Rehabilitation, 3Department of Anatomy, Shenyang Medical University, Shenyang 110034, Liaoning Province, China
摘要:
文章快速阅读:
.jpg) 文题释义:
肌卫星细胞:骨骼肌中除骨骼肌纤维(肌细胞)外的一种扁平、有突起的细胞。附着于肌纤维(肌细胞)表面;当肌纤维(肌细胞)受损后,肌卫星细胞可增殖分化,参与肌纤维(肌细胞)的修复,因此具有干细胞性质。
骨骼肌细胞:肌细胞呈纤维状,不分支,有明显横纹,核很多,且都位于细胞膜下方。肌细胞内有许多沿细胞长轴平行排列的细丝状肌原纤维。每个肌原纤维都有相间排列的明带(Ⅰ带)及暗带(A带)。
文题释义:
肌卫星细胞:骨骼肌中除骨骼肌纤维(肌细胞)外的一种扁平、有突起的细胞。附着于肌纤维(肌细胞)表面;当肌纤维(肌细胞)受损后,肌卫星细胞可增殖分化,参与肌纤维(肌细胞)的修复,因此具有干细胞性质。
骨骼肌细胞:肌细胞呈纤维状,不分支,有明显横纹,核很多,且都位于细胞膜下方。肌细胞内有许多沿细胞长轴平行排列的细丝状肌原纤维。每个肌原纤维都有相间排列的明带(Ⅰ带)及暗带(A带)。
.jpg) 文题释义:
肌卫星细胞:骨骼肌中除骨骼肌纤维(肌细胞)外的一种扁平、有突起的细胞。附着于肌纤维(肌细胞)表面;当肌纤维(肌细胞)受损后,肌卫星细胞可增殖分化,参与肌纤维(肌细胞)的修复,因此具有干细胞性质。
骨骼肌细胞:肌细胞呈纤维状,不分支,有明显横纹,核很多,且都位于细胞膜下方。肌细胞内有许多沿细胞长轴平行排列的细丝状肌原纤维。每个肌原纤维都有相间排列的明带(Ⅰ带)及暗带(A带)。
文题释义:
肌卫星细胞:骨骼肌中除骨骼肌纤维(肌细胞)外的一种扁平、有突起的细胞。附着于肌纤维(肌细胞)表面;当肌纤维(肌细胞)受损后,肌卫星细胞可增殖分化,参与肌纤维(肌细胞)的修复,因此具有干细胞性质。
骨骼肌细胞:肌细胞呈纤维状,不分支,有明显横纹,核很多,且都位于细胞膜下方。肌细胞内有许多沿细胞长轴平行排列的细丝状肌原纤维。每个肌原纤维都有相间排列的明带(Ⅰ带)及暗带(A带)。摘要
背景:周围神经损伤可引起支配肌肉萎缩,目前尚无明确的方法治疗肌肉萎缩。肌细胞是实现肌肉收缩功能的结构单位,体外培养的骨骼肌细胞可用于失神经肌肉萎缩相关研究。
目的:观察神经元分泌因子对体外骨骼肌细胞的生长的促进作用。
方法:将体外原代培养的骨骼肌细胞分为2组,实验组加神经细胞分泌因子培养,对照组加普通培养液培养,用苏木精-伊红染色、免疫组织化学染色检测神经元分泌因子作用后骨骼肌细胞数目及α肌动蛋白表达的变化。
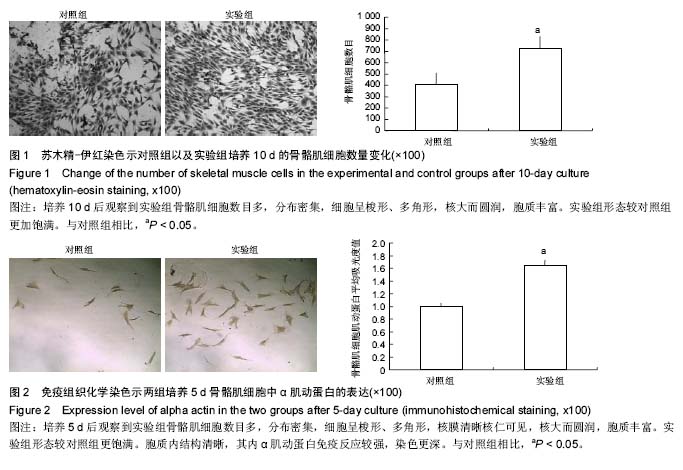
结果与结论:①骨骼肌细胞数量、骨骼肌细胞肌动蛋白的表达:实验组骨骼肌细胞数量、骨骼肌细胞α肌动蛋白的表达均多于对照组(P < 0.05);②结果说明:神经元分泌因子有促进大鼠骨骼肌细胞生长的作用,可能具有治疗失神经肌肉萎缩的作用。
中国组织工程研究杂志出版内容重点:组织构建;骨细胞;软骨细胞;细胞培养;成纤维细胞;血管内皮细胞;骨质疏松;组织工程
ORCID:0000-0002-5462-4452(王正东)
中图分类号:
.jpg) 文题释义:
肌卫星细胞:骨骼肌中除骨骼肌纤维(肌细胞)外的一种扁平、有突起的细胞。附着于肌纤维(肌细胞)表面;当肌纤维(肌细胞)受损后,肌卫星细胞可增殖分化,参与肌纤维(肌细胞)的修复,因此具有干细胞性质。
骨骼肌细胞:肌细胞呈纤维状,不分支,有明显横纹,核很多,且都位于细胞膜下方。肌细胞内有许多沿细胞长轴平行排列的细丝状肌原纤维。每个肌原纤维都有相间排列的明带(Ⅰ带)及暗带(A带)。
文题释义:
肌卫星细胞:骨骼肌中除骨骼肌纤维(肌细胞)外的一种扁平、有突起的细胞。附着于肌纤维(肌细胞)表面;当肌纤维(肌细胞)受损后,肌卫星细胞可增殖分化,参与肌纤维(肌细胞)的修复,因此具有干细胞性质。
骨骼肌细胞:肌细胞呈纤维状,不分支,有明显横纹,核很多,且都位于细胞膜下方。肌细胞内有许多沿细胞长轴平行排列的细丝状肌原纤维。每个肌原纤维都有相间排列的明带(Ⅰ带)及暗带(A带)。