中国组织工程研究 ›› 2026, Vol. 30 ›› Issue (27): 7044-7052.doi: 10.12307/2026.299
• 骨与关节生物力学Bone and joint biomechanics • 上一篇
L型钢板治疗骨质疏松性Schatzker Ⅱ型胫骨平台骨折的有效性及生物力学分析
史高龙,胡正辉,凌卓彦,谢宗刚
- 苏州大学附属第二医院关节外科,江苏省苏州市 215000
Efficacy and biomechanical analysis of L-shaped plate treatment for osteoporotic Schatzker type II tibial plateau fractures
Shi Gaolong, Hu Zhenghui, Ling Zhuoyan, Xie Zonggang
- Department of Orthopedics, The Second Affiliated Hospital of Soochow University, Suzhou 215000, Jiangsu Province, China
摘要:
文题释义:
骨质疏松:是一种以骨量减少、骨微结构破坏为特征的全身性骨病,导致骨骼脆性增加,易发生骨折。世界卫生组织(WHO)将其定义为骨密度T值≤-2.5(即较正常年轻人群骨密度低2.5个标准差)。骨质疏松患者骨骼中皮质骨变薄,松质骨小梁减少,骨强度显著下降,在老年人中尤为显著。
有限元分析:是一种数值模拟方法,广泛应用于工程和生物力学领域,用于分析复杂结构的力学性能。在骨科研究中,有限元分析通过构建骨骼和内固定装置的三维模型,划分有限单元(网格),并设置材料属性(如弹性模量、泊松比)和边界条件,模拟不同载荷下的应力、应变和位移。
摘要
背景:Schatzker Ⅱ型骨折往往累及后外侧平台,导致骨强度减弱、固定挑战增大及术后塌陷风险升高,亟需优化治疗策略以平衡稳定性和创伤最小化。
目的:评估单纯外侧L型钢板固定治疗骨质疏松性Schatzker Ⅱ型累及后外侧胫骨平台骨折的临床效果,并通过有限元分析比较其与外侧L型钢板联合后方T型钢板固定的生物力学性能。
方法:回顾性分析2018年1月至2023年12月苏州大学附属第二医院关节外科收治的39例骨质疏松性Schatzker Ⅱ型累及后外侧胫骨平台骨折患者的病历资料,分为L型钢板组(单纯外侧L型钢板固定,n=24)及联合组(外侧L型钢板联合后方T型钢板固定,n=15)。对比两组患者在手术时间、术中出血量、骨密度、术前胫骨平台塌陷、受伤至手术时间、术后影像学指标(胫骨平台内翻角、后倾角)、膝关节活动度及美国特种外科医院评分、Lysholm评分等方面的差异。同时基于健康成年男性膝关节CT数据建立Schatzker Ⅱ型胫骨平台骨折有限元模型,模型分为非骨质疏松组(A组:单纯L型钢板;B组:L型钢板+T型钢板)与骨质疏松组(C组:单纯L型钢板;D组:L型钢板+T型钢板)。在250,500,750 N轴向载荷下,分析各组模型的整体位移、胫骨应力及内固定应力。
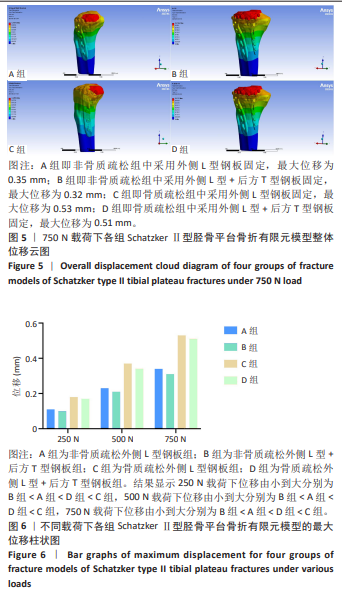
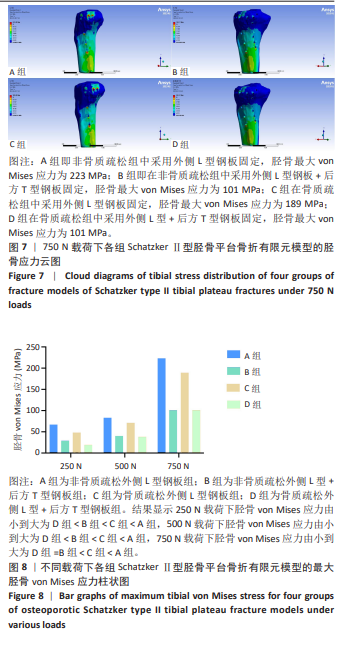
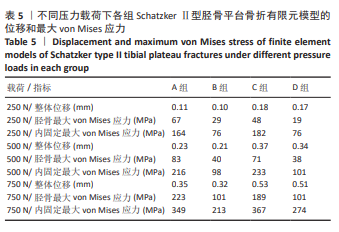
结果与结论:①临床试验结果:两组患者在年龄、性别、体质量指数、骨密度、术前胫骨平台塌陷情况以及受伤至手术时间方面无显著性差异(P > 0.05);L型钢板组手术时间及术中出血量均显著少于联合组(P < 0.000 1);术后即刻胫骨平台内翻角及后倾角组间比较无显著性差异(P > 0.05);末次随访时内翻角L型钢板组小于联合组(P=0.04),后倾角组间比较仍无显著性差异(P > 0.05);末次随访时膝关节活动度、美国特种外科医院评分、Lysholm评分组间均无显著性差异(P > 0.05)。②有限元结果:在相同载荷下,无论是非骨质疏松骨模型还是骨质疏松骨模型,采用T型钢板辅助固定(B/D组)比单纯L型钢板固定(A/C组)在整体位移和胫骨、内固定应力上具有更优异的性能。③提示对于骨质疏松性Schatzker Ⅱ型累及后外侧胫骨平台的骨折,单纯外侧L型钢板固定可获得满意的复位稳定性及功能恢复,其临床效果与双钢板技术相当;有限元分析表明双钢板固定力学性能更优,但考虑到单纯外侧L型钢板固定手术创伤显著更小且临床效果良好,无需常规加用后方T型钢板。
中国组织工程研究杂志出版内容重点:人工关节;骨植入物;脊柱;骨折;内固定;数字化骨科;组织工程
中图分类号: