Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (22): 3583-3590.doi: 10.12307/2024.526
Previous Articles Next Articles
Potential and advantages of metal organic frameworks-based hydrogel materials for repairing soft and hard tissues
Zhao Zipei1, Wang Xu1, Zhao Weifeng2, Pei Xibo1
- 1State Key Laboratory of Oral Diseases & National Center for Stomatology & National Clinical Research Center for Oral Diseases, Department of Prosthodontics of West China Hospital of Stomatology, Sichuan University, Chengdu 610041, Sichuan Province, China; 2College of Polymer Science and Engineering, Sichuan University, Chengdu 610065, Sichuan Province, China
-
Received:2023-09-21Accepted:2023-10-30Online:2024-08-08Published:2024-01-20 -
Contact:Pei Xibo, Associate professor, Master’s supervisor, State Key Laboratory of Oral Diseases & National Center for Stomatology & National Clinical Research Center for Oral Diseases, Department of Prosthodontics of West China Hospital of Stomatology, Sichuan University, Chengdu 610041, Sichuan Province, China -
About author:Zhao Zipei, Master candidate, State Key Laboratory of Oral Diseases & National Center for Stomatology & National Clinical Research Center for Oral Diseases, Department of Prosthodontics of West China Hospital of Stomatology, Sichuan University, Chengdu 610041, Sichuan Province, China -
Supported by:National Natural Science Foundation of China, No. 82271016 (to PXB); Interdisciplinary Innovation Project of West China Hospital of Stomatology of Sichuan University, No. RD-03-202310 (to PXB)
CLC Number:
Cite this article
Zhao Zipei, Wang Xu, Zhao Weifeng, Pei Xibo. Potential and advantages of metal organic frameworks-based hydrogel materials for repairing soft and hard tissues[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(22): 3583-3590.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

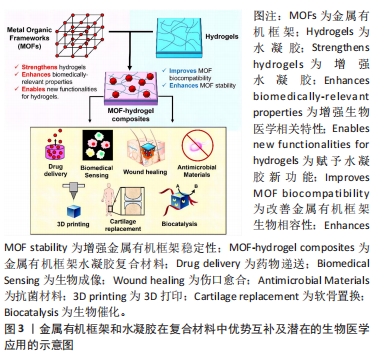
2.1 金属有机框架材料的生物应用 组成金属有机框架材料的金属离子节点常见的包括锌离子、铜离子和铁离子等,有机配体包括苯环和卟啉等。通过多种金属离子节点和有机配体的不同组合,可得到不同结构与功能的金属有机框架[5]。金属有机框架呈现出一种高度有序的多孔结构,其孔径可根据需要调整,该结构可为金属有机框架提供较大的比表面积,并且暴露更多的活性位点用于进一步的修饰,从而有利于对金属有机框架性能进行调整[6]。作为一种有机无机杂化材料,不同组成结构的金属有机框架还表现出诸多个性。例如由铁离子和氰基相互配位形成的普鲁士蓝纳米颗粒(prussian blue nanoparticles,PBNPs)具有良好的近红外光热活性,是一种常见的光热剂[7]。由锌离子和2-甲基咪唑制备的沸石咪唑酸骨架8 (zeolitic imidazolate framework-8,ZIF-8)可以通过缓慢释放锌离子发挥成骨作用[8]。因此,性能可调、功能多样的金属有机框架被用于多种领域,包括组织工程、污水处理、气体储存及传感检测等。 应用于生物医学领域的金属有机框架需要满足特定的条件。首先,为了确保金属有机框架在机体内具有良好的生物相容性和可代谢性,研究人员制备了具有更小颗粒尺寸的纳米金属有机框架材料,降低了金属离子潜在的生物毒性。其次,金属有机框架在生理液体中的稳定性也至关重要[9]。然而,由于金属配位键的存在,大部分的金属有机框架在水中相对易分解,存在稳定性不佳、利用率低且难以保持其固有特性的问题,这极大地限制了金属有机框架在生物医学领域的应用[10]。研究人员采取了多种方法来解决这些问题,例如优化合成途径、构建新型结构的金属有机框架、表面功能化以及利用金属有机框架上存在的活性位点与其它材料相连接开发新的复合材料等。 2.2 纳米水凝胶复合材料的优势 水凝胶是一类3D网络结构凝胶,其结构中含有相当数量的羟基,能吸收并保有大量的水且不溶解,并保持良好的弹性和强度[11]。水凝胶在受力情况下可发生一定程度的弹性形变,撤除外力后能够恢复原状。具有良好的孔隙结构,可将需要运载的药物分散在孔隙之中构建载药水凝胶,并运送至指定部位[12]。此外,水凝胶还具有良好的组织相似性和生物相容性,被广泛用作伤口敷料的基质材料[13]。 然而,单纯水凝胶材料在应用过程中仍存在一些常见的问题。首先,单纯水凝胶材料内部交联结构较脆弱,常表现出较差的机械性能,用于伤口敷料时易破碎,不能有效保护伤口。其次,LEI等[14]既往的研究表明,水凝胶具有多孔结构,当其出现不可控的降解时,负载的生物分子和药物可能在递送过程中发生泄漏或出现爆发性释放,造成生物利用率的降低和潜在的生物毒性。此外,单纯水凝胶材料仅由聚合物基质组成,功能单一,无法有效应对复杂的伤口微环境。 为了解决上述问题,研究人员将水凝胶材料和纳米结构材料相结合,通过纳米颗粒与水凝胶网络之间的相互作用实现或加强水凝胶的交联,赋予水凝胶更好的机械性能。这种相互作用还可以维持纳米颗粒在水凝胶中的高分散性,从而提高其在疾病治疗中的生物利用度。此外,纳米结构材料的引入还可以为水凝胶材料带来额外的功能,构建用于更复杂的应用场景的复合材料[15]。例如,既往研究表明氧化铈纳米颗粒具有清除活性氧的巨大潜力,并在各种产生过度活性氧的疾病中发挥积极的保护作用,CHENG等[16]将氧化铈纳米颗粒和抗菌肽分散儿茶酚基团修饰的甲基丙烯酰化明胶(gelatin methacryloyl,GelMA)中,为单纯的水凝胶带来了良好的抗菌和清除活性氧的能力,制备了一种可喷雾水凝胶伤口敷料。 2.3 金属有机框架在水凝胶材料中的作用 与传统的纳米材料相比,金属有机框架作为一种有机无机杂化的纳米材料,在与水凝胶的结合中具有显著的优势。首先,金属有机框架具有多种类型的活性位点,不仅可以直接与水凝胶产生相互作用,还可以根据不同的水凝胶基质在金属有机框架结构中设计接枝不同的修饰基团,在水凝胶基质与修饰基团之间产生额外的交联,从而增强复合材料内部的交联程度[4];其次,金属有机框架可以作为生物活性储层,提高给药过程的效率和安全性,使负载药物达到响应性、控制性释放[17];最后,金属有机框架具有其它纳米材料无法比拟的多功能性,可根据应用需求选取合适功能的金属有机框架与水凝胶结合[18]。因此金属有机框架作为一种新型纳米材料,被用作与水凝胶材料相结合,进一步开发出新颖高效的金属有机框架基水凝胶复合材料,并在生物医学领域得到了广泛应用。 在金属有机框架基水凝胶复合材料中,金属有机框架的引入能够起到加强水凝胶机械性能、增强水凝胶生物相关特性、赋予水凝胶新功能等作用,水凝胶能够改善金属有机框架的生物相容性、增强金属有机框架的稳定性,起到双赢的作用。在生物医学领域,金属有机框架基水凝胶复合材料具有药物递送、生物成像及促进伤口愈合等诸多应用。金属有机框架和水凝胶在复合材料中优势互补及潜在的生物医学应用的示意图见图3。"
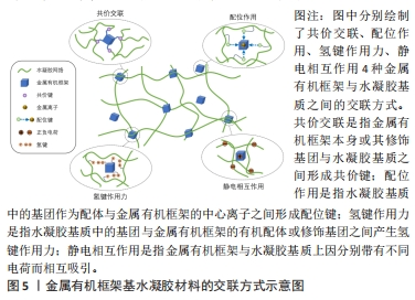
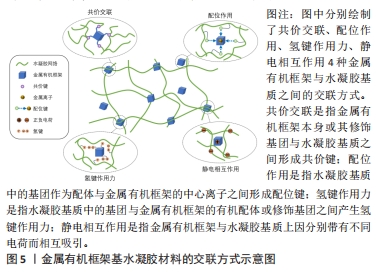
2.3.1 加强水凝胶交联 水凝胶通常是通过物理或化学交联形成的。其物理交联主要指分子通过静电相互作用及氢键等成胶,该过程通常是可逆的。物理交联的水凝胶通常稳定性较低,机械强度较差,在受力或周围环境改变(如温度和pH值等)时,易出现分解、破裂等现象。水凝胶的化学交联是指通过光聚合、酶诱导交联等反应,在聚合物链之间形成共价键构成水凝胶的交联网络。虽然这种交联能够形成稳定而持久的连接,但是合成过程中额外加入的化学交联剂可能具有潜在的生物毒性,带来了新的风险[25]。 研究人员向水凝胶中引入金属有机框架与聚合物基质之间形成额外的交联来加强水凝胶内部交联程度。在金属有机框架基水凝胶材料中,构成金属有机框架的金属离子、有机配体或其修饰基团可通过多种方式与聚合物发生交联,包括共价交联、配位作用、静电相互作用和氢键作用力等[26-30]。当金属有机框架和聚合物之间通过共价键相连时,金属有机框架通常需要进一步修饰,将一些能与大分子主链或侧枝发生化学反应形成共价键的官能团接枝于金属有机框架上,修饰后的金属有机框架即能够充当一种“水凝胶基质”参与交联,甚至能够作为一种无机交联剂促进聚合物基质凝胶化。WENG等[31]将经硅烷偶联剂修饰的一种多孔金属有机骨架液体(ZIF-91-PL)与GelMA混合得到透明预凝胶,接着在紫外光照射下,ZIF-91-PL接枝侧链上的丙烯酸基团通过自由基聚合反应与GelMA发生共价交联,合成了金属有机框架基水凝胶复合材料。研究发现,随着加入的ZIF-91-PL含量的增加,所得复合水凝胶的弹性模量逐渐增加,与纯水凝胶相比,其弹性模量最高提高约100%,可承受最大应力约达0.1 MPa。配位键是一种特殊的共价键,是由中心原子或离子的“空轨道”接受配体的孤对电子形成的,金属有机框架结构就是由金属离子与有机配体之间的配位键形成的。在复合材料中,中心金属离子不仅可以接受来自原有机配体的配位作用,还可以与水凝胶基质中的某些基团形成额外的配位键。 其他的非共价交联包括静电相互作用和氢键作用力等。研究表明金属有机框架与水凝胶之间可因携带不同电荷而相互吸引,HAN等[7]以改性壳聚糖和PBNPs为原料,通过自由基聚合法制备了一种复合水凝胶。PBNPs在复合水凝胶中充当交联点,聚合物通过静电吸引吸附于PBNPs上,加强了水凝胶的交联程度,最终增强了其力学性能。实验结果表明,随着PBNPs加入量的增加,水凝胶的力学性能逐渐增加,弹性模量较纯水凝胶最多增加约35%。 此外,据报道,对于一些天然聚合物如丝素蛋白(silk fibroin,SF)来说,它们的二级蛋白质结构排列得越规律,所形成的水凝胶材料机械强度越大。ZHU等[32]的研究发现金属有机框架可能通过影响聚合物的二级结构来增强水凝胶的机械强度,他们构建了一种由改性丝基水凝胶与负载了2-脱氧-D-核糖的ZIF-8构成的复合水凝胶,通过对全原子分子动力学模拟等相关实验结果的分析,ZIF-8的引入改变了丝基水凝胶的二级结构。具体来说,ZIF-8能够使丝基水凝胶中无序结构明显减少,β-折叠大幅增加,从而形成规则的二级结构;与纯水凝胶相比,引入了ZIF-8的复合水凝胶可提高其80%的机械强度和40%的黏合强度,能够更有效地保护伤口。 在制备金属有机框架水凝胶材料时,研究人员可以利用两者之间的交联作用使材料凝胶化原位成胶,或使金属有机框架均匀分散于已合成的水凝胶之中,加强其交联程度,改善其稳定性、流变性和机械性能等[33]。金属有机框架 基水凝胶材料的交联方式见图5。用于软硬组织修复领域的金属有机框架 基水凝胶材料的交联方式见表1。"

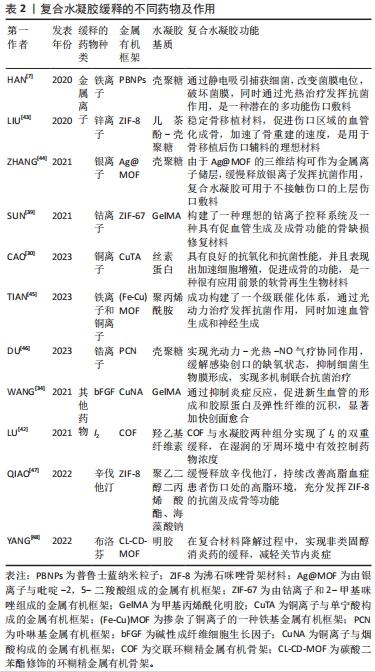
2.3.2 增强水凝胶药物递送能力 水凝胶是一种多功能的药物运输平台。基于水凝胶的交联机制,研究人员可以设计不同的方法来封装和释放药物,使其具备缓释和响应性释放等多种性能[35]。但水凝胶载药运输时仍面临着一些问题,如载药量较小,药物相互聚集,爆发性释放等[36]。金属有机框架的引入可从多方面增强水凝胶药物递送能力,是解决上述问题的有效策略。 首先,金属有机框架可以看作金属离子的存储库,能够实现水凝胶体系中金属离子的控释。在软硬组织修复过程中,金属离子如银离子、锌离子等不仅能发挥广谱抗菌作用[37],还参与许多与促进组织修复相关的过程,包括诱导骨生成,诱导血管内皮生长因子高表达和诱导血管生成等[38]。但局部金属离子浓度过高也会杀伤正常组织细胞,造成生物毒性,因此如何在充分利用金属离子性能的同时,实现金属离子持续、稳定、可控的释放成为研究人员不断探索的问题。SUN等[39]制备了掺杂2-乙基咪唑的2-甲基咪唑钴(ZIF-67),随后将其与GelMA混合,制备了一种具有持续释放钴离子功能的复合水凝胶。该研究发现通过改变前驱液中2-甲基咪唑和2-乙基咪唑的比例,可以精确调节钴离子的释放速度,持续释放时间可以在7-21 d调节,这与骨再生过程中早期血管的生成相匹配,并且避免了过长时间的钴离子释放导致骨吸收等不利影响[40]。 其次,金属有机框架呈现多孔结构且具有高表面活性,研究人员可通过物理吸附,化学交联等多种方式对金属有机框架进行修饰,将需要递送的药物装载于金属有机框架上,将其运送到指定位置[41]。金属有机框架作为药物载体时,随着其多孔结构的逐步崩解,可使负载的药物以较为恒定的速率均匀释放。同时,水凝胶也可通过交联网络的分解,使分散其中的药物缓慢释放,因此金属有机框架基水凝胶材料有望实现双重缓释,从而很好地控制局部药物浓度。LU等[42]以交联环糊精金属有机框架作为碘载体,再将其分散于羟乙基纤维素水凝胶中制得可在口腔湿润环境中用于治疗牙周炎的复合水凝胶。与环糊精金属有机框架相比,交联环糊精金属有机框架在水中有较好的稳定性,可用于I2的包封与控释。体外研究结果表明,在人工唾液中,与负载I2的交联环糊精金属有机框架相比,分散于羟乙基纤维素水凝胶后I2的释放时间延长了5 d,这说明水凝胶基质在该体系中也发挥了缓释I2的作用,实现了I2的双重缓释。文章总结了复合水凝胶缓释的不同药物及作用[7,30,34,39,42-48],见表2。"

2.3.3 赋予水凝胶多种功能 基于种类丰富的金属节点和有机配体,构成金属有机框架的组合几乎是无限的,这是金属有机框架多功能性的基础[49]。此外,金属有机框架具有清晰的晶体结构,并与其功能之间存在良好的对应关系。研究人员可通过调整金属有机框架的组成和结构,精确地定制目标功能,实现功能导向的材料设计,并进一步与水凝胶结合,赋予水凝胶多种功能。 无机纳米酶既表现出天然酶类的高效催化特性,又较少受环境影响,能够稳定发挥催化作用[50],而与其他无机纳米酶相比,金属有机框架具有高度规则的多孔结构和均匀的活性位点,能够充分地与底物接触,更加高效发挥催化作用[51]。例如铁基金属有机框架具有过氧化物酶样活性,可将H2O2转化为活性氧如?OH等,从而发挥抗菌、抗肿瘤等作用,TIAN等[45]使用了铁铜双金属有机框架来负载葡萄糖氧化酶(GOx),再将其分散至水凝胶基质中,构建了一种具有高效抗菌和炎症调节功能的多功能伤口敷料。该复合水凝胶成功构建了一个级联催化体系,具体来说,它可以通过GOx分解微环境中的葡萄糖产生葡萄糖酸和H2O2,其中葡萄糖酸可以降低微环境的pH值,进一步增强双金属有机框架的催化性能。而H2O2可以作为原料,在双金属铁铜双金属有机框架的催化下产生大量?OH,从而更加高效地发挥抗菌作用。 此外,某些金属有机框架还可以作为光敏剂,通过光动力治疗发挥抗菌作用[52]。研究人员通过有机卟啉分子与金属离子或团簇的桥接,成功制备了具有光敏作用的卟啉基金属有机框架[53]。CHEN等[54]构建了一种金属铂与上转换纳米粒子修饰的锆基卟啉金属有机框架,再将其分散至水凝胶中构建了一种具有良好抗菌性能的伤口敷料。在该材料中,上转换纳米颗粒能够有效地将近红外光转化为可见光来激活锆基卟啉金属有机框架产生活性氧用于光动力抗菌治疗。此外,具有过氧化氢酶样活性的金属铂可将创面中高浓度的H2O2转化为O2,既能增强光动力疗法的抗菌疗效,又能缓解感染创面的缺氧,改善创口微环境。 传感技术是利用传感材料特异性结合某种物质,并通过一定机制发出信号,实现定性或定量的检测。金属有机框架内部多样化的活性位点及其高度可修饰性使其适用于该领域,尤其是具有发光能力的金属有机框架,能够监测或检测生物体中不同的物质及其浓度,将生物信号转化为光信号,从而用于疾病诊断、代谢物监测以及相关病理机制的研究[55]。将金属有机框架传感器引入具有良好生物相容性的水凝胶基质中,构建用于传感领域的新型复合材料是一条具有研究价值的思路[56]。 2.4 金属有机框架基水凝胶材料在软硬组织修复中的应用 2.4.1 硬组织修复 骨缺损:创伤、肿瘤、手术等因素引起的骨缺损严重影响患者的外观和正常功能运动,尽管骨组织具有一定程度的自愈能力,但严重的骨缺损仍需要临床干预,如骨移植、诱导骨再生及骨组织工程学等[57]。既往研究利用金属有机框架作为支架材料负载相关细胞因子,在其降解过程中能逐步释放金属离子和细胞因子,发挥抗菌成骨协同作用,在骨缺损的治疗方面已取得一定成果[58]。水凝胶具有优异的生物相容性,能很好地模仿细胞外基质,为骨损伤创面提供稳定的微环境,促进成骨细胞的生长、增殖和分化。因此,将两者结合用于骨缺损修复成为近年来的研究热点。 骨移植手术是治疗大面积骨缺损的有效手段,成功的骨移植治疗需要考虑多个因素,包括移植材料的稳定性、稳定的微环境和充足的血供。因此,设计具有黏附性、稳定性、生物相容性及一定生物功能的伤口辅料对于骨移植修复手术具有重要的现实意义。LIU等[43]设计了一种由ZIF-8和儿茶酚-壳聚糖组成的多功能水凝胶(CA-CS/Z)。该复合水凝胶可通过负载的ZIF-8持续释放锌离子,从而上调成骨相关基因,促进成骨相关蛋白的分泌,持续刺激伤口处成骨,充分发挥锌离子的成骨作用[59]。CA-CS/Z还能够通过提高血管表皮生长因子A旁分泌水平,进而激活血管内皮的成血管能力,并最终保证缺损骨的顺利再生。体内实验证实,CA-CS/Z能够稳定骨移植材料,促进伤口区域的血管化成骨,极大地加速了骨重建的速度。 高脂血症患者的骨缺损伤口中常存在过量的脂质浸润和难以控制的炎症,这极大地影响了骨代谢的过程,导致骨再生异常,影响伤口愈合[60]。然而,用于骨组织工程的生物材料很少能够改善高血浆脂质和脂蛋白水平下的骨缺损修复。QIAO等[47]针对这一现象,将血脂调节剂辛伐他汀负载于ZIF-8上,再将其分散至水凝胶基质中制备了复合水凝胶(nSZPS)。在该材料中,辛伐他汀和ZIF-8发挥良好的协同作用。通过辛伐他汀的缓慢释放,nSZPS能够抑制局部脂质的形成,改善伤口处的高脂环境;微环境的改善为锌离子的抗菌、成骨及成血管的特性创造了良好的条件。体外和体内实验结果均表明nSZPS能有效诱导骨髓间充质干细胞向成骨细胞分化,抑制其向脂肪细胞分化,在抗脂肪生成和促骨生成中发挥重要作用。 临床研究和基础实验证据证实,伴有糖尿病的骨缺损患者的伤口微环境中促炎细胞因子水平升高,巨噬细胞向于M1型极化,进而促进炎症过程,导致细胞凋亡。此外,在糖尿病病理条件下,线粒体功能障碍、能量代谢异常激活和细胞内抗氧化系统抑制导致骨缺损伤口处活性氧过度产生,加剧炎症状态并阻碍骨修复过程。针对糖尿病骨缺损治疗困境,LAO等[61]将负载了二甲双胍的ZIF-8纳米颗粒与GelMA水凝胶结合,开发了一种多功能复合水凝胶。二甲双胍作为治疗糖尿病的一线用药,在抗氧化、抗炎、降糖及减少线粒体损伤等方面具有综合作用。研究表明该复合水凝胶体系不仅能够促使巨噬细胞向M2型极化,特异性修复功能失调的线粒体,清除过量活性氧,降低炎症反应,并且进一步研究了其调节亚细胞细胞器的功能,如恢复内质网膜与线粒体之间的系结,促进功能失调的线粒体通过自噬降解等。在糖尿病颅骨缺损的大鼠模型中,复合水凝胶治疗组的再生骨量约为空白组的7倍,有效促进了骨缺损再生。 因此,在复杂的骨缺损伤口修复中,金属有机框架基水凝胶材料能够从稳定保护伤口、抗炎、抗氧化、改善微环境及促进成骨等多方面发挥作用,表现出多种优异性能。尽管目前金属有机框架基水凝胶复合材料在骨缺损修复领域的研究仍处于起步阶段,应用范围有待进一步发掘,但其巨大的潜力尚未实现,我们相信未来几年在这一方面会有更多有价值的研究进展。 骨软骨缺损:软骨损伤是常见的肌肉骨骼损伤类型之一,软骨损伤后,由于局部生物力学的改变和保护能力的丧失通常会导致软骨下的骨组织也发生破坏,合称为骨软骨缺损(OCD)。由于软骨组织缺乏血管和神经,其再生能力非常有限,同时骨软骨缺损的伤口处存在氧化应激、炎症等病理微环境,在临床上对骨软骨缺损的治疗修复存在很大困难[62]。针对这一难题,CAO等[30]利用铜纳米颗粒与单宁酸(Tannic acid,TA)制备了具有酶类活性的铜基金属有机框架材料(CuTA),再将其与丝素蛋白结合,合成了具备抗氧化、抗炎和抗菌协同作用的丝基复合水凝胶(CuTA@SF)。丝素蛋白与单宁酸通过氢键相连接,进一步加强了水凝胶的交联程度,同时使CuTA获得良好的分散性,CuTA纳米酶的加入还使水凝胶呈现更均匀的微观结构和更高的亲水性。研究人员将该材料植入兔骨软骨缺损模型中,12周后,对照组缺损区均有白色新生组织填充,再生区均有裂缝,而CuTA@SF修复后的组织表面规则,与周围组织融合良好。通过定量显微CT分析,CuTA@SF修复的再生骨具有最高的骨密度达(0.24±0.05) g/cm3。实验结果表明CuTA@SF水凝胶具有良好的抗氧化和抗菌性能,并且表现出加速细胞增殖、增强细胞活力、促进间充质干细胞成骨的功能,是一种很有应用前景的软骨再生生物材料。 骨关节炎:是一种涉及关节软骨内细胞外基质稳态破坏的退行性关节疾病,这种破坏会导致软骨退变和骨增生,其病理特征包括关节软骨退行性变和关节内炎症,关节中促炎递质增加,导致蛋白水解酶过量产生,加速软骨破裂,继而反过来进一步放大炎症,因此治疗需要抗炎和营养关节相结合[63]。YANG等[48]应用碳酸二苯酯修饰的环糊精金属有机框架来负载非类固醇消炎药布洛芬(IBU),接着将其作为交联剂,以具有营养关节作用的盐酸氨基葡萄糖(GH)和明胶作为基质,制备了一种用于骨软骨修复联合抗炎治疗的复合水凝胶材料。实验结果表明,该材料可实现非类固醇消炎药布洛芬和盐酸氨基葡萄糖的长期缓慢释放,在提供软骨细胞营养物质的同时,利用非类固醇消炎药减轻关节内部炎症;同时,该材料在降解过程中仍保持良好的机械性能,有效保证长期给药的稳定性,为骨关节炎的治疗提供了新的策略。 2.4.2 软组织修复 软组织缺损是指由于创伤、感染、疾病或手术等原因造成的软组织缺失或损伤,如果不及时进行医疗干预,可能导致伤口反复感染,难以愈合,甚至危及患者生命。组织缺损创面的微环境中存在诸多不利于愈合的因素,包括出血、反复感染、长期处于炎症状态和氧化应激等问题[64]。针对这些问题,研究人员开发出性能各异的伤口敷料来保护创面,改善创口微环境,促进软组织修复。水凝胶呈现出三维网状结构,具有良好的渗透性和生物相容性,并能够为伤口修复提供湿润的环境,被认为是一种用于伤口敷料的理想材料[65]。而金属有机框架具有优异的多功能性,既可以抑制细菌感染,又能够调节氧化应激状态,很好地应对复杂的创面微环境。因此,金属有机框架基水凝胶材料是一种适用于软组织缺损修复的良好生物医学材料。 止血:伤口愈合通常被认为是一个复杂的动态过程,包括止血、炎症、增殖和重塑等阶段。在伤口产生初期若不能有效止血,不仅会导致细菌、异物进入伤口,增加感染风险,而且会阻碍局部血液循环,影响伤口处氧气和营养物质的供应。因此在伤口愈合过程中,止血具有重要意义。ZHANG等[44]设计了一种用于伤口敷料的双层水凝胶,上层为负载了银离子修饰的金属有机框架的壳聚糖水凝胶,具有良好的抗菌活性,下层为聚乙烯醇、海藻酸钠和壳聚糖交联形成的水凝胶,具有均匀的孔径分布、良好的机械性能和生物相容性。红细胞和血小板黏附实验表明,壳聚糖的加入导致黏附在辅料表面的红细胞和血小板数量增加,研究者认为这是由于壳聚糖能够介导血小板的黏附和聚集,附着于辅料表面的大量红细胞和血小板进一步积聚形成凝块,促进血液凝固。在小鼠全层皮肤创伤模型中,术后第12天,双层水凝胶的创面愈合率高达95.3%,远高于单独使用上层水凝胶的62.3%和单独使用下层水凝胶的85.4%,说明双层水凝胶能够有效促进伤口愈合。 抗感染:在皮肤屏障损伤后,微生物能够不受阻碍地进入伤口引发感染,造成局部炎症环境,抑制伤口愈合,并可能导致许多严重问题。作为潜在的多功能诊疗平台,研究人员使用金属有机框架基水凝胶材料整合多种抗菌疗法,实现高效抗菌治疗。DU等[46]将用于光热治疗的光热剂硝普钠加载到金属铂修饰的锆基卟啉金属有机框架中,并使用金纳米颗粒进行修饰,制备了可注射的复合水凝胶材料(PSPG)。在双重激发光照射下,该复合水凝胶能够充分发挥光动力治疗、光热治疗、NO三者协同作用,同时能够缓解感染创口的缺氧状态,抑制细菌生物膜形成,实现多机制联合抗菌治疗。实验表明,PSPG在双重激发光下对大肠杆菌和金黄色葡萄球菌均具有较好的抗菌能力,伤口的总体细菌负担减少99.9%。此外,细菌黏附和定植是导致软组织损伤后细菌进入伤口造成感染的关键过程,因此研究人员通过设计合适的伤口敷料阻断这一过程,有效减少伤口处炎症反应。YAO等[66]利用亲水性聚合物合成了全疏水性敷料,通过微流控乳液模板法制备了含有ZIF-8的超疏水多孔水凝胶伤口敷料(ZIF-8@PVA)。这种材料本质上是亲水的,能够有效负载水溶性抗菌剂,但其表现出超疏水性,对多种溶液均表现出了较高的接触角,这种独特的组合有效阻止了细菌的黏附定植,并具有优异的抗菌性能。在感染的大鼠全层皮肤缺损模型中,ZIF-8@PVA处理的伤口在11 d后几乎完全愈合,治愈率高达89.6%。 伤口处细菌感染的早期诊断对于防止细菌进一步增殖具有重要意义,因此亟需开发一种具有实时监测伤口感染功能的伤口辅料。在目前的细菌感染诊断策略中,原位可视化检测由于无需复杂的分析过程,能够直接通过肉眼实时监测细菌的生长和代谢而受到极大关注。ZHOU等[67]采用单磷酸鸟苷、环丙沙星(CIP)、铕离子(Eu3+)和铽离子(Tb3+)自组装制备镧系配位聚合物,再将其固定于葡聚糖醛和壳聚糖组成的水凝胶基质上,制备了一种pH响应型多色发光镧系水凝胶。该水凝胶可以分别发出CIP、Tb3+和Eu3+的蓝色、绿色和红色荧光。由于配体与镧系离子之间的配位作用受到环境pH值的影响,随着pH值的升高,Tb3+的绿色荧光和CIP的蓝色荧光逐渐减弱,而Eu3+的红色荧光逐渐增强。研究表明,在感染伤口中,细菌生长过程中产生的质子可使凝胶的颜色由红色变为白色或绿色,实现细菌感染的早期可视化诊断。同时,由于动态席夫碱键和配位作用在酸性环境中不稳定,CIP也随之逐步释放,发挥抗菌活性,实现感染伤口诊疗一体化。 炎症调节:进入伤口的细菌会激活机体免疫系统产生适当的免疫细胞进入炎症组织消灭微生物,然而,生长因子和促炎细胞因子等失调会导致过度免疫反应,加重局部炎症状态,影响伤口愈合过程[68]。因此,除了抗菌治疗外,控制过度的炎症和免疫反应是缩短伤口炎症期的关键。LI等[69]将负载了类固醇类抗炎药物地塞米松的ZIF-8纳米颗粒掺入水凝胶基质中,制备了一种用于牙周炎治疗的可注射复合水凝胶材料。前期研究表明,ZIF-8具有持续的抗菌活性和酸反应性药物释放特征,但缺乏抗炎特性,单独使用时难以很好地控制牙周炎症。地塞米松是一种有效的类固醇类抗炎和免疫抑制剂,还能够促进骨髓间充质干细胞和牙周膜干细胞的增殖与分化。负载了地塞米松的ZIF-8能够在牙菌斑酸性微环境的刺激下释放药物,发挥抗炎抗菌双重作用,构建稳定的微环境。实验结果表明,该材料能够有效减少牙周炎大鼠模型的牙周炎症和炎症引起的骨质流失。 调节氧化应激状态:在糖尿病患者的创面微环境中,较高的血糖浓度会破坏正常的氧化还原反应,产生高浓度的活性氧,继而导致伤口处发生慢性炎症,迁延不愈[70]。CHAO等[71]将一种具有抗氧化酶样活性的金属有机框架材料(MOF-818)与明胶结合,构建了一种能够持续清除活性氧,调节糖尿病慢性创面氧化应激微环境的复合水凝胶。在研究中,他们发现MOF-818同时具有超氧化物歧化酶样和过氧化氢酶样活性,并且其活性高于许多已报道的抗氧化纳米酶;此外,MOF-818在水溶液中可至少保持催化活性180 d,这证明MOF-818具有长期治疗的潜力;实验表明,一次性使用该复合水凝胶能够与多次使用人表皮生长因子凝胶的常规疗法取得同等治疗效果。 血管生成:是指血管内皮细胞增殖、迁移,最终形成新生血管的过程。新生血管能够为创口提供足够的氧气和营养物质,促进细胞增殖和迁移,加速伤口愈合,因此在软组织损伤愈合过程中,血管生成起着至关重要的作用[72]。WANG等[34]使用一种环状铜基金属有机框架材料来装载碱性成纤维细胞生长因子,并将其与GelMA相结合,合成具有多种功能的复合水凝胶。铜离子具有良好的抗菌特性,且能刺激生长因子和细胞因子的表达;碱性成纤维细胞生长因子能够刺激血管内皮细胞的生长和迁移,有利于新生血管形成,还能刺激成纤维细胞和内皮细胞增殖生成肉芽组织,加快再上皮化和组织重塑进程。在该材料中,两者成功发挥高效协同作用。在大鼠全层皮肤缺损模型中,与对照组相比,复合水凝胶组的CD34、CD31和α-平滑肌肌动蛋白免疫荧光染色的阳性表达更强,说明其具有显著的促血管生成的生物活性,能够加速伤口愈合。 减少瘢痕形成:目前的研究认为成纤维细胞的过度产生和伤口周围生物电的消失可能是瘢痕形成的主要原因,尤其是生物电在缓慢的创面修复过程中逐渐减弱甚至消失,会导致创面修复基因调控紊乱,胶原纤维沉积紊乱,并最终形成瘢痕。金属有机框架基水凝胶的形态高度可塑,已被证明能够制备成微针阵列,实现无痛、微创的经皮或皮内给药。ZHANG等[73]设计并制造了一种自供电的酶联微针贴片,该贴片由阳极和阴极微针阵列组成,阳极是负载了葡萄糖氧化酶的ZIF-8纳米颗粒,阴极是负载了辣根过氧化物酶的ZIF-8纳米颗粒,贴片基质为具有良好导电性的改性聚吡咯。葡萄糖氧化酶催化葡萄糖氧化生成葡萄糖酸和过氧化氢,辣根过氧化物酶则能够催化过氧化氢生成水,当这两者分布于具有良好导电性的贴片的正负两极时,就形成了一个生物酶促电池,通过消耗血糖保证稳定的微电流输出,降低血糖浓度的同时模拟内源性生物电,促进包括血管、皮肤附属器在内的组织重建,同时预防瘢痕的形成。Masson染色显示空白组再生的胶原纤维是不连续、无组织的,而使用自供电酶联微针贴片处理组的胶原纤维是相对完整、连续、规则、有序的,这说明贴片产生的微电流促进了胶原的有序排列。金属有机框架基水凝胶材料软硬组织修复相关研究见表3。"

| [1] FINGERHUT LA, HARRISON J, HOLDER Y, et al. Addressing the growing burden of trauma and injury in low- and middle-income countries. Am J Public Health. 2005;95(7):1089-1090. [2] PEPPAS NA, HILT JZ, KHADEMHOSSEINI A, et al. Hydrogels in biology and medicine: from molecular principles to bionanotechnology. Adv Mater. 2006;18(11):1345-1360. [3] ANNAMALAI J, MURUGAN P, GANAPATHY D, et al. Synthesis of various dimensional metal organic frameworks (MOFs) and their hybrid composites for emerging applications-A review. Chemosphere. 2022;298:134184. [4] SUN W, ZHAO X, WEBB E, et al. Advances in metal–organic framework-based hydrogel materials: preparation, properties and applications. J Mater Chem A. 2023;11(5):2092-2127. [5] YANG J, YANG YW. Metal-organic frameworks for biomedical applications. Small. 2020;16(10): e1906846. [6] ZHANG YP, XU JX, ZHOU J, et al. Metal-organic framework-derived multifunctional photocatalysts. Chin J Catal. 2022;43(4):971-1000. [7] HAN D, LI Y, LIU X, et al. Rapid bacteria trapping and killing of metal-organic frameworks strengthened photo-responsive hydrogel for rapid tissue repair of bacterial infected wounds. Chem Eng J. 2020. doi: 10.1016/j.cej.2020.125194. [8] HOSEINPOUR V, SHARIATINIA Z. Applications of zeolitic imidazolate framework-8 (ZIF-8) in bone tissue engineering: a review. Tissue Cell. 2021;72:101588. [9] VODYASHKIN AA, SERGORODCEVA AV, KEZIMANA P, et al. Metal-organic framework (MOF)—a universal material for biomedicine. Int J Mol Sci. 2023;24(9):7819. [10] MOHARRAMNEJAD M, EHSANI A, SHAHI M, et al. MOF as nanoscale drug delivery devices: Synthesis and recent progress in biomedical applications. J Drug Delivery Sci Technol. 2023. doi: 10.1016/j.jddst.2023.104285. [11] HOU YS, MA SH, HAO JL, et al. Construction and ion transport-related applications of the hydrogel-based membrane with 3D nanochannels. Polymers. 2022;14(19):4037. [12] BAI L, TAO G, FENG MG, et al. Hydrogel drug delivery systems for bone regeneration. Pharmaceutics. 2023;15(5):1334. [13] 杨航,熊玉竹,兰显玉,等.抗菌水凝胶在伤口敷料中的应用[J].化工新型材料,2022, 50(8):267-272. [14] LEI LJ, BAI YJ, QIN XY, et al. Current understanding of hydrogel for drug release and tissue engineering. Gels. 2022;8(5):301. [15] ZHANG X, WEI PY, YANG ZY, et al. Current progress and outlook of nano-based hydrogel dressings for wound healing. Pharmaceutics. 2023;15(1):68. [16] CHENG H, SHI Z, YUE K, et al. Sprayable hydrogel dressing accelerates wound healing with combined reactive oxygen species-scavenging and antibacterial abilities. Acta Biomater. 2021; 124:219-232. [17] ZONG Z, TIAN GH, WANG JL, et al. Recent advances in metal-organic-framework-based nanocarriers for controllable drug delivery and release. Pharmaceutics. 2022;14(12):2790. [18] MOHARRAMNEJAD M, MALEKSHAH RE, EHSANI A, et al. A review of recent developments of metal-organic frameworks as combined biomedical platforms over the past decade. Adv Colloid Interface Sci. 2023;316:102908. [19] WICHTERLE O, LÍM D. Hydrophilic gels for biological use. Nature. 1960;185(4706):117-118. [20] TOMIC EA. Thermal stability of coordination polymers. J Appl Polym Sci. 1965;9(11):3745-3752. [21] YAGHI OM, LI G, LI H. Selective binding and removal of guests in a microporous metal–organic framework. Nature. 1995;378(6558):703-706. [22] CHUJO Y, SADA K, SAEGUSA T. Iron(II) bipyridyl-branched polyoxazoline complex as a thermally reversible hydrogel. Macromolecules. 1993;26(24):6315-6319. [23] LIU Y, MA W, LIU W, et al. Silver(I)-glutathione biocoordination polymer hydrogel: effective antibacterial activity and improved cytocompatibility. J Mater Chem. 2011;21(48):19214-19218. [24] MAURIN G, SERRE C, COOPER A, et al. The new age of MOFs and of their porous-related solids. Chem Soc Rev. 2017;46(11):3104-3107. [25] HAMEDI H, MORADI S, HUDSON SM, et al. Chitosan based hydrogels and their applications for drug delivery in wound dressings: a review. Carbohydr Polym. 2018;199:445-460. [26] ZHANG Y, WU H, LI P, et al. Dual-light-triggered in situ structure and function regulation of injectable hydrogels for high-efficient anti-infective wound therapy. Adv Healthc Mater. 2022;11(1):e2101722. [27] DE LIMA HHC, DA SILVA CTP, KUPFER VL, et al. Synthesis of resilient hybrid hydrogels using UiO-66 MOFs and alginate (hydroMOFs) and their effect on mechanical and matter transport properties. Carbohydr Polym. 2021;251:116977. [28] SHAO G, WANG S, ZHAO H, et al. Tunable arrangement of hydrogel and cyclodextrin-based metal organic frameworks suitable for drug encapsulation and release. Carbohydr Polym. 2022;278:118915. [29] CHAKRABORTY A, SUTAR P, YADAV P, et al. Charge-assisted self-assembly of ZIF-8 and laponite clay toward a functional hydrogel nanocomposite. Inorg Chem. 2018;57(23):14480-14483. [30] CAO Z, WANG H, CHEN J, et al. Silk-based hydrogel incorporated with metal-organic framework nanozymes for enhanced osteochondral regeneration. Bioact Mater. 2023;20:221-242. [31] WENG P, LIU K, YUAN M, et al. Development of a ZIF-91-porous-liquid-based composite hydrogel dressing system for diabetic wound healing. Small. 2023:e2301012. [32] ZHU Z, LIU Y, CHEN J, et al. Structural-functional pluralistic modification of silk fibroin via mof bridging for advanced wound care. Adv Sci (Weinh). 2022;9(35):e2204553. [33] 杨宇州, 李政, 黄艳凤,等. MOF基水凝胶材料的制备及其应用[J].化学进展,2021,33(5):726-739. [34] WANG TL, ZHOU ZF, LIU JF, et al. Donut-like MOFs of copper/nicotinic acid and composite hydrogels with superior bioactivity for rh-bFGF delivering and skin wound healing. J Nanobiotechnol. 2021;19(1):275. [35] NELE V, WOJCIECHOWSKI JP, ARMSTRONG JPK, et al. Tailoring gelation mechanisms for advanced hydrogel applications. Adv Funct Mater. 2020. doi: 10.1002/adfm.202002759. [36] RAINA N, PAHWA R, BHATTACHARYA J, et al. Drug delivery strategies and biomedical significance of hydrogels: translational considerations. Pharmaceutics. 2022;14(3):574. [37] 包佳伟,刘鉴峰,张嘉敏,等.金属-有机框架材料在细菌感染治疗中的研究进展[J].科学通报,2023,68(13):1677-1688. [38] LI SR, CUI YT, LIU H, et al. Application of bioactive metal ions in the treatment of bone defects. J Mater Chem B. 2022;10(45):9369-9388. [39] SUN Y, LIU X, ZHU Y, et al. Tunable and controlled release of cobalt ions from metal-organic framework hydrogel nanocomposites enhances bone regeneration. ACS Appl Mater Interfaces. 2021;13(49):59051-59066. [40] CHEN ZT, YUEN J, CRAWFORD R, et al. The effect of osteoimmunomodulation on the osteogenic effects of cobalt incorporated beta-tricalcium phosphate. Biomaterials. 2015;61:126-138. [41] SUN ZY, LI TY, MEI TX, et al. Nanoscale MOFs in nanomedicine applications: from drug delivery to therapeutic agents. J Mater Chem B. 2023;11(15):3273-3294. [42] LU S, REN X, GUO T, et al. Controlled release of iodine from cross-linked cyclodextrin metal-organic frameworks for prolonged periodontal pocket therapy. Carbohydr Polym. 2021;267:118187. [43] LIU Y, ZHU Z, PEI X, et al. ZIF-8-Modified Multifunctional bone-adhesive hydrogels promoting angiogenesis and osteogenesis for bone regeneration. ACS Appl Mater Interfaces. 2020; 12(33):36978-36995. [44] ZHANG M, WANG G, WANG D, et al. Ag@MOF-loaded chitosan nanoparticle and polyvinyl alcohol/sodium alginate/chitosan bilayer dressing for wound healing applications. Int J Biol Macromol. 2021;175:481-494. [45] TIAN M, ZHOU L, FAN C, et al. Bimetal-organic framework/GOx-based hydrogel dressings with antibacterial and inflammatory modulation for wound healing. Acta Biomater. 2023;158:252-265. [46] DU T, XIAO Z, ZHANG G, et al. An injectable multifunctional hydrogel for eradication of bacterial biofilms and wound healing. Acta Biomater. 2023;161:112-133. [47] QIAO M, XU Z, PEI X, et al. Nano SIM@ZIF-8 modified injectable High-intensity biohydrogel with bidirectional regulation of osteogenesis and Anti-adipogenesis for bone repair. Chem Eng J. 2022;434. [48] YANG H, HU Y, KANG M, et al. Gelatin-glucosamine hydrochloride/crosslinked-cyclodextrin metal-organic frameworks@IBU composite hydrogel long-term sustained drug delivery system for osteoarthritis treatment. Biomed Mater. 2022. doi: 10.1088/1748-605X/ac61fa. [49] LEE SJ, TELFER SG. Multicomponent metal-organic frameworks. Angew Chem Int Ed Engl. 2023; 62(44):e202306341. [50] SALEEM G, CHEN X, GU RX, et al. Nanozymes - A route to overcome microbial resistance: a viewpoint. Nanotechnol Rev. 2022;11(1):2575-2583. [51] CHANDIO I, AI YJ, WU L, et al. Recent progress in MOFs-based nanozymes for biosensing. Nano Res. 2023. doi: 10.1007/s12274-023-5770-3. [52] MATLOU GG, ABRAHAMSE H. Nanoscale metal-organic frameworks as photosensitizers and nanocarriers in photodynamic therapy. Front Chem. 2022;10:971747. [53] XU DX, DUAN Q, YU H, et al. Photodynamic therapy based on porphyrin-based metal-organic frameworks. J Mater Chem B. 2023;11(26):5976-5989. [54] CHEN Y, LI D, ZHONG Y, et al. NIR regulated upconversion nanoparticles@metal-organic framework composite hydrogel dressing with catalase-like performance and enhanced antibacterial efficacy for accelerating wound healing. Int J Biol Macromol. 2023;235:123683. [55] ASHRAF G, AHMAD T, AHMED MZ, et al. Advances in metal-organic frameworks (MOFs) based Biosensors for diagnosis: an update. Curr Top Med Chem. 2022;22(27):2222-2240. [56] NISHAT ZS, HOSSAIN T, ISLAM MN, et al. Hydrogel nanoarchitectonics: an evolving paradigm for ultrasensitive biosensing. Small. 2022;18(26):e2107571.. [57] XUE NN, DING XF, HUANG RZ, et al. Bone tissue engineering in the treatment of bone defects. Pharmaceuticals. 2022;15(7):879. [58] SHYNGYS M, REN J, LIANG XQ, et al. Metal-organic framework (MOF)-based biomaterials for tissue engineering and regenerative medicine. Front Bioeng Biotechnol. 2021;9:603608. [59] WANG SY, LI R, XIA DD, et al. The impact of Zn-doped synthetic polymer materials on bone regeneration: a systematic review. Stem Cell Res Ther. 2021;12(1):123. [60] ZHENG J, BRION MJ, KEMP JP, et al. The effect of plasma lipids and lipid-lowering interventions on bone mineral density: a mendelian randomization study. J Bone Miner Res. 2020;35(7):1224-1235. [61] LAO A, WU J, LI D, et al. Functionalized metal-organic framework-modified hydrogel that breaks the vicious cycle of inflammation and ROS for repairing of diabetic bone defects. Small. 2023;19(36):e2206919. [62] CHEN RY, PYE JS, LI JR, et al. Multiphasic scaffolds for the repair of osteochondral defects: Outcomes of preclinical studies. Bioact Mater. 2023;27:505-545. [63] WONG HL, TSANG CY, BEYER S. Metal-organic frameworks (MOFs) and their composites as emerging biomaterials for osteoarthritis treatment. Biomimetics (Basel). 2023;8(1):97. [64] LI Y, FU R, DUAN Z, et al. Construction of multifunctional hydrogel based on the tannic acid-metal coating decorated MoS2 dual nanozyme for bacteria-infected wound healing. Bioact Mater. 2022;9:461-474. [65] XU Z, HAN S, GU Z, et al. Advances and impact of antioxidant hydrogel in chronic wound healing. Adv Healthcare Mater. 2020;9(5):e1901502. [66] YAO X, ZHU G, ZHU P, et al. Omniphobic ZIF-8@hydrogel membrane by microfluidic-emulsion-templating method for wound healing. Adv Funct Mater. 2020. doi: 10.1002/adfm.201909389. [67] ZHOU Q, DONG X, ZHANG B, et al. Naked-eye sensing and target-guiding treatment of bacterial infection using pH-tunable multicolor luminescent lanthanide-based hydrogel. J Colloid Interface Sci. 2022;610:731-740. [68] AHMAD N. In vitro and in vivo characterization methods for evaluation of modern wound dressings. Pharmaceutics. 2023;15(1):42. [69] LI N, XIE L, WU Y, et al. Dexamethasone-loaded zeolitic imidazolate frameworks nanocomposite hydrogel with antibacterial and anti-inflammatory effects for periodontitis treatment. Mater Today Bio. 2022;16:100360. [70] WORSLEY AL, LUI DH, NTOW-BOAHENE W, et al. The importance of inflammation control for the treatment of chronic diabetic wounds. Int Wound J. 2023;20(6):2346-2359. [71] CHAO D, DONG Q, YU Z, et al. Specific nanodrug for diabetic chronic wounds based on antioxidase-mimicking MOF-818 nanozymes. J Am Chem Soc. 2022;144(51):23438-23447. [72] HAN C, BARAKAT M, DIPIETRO LA. Angiogenesis in wound repair: too much of a good thing? Cold Spring Harbor Perspect Biol. 2022;14(10):a041225. [73] ZHANG X, WANG Z, JIANG H, et al. Self-powered enzyme-linked microneedle patch for scar-prevention healing of diabetic wounds. Sci Adv. 2023;9(28):eadh1415. |
| [1] | Yang Yufang, Yang Zhishan, Duan Mianmian, Liu Yiheng, Tang Zhenglong, Wang Yu. Application and prospects of erythropoietin in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1443-1449. |
| [2] | Chen Kaijia, Liu Jingyun, Cao Ning, Sun Jianbo, Zhou Yan, Mei Jianguo, Ren Qiang. Application and prospect of tissue engineering in treatment of osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1450-1456. |
| [3] | Mei Jingyi, Liu Jiang, Xiao Cong, Liu Peng, Zhou Haohao, Lin Zhanyi. Proliferation and metabolic patterns of smooth muscle cells during construction of tissue-engineered blood vessels [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1043-1049. |
| [4] | Wang Shanshan, Shu Qing, Tian Jun. Physical factors promote osteogenic differentiation of stem cells [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1083-1090. |
| [5] | Chen Zan, Lei Fei, Ye Fei, Zhou Qingzhong, Yuan Hao, Zheng Lipeng, Zha Xian, Feng Daxiong. Relationship between drainage time and early efficacy after short-segment lumbar fusion [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 927-933. |
| [6] | Wang Wu, Fan Xiaolei, Xie Jie, Hu Yihe, Zeng Min. Hydroxyapatite-polyvinyl alcohol/collagen-chitosan-gelatin composite hydrogel for repairing rabbit osteochondral defect [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 682-689. |
| [7] | Zhang Ya, Mu Qiuju, Wang Zilin, Liu Hongjie, Zhu Lili. Hydrogel loaded with platelet-rich plasma promotes wound healing in diabetic rats [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 690-696. |
| [8] | Shen Ziqing, Xia Tian, Shan Yibo, Zhu Ruijun, Wan Haoxin, Ding Hao, Pan Shu, Zhao Jun. Vascularized tracheal substitutes constructed by exosome-load hydrogel-modified 3D printed scaffolds [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 697-705. |
| [9] | Li Jiaqi, Huang Yuanli, Li Yan, Wang Chunren, Han Qianqian. Mechanism and influencing factors in molecular weight degradation of non-cross-linked hyaluronic acid [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 747-752. |
| [10] | Zhu Liwei, Wang Jiangyue, Bai Ding. Application value of nanocomposite gelatin methacryloyl hydrogels in different bone defect environments [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 753-758. |
| [11] | Yin Kaiwen, Li Yunfeng. Application of metal-organic frameworks in implant surface modification [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 783-788. |
| [12] | Chen Xiaofang, Zheng Guoshuang, Li Maoyuan, Yu Weiting. Preparation and application of injectable sodium alginate hydrogels [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 789-794. |
| [13] | Wang Jiani, Chen Junyu. Angiogenesis mechanism of metal ions and their application in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 804-812. |
| [14] | Yang Yuqing, Chen Zhiyu. Role and application of early transient presence of M1 macrophages in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 594-601. |
| [15] | Xing Hao, Meng Qingfeng, Chang Zhengqi. Mechanism of negative pressure wound therapy in the auxiliary treatment of bone and soft tissue infection [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 621-626. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||



