Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (31): 5071-5077.doi: 10.12307/2023.676
Previous Articles Next Articles
Properties, functions and applications of three-dimensional models of bone for drug screening
Huang Miao1, Wu Xiesheng2, Huang Wenshi2, Huang Haina1, Chen Longyun1, Peng Weijie1
- 1Gannan Medical University, Ganzhou 341000, Jiangxi Province, China; 2School of Pharmacy, Nanchang University, Nanchang 330006, Jiangxi Province, China
-
Received:2022-09-09Accepted:2022-10-18Online:2023-11-08Published:2023-01-31 -
Contact:Peng Weijie, PhD, Professor, Doctoral supervisor, Gannan Medical University, Ganzhou 341000, Jiangxi Province, China -
About author:Huang Miao, Master candidate, Gannan Medical University, Ganzhou 341000, Jiangxi Province, China -
Supported by:National Natural Science Foundation of China, No. 81860327 (to PWJ)
CLC Number:
Cite this article
Huang Miao, Wu Xiesheng, Huang Wenshi, Huang Haina, Chen Longyun, Peng Weijie. Properties, functions and applications of three-dimensional models of bone for drug screening[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(31): 5071-5077.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

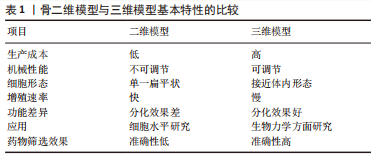
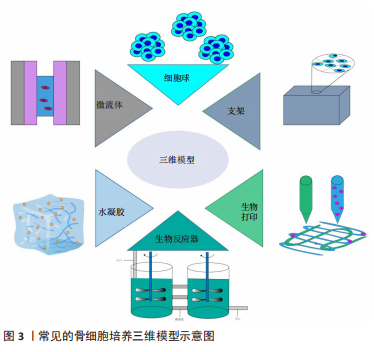
2.1 体外模型概括 2.1.1 二维细胞培养模型 传统的二维细胞培养模型包括烧瓶、玻璃板、聚苯乙烯培养皿或板[8-9],细胞黏附在这些平面上可以快速生长。然而,这些二维模型大多不能很好地模拟骨细胞的生长环境,它改变了细胞骨架的自然分布和基因表达,使得骨细胞在这些二维层面上变成了扁平状[10]。后来研究者改进产生了三明治培养技术[11],它通过构建一个上下两层的微孔结构来吸附生长因子,为细胞提供营养物质,而中间那一层通常是模仿体内的天然细胞外基质成分的结构,能够促进营养扩散和细胞浸润,这种技术在骨组织工程应用中具有出色潜力。微孔阵列通过修改基底形貌创造各种不同的微环境,为骨细胞建立合适的生长条件[12]。基质的材料、形状、宽度和粗糙度等是影响骨细胞形态、黏附和增殖的关键因素,很大程度上会影响细胞的功能[13]。然而,传统的二维模型以及这些改进的培养模型仍不足以代表真实的骨骼形态,无法反映骨细胞的微环境。因此,研究者们必须了解骨骼的生物力学特性及其生长环境的特征才能更好地开发出合适的骨三维模型。 2.1.2 三维细胞培养模型 体外骨骼发育需要三维组织来模拟自然细胞外基质的结构、机械性能(即刚度和强度)和组成成分。三维培养系统通过提供细胞和细胞相互作用的空间,来研究细胞在体内的相互作用机制。 目前,已经开发了各种各样的三维模型用于骨细胞培养,见图3。主要可分为两种:一种是无支架的三维细胞模型,细胞通过沉淀法、悬滴法或搅拌法在悬浮液中形成聚集体;另外一种是有支架的三维细胞模型,它们在体外模仿细胞外基质框架,让细胞像在体内一样进行增殖分化。它们可以通过提供对生化和机械微环境线索的控制来克服当前二维模型的局限性,为研究潜在的生化和生物力学信号开辟新的可能性[14]。不同三维模型的生产方式和基本特性不同,在后期的实际应用中也各有优势。体外骨细胞三维培养模型的开发可以为实现良好的骨形成提供新的见解。除了体外应用,三维骨细胞模型还有望成为组织工程和再生医学的潜在工具。"

很多研究已经证明,二维细胞培养体系使得所有细胞从培养基中均匀获得养分和生长因子[15]。而在三维培养体系中,细胞形状与其在体内的自然形状非常相似,具有相似的细胞骨架可以更好地模拟内部生长过程[16]。在二维基质上,细胞必须适应人造的刚性表面,这就意味着不同于在体内自然生长的特性。有研究已经证明,二维平面培养和三维球状培养的细胞整体形态是不同的,更准确地说,在三维状态下培养的细胞比在二维基质上更类似于体内形态[17]。此外,两种模型培养的细胞,增殖速率一般不同,与二维培养的细胞相比,三维培养状态下的增殖率较低[18]。 很多研究表明,细胞外基质在骨骼形成中起重要作用,细胞通过细胞外基质进行相互作用和相互通信,即三维模型通过模拟细胞外基质来增强细胞的成骨效应[19-20]。KIM等[21]在二维和三维培养条件下对人脂肪源性干细胞的成骨分化效应进行了研究,并采用多种生物信息学方法进行分析,发现不同培养体系下人脂肪源性干细胞成骨分化相关基因表达存在显著差异,在培养3周时,三维培养条件下的表达水平均高于二维培养条件下的表达水平,说明三维培养对干细胞的成骨分化效应具有促进作用。此外,TORTELLI等[22]开发了一种支架作为三维骨细胞培养模型,用于培养小鼠原代成骨细胞,相关数据表明,三维环境增强了成骨细胞的分化,从而促进了早期的破骨细胞分化,但功能性三维组织模型仍缺乏形成分层的、有序的架构和结构的能力。因此,研究者们可以发现三维模型在骨组织工程中具有很大的应用潜能,但要进一步改进技术,开发出性能更合适的三维模型。"

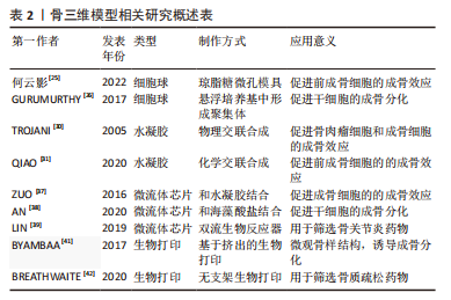
2.2 三维骨组织模型的构建及其药物筛选 与传统的二维药物筛选模型相比,三维模型可以根据骨细胞生长环境的特点,模拟实体组织的药敏和耐药模式,从而提高药物筛选的准确性,表明这可能是一个很好的体内药物反应的载体[23]。 2.2.1 细胞球 细胞球培养体系已经广泛用于骨细胞培养中,细胞在基质或悬浮培养基中形成聚集体,还原细胞-细胞和细胞-基质相互作用过程[24]。 当前构建细胞球的方法有很多种,最近报告了一种采用琼脂糖和聚丙烯酸模具,利用层层自组装技术构建细胞球三维培养模型的方法,通过和常规培养小鼠前体成骨细胞比较,发现此三维培养模型还原了细胞宏观及微观生理环境,成骨分化相关指标检测后表明,此模型具有明显的促进成骨分化效应的潜能,为骨组织工程进一步研究提供了依据和思路[25]。细胞成骨分化常常通过向培养基中添加诱导剂来实现[26],诱导剂通常由抗坏血酸,β-甘油磷酸盐和地塞米松组成。RUMINSKI等[27]通过将脂肪间充质干细胞培养成单层和球状体来比较它的成骨潜力,通过蛋白质印迹和免疫荧光结果表明,球状体培养的成骨细胞标志物Runx2和IBSP显著上调。最近,KIM等[28]对比了诱导剂和三维结构效应对成骨分化的作用,发现化学效应的影响不如三维结构效应。他们的结果表明,前成骨细胞的分化强烈依赖于三维结构效应,使用三维球形结构的细胞聚集触发了前成骨细胞更大程度地分化。 总之,成骨细胞和干细胞的细胞球培养体系结果显示,细胞球可以显著增强成骨效应,在骨组织的形成中具有明显的促进作用。球状培养的细胞不论是基因表达,还是活性和形态均呈接触依赖性,三维结构对细胞功能有显著影响。但是,这种微球模型在基础研究中也存在一定的局限性,如缺乏结构支撑、细胞无法有效氧化、缺乏营养物质和代谢物交换系统等。这些不足之处为研究者们今后的技术改进提供了方向。 2.2.2 水凝胶 水凝胶是由胶原蛋白、明胶、纤维蛋白、海藻酸盐、琼脂糖和壳聚糖等聚合物制成的支架,水凝胶模型具有吸收大量水的能力,类似于体内组织。此外,它们具有良好的细胞封装能力,可调节的生化和机械性能,以及良好的生物相容性和低免疫原性[29]。 用于骨组织工程的水凝胶大多通过模拟骨组织的成分与结构来实现,目前水凝胶的制备大多是采用物理交联法或化学交联法,将多种不同小分子结合形成促进成骨分化或骨再生的支架。有研究将几种骨肉瘤细胞系和原代成骨细胞培养在一种由硅化羟丙基甲基纤维素组成的新型水凝胶中,通过检测成骨细胞标志物和细胞因子的表达,发现在水凝胶中的细胞具有良好的活力和增殖能力,且成骨分化效果更好[30],这提示研究者们支架可以和细胞共存。有研究使用紫外线辐射将明胶与成骨生长肽交联创建了一种新型成骨多肽水凝胶,用于培养小鼠成骨前体细胞,结果表明此共培养体系促进了细胞的增殖,增强了成骨相关基因的表达[31]。目前,很多水凝胶还可作为一个药物递送平台,通过负载药物来筛选出治疗骨骼系统疾病的有效药物。例如,LI等[32]制备了一种可注射水凝胶,NAFEE等[33]报道了一种温度敏感型水凝胶,他们可以根据各自的水凝胶特性长期输送阿仑膦酸盐,以促进骨质疏松症的治疗。 以上这些结果揭示了水凝胶在骨组织工程中的巨大优势。不同的水凝胶在骨组织工程中有各自的特性,但总体而言都具有促进成骨分化效应的巨大潜能。然而,尽管各种各样的水凝胶在人类成骨细胞培养中显示出了良好的结果,但大多数水凝胶在促进细胞增殖和基质生成方面仍然有限,并且逐步降解过程会改变它们的生化和机械性能,这些因素使得水凝胶的性能需要进一步提高,才能更好地应用于骨骼疾病的药物筛选中。 2.2.3 微流控芯片 微米级和纳米级制造的发展衍生出了一种新型的细胞培养系统,接近生物反应器,但规模较小,被称为微流控芯片[34]。与其他传统培养技术相比,使用微流体装置可以开发更复杂的微环境,并具有模拟体内真实环境的可能性,从而更容易地控制机械表面和生化参数,构建骨三维药物筛选模型[35-36],微流控芯片也被称为芯片实验室或器官芯片,被广泛用于骨组织工程研究。 有研究者将甲基丙烯化明胶和海藻酸盐结合用于制备基于微流体的纤维体系[37],这是一种双层空心超细纤维,填充在里面的成骨细胞表现出良好的生存能力,且Ⅰ型胶原蛋白和骨形态发生蛋白的水平均较高。AN等[38]开发了一种基于微流体的方法,使用海藻酸盐微凝胶在单细胞水平上连续包封干细胞,相关数据显示,此体系具有明显增强体外矿化和体内骨细胞形成的能力;从该研究结果可以看出,微流体技术的出现为细胞微环境的构建提供了很大的帮助,这种培养体系不仅保留了细胞的良好活力,还在一定程度上促进了成骨分化效应,推动了干细胞在骨再生中的应用,此外,它还被广泛用于骨骼系统疾病体外药物检测以及各种骨组织工程中。最近,LIN等[39]将多能干细胞封装在明胶中并在双流生物反应器中培养,该模型更紧密地概括了内源性关节环境,其中构建体底部的细胞暴露于成骨线索,而顶部的细胞暴露于软骨线索,培养28 d后,芯片的上部和下部区域分别观察到良好的软骨和成骨相关基因的表达,通过塞来昔布用药后的定量RT-PCR和组织学评估进一步证明了其作为骨关节炎药物筛选平台的潜力。 2.2.4 生物打印 三维生物打印技术通过沉积生物材料,以创建类似组织的结构,然后用于医学和组织工程。这些生物材料被称为“生物墨水”,生物打印技术中主要的生物墨水材料包括细胞聚集体、水凝胶、微载体和去细胞化基质组分[40]。生物打印有多种模式(例如,基于喷墨的生物打印、基于压力挤出的生物打印、激光生物打印、声学生物打印,基于立体光刻的生物打印和磁性生物打印等)。这些生物打印策略可以单独使用或组合使用,以实现不同材料和不同功能的结合。 修复骨缺损一直是一个巨大挑战。BYAMBAA等[41]利用基于挤出的生物打印策略开发了由GelMA水凝胶制成的微观骨样组织结构,其中装载有硅酸盐纳米片来诱导成骨分化,并合成了具有血管内皮生长因子的水凝胶制剂,可以促进血管扩散,结果发现此结构能够在体外成熟期间支持细胞存活和增殖,从而为骨组织模型的构建奠定基础。也有人通过生物打印骨骼系统模型,提供了一个药物筛选平台,筛选出4种预测促进(淫羊胍素和莤胏素)或损害(PD98059和U0126)成骨的药物[42]。这些研究结果表明,通过生物打印可以治疗部分骨损伤,同时在药物筛选中也具有巨大潜能,为骨组织工程的发展提供一个可行的方向。不仅如此,近几年,为了构建复杂功能结构,时间概念与三维生物打印结合在一起形成了新的建模体系,目前已成为组织工程的下一代解决方案,其可用于制造动态的三维生物结构,这些结构将通过采用刺激响应材料在各种刺激下改变其形状,在骨组织工程方面具有巨大的潜力[43]。 近年来,三维药物筛选模型地构建引起了广泛关注。常见的骨三维模型包括球体、水凝胶、生物反应器、生物打印和微流控芯片等,见表2。"

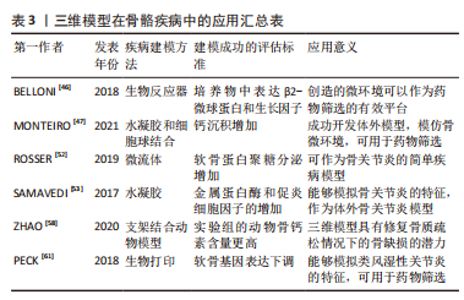
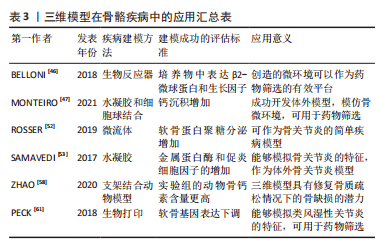
2.3 三维骨疾病模型的构建及药物筛选 疾病模型是理解发病的分子机制不可或缺的工具,同时也能促进新疗法的发展。目前骨骼疾病研究的模型主要有动物、组织器官、干细胞分化的骨细胞和原代成骨细胞等[44]。 2.3.1 骨髓瘤骨病 多发性骨髓瘤,世界上最普遍的血液系统癌症之一,它是一种浆细胞癌,其特征为恶性骨浸润、高钙血症、贫血和肾衰竭。多发性骨髓瘤引起的正常骨稳态失衡,可导致骨髓瘤骨病[45]。 目前研究者们已经开发了模仿多发性骨髓瘤的三维体外模型,并用它们来探索细胞-细胞相互作用对多发性骨髓瘤药物耐药性的影响。BELLONI等[46]利用生物反应器技术在明胶支架中进行骨髓瘤细胞-骨髓细胞共培养,结果发现,生物反应器中重建的人多发性骨髓瘤微环境可能代表了药物测试和研究肿瘤-基质分子相互作用的有效平台。他们通过骨髓瘤细胞建立体外疾病模型,生物反应器重建细胞生长微环境,在二者的结合下通过药物进一步证明了此体系的可行性,展现了三维模型在体外疾病模型中进行药物筛选的巨大优势。最近,MONTEIRO等[47]提出了一个三维骨肉瘤模型,他们将肿瘤结构和水凝胶概括为一个球体,与成骨细胞和干细胞共培养,通过阿霉素反应剂量测试来评估骨肉瘤模型在药物开发和筛选方面的潜力,这项研究结果表明,这种模型在骨肉瘤的生长速率、侵袭能力和对阿霉素治疗的耐药性方面具有积极的效应。在药物筛选方面,骨肉瘤球体被证明对阿霉素、顺铂、牛磺酸和紫杉醇等化疗药物的耐药性高于二维状态下培养的细胞,使其成为研究耐药性的有吸引力的平台[48]。 2.3.2 骨关节炎 骨关节炎是最常见的关节疾病[49],对全球老龄化人口的健康具有重大影响,但目前的预防措施或治疗方案不够完善[50]。骨关节炎患者的关节软骨会显示出衰老的特征,软骨细胞释放的衰老相关分泌表型因子(例如促炎症细胞因子和细胞外基质降解酶),已被确定为促进骨关节炎进程的主要介质[51]。 微流体和水凝胶等三维模型已被广泛用于骨关节炎治疗相关研究。ROSSER等[52]制备了一种基于营养梯度的微流体三维细胞培养模型,用于培养来自骨关节炎患者的软骨细胞,结果发现此模型可以很好地模拟软骨的生长环境,为了解细胞如何在病理生理状态下做出不同反应提供一个新的平台。近几年,也有研究报告了一种水凝胶三维共培养系统,通过在经典活化的促炎症巨噬细胞的存在下,共培养正常的和患病的软骨细胞来研究骨关节炎炎症的进展,结果发现,此三维模型可以很好地了解巨噬细胞和软骨细胞在骨关节炎疾病进展中的相互作用,在促进骨关节炎治疗药物的开发和筛选方面具有巨大的潜力[53]。此外,生物打印技术也逐渐用于仿生软骨组织的开发和软骨组织的修复中,但较低的机械性能和相对较高的成本限制了其在临床中的广泛应用。 2.3.3 骨质疏松症 骨质疏松症是一种常见的系统性骨骼疾病,可导致骨骼脆弱,增加骨折风险,在老年人和绝经妇女中发病率较高[54]。骨质疏松症是一种退行性病变,即使是药物治疗,也存在一个长期依赖性问题,目前还没有很好的应对措施,为此,现在很多研究者致力于寻找合适的方案去预防或者治疗骨质疏松症[55]。 成骨细胞与破骨细胞之间的骨稳态失衡是诱发骨质疏松的主要原因,目前已经开发出了多种可注射水凝胶系统,可以递送药物或者细胞以促进骨量增加[56]。林建立等[57]的一项科技成果指出,微流控芯片已经大量应用于骨质疏松症的临床治疗中,他们引入微流控芯片技术体系,运用片层三维细胞培养技术,通过细胞捕获、分选、裂解、细胞内涵物分析和蛋白修饰示踪等, 探讨骨质疏松症的发病过程,为预防和治疗骨质疏松症提供了新的思路和方法。ZHAO等[58]通过水热法设计并制备了锶掺入的三维羟基磷灰石晶须生物陶瓷,并在动物模型中证明了其在骨质疏松条件下成功修复骨缺损的潜力。最近,也有研究报道了一种新型三维支架,它由两种不用的环糊精制备而成,装载了盐酸雷洛昔芬,利用支架良好的孔隙率来评估其药物效果[59]。总之,三维模型的开发为骨质疏松症的治疗提供了一种可行的方案。 2.3.4 类风湿性关节炎 类风湿性关节炎是一种病因不明的全身性自身免疫性疾病,形成一种以巨噬细胞和成纤维样滑膜细胞为主体的增生滑膜组织,不仅影响关节的活动和健康,还累及全身多个组织器官。类风湿性关节炎目前的药物治疗体系不够完善,是国内外研究的热点和难点,构建合适的三维药物筛选模型,提高治疗该疾病的新药研发成功率至关重要[60]。 为了进一步了解类风湿软骨损伤的过程,PECK等[61]建立了一种由滑膜成纤维细胞、巨噬细胞和原代软骨细胞组成的球体共培养体外模型,通过免疫染色和生化分析表明,此模型能够概括类风湿性关节炎软骨的某些病理特征,用塞来昔布进一步证明,它通过逆转软骨损伤来响应药物的治疗效果,从而说明如果得到适当地验证,该模型可能可用于筛选新的治疗药物,从而有助于改善风湿的治疗效果。最近,AGOSRINI等[62]采用电解质络合法,制备了一种递送甲氨蝶呤的水凝胶模型,此水凝胶是由聚环氧乙烷和聚环氧丙烷三嵌段组成的聚合物-泊洛沙姆在体温条件下形成的。体内动物实验表明,使用基于泊洛沙姆的热敏水凝胶可有效延长体外药物甲氨蝶呤的释放,最大限度地减少全身药物暴露,从而提高治疗依从性并减少不良反应,为类风湿性关节炎的治疗开辟了新的方法。 文章列举了几种常见的骨骼疾病以及相关三维模型在药物筛选中的运用进展,见表3。"
| [1] DIMASI JA, GRABOWSKI HG. Economics of new oncology drug development. J Clin Oncol. 2007;25(2):209-216. [2] AMELIAN A, WASILEWSKA K, MEGIAS D, et al. Application of standard cell cultures and 3D in vitro tissue models as an effective tool in drug design and development. Pharmacol Rep. 2017;69(5):861-870. [3] TOVAR-LOPEZ FJ, DOMINGUEZ-HERNANDEZ VM, DIEZ-GARCIA MDEL P, et al. Finite-element analysis of the effect of basic hip movements on the mechanical stimulus within a proximal femur. Rev Invest Clin. 2014;66 Suppl 1:S32-S38. [4] WRZESINSKI K, FEY S J. From 2D to 3D--a new dimension for modelling the effect of natural products on human tissue. Cur Pharm Design. 2015;21(38):5605-5616. [5] MALTMAN DJ, PRZYBORSKI SA. Developments in three-dimensional cell culture technology aimed at improving the accuracy of in vitro analyses. Biochem Soc Transact. 2010;38(4):1072-1075. [6] LANGHANS SA. Three-dimensional in vitro cell culture models in drug discovery and drug repositioning. Front Pharmacol. 2018;9:6. [7] 刘劲松.体外构建三维肝肿瘤模型及药物筛选[J].中国组织工程研究,2014,18(27):4389-4394. [8] OLIVEIRA FA, MATOS AA, SANTESSO MR, et al. Low intensity lasers differently induce primary human osteoblast proliferation and differentiation. J Photochem Photobiol B. 2016;163:14-21. [9] WEYTS FA, BOSMANS B, NIESING R, et al. Mechanical control of human osteoblast apoptosis and proliferation in relation to differentiation. Calcif Tissue Int. 2003;72(4):505-512. [10] KNIGHT E, PRZYBORSKI S. Advances in 3D cell culture technologies enabling tissue-like structures to be created in vitro. J Anat. 2015; 227(6):746-756. [11] RAVICHANDRAN R, SUNDARAMURTHI D, GANDHI S, et al. Bioinspired hybrid mesoporous silica–gelatin sandwich construct for bone tissue engineering. Microporous Mesoporous Mater. 2014;187:53-62. [12] XU X, WANG W, KRATZ K, et al. Controlling major cellular processes of human mesenchymal stem cells using microwell structures. Adv Healthc Mater. 2014;3(12):1991-2003. [13] IHALAINEN T O, AIRES L, HERZOG F A, et al. Differential basal-to-apical accessibility of lamin A/C epitopes in the nuclear lamina regulated by changes in cytoskeletal tension. Nat Mater. 2015; 14(12):1252-1261. [14] BOUET G, MARCHAT D, CRUEL M, et al. In vitro three-dimensional bone tissue models: from cells to controlled and dynamic environment. Tissue Eng Part B Rev. 2015;21(1):133-156. [15] BUTTERY L, BIELBY R, HOWARD D, et al. Osteogenic differentiation of embryonic stem cells in 2D and 3D culture. Methods Mol Biol. 2011; 695:281-308. [16] RAVI M, PARAMESH V, KAVIYA SR, et al. 3D cell culture systems: advantages and applications. J Cell Physiol. 2015;230(1):16-26. [17] LIU X, SUN Q, WANG Q, et al. Epithelial cells in 2D and 3D cultures exhibit large differences in higher-order genomic interactions. Genomics Proteomics Bioinformatics. 2022;20(1):101-109. [18] SON YB, BHARTI D, KIM S B, et al. Comparison of pluripotency, differentiation, and mitochondrial metabolism capacity in three-dimensional spheroid formation of dental pulp-derived mesenchymal stem cells. BioMed Res Int. 2021;2021:5540877. [19] HAN X, TANG S, WANG L, et al. Multicellular spheroids formation on hydrogel enhances osteogenic/odontogenic differentiation of dental pulp stem cells under magnetic nanoparticles induction. Int J Nanomedicine. 2021;16:5101-5115. [20] WHITEHEAD J, GRIFFIN K H, GIONET-GONZALES M, et al. Hydrogel mechanics are a key driver of bone formation by mesenchymal stromal cell spheroids. Biomaterials. 2021;269:120607. [21] KIM BC, KWACK KH, CHUN J, et al. Comparative transcriptome analysis of human adipose-derived stem cells undergoing osteogenesis in 2D and 3D culture conditions. Int J Mol Sci. 2021. doi:10.3390/ijms22157939. [22] TORTELLI F, PUJIC N, LIU Y, et al. Osteoblast and osteoclast differentiation in an in vitro three-dimensional model of bone .Tissue engineering Part A. 2009;15(9):2373-2383. [23] CUI X, BREITENKAMP K, LOTZ M, et al. Synergistic action of fibroblast growth factor-2 and transforming growth factor-beta1 enhances bioprinted human neocartilage formation. Biotechnol Bioeng. 2012; 109(9):2357-2368. [24] LIN RZ, CHANG HY. Recent advances in three-dimensional multicellular spheroid culture for biomedical research. Biotechnol J. 2008;3(9-10): 1172-1184. [25] 何云影,李玲婕,张舒淇,等.聚丙烯酸/琼脂糖三维培养构建细胞球的方法[J].中国组织工程研究,2022,26(4):553-559. [26] GURUMURTHY B, BIERDEMAN PC, JANORKAR AV. Spheroid model for functional osteogenic evaluation of human adipose derived stem cells. J Biomed Mater Res A. 2017;105(4):1230-1236. [27] RUMINSKI S, KALASZCZYNSKA I, DLUGOSZ A, et al. Osteogenic differentiation of human adipose-derived stem cells in 3D conditions - comparison of spheroids and polystyrene scaffolds. Eur Cell Mater. 2019;37:382-401. [28] KIM J, ADACHI T. Cell condensation triggers the differentiation of osteoblast precursor cells to osteocyte-like cells. Front Bioeng Biotechnol. 2019;7:288. [29] MA Y, LIN M, HUANG G, et al. 3D spatiotemporal mechanical microenvironment: a hydrogel-based platform for guiding stem cell fate. Adv Mater. 2018;30(49):e1705911. [30] TROJANI C, WEISS P, MICHIELS JF, et al. Three-dimensional culture and differentiation of human osteogenic cells in an injectable hydroxypropylmethylcellulose hydrogel. Biomaterials. 2005;26(27): 5509-5517. [31] QIAO Y, LIU X, ZHOU X, et al. Gelatin templated polypeptide co-cross-linked hydrogel for bone regeneration. Adv Healthc Mater. 2020;9(1): e1901239. [32] LI D, ZHOU J, ZHANG M, et al. Long-term delivery of alendronate through an injectable tetra-PEG hydrogel to promote osteoporosis therapy. Biomater Sci. 2020;8(11):3138-3146. [33] NAFEE N, ZEWAIL M, BORAIE N. Alendronate-loaded, biodegradable smart hydrogel: a promising injectable depot formulation for osteoporosis. J Drug Target. 2018;26(7):563-575. [34] LI XJ, VALADEZ AV, ZUO P, et al. Microfluidic 3D cell culture:potential application for tissue-based bioassays. Bioanalysis. 2012;4(12):1509-1525. [35] VAN DUINEN V, TRIETSCH SJ, JOORE J, et al. Microfluidic 3D cell culture: from tools to tissue models. Curr Opin Biotechnol. 2015; 35:118-126. [36] KNOWLTON S, YU CH, ERSOY F, et al. 3D-printed microfluidic chips with patterned, cell-laden hydrogel constructs. Biofabrication. 2016; 8(2):025019. [37] ZUO Y, HE X, YANG Y, et al. Microfluidic-based generation of functional microfibers for biomimetic complex tissue construction. Acta Biomater. 2016;38:153-162. [38] AN C, LIU W, ZHANG Y, et al. Continuous microfluidic encapsulation of single mesenchymal stem cells using alginate microgels as injectable fillers for bone regeneration. Acta Biomater. 2020;111:181-196. [39] LIN Z, LI Z, LI E N, et al. Osteochondral tissue chip derived from iPSCs: modeling OA pathologies and testing drugs. Front Bioeng Biotechnol. 2019;7:411. [40] HOSPODIUK M, DEY M, SOSNOSKI D, et al. The bioink: a comprehensive review on bioprintable materials. Biotechnol Adv. 2017;35(2):217-239. [41] BYAMBAA B, ANNABI N, YUE K, et al. Bioprinted osteogenic and vasculogenic patterns for engineering 3D bone tissue. Adv Healthc Mater. 2017. doi:10.1002/adhm. 201700015. [42] BREATHWAITE E, WEAVER J, ODANGA J, et al. 3D bioprinted osteogenic tissue models for in vitro drug screening. Molecules. 2020. doi:10.3390/molecules25153442. [43] LI Y C, ZHANG YS, AKPEK A, et al. 4D bioprinting:the next-generation technology for biofabrication enabled by stimuli-responsive materials. Biofabrication. 2016;9(1):012001. [44] 高彤,丁冠守,苏萍萍,等.药物筛选模型的研究进展[J].海峡药学, 2021,33(7):1-5. [45] HAMEED A, BRADY JJ, DOWLING P, et al. Bone disease in multiple myeloma: pathophysiology and management.Cancer Growth Metastasis. 2014;7:33-42. [46] BELLONI D, HELTAI S, PONZONI M, et al. Modeling multiple myeloma-bone marrow interactions and response to drugs in a 3D surrogate microenvironment. Haematologica. 2018;103(4):707-716. [47] MONTEIRO CF, CUSTODIO CA, MANO JF. Bioengineering a humanized 3D tri-culture osteosarcoma model to assess tumor invasiveness and therapy response. Acta Biomater. 2021;134:204-214. [48] RIMANN M, LATERNSER S, GVOZDENOVIC A, et al. An in vitro osteosarcoma 3D microtissue model for drug development. J Biotechnol. 2014;189:129-135. [49] CORTES I, MATSUI R AM, AZEVEDO MS, et al. A scaffold- and serum-free method to mimic human stable cartilage validated by secretome. Tissue Eng Part A. 2021;27(5-6):311-327. [50] LOTZ MK, CARAMES B. Autophagy and cartilage homeostasis mechanisms in joint health, aging and OA. Nat Rev Rheumatol. 2011; 7(10):579-587. [51] DIEKMAN BO, SESSIONS GA, COLLINS J A, et al. Expression of p16(INK) (4a) is a biomarker of chondrocyte aging but does not cause osteoarthritis. Aging Cell. 2018;17(4):e12771. [52] ROSSER J, BACHMANN B, JORDAN C, et al. Microfluidic nutrient gradient-based three-dimensional chondrocyte culture-on-a-chip as an in vitro equine arthritis model. Mater Today Bio. 2019;4:100023. [53] SAMAVEDI S, DIAZ-RODRIGUEZ P, ERNDT-MARINO JD, et al. A three-dimensional chondrocyte-macrophage coculture system to probe inflammation in experimental osteoarthritis. Tissue Eng Part A. 2017; 23(3-4):101-114. [54] REID IR. A broader strategy for osteoporosis interventions. Nat Rev Endocrinol. 2020;16(6):333-339. [55] CHEN LR, KO NY, CHEN KH. Medical treatment for osteoporosis: from molecular to clinical opinions. Int J Mol Sci. 2019. doi:10.3390/ijms20092213. [56] ZHENG Z, YU C, WEI H. Injectable hydrogels as three-dimensional network reservoirs for osteoporosis treatment. Tissue Eng Part B Rev. 2021;27(5):430-454. [57] 林建立,蔡敏,林庆明,等. 微流控芯片关键技术及其在骨质疏松症和糖尿病发病机制研究的应用[Z].福建省立医院.2017. [58] ZHAO R, CHEN S, ZHAO W, et al. A bioceramic scaffold composed of strontium-doped three-dimensional hydroxyapatite whiskers for enhanced bone regeneration in osteoporotic defects. Theranostics. 2020;10(4):1572-1589. [59] KAMEL R, EL-WAKIL NA, ABDELKHALEK AA, et al. Nanofibrillated cellulose/cyclodextrin based 3D scaffolds loaded with raloxifene hydrochloride for bone regeneration. Int J Biol Macromol. 2020;156: 704-716. [60] 李利青,张逢,彭馥芝,等.类风湿关节炎实验性动物模型研究进展[J].中国药理学通报,2021,37(11):1492-1497. [61] PECK Y, LEOM LT, LOW PFP, et al. Establishment of an in vitro three-dimensional model for cartilage damage in rheumatoid arthritis. J Tissue Eng Regen Med. 2018;12(1): e237-e249. [62] AGOSTINI SBN, MALTA IHS, RODRIGUES RF, et al. Preclinical evaluation of methotrexate-loaded polyelectrolyte complexes and thermosensitive hydrogels as treatment for rheumatoid arthritis. Eur J Pharm Sci. 2021; 163:105856. |
| [1] | Sun Kexin, Zeng Jinshi, Li Jia, Jiang Haiyue, Liu Xia. Mechanical stimulation enhances matrix formation of three-dimensional bioprinted cartilage constructs [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-7. |
| [2] | Nong Fuxiang, Jiang Zhixiong, Li Yinghao, Xu Wencong, Shi Zhilan, Luo Hui, Zhang Qinglang, Zhong Shuang, Tang Meiwen. Bone cement augmented proximal femoral nail antirotation for type A3.3 intertrochanteric femoral fracturalysis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-10. |
| [3] | Pan Zhongjie, Qin Zhihong, Zheng Tiejun, Ding Xiaofei, Liao Shijie. Targeting of non-coding RNAs in the pathogenesis of the osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1441-1447. |
| [4] | Cai Zhihao, Xie Zhaoyong. Femoral neck anteversion measurement assessment: how to establish a unified method and standard [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1448-1454. |
| [5] | Dang Yi, Du Chengyan, Yao Honglin, Yuan Nenghua, Cao Jin, Xiong Shan, Zhang Dingmei, Wang Xin. Hormonal osteonecrosis and oxidative stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1469-1476. |
| [6] | Nie Chenchen, Su Kaiqi, Gao Jing, Fan Yongfu, Ruan Xiaodi, Yuan Jie, Duan Zhaoyuan, Feng Xiaodong. The regulatory role of circular RNAs in cerebral ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1286-1291. |
| [7] | Gao Yu, Han Jiahui, Ge Xin. Immunoinflammatory microenvironment after spinal cord ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1300-1305. |
| [8] | Wu Chuang, Muhetaer · Kelimu, Maimaitili · Aisha, Yang Hang. Influence of blood components on blood flow characteristics of individualized communicating aneurysm [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1219-1223. |
| [9] | Wang Ji, Zhang Min, Yang Zhongya, Zhang Long. A review of physical activity intervention in type 2 diabetes mellitus with sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1272-1277. |
| [10] | Liu Xiaolin, Mu Xinyue, Ma Ziyu, Liu Shutai, Wang Wenlong, Han Xiaoqian, Dong Zhiheng. Effect of hydrogel-loaded simvastatin microspheres on osteoblast proliferation and differentiation [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 998-1003. |
| [11] | Xu Xingxing, Wen Chaoju, Meng Maohua, Wang Qinying, Chen Jingqiao, Dong Qiang. Carbon nanomaterials in oral implant [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1062-1070. |
| [12] | Yang Yitian, Wang Lu, Yao Wei, Zhao Bin. Application of the interaction between biological scaffolds and macrophages in bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1071-1079. |
| [13] | Li Cheng, Zheng Guoshuang, Kuai Xiandong, Yu Weiting. Alginate scaffold in articular cartilage repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1080-1088. |
| [14] | Xu Cong, Zhao He, Sun Yan. Regeneration of facial nerve injury repaired by biomaterial nerve conduits [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1089-1095. |
| [15] | Chen Shisong, Liu Xiaohong, Xu Zhiyun. Current status and prospects of bioprosthetic heart valves [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1096-1102. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||