Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (16): 2548-2555.doi: 10.12307/2023.173
Previous Articles Next Articles
Application of injectable hydrogel in spinal cord injury
Tao Jingwei, Fan Xiao, Jiang Shengyuan, Deng Bowen, Zhang Yaqi, Liu Gang, Zuo Xinwei, Zhou Zhuoluo, Zhao Yi, Ren Jingpei, Xu Lin, Mu Xiaohong
- Dongzhimen Hospital, Beijing University of Chinese Medicine, Beijing 100700, China
-
Received:2022-03-21Accepted:2022-05-21Online:2023-06-08Published:2022-11-11 -
Contact:Mu Xiaohong, MD, Professor, Chief physician, Doctoral supervisor, Dongzhimen Hospital, Beijing University of Chinese Medicine, Beijing 100700, China -
About author:Tao Jingwei, Doctoral candidate, Dongzhimen Hospital, Beijing University of Chinese Medicine, Beijing 100700, China -
Supported by:National Natural Science Foundation of China (General Program), No. 81874467 (to MXH)
CLC Number:
Cite this article
Tao Jingwei, Fan Xiao, Jiang Shengyuan, Deng Bowen, Zhang Yaqi, Liu Gang, Zuo Xinwei, Zhou Zhuoluo, Zhao Yi, Ren Jingpei, Xu Lin, Mu Xiaohong. Application of injectable hydrogel in spinal cord injury[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(16): 2548-2555.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
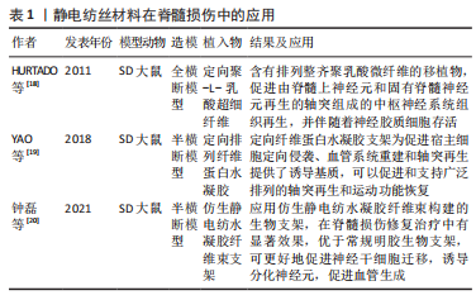
2.1 可注射水凝胶的理化特性研究 2.1.1 生物材料的应用 传统的手术治疗通常需要一个较大的切口,具有内在感染风险、患者疼痛、住院时间长、恢复时间长以及医疗系统的高昂成本等缺陷。人们已经广泛地研究和提出了生物材料,如纳米颗粒、智能水凝胶、可注射脂质微管、自组装肽、自组装纳米纤维等[16-17]。静电纺丝是利用聚合物发射源和接地集电极之间的大电压梯度,从聚合物溶液或熔体中拉出含有微米和纳米直径纤维支架的过程。在中枢神经系统中,高度排列的电纺纤维能够模仿有髓轴突白质束的排列结构。HURTADO等[18]在脊髓损伤动物模型中发现,具有高度排列的电纺纤维的支架实现了更强劲的、定向的轴突再生。静电纺丝已经成为一种强大的工具,可以创建具有高表面积/体积比的纤维结构,可以很容易地进行修改,将干细胞、药物或基因治疗输送到局部再生组织环境中。有研究将超顺磁性纳米氧化铁掺入到聚乳酸纤维中,制备了电纺纤维复合材料。YAO等[19]通过静电纺丝和同步分子自组装过程制备了具有定向形貌和柔软硬度的三维分层排列纤维蛋白水凝胶,通过将纤维蛋白水凝胶植入半横断脊髓损伤模型大鼠观察脊髓修复情况。磁控电纺纤维将引导轴突沿着纤维蛋白或胶原水凝胶中定向纤维的方向生长,促进神经轴突再生和损伤修复[20]。但是电仿纤维材料多为预成型的植入物,其研究多采用全切或半切模型,与临床中的挤压伤钝挫伤差异较大,植入过程也容易造成较大的二次损伤。静电纺丝材料在脊髓损伤研究中的应用,见表1。"

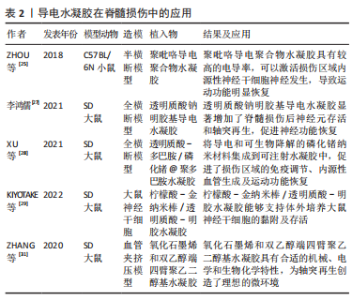
并且,可注射水凝胶材料允许微创植入并具有形状多功能性,能够通过注射的方式植入损伤部位,并通过原位交联在损伤部位形成符合缺损轮廓的不规则形状;它们可以重复注射,直到形成完整的功能组织。其中多数材料能够与黏附配体、生长因子、酶和抗炎分子结合,以实现细胞的附着、更新、萌芽和细胞外基质的再生[22]。可注射水凝胶是在损伤区域注射相对低黏度的聚合物溶液,通过自身凝胶化的过程实现填补损伤区域、生物支架、携带细胞及生物大分子等功能[23]。可注射水凝胶材料凝胶化的速度至关重要,凝胶速度不宜过快,使注射完成并充分填充缺损部位;凝胶速度也不应过慢,防止水凝胶流出病变部位。通常根据聚合物类型、其相对分子质量、浓度和交联类型,通过化学或物理交联等方式来调整凝胶速率,如紫外线、pH值、温度变化等[24]。 然而,关于可注射水凝胶材料的使用已经报道了几个问题:注射的材料可能形成内源性沉积,造成组织再生障碍;材料的过度膨胀可能增加局部压力,导致对实质的二次损害等。可注射水凝胶材料在脊髓损伤治疗研究中仍有问题有待解决。 2.1.3 具有导电性能的可注射水凝胶 生物电刺激维持着神经系统的生物功能,如肌肉收缩和信号传导。神经信号传导的关键部分是突触产生的动作电位,通过化学信号或电信号实现神经元之间的信号传导通信,其机制与神经细胞膜去极化释放钙离子有关。神经纤维束的损伤会导致信号传导受阻,抑制神经细胞的增殖和迁移。适当的电导率有利于神经元生长,电导率为1-10 S/m时能够观察到更好的轴突再生长度、轴突生长速率和轴突再髓鞘的形成[25]。导电性水凝胶在修复心肌、骨骼肌和神经等电活性生物组织方面具有广阔的应用前景,因为导电水凝胶基质可以改善相邻细胞之间的电信号传导,从而促进组织运动和感觉信号的重建[26-27]。用于构建导电水凝胶的导电纳米材料包括聚苯胺和聚吡咯等共轭聚合物、石墨烯和碳纳米管等碳基纳米材料及金纳米线等金属纳米材料,但是导电生物材料的应用也面临着挑战:①导电复合材料的导电性低。多数组织工程材料都是绝缘体,导电复合材料多是由生物材料与导电元件(如例如碳基结构、导电聚合物、金属基颗粒等)相结合构成的,故导电性能较弱。②大多数导电成分具有细胞毒性。一些导电生物材料难以降解,代谢残留的导电颗粒及表面活性剂具有一定的细胞毒性。③大多数导电生物材料是预制的支架。预先形成的固相生物支架需要以外科手术的方式植入损伤部位,这与临床常见的钝挫伤所致脊髓损伤不相符,且外科手术常造成较大的创伤及二次损伤。而可注射导电水凝胶材料的应用给脊髓损伤带来新的治疗方向。 XU等[28]研究探索了一种基于导电和可生物降解的磷化锗纳米片与黏附性透明质酸-多巴胺水凝胶基质的可注射水凝胶,将聚多巴胺修饰的磷化锗纳米片引入透明质酸-多巴胺水凝胶基质中,显著提高了透明质酸-多巴胺/磷化锗@聚多巴胺水凝胶水凝胶的电导率;体外实验发现,透明质酸-多巴胺/磷化锗@聚多巴胺导电水凝胶可促进神经干细胞向神经元分化;在大鼠脊髓全横断模型中发现,植入透明质酸-多巴胺/磷化锗@聚多巴胺导电水凝胶可显著促进运动功能的恢复。该导电材料能够降解,减少了生物材料的残留与细胞毒性,有效解决了生物材料残留的弊端,但是在他们的研究中并未涉及电生理实验,该材料植入后对神经传导的改善尚未可知。KIYOTAKE 等[29]将高长径比柠檬酸-金纳米棒引入透明质酸-明胶水凝胶中,制备了一种导电水凝胶,通过将高长径比柠檬酸-金纳米棒的强键合成与间接配体交换相结合,将细胞毒性表面活性剂交换为无毒的柠檬酸盐,从而减少该材料的细胞毒性。PALZA等[30]认为将导电生物材料与电刺激相结合,能更好地将电信号直接输送到神经元,同时促进轴突再生和神经可塑性,增强功能恢复;而组织再生后的电刺激能够促进脊髓网络与再生轴突的重组,从而促进神经信号传导的重建。ZHANG等[31]报道了一种新型的超分子水凝胶来修复损伤脊髓,这种水凝胶是由氧化石墨烯薄片与四臂聚乙二醇交联而成,聚乙二醇由消炎药双乙酸乙酯官能化,游离双乙醇胺分子提供了一个可持续的抗炎环境;双乙醇胺和氧化石墨烯之间的非共价π-π堆积和疏水相互作用是动态的,使得水凝胶可注射和自我恢复。该水凝胶可以抑制星形胶质细胞的过度激活和炎症,促进脊髓损伤的修复。虽然氧化石墨烯的特性赋予了水凝胶高电导率,但是氧化石墨烯材料可能会降低水凝胶材料的生物降解性能,增加水凝胶产生细胞毒性和残留的风险。导电水凝胶在脊髓损伤中的的应用,见表2。"

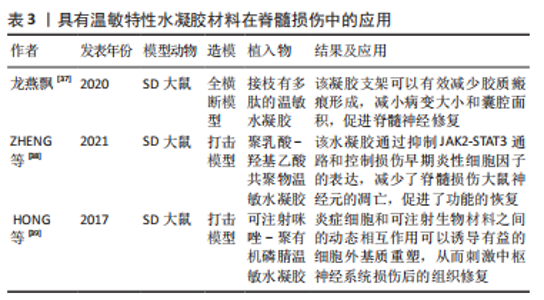
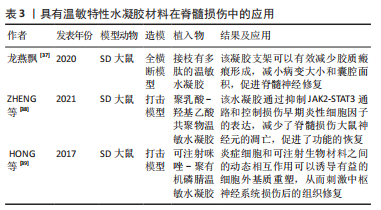
2.1.4 具有温敏特性的可注射水凝胶材料 温敏水凝胶是一种特殊的可注射水凝胶,这种生物材料在温度的刺激下通过物理交互作用而变为凝胶态。这种交联机制与溶液的临界温度有关,在接近临界温度时,亲水性聚合物会大量失水,形成以疏水相互作用为主的凝胶[32]。 目前研究较广泛的天然温敏性水凝胶是琼脂糖和纤维素衍生物,如甲基纤维素和一些以聚丙烯酰胺为基础的合成聚合物[33]。MASSENSINI等[34]研发了一种温敏水凝胶材料,在室温下该材料为液态,储能模数为0.000 1 kPa;当温度升高至37 ℃时,5 min后该材料转化为固体水凝胶,储能模数为0.01-0.5 kPa,并具有较好的生物相容性。透明质酸在细胞外基质中的含量很高,中枢神经系统细胞外基质中透明质酸约占25%。透明质酸是一种含有D-葡萄糖醛酸和D-N-乙酰葡萄糖胺的非硫酸化糖胺聚糖,具有可降解性、化学和机械可持续性、低免疫反应和高血管生成潜力等积极特征[35]。天然细胞外基质中的透明质酸纤维能够通过提供导致干细胞增殖和分化的物理路径,来引导神经细胞在大脑中的迁移。AVAL等[36]制备一种温敏性透明质酸多肽互穿网络,该材料将温敏性透明质酸与聚N-异丙基丙烯酰胺反应合成了热敏性透明质;然后,将透明质酸自组装肽与热敏性透明质酸结合,制备了一系列可注射的温敏性多肽互穿网络,该水凝胶互穿聚合物网络在生理温度下成功形成水凝胶;流变学测量表明水凝胶是弹性的,弹性模数约为500 Pa,与脑组织的弹性相似,有利于神经组织的再生和修复。 龙燕飘[37]制备了一种接枝有多肽的温敏水凝胶,低黏度的水凝胶溶液能够通过注射器在损伤局部原位注射,由于温度的变化进行原位交联,增加黏度,从而形成匹配缺损部位的凝胶;通过观察全横断脊髓损伤大鼠术后2周运动功能评分的变化,评估生物材料的性能。ZHENG等[38]将聚乳酸-聚乙二醇-聚乳酸制备成可注射温敏水凝胶材料,该材料在35 ℃时转化为凝胶,在3 d内可达到80%的降解率;聚乳酸-聚乙二醇-聚乳酸的凝胶温度强烈地依赖其质量分数,当凝胶质量分数为20%时,加热至37 ℃水凝胶由溶胶变为凝胶,当温度降至室温22 ℃时,水凝胶由凝胶转变为溶胶;他们将JAK2/STAT3通路抑制剂巴利替尼与生物材料相结合,较好地阐明了载药生物材料的分子生物学机制及对脊髓损伤大鼠的功能改善。HONG等[39]利用注射咪唑-聚(有机磷腈)水凝胶(一种具有温度敏感的溶胶-凝胶转变行为的水凝胶)干预打击脊髓损伤大鼠模型,发现大鼠纤维化细胞外基质内巨噬细胞表达的基质金属蛋白酶9减少,脊髓空洞囊腔变小,有利于运动功能的恢复。虽然上述温敏水凝胶的凝胶温度接近人体体温,能表现出较好的温敏特性,但是凝胶时间多在5-20 min,凝胶时间较长,无法保证水凝胶注射后的凝胶范围和有效形成贴合缺损部位的不规则形态能力。温敏水凝胶的研究还处于发展阶段,其随温度变化凝胶溶胶的形态转换功能已经成为未来研究的一大方向和趋势。具有温敏特性水凝胶材料在脊髓损伤中的应用,见表3。"
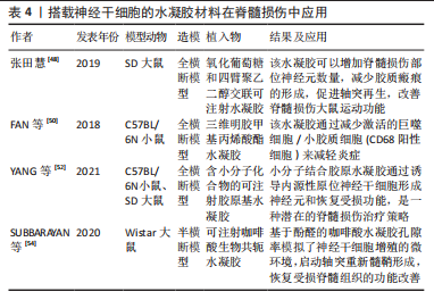
2.2 可注射水凝胶搭载生物大分子研究 2.2.1 搭载干细胞的可注射水凝胶 干细胞是一种未成熟的组织前体细胞,能够自我更新,具有形成克隆细胞群并分化为多个细胞系的能力[40],这些特殊性质对于恢复多种损伤组织功能的研究具有一定价值。目前干细胞可分为三大类:来源于早期胚胎的胚胎干细胞;诱导的多能干细胞;成体干细胞,包括造血干细胞、神经干细胞和间充质干细胞[41]。 干细胞的治疗可以归类3个关键的作用机制。第1种是“归巢”作用,干细胞由于化学梯度系统的迁移到急性损伤的中心,迁移由细胞表面受体(如趋化因子受体)介导与白细胞迁移的过程相似;第2种机制是“分化”作用,能够分化成多种细胞类型,通过局部植入增强或替换受损组织来并诱导损伤组织功能恢复;第3种主要机制是生物活性因子的“分泌”作用,这可能会潜在地影响局部和全身的生理过程[42]。 干细胞移植研究为修复受损的脊髓提供了一种潜在的有效方法。干细胞有一定的分化潜能,能够抑制脊髓损伤后神经元的缺失,促进脊髓神经轴突再生,但是干细胞移植治疗脊髓损伤也面临着一定的问题:直接移植细胞不可避免地造成损伤部位的细胞丢失[43];缺血和损伤部位的微环境会导致干细胞死亡或濒临死亡,从而破坏局部微环境并影响治疗效果[44];移植的干细胞向其成熟表型(包括神经元、星形胶质细胞和少突胶质细胞)的分化不受控制,容易造成畸胎瘤的形成[45]。 (1)搭载神经干细胞并促进神经干细胞定向分化:神经干细胞是一组多能、自我更新的细胞,能够产生神经谱系细胞,包括神经元、星形胶质细胞和少突胶质细胞。神经干细胞也存在于成人脊髓中,可以在体外增殖[46]。损伤后,神经干细胞可以从静止状态被直接激活,因此,诱导神经干细胞定向分化有望成为治疗脊髓损伤的新手段[47-48]。 TSENG等[49]研究发现组织工程材料的力学特性能够影响神经干细胞的存活和定向分化,神经干细胞在模量很低(< 0.1 kPa)或很高(> 100 kPa)的材料中不能很好地存活,而在软质支架(≈0.1?1 kPa)中更容易分化为神经元;神经干细胞在稍硬的材料(≈7?10 kPa)中更容易分化为星形胶质细胞。 FAN等[50]将三维明胶甲基丙烯酸酯水凝胶与神经干细胞结合起来,通过注射植入小鼠全横断脊髓损伤模型,观察小鼠脊髓损伤后神经功能恢复情况,发现三维水凝胶的力学性能易于控制,且与神经组织具有相似的特性,从而能够促进细胞存活和控制细胞分化;组织学分析显示,三维明胶甲基丙烯酸酯水凝胶与神经干细胞结合组空洞面积明显缩小,胶原沉积减少;此外,三维明胶甲基丙烯酸酯水凝胶和神经干细胞联合移植通过减少活化的巨噬细胞/小胶质细胞来减轻炎症,促进轴突再生。该研究说明了三维明胶甲基丙烯酸酯水凝胶能够为神经干细胞生长和分化提供更好的组织微环境,减少移植后干细胞的凋亡和丢失,对于促进干细胞定向分化的问题并未解决。 内源性神经干细胞在脊髓损伤病理条件下通常分化为星形胶质细胞[51]。YANG等[52]发现一些小分子物质可以诱导神经干细胞定向分化为神经元,参与脊髓损伤的修复,他们筛选了LDN193189、SB431542、CHIR99021和P7C3-A20四个小分子的组合,它们可以促进小鼠和大鼠脊髓神经干细胞的神经元分化;此外,通过负载小分子可注射胶原基水凝胶的干预,诱导全横断脊髓损伤小鼠损伤部位内源性神经干细胞向神经元定向分化,抑制内源性神经干细胞的星形胶质细胞形成,抑制胶质瘢痕,促进神经再生。他们通过搭载小分子化合物促进损伤部位内源性神经干细胞的定向分化,在一定程度上解决了干细胞移植后的无序分化问题,但是脊髓损伤后局部内源性神经干细胞存活和分化能力有限,通过小分子组合外源性神经干细胞的研究还有待开展。 LUO等[53]发现牙髓干细胞来源于神经细胞谱系,它保留了分化为神经元的能力,具有免疫调节剂的作用,并且表达多种适合轴突修复的因子,刺激血管形成,促进受损神经的再生和修复。并且人牙髓神经源干细胞是一种很好的干细胞来源,人牙龈源神经干细胞可以在不影响健康的情况下获得,而且移植的干细胞可以分化为神经细胞,恢复受损脊髓组织的运动功能。SUBBARAYAN等[54]将人牙龈源性神经干细胞移植到可注射咖啡酸生物共轭水凝胶中,通过体内生物发光成像系统发现该水凝胶移植有助于修复空洞,促进移植物在损伤脊髓组织中的植入和神经再生。这种水凝胶还能够调节免疫反应、抑制炎症反应,通过观察发现植入水凝胶后,免疫调节因子白细胞介素6、肿瘤坏死因子α、中性粒细胞弹性蛋白酶降低,白细胞介素10升高。通过不同来源的神经干细胞移植,能够发挥不同的干细胞分化能力,但是不同来源神经干细胞异质性又会产生干细胞在损伤部位存活能力等新问题。搭载神经干细胞的水凝胶材料在脊髓损伤中应用,见表4。"


(2)搭载间充质干细胞并促进间充质干细胞的旁分泌作用:骨髓间充质干细胞是一种类似成纤维细胞的群体,能够分泌与造血和其他组织再生过程相关的生长因子和细胞因子。早期的研究将植入骨髓间充质干细胞的治疗效果归因于它们的分化能力[55-56]。然而,骨髓间充质干细胞的植入时间通常太短,不能产生有效的治疗作用,药物干预后小于1%的干细胞存活超过1周,这表明骨髓间充质干细胞的主要作用可能是由旁分泌机制介导的[57]。最近的研究也引起了人们对骨髓间充质干细胞产生的广泛生物活性因子的关注,骨髓间充质干细胞分泌多种生长因子、趋化因子、细胞因子和胞外囊泡,作为信号分子的载体,调节细胞间和细胞外基质之间的信号传导,这些因子可能在多种生理过程的调节中发挥重要作用[58-59]。 BOIDO等[60]利用壳聚糖水凝胶作为骨髓间充质干细胞的载体,制备了一种可注射、高渗透性的壳聚糖基水凝胶,壳聚糖既具有良好的生物相容性,保证了间充质干细胞存活的良好环境,又能够提供抗炎和抗氧化环境。将骨髓间充质干细胞与水凝胶溶液混合的生物材料能够在0-37 ℃温度范围内迅速凝胶化,壳聚糖水凝胶不影响间充质干细胞活性,还能促进间充质干细胞的旁分泌作用,释放细胞外囊泡,限制胶质瘢痕的形成,减少损伤部位的细胞死亡。该研究中的生物材料以搭载间充质干细胞为主,虽然促进了细胞存活,但是通过促进间充质干细胞的旁分泌作用释放的细胞外囊泡仍然较少,相较于直接搭载间充质干细胞胞外囊泡还有所不足。 胞外囊泡是旁分泌的主要形式,可以通过将含有mRNAs、miRNAs和蛋白质的囊泡转移到靶细胞来调节细胞间的交互作用。近年来,细胞外囊泡已被证实在组织再生方面具有一定的研究价值[61]。骨髓间充质干细胞通过旁分泌作用产生的细胞外囊泡,能够减轻脊髓损伤后炎症、细胞凋亡等病理反应,促进感觉和运动功能的恢复[62]。WANG等[63]运用聚柠檬酸-聚乙烯亚胺水凝胶搭载骨髓间充质干细胞来源的细胞外囊泡替代间充质干细胞移植,模拟干细胞的旁分泌功能,通过抑制纤维瘢痕形成、减少炎症反应促进髓鞘再生和轴突再生,协同发挥治疗作用。柠檬酸聚合物具有合成简便、生物相容性高、生物降解可控、成本低等优点,在组织工程领域应用广泛。聚柠檬酸-聚乙二醇-聚乙烯亚胺具有良好的生物相容性,还可以促进骨骼肌再生中的细胞活性[64]。但是,通过生物材料搭载细胞外囊泡模拟骨髓间充质干细胞的旁分泌作用效果是否优于骨髓间充质干细胞自身旁分泌功能还需进一步探讨。可注射水凝胶搭载间充质干细胞并促进间充质干细胞旁分泌作用的研究,见表5。"

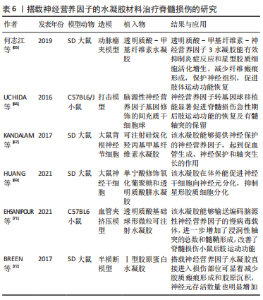
2.2.2 搭载神经营养因子的可注射水凝胶 脊髓损伤部位缺乏合适的生长刺激因子,神经元缺乏自我修复能力,常造成脊髓空洞和纤维胶质瘢痕的形成[65]。脑源性神经营养因子是神经营养因子家族的重要成员,可以通过TrkB受体发挥促进神经干细胞的增殖,提高神经轴突的生长能力,并诱导神经干细胞分化为神经元的作用[66],脑源性神经营养因子同样可以促进脊髓损伤后神经再生和运动功能的恢复。然而,脑源性神经营养因子作为一种大分子蛋白质,存在半衰期短、稳定性差、不能通过血脑屏障等缺点[66],这些因素使得使用脑源性神经营养因子维持长期活性和获得理想的药代动力学曲线变得困难。在组织工程研究中,脑源性神经营养因子可以通过物理吸附或化学结合的方式固定在水凝胶生物材料上[66],通过原位注射的方式注射在损伤部位,不涉及复杂的化学反应,也不影响脑源性神经营养因子的生物活性,从而起到治疗作用。 HUANG等[69]采用聚乳酸-羟基乙酸共聚物作为载体来包裹脑源性神经营养因子,然后用单宁酸对得到的微球进行修饰,将氧化葡聚糖和透明质酸肼组成的多糖水凝胶与单宁酸修饰的微球混合,形成搭载脑源性神经营养因子的聚乳酸-羟基乙酸共聚物/氧化葡聚糖-透明质酸肼水凝胶。他们发现该水凝胶的横截面形貌呈连续多孔结构,有利于营养物质的转运、细胞的黏附和增殖,这种水凝胶材料可以持续地输送脑源性神经营养因子用于脊髓损伤的修复,促进神经干细胞向神经元分化和神经再生,抑制星形胶质细胞分化和胶质瘢痕的形成;在水凝胶基质中加入单宁酸可以提高水凝胶的稳定性,单宁酸的引入还可以提高脑源性神经营养因子的生物活性,延长营养因子的释放时间,有利于干细胞的分化和新组织的形成。然而生物大分子或蛋白质的局部递送也面临着一些问题:随着时间的推移蛋白质会丧失其生物活性;为了达到治疗量,需要局部递送大量的生物大分子蛋白质;不同种类的生物大分子与组织工程材料的生物相容性存在一定差异,需要为不同的蛋白质分子设计定制组织工程载体[70]。EHSANIPOUR等[71]研究了利用组织工程支架作为基因载体进行局部输送的干预方法,将搭载神经营养因子的慢病毒载体由透明质酸为基础的球形微粒水凝胶材料进行原位注射和组装,实现神经营养因子的转基因输送治疗。神经营养因子3也是一种促进脊髓损伤后神经再生的生长因子,这种神经营养因子能够加强损伤轴突的再生能力,包括神经干细胞的分化、存活的功能。BREEN等[72]运用搭载神经营养因子3的胶原蛋白基水凝胶原位注射在脊髓损伤半切模型中,他们发现这种水凝胶具有生物相容性、可生物降解性和柔韧性,适用于脊髓损伤的修复,还能够通过减少胶质瘢痕、炎症和胶原沉积促进适宜的轴突再生环境形成,促进了神经功能恢复。神经营养因子3促进在体脊髓损伤后皮质脊髓轴突和上行感觉轴突的萌发,这有助于损伤部位近端和远端运动功能和感觉信号的恢复。不同类型神经营养因子的疗效差异还有待进一步研究。搭载神经营养因子水凝胶材料治疗脊髓损伤的研究,见表6。"

| [1] MORGADO PI, PALACIOS M, LARRAIN J. In situ injectable hydrogels for spinal cord regeneration: advances from the last 10 years. Biomed Phys Eng Express. 2019;6(1):12002. [2] JEONG HJ, YUN Y, LEE SJ, et al. Biomaterials and strategies for repairing spinal cord lesions. Neurochem Int. 2021;144:104973. [3] QI Z, ZHANG T, KONG W, et al. A dual-drug enhanced injectable hydrogel incorporated with neural stem cells for combination therapy in spinal cord injury. Chem Eng J. 2022;427:130906. [4] NIEMCZYK B, SAJKIEWICZ P, KOLBUK D. Injectable hydrogels as novel materials for central nervous system regeneration J Neural Eng. 2018; 15(5):51002. [5] 刘伟啸.超分子载药水凝胶修复脊髓损伤的实验研究[D].天津:天津医科大学,2020. [6] HLAVAC N, KASPER M, SCHMIDT CE. Progress toward finding the perfect match: hydrogels for treatment of central nervous system injury. Mater Today Adv. 2020;6:100039. [7] QURAISHE S, FORBES LH, ANDREWS MR. The Extracellular Environment of the CNS: Influence on Plasticity, Sprouting, and Axonal Regeneration after Spinal Cord Injury. Neural Plast. 2018;2018:2952386. [8] GHUMAN H, MASSENSINI AR, DONNELLY J, et al. ECM hydrogel for the treatment of stroke: Characterization of the host cell infiltrate. Biomaterials. 2016;91:166-181. [9] AVAL NA, EMADI R, VALIANI A, et al. An aligned fibrous and thermosensitive hyaluronic acid-puramatrix interpenetrating polymer network hydrogel with mechanical properties adjusted for neural tissue. J Mater Sci. 2022;57(4):2883-2896. [10] GELBARD HA. Neuroimmune Pharmacology, 2nd Edition - A Perspective. J Neuroimmune Pharmacol. 2017;12(2):211-212. [11] 陈钦润.嗅球成鞘细胞与VitroGel~(TM)3D-RGD水凝胶联合移植治疗大鼠脊髓完全横断损伤[D].蚌埠:蚌埠医学院,2021. [12] 涂雨洁.功能性自组装短肽/丝素蛋白复合纳米水凝胶促进脊髓损伤后神经再生的研究[D].广州:暨南大学,2020. [13] SUN HY, ZHANG LM, CHENG W, et al. Injectable Hydrogels in Repairing Central Nervous System Injuries. Adv Mater Sci Eng. 2021;1155: 7381980. [14] 相子千.多功能3D打印水凝胶系统的构建与修复脊髓损伤的实验研究[D].天津:天津医科大学,2020. [15] ABDULGHANI S, MITCHELL GR. Biomaterials for In Situ Tissue Regeneration: A Review. Biomolecules. 2019;9(11):750. [16] SANTI S, CORRIDORI I, PUGNO NM, et al. Injectable Scaffold-Systems for the Regeneration of Spinal Cord: Advances of the Past Decade. ACS Biomater Sci Eng. 2021;7(3):983-999. [17] 黄涛.柠檬酸交联壳聚糖神经修复支架的构建及其应用于脊髓损伤的研究[D].武汉:华中科技大学,2019. [18] HURTADO A, CREGG JM, WANG HB, et al. Robust CNS regeneration after complete spinal cord transection using aligned poly-L-lactic acid microfibers. Biomaterials. 2011;32(26):6068-6079. [19] YAO S, YU S, CAO Z, et al. Hierarchically aligned fibrin nanofiber hydrogel accelerated axonal regrowth and locomotor function recovery in rat spinal cord injury. Int J Nanomedicine. 2018;13:2883-2895. [20] 钟磊,许猛.仿生静电纺水凝胶纤维束支架在脊髓损伤修复中的效果研究[Z].2021.11,6-7. [21] 刘坤.壳聚糖水凝胶的研制及其改性研究[D].武汉:武汉理工大学,2019. [22] BELLOTTI E, SCHILLING AL, LITTLE SR, et al. Injectable thermoresponsive hydrogels as drug delivery system for the treatment of central nervous system disorders: A review. J Control Release. 2021;329:16-35. [23] CHEN S, LIU S, ZHANG L, et al. Construction of injectable silk fibroin/polydopamine hydrogel for treatment of spinal cord injury. Chem Eng J. 2020;399:125795. [24] 许盼盼.神经干细胞与骨髓间充质干细胞共培养结合光敏型水凝胶用于脊髓损伤修复的研究[D].蚌埠:蚌埠医学院,2021. [25] ZHOU L, FAN L, YI X, et al. Soft Conducting Polymer Hydrogels Cross-Linked and Doped by Tannic Acid for Spinal Cord Injury Repair. ACS Nano. 2018;12(11):10957-10967. [26] WILLETT NJ, BONINGER ML, MILLER LJ, et al. Taking the Next Steps in Regenerative Rehabilitation: Establishment of a New Interdisciplinary Field. Arch Phys Med Rehabil. 2020;101(5):917-923. [27] 李鸿儒.负载神经干细胞和多奈哌齐的导电水凝胶系统对脊髓损伤修复作用研究[D].长春:吉林大学,2021. [28] XU C, CHANG Y, WU P, et al. Two‐Dimensional‐Germanium Phosphide‐Reinforced Conductive and Biodegradable Hydrogel Scaffolds Enhance Spinal Cord Injury Repair. Adv Funct Mater. 2021;31(41):2104440. [29] KIYOTAKE EA, THOMAS EE, HOMBURG HB, et al. Conductive and injectable hyaluronic acid/gelatin/gold nanorod hydrogels for enhanced surgical translation and bioprinting. J Biomedater Res A. 2022;110(2): 365-382. [30] PALZA H, ZAPATA PA, ANGULO-PINEDA C. Electroactive Smart Polymers for Biomedical Applications Materials (Basel). 2019;12(2):277. [31] ZHANG K, LI J, JIN J, et al. Injectable, anti-inflammatory and conductive hydrogels based on graphene oxide and diacerein-terminated four-armed polyethylene glycol for spinal cord injury repair. Mater Design. 2020;196:109092. [32] XU Y, LI Z, LI X, et al. Regulating myogenic differentiation of mesenchymal stem cells using thermosensitive hydrogels. Acta Biomater. 2015;26:23-33. [33] HAQ MA, SU Y, WANG D. Mechanical properties of PNIPAM based hydrogels: A review. Mater Sci Eng C Mater Biol Appl. 2017;70(Pt 1): 842-855. [34] MASSENSINI AR, GHUMAN H, SALDIN LT, et al. Concentration-dependent rheological properties of ECM hydrogel for intracerebral delivery to a stroke cavity. Acta Biomater. 2015;27:116-130. [35] JENSEN G, HOLLOWAY JL, STABENFELDT SE. Hyaluronic Acid Biomaterials for Central Nervous System Regenerative Medicine. Cells. 2020;9(9):2113. [36] AVAL NA, EMADI R, VALIANI A, et al. An aligned fibrous and thermosensitive hyaluronic acid-puramatrix interpenetrating polymer network hydrogel with mechanical properties adjusted for neural tissue. J Mater Sci. 2022;57(4):2883-2896. [37] 龙燕飘.含肽温敏性水凝胶用于脊髓损伤修复的研究[D]. 武汉:武汉理工大学,2020. [38] ZHENG XQ, HUANG JF, LIN JL, et al. Controlled release of baricitinib from a thermos-responsive hydrogel system inhibits inflammation by suppressing JAK2/STAT3 pathway in acute spinal cord injury. Colloids Surf B Biointerfaces. 2021;199:111532. [39] HONG L, KIM YM, PARK HH, et al. An injectable hydrogel enhances tissue repair after spinal cord injury by promoting extracellular matrix remodeling. Nat Commun. 2017;8(1):533. [40] NAMESTNIKOVA DD, GUBSKIY IL, REVKOVA VA, et al. Intra-Arterial Stem Cell Transplantation in Experimental Stroke in Rats: Real-Time MR Visualization of Transplanted Cells Starting With Their First Pass Through the Brain With Regard to the Therapeutic Action. Front Neurosci. 2021;15:641970. [41] DOCHEVA D, POPOV C, MUTSCHLER W, et al. Human mesenchymal stem cells in contact with their environment: surface characteristics and the integrin system. J Cell Mol Med. 2007;11(1):21-38. [42] TEO GS, ANKRUM JA, MARTINELLI R, et al. Mesenchymal stem cells transmigrate between and directly through tumor necrosis factor-alpha-activated endothelial cells via both leukocyte-like and novel mechanisms. Stem Cells. 2012;30(11):2472-2486. [43] FUHRMANN T, TAM RY, BALLARIN B, et al. Injectable hydrogel promotes early survival of induced pluripotent stem cell-derived oligodendrocytes and attenuates longterm teratoma formation in a spinal cord injury model. Biomaterials. 2016;83:23-36. [44] BROGUIERE N, ISENMANN L, ZENOBI-WONG M. Novel enzymatically cross-linked hyaluronan hydrogels support the formation of 3D neuronal networks. Biomaterials. 2016;99:47-55. [45] MORITA R, SANZEN N, SASAKI H, et al. Tracing the origin of hair follicle stem cells. Nature. 2021;594(7864):547-552. [46] BARKER RA, GOTZ M, PARMAR M. New approaches for brain repair-from rescue to reprogramming. Nature. 2018;557(7705):329-334. [47] 李洋.3D打印构建新型药物传递系统的研究[D].镇江:江苏大学, 2020. [48] 张田慧.活性氧响应性高分子材料和多功能可注射水凝胶用于脊髓损伤治疗[D].合肥:中国科学技术大学,2019. [49] TSENG TC, TAO L, HSIEH FY, et al. An Injectable, Self-Healing Hydrogel to Repair the Central Nervous System. Adv Mater. 2015;27(23): 3518-3524. [50] FAN L, LIU C, CHEN X, et al. Directing Induced Pluripotent Stem Cell Derived Neural Stem Cell Fate with a Three-Dimensional Biomimetic Hydrogel for Spinal Cord Injury Repair. ACS Appl Mater Inter. 2018; 10(21):17742-17755. [51] LI X, FLORIDDIA EM, TOSKAS K, et al. Regenerative Potential of Ependymal Cells for Spinal Cord Injuries Over Time. EBioMedicine. 2016;13:55-65. [52] YANG Y, FAN Y, ZHANG H, et al. Small molecules combined with collagen hydrogel direct neurogenesis and migration of neural stem cells after spinal cord injury. Biomaterials. 2021;269:120479. [53] LUO L, HE Y, WANG X, et al. Potential Roles of Dental Pulp Stem Cells in Neural Regeneration and Repair. Stem Cells Int. 2018;2018:1731289. [54] SUBBARAYAN R, BARATHIDASAN R, RAJA S, et al. Human gingival derived neuronal cells in the optimized caffeic acid hydrogel for hemitransection spinal cord injury model. J Cell Biochem. 2020;121(3): 2077-2088. [55] HSU YC, WU YT, YU TH, et al. Mitochondria in mesenchymal stem cell biology and cell therapy: From cellular differentiation to mitochondrial transfer. Semin Cell Dev Biol. 2016;52:119-131. [56] 赵宣淇,张钰,秦川,等.神经营养因子-3基因修饰的骨髓间充质干细胞和水凝胶联合应用对脊髓损伤模型大鼠的治疗作用研究[J].中国比较医学杂志,2020,30(7):1-12. [57] SONG YS, LEE HJ, DOO SH, et al. Mesenchymal stem cells overexpressing hepatocyte growth factor (HGF) inhibit collagen deposit and improve bladder function in rat model of bladder outlet obstruction. Cell Transplant. 2012;21(8):1641-1650. [58] VIZOSO F, EIRO N, CID S, et al. Mesenchymal Stem Cell Secretome: Toward Cell-Free Therapeutic Strategies in Regenerative Medicine. Int J Mol Sci. 2017;18(9):1852. [59] 王健豪,刘洋,付玄昊,等.3D打印组织工程支架联合骨髓间充质干细胞移植修复脊髓损伤[J].中华骨科杂志,2021,41(6):376-385. [60] BOIDO M, GHIBAUDI M, GENTILE P, et al. Chitosan-based hydrogel to support the paracrine activity of mesenchymal stem cells in spinal cord injury treatment. Sci Rep-UK. 2019;9(1):6402. [61] SUN G, LI G, LI D, et al. hucMSC derived exosomes promote functional recovery in spinal cord injury mice via attenuating inflammation. Mater Sci Eng C Mater Biol Appl. 2018;89:194-204. [62] LANKFORD KL, ARROYO EJ, NAZIMEK K, et al. Intravenously delivered mesenchymal stem cell-derived exosomes target M2-type macrophages in the injured spinal cord. PLoS One. 2018;13(1):e190358. [63] WANG C, WANG M, XIA K, et al. A bioactive injectable self-healing anti-inflammatory hydrogel with ultralong extracellular vesicles release synergistically enhances motor functional recovery of spinal cord injury. Bio Mater. 2021;6(8):2523-2534. [64] GUO Y, WANG M, GE J, et al. Bioactive biodegradable polycitrate nanoclusters enhances the myoblast differentiation and in vivo skeletal muscle regeneration via p38 MAPK signaling pathway. Bioact Mater. 2020;5(3):486-495. [65] 何志江,朱雷,程世翔,等.神经营养因子3修饰透明质酸-甲基纤维素水凝胶修复脊髓损伤大鼠神经功能的恢复[J].中国组织工程研究,2019,23(14):2202-2207. [66] UCHIDA S, HAYAKAWA K, OGATA T, et al. Treatment of spinal cord injury by an advanced cell transplantation technology using brain-derived neurotrophic factor-transfected mesenchymal stem cell spheroids. Biomaterials. 2016;109:1-11. [67] KANDALAM S, SINDJI L, DELCROIX GJ, et al. Pharmacologically active microcarriers delivering BDNF within a hydrogel: Novel strategy for human bone marrow-derived stem cells neural/neuronal differentiation guidance and therapeutic secretome enhancement. Acta Biomater. 2017;49:167-180. [68] COOK DJ, NGUYEN C, CHUN HN, et al. Hydrogel-delivered brain-derived neurotrophic factor promotes tissue repair and recovery after stroke. J Cereb Blood Flow Metab. 2017;37(3):1030-1045. [69] HUANG F, CHEN T, CHANG J, et al. A conductive dual-network hydrogel composed of oxidized dextran and hyaluronic-hydrazide as BDNF delivery systems for potential spinal cord injury repair. Int J Biol Macromol. 2021;167:434-445. [70] SHEN N, WANG L, WU Y, et al. Adeno-associated virus packaged TRPC5 gene therapy alleviated spinal cord ischemic reperfusion injury in rats. Neuroreport. 2020;31(1):29-36. [71] EHSANIPOUR A, SATHIALINGAM M, RAD LM, et al. Injectable, macroporous scaffolds for delivery of therapeutic genes to the injured spinal cord. APL Bioeng. 2021;5(1):16104. [72] BREEN BA, KRASKIEWICZ H, RONAN R, et al. Therapeutic Effect of Neurotrophin-3 Treatment in an Injectable Collagen Scaffold Following Rat Spinal Cord Hemisection Injury. ACS Bio Sci Eng. 2017;3(7):1287-1295. |
| [1] | Nong Fuxiang, Jiang Zhixiong, Li Yinghao, Xu Wencong, Shi Zhilan, Luo Hui, Zhang Qinglang, Zhong Shuang, Tang Meiwen. Bone cement augmented proximal femoral nail antirotation for type A3.3 intertrochanteric femoral fracturalysis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-10. |
| [2] | Guo Shuhui, Yang Ye, Jiang Yangyang, Xu Jianwen. Screening and validation of neurogenic bladder miRNA-mRNA regulatory network [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(在线): 1-8. |
| [3] | Pan Zhongjie, Qin Zhihong, Zheng Tiejun, Ding Xiaofei, Liao Shijie. Targeting of non-coding RNAs in the pathogenesis of the osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1441-1447. |
| [4] | Cai Zhihao, Xie Zhaoyong. Femoral neck anteversion measurement assessment: how to establish a unified method and standard [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1448-1454. |
| [5] | Dang Yi, Du Chengyan, Yao Honglin, Yuan Nenghua, Cao Jin, Xiong Shan, Zhang Dingmei, Wang Xin. Hormonal osteonecrosis and oxidative stress [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(9): 1469-1476. |
| [6] | Wang Ji, Zhang Min, Yang Zhongya, Zhang Long. A review of physical activity intervention in type 2 diabetes mellitus with sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1272-1277. |
| [7] | Nie Chenchen, Su Kaiqi, Gao Jing, Fan Yongfu, Ruan Xiaodi, Yuan Jie, Duan Zhaoyuan, Feng Xiaodong. The regulatory role of circular RNAs in cerebral ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1286-1291. |
| [8] | Gao Yu, Han Jiahui, Ge Xin. Immunoinflammatory microenvironment after spinal cord ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1300-1305. |
| [9] | Yang Jiujie, Li Zhi, Wang Shujie, Tian Ye, Zhao Wei. Intraoperative neurophysiological monitoring of functional changes following durotomy with decompression for acute spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(8): 1232-1236. |
| [10] | Xu Xingxing, Wen Chaoju, Meng Maohua, Wang Qinying, Chen Jingqiao, Dong Qiang. Carbon nanomaterials in oral implant [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1062-1070. |
| [11] | Li Cheng, Zheng Guoshuang, Kuai Xiandong, Yu Weiting. Alginate scaffold in articular cartilage repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1080-1088. |
| [12] | Chen Shisong, Liu Xiaohong, Xu Zhiyun. Current status and prospects of bioprosthetic heart valves [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1096-1102. |
| [13] | Lu Di, Zhang Cheng, Duan Rongquan, Liu Zongxiang. Osteoinductive properties of calcium phosphate ceramic bone repair materials [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1103-1109. |
| [14] | Shi Yehong, Wang Cheng, Chen Shijiu. Early thrombosis and prevention of small-diameter blood vessel prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1110-1116. |
| [15] | Tang Haotian, Liao Rongdong, Tian Jing. Application and design of piezoelectric materials for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(7): 1117-1125. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||