Chinese Journal of Tissue Engineering Research ›› 2019, Vol. 23 ›› Issue (15): 2436-2442.doi: 10.3969/j.issn.2095-4344.1157
Previous Articles Next Articles
Prospects and application of curvilinear distraction osteogenesis
Zhou Yang, Zhou Libin, Piao Zhengguo
- (Department of Maxillofacial Surgery, Affiliated Stomatology Hospital of Guangzhou Medical University, Guangzhou Institute of Oral Disease, Key Laboratory of Oral Medicine, Guangzhou 510140, Guangdong Province, China)
-
Received:2018-12-25Online:2019-05-28Published:2019-05-28 -
Contact:Zhou Libin, MD, Associate chief physician, Department of Maxillofacial Surgery, Affiliated Stomatology Hospital of Guangzhou Medical University, Guangzhou Institute of Oral Disease, Key Laboratory of Oral Medicine, Guangzhou 510140, Guangdong Province, China -
About author:Zhou Yang, Master candidate, Department of Maxillofacial Surgery, Affiliated Stomatology Hospital of Guangzhou Medical University, Guangzhou Institute of Oral Disease, Key Laboratory of Oral Medicine, Guangzhou 510140, Guangdong Province, China -
Supported by:the Beijing Science and Technology New Star Project, No. Z161100004916140 (to ZLB)
CLC Number:
Cite this article
Zhou Yang, Zhou Libin, Piao Zhengguo. Prospects and application of curvilinear distraction osteogenesis[J]. Chinese Journal of Tissue Engineering Research, 2019, 23(15): 2436-2442.
share this article
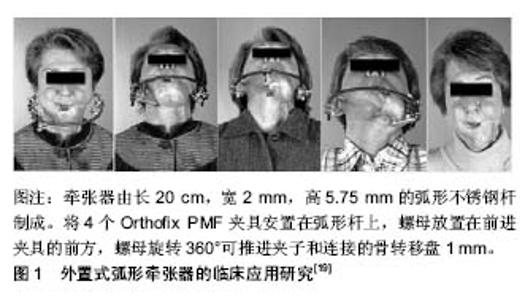
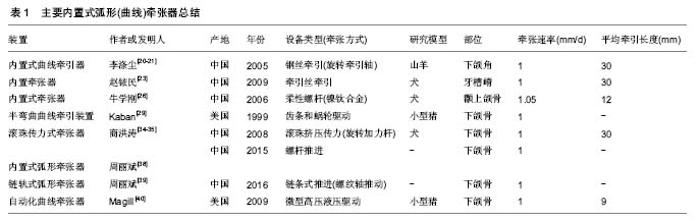
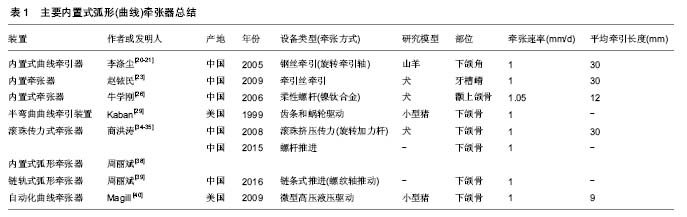
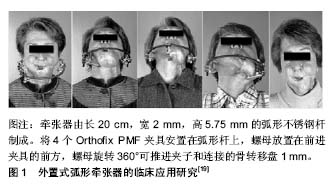
2.1 牵张器的发展 用于牵张成骨的装置,即为牵张器。牵张成骨技术的广泛应用,得益于牵张器的不断改进。早期的牵张成骨装置多为外置式单方向的牵张器[5],随后出现了双方向、三维骨牵张器及多方向牵张器进行转移盘的牵引。随着各项技术的发展,出现了各种口内牵张器,例如螺旋牵张器、双向牵张器、曲线牵张器、三焦点牵张器以及自动牵张器。鉴于颌骨特殊的解剖形态,存在多处弧面结构,如下颌角、颏正中联合、上颌牙槽骨等,为了使生成的新骨更加接近颌骨的轮廓形态,弧形(曲线)牵张成骨也逐渐成为研究热点。 2.2 二维和三维牵张器 在同一个牵张器上设计2个牵引轴,则可实现二维甚至三维方向的牵张成骨,例如Stryker Leibinge公司推出的Multiguide牵张器以及Synthes公司的Multivector牵张器[6]。这类牵张器的2个牵引轴之间由铰链连接,通过调节铰链可以调节2个导向体之间的角度从而可以实现在二维平面上进行多方向的牵张成骨。王恩群等[7]设计的颧骨三维牵张器,利用2块在一定范围内可在2个垂直方向任意移动的支撑板,带动牵引杆改变牵张方向。最终在离体羊颅骨模型上完成了牵引杆前后移动约2.0 cm、上下移动约3.5 cm,向外移动约3.0 cm的三维牵张过程。应彬彬等[8]也设计出可调式多平面牵张器:固定夹板固定输送盘,纵向螺杆用以引导输送盘向前运动,横向螺杆用以调节输送盘向中线内收,以近似曲线地整复下颌前部缺损。 双向、多平面骨牵张器的问世使牵张成骨技术实现了由单向、单平面成骨向双向、多向、多平面成骨的突破。林小臻等[9-10]发明的新型内置式二维牵张器,在动物实验中将双联固定翼分别固定于升支及下颌骨体部[11],此2个活动翼均可以顺利牵张至导向体末端,下颌支和下颌体实现同时延长,牵张间隙呈弧形。并成功运用于2例下颌后缩畸形病例[12],恢复下颌骨形态。有研究研制出了锥齿轮传动和蜗杆传动的双向对称移动牵张器[13-14]。前者特别适用于下颌骨小颌畸形患者的内置式双向对称移动牵张术,以螺杆、大小锥齿轮和活动翼的机械组合运动,使左右翼同时向外侧或内侧以相同速度移动,实现下颌骨的对称牵张过程。后者外部通过6方头的旋转来切换牵引螺杆向不同方向转动。双向对称螺杆向不同方向转动时,通过螺纹传动带动左右翼同时向外侧或内侧以相同速度运动,实现下颌骨的对称牵张过程。有研究采用的内置式整型牵张成骨器能够在万向节驱动双向丝杠运动时,直接带动两个活动翼反向运动,使牵张成骨的时间缩短一半[15]。除此,使用该装置仅通过一次手术可同时实施对下颌骨整型与牵张成骨。黄代营等[16]设计了双维控制牙槽骨牵张器,用于犬动物实验,发现双维控制垂直牙槽骨牵张器能较好的控制移动骨块垂直或颊向的移动方向,可防止单向直线牵张器行牙槽骨牵张发生轴向移位。林成等[17]发明出一种牙槽嵴三维成骨牵引器。其水平牵引器和垂直牵引器两部分相互垂直连接,通过各自相连的牵引螺丝带动截骨块实现垂直、水平两个方向的移动,能同时增高、增宽萎缩牙槽嵴,可一次性解决3个方向的成骨问题。 2.3 外置式弧形(曲线)牵张器 上述二维或三维牵张器通过对器械角度的调整可实现牵引骨段一定程度的转向、侧移,整合形成弧形(或曲线)运动轨迹,但并非真正意义上的曲线式牵引。因此,更多学者们致力于研制开发弧形(曲线)骨牵张器,试图突破牵张器在设计制作上的瓶颈,进一步拓展颅颌面牵张成骨技术的应用范围和施用效果。Annino等[18]于1994年最早报道外置式曲线牵张器,该牵张器主体结构为围绕下颌骨的弧形轨道,通过连接骨转移盘的滑块沿弧形轨道滑行产生牵引力,在动物实验中进行弧形牵引,生成了长4.5-5.5 cm、高2.2-3.0 cm及宽1.3-1.5 cm的新骨。此后,Jonsson等[19]设计了用于修复下颌骨前部缺损的外置式弧线骨牵张器,该牵张器由长20 cm,宽2 mm,高5.75 mm的弧形不锈钢杆制成,顶部和底部带有螺纹。将4个Orthofix PMF夹具安置在弧形杆上,螺母放置在前进夹具的前方,螺母旋转360°可推进夹子和连接的骨转移盘1 mm,通过动物实验和临床应用,成功地验证了弧形牵张成骨的可行性和有效性,见图1。"

外置牵张器存在体积、质量大、结构复杂、易于碰撞及影响患者美观和日常生活等缺点。另外,外置式器械因与骨皮质之间存在较大距离而使牵引加力时的大部分牵引力转化为钢钉或骨钉的弯曲力矩,并非完全转化为断端间的牵引距离,易造成牵引刻度与设计骨延长量之间的较大差距。更为严重的是,外置式弧形牵张器牵引时容易引起局部水肿及感染,损伤面神经,及牵引后面部遗留瘢痕等问题。且牵引量愈大,此现象愈明显。因此内置牵张成骨逐渐成为曲线牵张的发展趋势。 2.4 内置式弧形(曲线)牵张器 有研究于2005年发明了一款内置式曲线牵引器,技术核心为含牵引轴的承载管和带导槽的弧形导轨[20-21]。将导轨、传送盘和固定盘置入体内,传送盘与传送骨固定一起,承载管和牵引轴放置体外,旋转牵引轴,通过钢丝带动传送盘运动,从而带动传送骨沿弧形导轨运动。采用该牵张器对羊下颌角30 mm弧形缺损进行牵张修复实验,并获得了成功。课题组随后设计了2种牵张器[22],分别用于下颌角区域及下颌骨正中联合部,均为完全置于皮内的弧形导轨和滑块及牵引钢丝组成。连接骨转移盘的滑块在导轨上自由滑动,牵引装置通过旋转加力杆,使缠绕于加力杆上的牵引钢丝收紧,从而牵引滑块沿导轨移动,实现弧形牵张成骨。有研究设计了一款原理类似的上颌骨专用弧形牵张器,转动加力杆使导轨凹槽内的牵引丝绕杆缠绕,带动滑块、固定板及骨转移盘一起沿导轨移动,从而达到牵张成骨的目的[23]。动物实验研究发现新生骨组织向弧形轨迹的腭侧偏移2.0-3.0 mm,经过改良牵张器(在滑块移动范围内向颊侧扩展了弧形导轨),在模拟实验中实现了牵张间隙的颊侧扩展[24]。牛学刚等[25-27]设计的内置式牵张器则采用钛镍合金丝制造的柔性螺杆牵引结构,弧形的柔性螺杆可以在弧形的管道形轨道内转动,推动转移盘沿弧形轨道移动。将其应用于一例部分下颌骨下缘完整、体部缺损17 mm的患者[28],成功修复了弧形骨缺损。Kaban课题组[29]介绍了Synthes公司研制的一种内置式弧形牵张器,其核心部件——弧形轨道上开凿有与其弧线垂直、呈扇形排列的沟槽,套在轨道上的移动盒内装配的蜗杆的螺旋齿与沟槽相啮合。转动螺杆,形成齿条蜗杆传动,驱动蜗杆和转移盒沿着弧形轨道移动,带动骨块实现弧形牵张运动,见图2。"

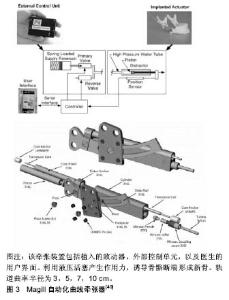
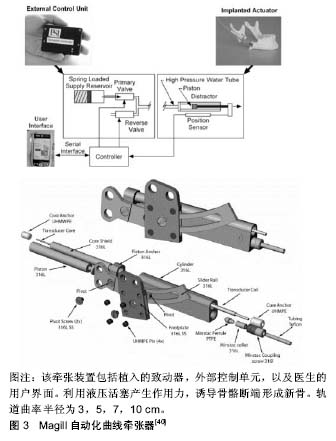
该课题组通过数字化技术,制定弧形牵张成骨治疗计划,为13例重度下颌后缩畸形的患儿实施了弧形牵张成骨,使下颌骨前徙的同时作逆时针旋转,同时矫治了下颌后缩和前牙开颌畸形[30-31]。不过这种弧形牵张器的轨道长度有限,无法应用于大范围的弧形缺损区域,且加力杆随着牵引过程而逐渐向体内推进。因而需要足够长的加力杆,在牵引初期带来操作的不便,且有将感染带入体内的风险。Herford[32]和Hibi等[33]分别运用接骨成型板作为导向,在其引导下控制牵张方向,对下颌骨节段性缺损患者施行了牵张成骨,均获得了软硬组织再生。但由于加力方式仍采用金属丝牵引方式,对于弧度较小的骨缺损尚可使用,弧度较大的骨缺损则难以保证牵引力的有效传导,且牵引金属丝自身强度所限,力量较大时容易断裂,直接影响牵张的成功率。有研究设计出一种内置式弧形牵张成骨器,其内圆柱导向槽内充填有与其紧配合滑动式连接的若干滚珠,通过旋转传力螺杆,即可推动最右端滚珠沿内圆柱导轨依次将牵引力传递给最左端滚珠固联的移动翼,使移动翼沿内圆柱导轨移动[34-35]。该设计可根据导向槽的形状实现任意方向上的曲线或者三维牵张成骨。离体实验和动物实验考察了内置式弧形牵张成骨修复下颌骨颏部缺损的可行性[36-37]。牵张过程中传送盘及骨转移盘在滚珠的推动下,沿着弧形导轨从缺损间隙的一端逐渐移至另一端。新骨呈弧形,弧度略小于牵张器导轨弧度。周丽斌设计出一种内置式弧形牵张器,该牵张器设置弧形导轨、弧形槽及螺杆配合使用,通过转动万向节进行驱动。受弧形导轨的约束,螺杆沿弧形导轨的弧度移动,带动转移盘移动,从而实现弧形牵张成骨的目的[38]。在能够达到手术要求的足够强度前提下牵引不容易引起局部水肿、感染,损伤面神经及牵引后面部遗留瘢痕。但由于其体积较大,在体内随着牵张的过程推进螺杆的位置逐渐变化,推进速率和转移盘实际移动速率不一致,可能造成螺杆与导轨之间软组织损伤,影响弧形牵张过程。随后周丽斌[39]又研制出一种链轨式弧形牵张器。通过设置弧形导轨和链条式推进装置,直线的螺纹轴推进链条沿弧形部做弧形运动,实现弧形牵张成骨。该装置结构简单,操作方便,转移盘的移动速率与推进螺纹轴的推进速率一致易于控制,防止软组织嵌入导轨内影响牵张过程。 近年来也有不少关于自动化牵张器的研究,Magill等[40-41]设计的自动化曲线牵张器使用微型高压液压系统,位置反馈和数字控制器来实现对牵引过程的闭环控制。该制动器利用势能储存装置和受控释放的能量来提供牵张力。预充电的加压流体储存器使其中的流体在储存器被植入到植入部位之前被加压;所用控制器打开阀门一段时间通过调节流体的流动以提供牵张力,其牵张力有效地将骨骼断端之间的距离增加到一定程度以有效地诱导骨骼之间的新骨生成,见图3。"
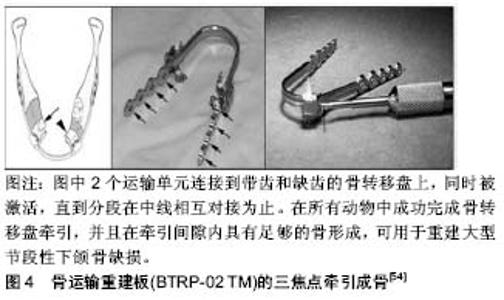
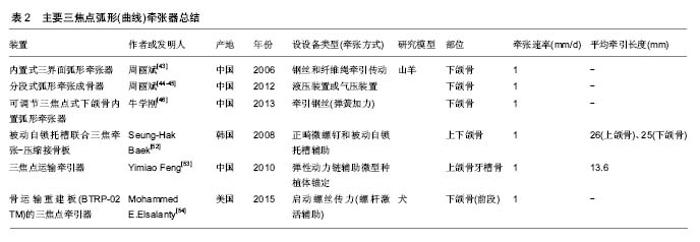
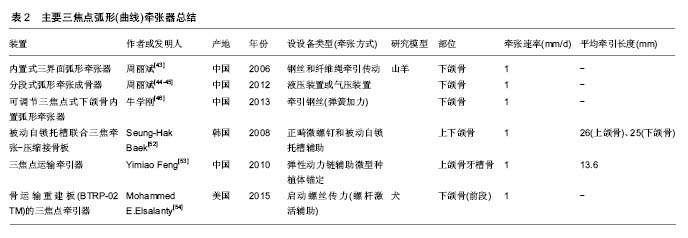
2.5 三焦点弧形(曲线)牵张器 对于大型的颌骨缺损,采取以往的牵张技术难以完成较大弧度牵张的难题,针对这一现状,有学者利用三焦点牵张原理,将一个弧度大的骨缺损分解为2个弧度较小的骨缺损或多个区域分别进行牵张,力图达到弧形牵张的效果。国内外均报道了一些应用三焦点牵张器成功修复颌骨缺损的实验研究及临床应用。周丽斌[43]根据三界面弧形牵张成骨的技术要求,对已有的双界面弧形牵张器加以改进,进一步设计内置式三界面弧形牵张器。在双界面弧形牵张器的基础上,增加一个传送盘,牵引时旋转牵引轴,缠绕收紧钢丝和纤维绳,升支传送盘在钢丝的牵引下,近中传送盘在纤维绳的牵引下,沿弧形导轨向中间滑动,二者相向运动,实现了三界面弧线牵张运动。为使牵张效果更加精确,周丽斌等[44-45]进一步提出了分段式弧形牵张成骨技术,将需要弧形牵张成骨修复6.0 cm长的弧形骨缺损分3阶段进行牵张,每阶段牵张 2.0 cm。每阶段结束时,通过手术将骨转移盘后部的骨质切开,固定于弧形导轨,骨转移盘形成新的骨切开线,在此进一步沿弧形导轨行下一阶段2.0 cm牵张,如此完成3次分段的牵张成骨,形成3个弧形的牵张间隙,生成3段新骨,每两段新骨之间是原有的小块转移盘骨质。而3段新骨和骨转移盘一同占据弧形的牵张路径,达到弧形骨缺损修复效果。牛学刚[46]设计出可调节3焦点式下颌骨内置弧形牵张器。通过弹簧加力使柔性中心螺杆在顺应弧形轨道弧度状态下旋转,带动两侧滑块作弧形运动并向中线靠拢,在中线处形成骨结合,从而完成3焦点式弧形牵张成骨修复颏部缺损。刘遵望等[47-48]发明的下颌骨内置弧形牵引式牵张成骨器与前者原理类似,牵引力通过加力弹簧向加力螺丝杆传递,通过牵引钢丝施加在骨输送盘上,两侧输送盘被牵张器引导向前,并向中线对称移动,骨输送盘远心端在正中对接,颏部弧形缺损被整复。该牵张器的对称设计使骨输送盘只能移动至弧形轨道板的中间位置。但是,临床中下颌骨缺损形式各异,少有完全对称的弧形骨缺损。为弥补上述缺陷,刘遵望等[49]又进一步研发了线式下颌颏部牵张成骨器:两根牵引钢丝交叉设置于弧形轨道板外侧,当两根牵引钢丝分别向各自连接的加力螺杆一端移动时,两个骨输送盘固定夹随之相向移动,且骨输送盘固定夹可在弧形轨道板上任意滑动,如此可将3焦点弧形牵张成骨应用于各种类型的弧形骨缺损修复。蔡鸣等[50-51]研制的个体化3焦点圆弧牵引器,其转移盘固定部件与轨道连接处为牵引杆插入并转动牵引的部位,内外两侧均可以转动、牵引,使转移盘处于圆弧轨道不同位置时都可以从口腔前部进行牵引杆的转动。 外文报道中,关于三焦点牵张成骨也有一些新进展。Baek等[52]设计被动自锁托槽联合3焦牵张-压缩接骨板,为了修复上颌骨和下颌前部的大型骨缺损,使用正畸微型螺钉控制运输矢量,通过弹性牵引将再生骨与舌侧弓、被动自锁托槽及正畸弓线一起弯曲,产生正常的前曲率,为植入物提供优质的连续性再生骨且成功地使植入物实现骨愈合。Feng等[53]定制的3焦点运输牵引器,通过弹性动力链激活牵张器,将力施加在微型落定种植体固定装置和滑道轨道上的按钮上,并由微型种植支抗系统(micro-implant anchorage system,MIAS)以1 mm/d的速率辅助正畸弹力激活,有2个运输圆盘被引导沿着圆弧轨道滑动引导运输骨段到达预期位置。Elsalanty等[54]设计骨运输重建板(BTRP-02 TM)的3焦点牵引成骨来完成重建,其中2个运输单元同时被激活,直到分段在中线相互对接为止。最终在所有动物中成功完成骨运输牵引,并且在牵引间隙内具有足够的骨形成。该牵张器可以将带齿骨转移盘远距离运输,且牙齿在骨转移盘上保持完好,由此产生的再生骨与缺齿骨转移盘的结果相似。此外,这项研究使用了一种新型骨输送装置(BTRP)的改进版本,其中骨输送盘沿着支撑板本身而不是在安装的轨道上运送,见图4。"
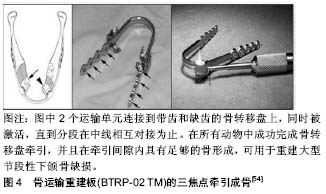
| [1] Codivilla A. On the means of lengthening, in the lower limbs, the muscles and tissues which are shortened through deformity. Am J Orthop Surg. 1905;2:235. [2] Ilizarov GA. The principles of the Ilizarov method. Bull Hosp Jt Dis Orthop Inst. 1988;48(1):1-11. [3] Ilizarov GA. The tension-stress effect on the genesis and growth of tissues. Part I. The influence of stability of fixation and soft-tissue preservation. Clin Orthop Relat Res. 1989;238(238):249-281. [4] Mccarthy JG, Schreiber J, Karp N, et al. Lengthening the human mandible by gradual distraction. Plast Reconstr Surg. 1992;89(1):1-8. [5] Ortakoglu K, Karacay S, Sencimen M, et al. Distraction osteogenesis in a severe mandibular deficiency. Head Face Med. 2007;3(1): 700-707. [6] Hurmerinta K, Hukki J. Vector control in lower jaw distraction osteogenesis using an extra-oral multidirectional device. J Craniomaxillofac Surg. 2001;29(5):263-270. [7] 王恩群,张菊会,程龙,等.颧骨三维牵张器的初步研制[J].中国美容医学, 2004,13(6):705-707.[8] 应彬彬,胡静,李继华,等.用三焦点牵张成骨技术修复重建颏部骨缺损的实验研究[J].实用口腔医学杂志,2006,22(3):295-298.[9] 林小臻.新型内置式二维牵张器的应用研究[D].西安:第四军医大学,2009.[10] 薄斌,周雁麓,西安中邦钛生物材料有限公司.下颌骨内置型双向式牵引器:中国,CN200720126013.9[P].2008-06-11.[11] 林小臻,商洪涛,赵晋龙,等.内置式山羊下颌骨二维牵张器的实验研究[J].中国美容医学,2009,18(3):310-312.[12] 薄斌,林小臻,周雁麓,等.应用双向内置式牵引器矫正下颌骨短小畸形[J].实用口腔医学杂志,2005,25(2):218- 221.[13] 西安中邦钛生物材料有限公司.锥齿轮传动双向对称移动牵张器:中国, CN201120111242.X[P].2011-11-02.[14] 西安中邦钛生物材料有限公司.蜗杆传动双向对称移动牵张器:中国, CN201120111243.4[P].2011-11-02.[15] 中国人民解放军第四军医大学口腔医院,西安中邦钛生物材料有限公司.一种内置式整型牵张成骨器:中国,CN201310200222.3[P].2013-08-14.[16] 黄代营,聂二民,孙明,等.双维控制牙槽骨牵张器的成骨效应[J].中国组织工程研究,2011,15(37):6855-6858.[17] 林成,刘宝林,刘彦普.牙槽嵴三维成骨牵引器:中国,CN200620078906. 6[P].2006-05-23.[18] Annino DJ, Goguen LA, Karmody CS. Distraction osteogenesis for reconstruction of mandibular symphyseal defects. Arch Otolaryngol Head Neck Surg. 1994;120(9):911-916. [19] Jonsson B, Siemssen SJ. Arced segmental mandibular regeneration by distraction osteogenesis. Plast Reconstr Surg. 1998;101(7): 1925-1930. [20] 西安交通大学.应用于颌面骨缺损修复的弧形牵引器:中国, CN200510042750.6[P].2005-11-23.[21] 周丽斌,刘彦普,赵晋龙,等.内置式曲线牵张器修复下颌角缺损的实验研究[J].临床口腔医学杂志,2005,21(11):655-657.[22] 周丽斌,刘彦普,赵晋龙,等.用山羊建立下颌骨曲线牵张成骨实验动物模型[J].实用口腔医学杂志,2006,22(1):11-13.[23] 中国人民解放军第四军医大学口腔医院.个体化上颌牙槽骨弧形牵张器:中国,CN200910022352.6[P].2009-11-04.[24] 冯志宏.牙槽骨弧形牵张成骨修复单侧上颌骨缺损的实验研究[D].西安:第四军医大学,2009.[25] 牛学刚,赵铱民,韩小宪.颧骨弧线式牵张成骨修复部分上颌骨缺损的初步实验[J].中华口腔医学杂志,2006,41(9):547-548.[26] 牛学刚.颧骨内置弧形骨牵张器:中国, CN200710007151.X[P]. 2007-09-26.[27] 牛学刚,韩小宪,郝永.颧骨内置弧形牵张成骨器修复部分上颌骨缺损的可行性(英文)[J].中国组织工程研究与临床康复, 2007,11(41):8398-8400.[28] 牛学刚,韩小宪,郝永,等.内置弧形牵张成骨修复下颌骨缺损的临床应用[J].口腔材料器械杂志,2007,16(4):213-216.[29] Seldin EB, Troulis MJ, Kaban LB. Evaluation of a semiburied, fixed-trajectory, curvilinear, distraction device in an animal model. J Oral Maxillofac Surg. 1999;57(12):1442-1446. [30] Ritter L, Yeshwant K, Seldin EB, et al. Range of curvilinear distraction devices required for treatment of mandibular deformities. J Oral Maxillofac Surg. 2006;64(2):259-264. [31] Kaban LB, Seldin EB, Kikinis R, et al. Clinical application of curvilinear distraction osteogenesis for correction of mandibular deformities. J Oral Maxillofac Surg. 2009;67(5):996-1008. [32] Herford AS. Use of a plate-guided distraction device for transport distraction osteogenesis of the mandible. J Oral Maxillofac Surg. 2004;62(4):412-420. [33] Hibi H, Ueda M. New internal transport distraction device for reconstructing segmental defects of the mandible. J Oral Maxillofac Surg. 2006;44(5):382-385. [34] 中国人民解放军第四军医大学,西安中邦钛生物材料有限公司.一种内置式弧形牵张成骨器:中国,CN200810150721.5[P].2010-03-03.[35] 中国人民解放军第四军医大学,西安中邦钛生物材料有限公司.一种三维弧形滚珠传力式牵张成骨器:中国, CN200820221894.7[P].2009-08-19.[36] 杜靖华.滚珠传力式牵张器的研制与犬颏部缺损修复的初步实验研究[D].西安:第四军医大学,2010.[37] 张国华,商洪涛,郭宇轩,等.曲线牵张成骨的初步实验研究[J].实用口腔医学杂志,2015,31(2):153-156.[38] 中国人民解放军第306医院.一种内置式弧形牵张器:中国, CN201510051701.2[P].2015-05-06.[39] 周丽斌.一种链轨式弧形牵张器:中国, CN201620180292.6[P].2016-10-05.[40] Magill JC, Byl MF, Goldwaser B, et al. Automating skeletal expansion: an implant for distraction osteogenesis of the mandible. J Med Device. 2009;3(1):14502. [41] Goldwaser BR, Magill J, Papadaki ME, et al. Continuous mandibular distraction osteogenesis: novel device and preliminary results in minipigs. J Oral Maxillofac Surg. 2013;71(4):e168-e177. [42] Peacock ZS, Tricomi BJ, Faquin WC, et al. Bilateral continuous automated distraction osteogenesis: proof of principle. J Craniofac Surg. 2015;26(8):2320-2324. [43] 周丽斌.应用内置式弧形牵张器修复下颌骨缺损的实验研究[D].西安:第四军医大学,2006.[44] Zhou L, Shang H, Feng Z, et al. Segmental curvilinear distraction osteogenesis. Med Hypotheses. 2012;79(4):427-429. [45] 中国人民解放军第306医院.一种分段式弧形牵张成骨器:中国, CN201510052491.9[P].2015-05-27.[46] 牛学刚.可调节三焦点式下颌骨内置弧形骨牵张器:中国, CN201320139578.6[P].2013-11-06.[47] 刘遵望.下颌骨内置弧形牵引式牵张成骨器修复犬下颌颏部骨缺损的实验研究[D].长沙:中南大学,2009.[48] 刘遵望.下颌骨内置式弧形牵引式牵张成骨器:中国, CN200720309472.0[P].2007-12-31.[49] 刘遵望.线式下颌颏部牵张成骨器:中国,CN201410826138.7[P].2015-04-29.[50] 蔡鸣,卢晓峰,沈国芳,等.口内入路个体化三焦点圆弧牵引器修复下颌骨大型缺损[J].中国口腔颌面外科杂志,2013,11(2):113-118.[51] Cai M, Lu X, Yang D, et al. Application of a novel intraorally customized transport distraction device in the reconstruction of segmental mandibular defect. J Craniofac Surg. 2014;25(3):1015-1018. [52] Baek SH, Kim NY, Paeng JY, et al. Trifocal distraction-compression osteosynthesis in conjunction with passive self-ligating brackets for the reconstruction of a large bony defect and multiple missing teeth. Am J of Orthod Dentofacial Orthop. 2008;133(4):601-611. [53] Feng Y, Fang B, Shen G, et al. Reconstruction of partial maxillary defect with intraoral distraction osteogenesis assisted by miniscrew implant anchorages. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2010;110(3):e1-e7. [54] Elsalanty ME, Malavia V, Zakhary I, et al. Dentate transport discs can be used to reconstruct large segmental mandibular defects. J Oral and Maxillofac Surg. 2015;73(4):745-758. [55] Pereira AR, Neves P, José Rosa, et al. Curvilinear segmental mandibular reconstruction utilizing distraction osteogenesis and early open callus manipulation. Plast Reconstr Surg Glob Open. 2017;5(1): e1229. [56] Bastidas N, Bartlett SP. Optimization of curvilinear mandible distraction using 3-dimensional computer-simulated modeling. J Craniofac Surg. 2012;23(6):1713-1716. [57] 赵亮.牵张修复下颌骨颏部弧形缺损的生物力学分析[D].西安:第四军医大学,2013.[58] 胥雷,蔡鸣,于雯雯,等.导航专用下颌骨牵引器在山羊下颌骨牵引成骨术中的精度研究[J].中国口腔颌外科杂志,2016,14(1):8-13. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Liu Yafei, Wang Yalin, Zuo Yanping, Sun Qi, Wei Jing, Zhao Lixia. Structural changes of the temporomandibular joint in adolescents with skeletal Class III malocclusions after maxillary protraction: an X-ray measurement analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1154-1159. |
| [3] | Fan Jiabing, Zhang Junmei. Morphological measurement and analysis of the mandible in adult females with different vertical skeletal types [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1177-1183. |
| [4] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [5] | Zhang Bin, Sun Lihua, Zhang Junhua, Liu Yusan, Cui Caiyun. A modified flap immediate implant is beneficial to soft tissue reconstruction in maxillary aesthetic area [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 707-712. |
| [6] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [7] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [8] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [9] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [10] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [11] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [12] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [13] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [14] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [15] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||