Chinese Journal of Tissue Engineering Research ›› 2026, Vol. 30 ›› Issue (29): 7632-7638.doi: 10.12307/2026.256
Previous Articles Next Articles
Blood cells and the occurrence and progression of osteoporosis: biomarkers and emerging therapeutic strategies
Hu Yingnan1, Shi Wanwan1, Wang Datao1, 2, 3
- 1Institute of Special Animal and Plant Sciences, Chinese Academy of Agricultural Sciences, Changchun 130112, Jilin Province, China; 2Jilin Provincial Key Laboratory of International Cooperation for Special Animal and Plant Science and Technology Innovation, Changchun 130112, Jilin Province, China; 3Hebei Provincial Innovation Center for Pet Stem Cell Application Technology, Xingtai 054400, Hebei Province, China
-
Received:2025-08-14Revised:2025-11-28Online:2026-10-18Published:2026-03-06 -
Contact:Wang Datao, PhD, Research fellow, Institute of Special Animal and Plant Sciences, Chinese Academy of Agricultural Sciences, Changchun 130112, Jilin Province, China; Jilin Provincial Key Laboratory of International Cooperation for Special Animal and Plant Science and Technology Innovation, Changchun 130112, Jilin Province, China; Hebei Provincial Innovation Center for Pet Stem Cell Application Technology, Xingtai 054400, Hebei Province, China -
About author:Hu Yingnan, MS candidate, Institute of Special Animal and Plant Sciences, Chinese Academy of Agricultural Sciences, Changchun 130112, Jilin Province, China -
Supported by:National Natural Science Foundation of China, No. 32370899 (to WDT); Outstanding Young Scientific and Technological Talent Project of Jilin Province, No. 20240602030RC (to WDT)
CLC Number:
Cite this article
Hu Yingnan, Shi Wanwan, Wang Datao. Blood cells and the occurrence and progression of osteoporosis: biomarkers and emerging therapeutic strategies[J]. Chinese Journal of Tissue Engineering Research, 2026, 30(29): 7632-7638.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
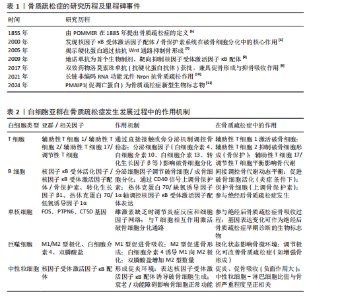
带氧气和释放生长因子等方式间接影响骨代谢;这些血液细胞之间存在着相互影响,见图4。深入研究这些血液细胞的作用机制及其相互作用,为骨质疏松症的治疗提供了潜在的靶点和新的研究方向。 2.2.1 白细胞亚群的关键作用 白细胞亚群(T细胞、B细胞、单核细胞与巨噬细胞、中性粒细胞)在骨质疏松症的发生发展过程中发挥着重要的调控作用,见表2。 (1) T细胞的免疫调控作用:T细胞通过与骨组织细胞的直接接触或旁分泌机制参与骨稳态调控,传统观点认为T细胞在炎症环境中分泌破骨细胞因子促进骨丢失,但研究表明T细胞也可能促进骨形成。 T细胞亚群免疫稳态调控网络理论上阐明了辅助性T细胞1/辅助性T细胞2/辅助性T细胞17/调节性T细胞亚群在骨质疏松症中的动态平衡,研究显示幼稚CD4+T细胞在白细胞介素4刺激下可分化为辅助性T细胞2,并分泌白细胞介素4、白细胞介素10和白细胞介素13等细胞因子直接抑制破骨细胞并发挥骨保护作用[12]。辅助性T细胞1通过肿瘤坏死因子α激活破骨细胞功能,而辅助性T细胞2可以通过白细胞介素4阻止破骨细胞的形成[13]。在骨免疫学研究中,辅助性T细胞17/调节性T细胞平衡及相关细胞因子与骨代谢失调密切相 关[14]。调节性T细胞产生白细胞介素10、转化生长因子β等细胞因子可以抑制体内许多免疫细胞[15]。由此可见,T细胞兼具促骨丢失和促骨形成的双重能力。 (2) B细胞在骨代谢中的间接调控:B细胞通过多种机制间接影响骨质疏松症的发生和发展。唐志等[16]利用单细胞分辨率技术结合免疫组化、定量聚合酶链反应和蛋白免疫印迹等方法揭示了骨质疏松症股骨头组织中B细胞特定亚群能够对成骨细胞的分化和凋亡产生影响。B细胞通过细胞因子如核因子κB受体活化因子配体和骨保护素与破骨细胞和成骨细胞交流并调节骨代谢平衡,在炎症条件下的B细胞促进破骨细胞活化和分化并具有免疫调节特性,通过分泌转化生长因子β1以抑制致病性破骨细胞的生成[17]。此外,骨保护素可以通过"
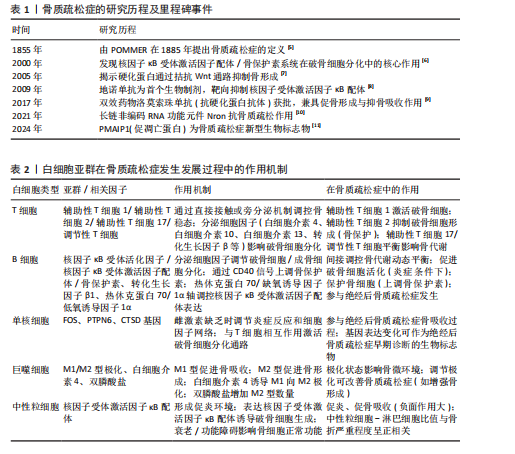
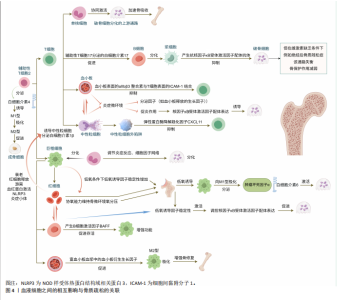
高亲和力与核因子κB受体活化因子配体结合,阻断核因子κB受体活化因子与核因子κB受体激活因子配体的相互作用,从而抑制骨质侵蚀,而B细胞可通过上调CD40共刺激信号促进骨保护素的产生,从而保护骨细胞[18]。由此可见,核因子κB受体活化因子/核因子κB受体激活因子配体/骨保护素通路在骨质疏松症发生和发展中发挥关键作用。 B细胞对绝经后骨质疏松症也有一定的影响,例如雌激素可诱导热休克蛋白70表达上调进而降解低氧诱导因子1α[19]。还有研究发现去卵巢小鼠低氧诱导因子1α表达上调,B细胞中低氧诱导因子1α信号激活调控核因子κB受体激活因子配体基因表达,促进破骨细胞形成并诱导骨质疏松症[20],提示热休克蛋白70/低氧诱导因子1α轴可能是潜在的治疗靶点。 (3)单核细胞与巨噬细胞的微环境调控:单核细胞与绝经后骨质疏松症的发生密切相关,雌激素水平下降导致骨吸收增加,单核细胞通过调节炎症反应和细胞因子网络在骨代谢中发挥关键作用。研究表明,单核细胞在雌激素缺乏状态下调节骨代谢并确定FOS、PTPN6和CTSD这3个基因是绝经后骨质疏松症的潜在生物标志物[21],这项研究发现为绝经后骨质疏松症的早期诊断提供了新型候选血液细胞相关生物标志物。吴晶云[22]研究表明单核细胞通过上调与破骨细胞形成和分化密切相关的多种基因和通路参与骨质疏松症的调控,T细胞与单核细胞间的相互作用增强,破骨细胞分化的重要上游通路被高度激活,骨吸收速度增加从而导致骨质疏松症的发生和发展。由此可知,单核细胞在骨质疏松症的发生发展过程中扮演了重要角色,单核细胞通过调节炎症反应、细胞因子网络以及与T细胞的相互作用,影响破骨细胞的分化和骨吸收。 巨噬细胞在免疫反应中占据重要地位,具有调节组织稳态、促进或抑制炎症反应等作用。巨噬细胞极化是指巨噬细胞根据微环境信号转变为不同的活化状态,如抗炎的M2型和促炎的M1型[23]。有研究表明可以通过调节巨噬细胞的极化状态从而改善骨质疏松症,例如用白细胞介素4可以诱导M1型巨噬细胞向M2型极化增强骨形成。此外,双膦酸盐脂质体能够增加M2型巨噬细胞的数量,从而提高骨量[24]。由此可见,巨噬细胞对于骨质疏松症来说也是极具潜力的治疗靶点。 (4)中性粒细胞的炎症反应:中性粒细胞是血液中数量最多的白细胞,在免疫中起着保护和致病的双重作用。研究发现中性粒细胞衰老和功能障碍会影响破骨细胞、成骨细胞和间充质干细胞的正常功能,导致骨质疏松症等问题[25]。中性粒细胞在炎症部位活化的过程中可以表达核因子κB受体激活因子配体并直接诱导破骨细胞的生成[26]。中性粒细胞-淋巴细胞比值是炎症性疾病较为常见的指标,炎症反应可能会影响到骨骼系统,中性粒细胞-淋巴细胞比值越高,骨质疏松性椎体骨折和股骨颈骨折越严重[27]。中性粒细胞在骨质疏松症中的主要表现是促炎和促骨吸收的负面作用,尤其在衰老或炎症状态下的功能异常会加剧骨丢失,尽管中性粒细胞的免疫防御功能可能间接保护骨骼,但在骨代谢中是弊大于利的。"
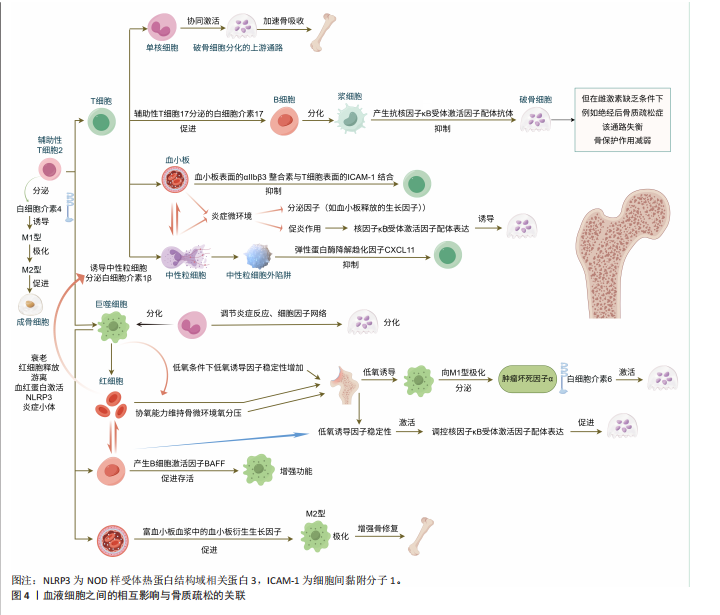
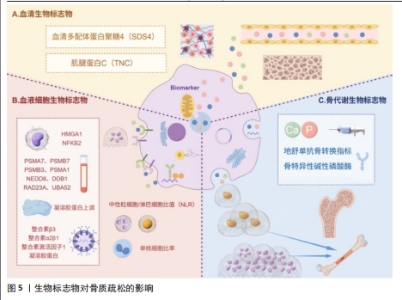
中性粒细胞是具有可塑性的异质群体并且能根据不同刺激调整功能,中性粒细胞的多重作用对于开发靶向治疗策略、增强保护功能及减轻在骨质疏松症中的致病作用至关重要。 2.2.2 红细胞系统的潜在作用 红细胞作为血液中主要的携氧细胞,其功能与骨质疏松症发生与发展的关联逐渐受到关注,红细胞通过低氧诱导因子1α转录因子影响破骨细胞的形成和骨吸收,从而调节骨稳态[28],低氧诱导因子1α作为调节骨代谢的关键因子具有潜在的治疗价值。 红细胞计数和红细胞分布宽度等血液指标与骨密度及骨质疏松症具有一定的关联。研究发现红细胞分布宽度升高与骨质疏松或骨折发生有关,对骨质疏松症具有重要的预测价值[29]。红细胞计数与骨密度呈正相关,骨量减少组及骨质疏松组的红细胞计数低于正常骨密度组[30],这种相关性表明红细胞计数可能在评估骨密度和骨质疏松症风险方面具有潜在的临床价值。王晗等[31]研究发现红细胞计数、平均红细胞血红蛋白浓度等可能是反映骨质疏松症中骨代谢状态的指标。 在红细胞系统中铁缺乏可能是骨质疏松发生的预警,细胞内铁的减少会造成成骨细胞和破骨细胞的活性和功能紊乱,导致骨稳态失衡和骨量丢失[32]。LI等[33]通过骨靶向口服微纳水凝胶系统实现去铁胺的精准递送,证实铁代谢紊乱通过破坏H型血管引发骨质疏松,该研究通过激活低氧诱导因子1α/血管内皮生长因子信号通路促进骨内血管生成可显著缓解骨量丢失。铁缺乏不仅影响红细胞的携氧能力,还会影响骨细胞的功能,从而影响骨代谢,因此监测红细胞相关指标和铁水平的变化对于早期识别和预防骨质疏松症具有重要意义。 2.2.3 血小板在骨代谢中的作用 血小板在骨代谢中的作用日益受到关注,富血小板血浆可促进骨蛋白素的分泌,从而抑制破骨细胞的形成,沉默Beclin1表达使富血小板血浆刺激成骨细胞分泌骨保护素的能力下降,导致局部骨微环境中骨保护素/核因子κB受体活化因子配体比值降低,最终表现为骨吸收增强和骨稳态失衡。富血小板血浆的持续释放和骨形态发生蛋白2修饰的间充质干细胞可以显著促进骨再生[34]。研究表明血小板富含生长因子,在骨重塑中起着至关重要的作用[35]。此外,血小板浓度与骨密度呈正相关,相比于正常骨密度组和骨密度降低组,骨质疏松人群血小板浓度最低[36]。血小板计数与骨密度呈负相关,血小板计数水平与骨密度联合检测可提高骨质疏松症的诊断效能[37]。徐定波等[38]研究发现老年人血小板聚集率高可导致骨吸收增强而骨形成减少,更容易发生骨质疏松症。这些发现为血小板在骨代谢调控中的作用提供了新的视角,并为骨质疏松症的治疗提供了潜在的干预靶点。 2.3 生物标志物对骨质疏松症的影响 传统方法诊断骨质疏松症依靠骨密度测量与影像学检查,可这些方式在疾病早期很难精准地反映骨骼的变化,因此当下寻找无创且便捷的生物标志物成为了研究的热点,识别有价值的生物标志物有助于改善骨质疏松治疗的现状[39],见图5。"
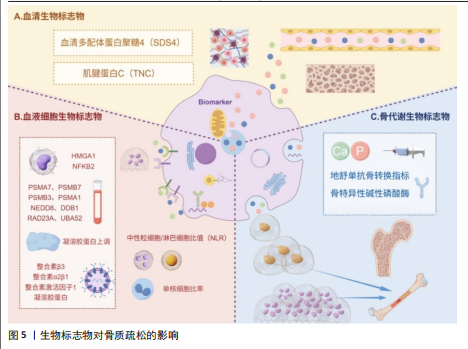

2.3.1 血液细胞相关生物标志物的应用 血液细胞相关生物标志物不仅能作为骨质疏松症早期筛查的工具,还能用于监测治疗效果,进而为制定个体化治疗策略提供依据。研究表明外周血单核细胞可作为骨密度研究的细胞模型,外周血单核细胞作为破骨细胞的祖细胞,为破骨细胞生成的重要细胞因子,可根据富集分析预测差异表达基因的转录因子,其中HMGA1和NFKB2在高骨密度组和低骨密度组之间的表达存在差异[40],这为解析骨密度提供了新的研究方向。史晓林等[41]研究发现以全血作为样本可筛选出数量丰富的绝经后骨质疏松症差异蛋白,其中PSMA7、PSMB7、PSMB3、PSMA1、NEDD8、DDB1、RAD23A、UBA52可能是绝经后骨质疏松症的潜在有效血液标志物,该研究为绝经后骨质疏松症的血液学诊断标志物开发及骨稳态失衡的分子机制研究提供了新方向。通过对血浆和单核细胞蛋白质组学研究发现女性和男性骨质疏松患者血液中凝溶胶蛋白表达均明显上调[42],可以广泛应用于临床早期筛查。此外,霍春晖等[43]研究发现17个蛋白质的表达量在骨质疏松组和骨量减少组有显著改变,包括整合素β3、整合素α2β1、整合素激活因子1和凝溶胶蛋白等,说明人体骨质在衰变过程中发生了系统性变化。血液细胞相关生物标志物不仅有助于疾病的早期诊断与治疗策略的优化,还有助于深刻理解发病机制,为未来的研究奠定基础。 在骨质疏松症的早期筛查中,血液细胞相关生物标志物可反映骨代谢(骨吸收与骨形成失衡)及免疫细胞(调控骨细胞活性)的功能状态,例如中性粒细胞/淋巴细胞比值,检测血常规样本即可并且成本低;BAI等[44]采用荟萃分析发现免疫炎症指数与骨质疏松风险呈正相关,中性粒细胞与淋巴细胞比值升高与骨质疏松风险增加显著相关,说明中性粒细胞与淋巴细胞比值可以作为早期诊断骨质疏松症的血液细胞标志物。YE等[45]通过分析487例患者,发现单核细胞比率与股骨颈骨密度T值呈显著负相关且在绝经后女性中相关性更强,证实血常规单核细胞计数可作为骨质疏松早期筛查的独立预测指标,在临床实验室可以开展应用。 2.3.2 骨代谢和血清生物标志物的应用 骨代谢标志物在骨质疏松症、骨折风险预测和药物疗效评价等方面具有重要的临床应用价值[46],主要包括钙磷调节指标和骨转换指标[47]。陈远程等[48]研究发现地舒单抗能将骨转换指标抑制在较低水平且能有效抑制骨吸收,对骨质疏松患者有良好的治疗效果。地舒单抗也对绝经后骨质疏松症的治疗安全有效,可以显著改善骨密度及骨代谢异常[49]。此外,骨特异性碱性磷酸酶是一种由成骨细胞分泌的重要骨代谢标志物,骨特异性碱性磷酸酶与骨密度呈正相关,可作为评估骨质疏松症风险的潜在生物标志物[50]。骨转化生物标志物可以为骨代谢提供更全面的视角,但仍需大规模研究验证它在骨质疏松症筛查中的有效性和准确性[51]。 血清生物标志物的优点是检测创伤小、检测方便且价格较低,能够动态反映疾病进展,具有较高的应用价值。向奎[52]研究发现老年骨质疏松性患者血清多配体蛋白聚糖4、肌腱蛋白C表达水平均升高,对老年骨质疏松患者骨折具有较高的预测价值。骨代谢标志物结合骨密度可反映围绝经期女性患者早期骨代谢情况,预测骨质疏松症发生风险[53]。 2.4 血液细胞在骨质疏松症中的新兴治疗进展与潜力 随着研究的不断深入和技术的不断进步,血液细胞在骨质疏松症中的应用将更加广泛和有效。 2.4.1 骨髓间充质干细胞治疗技术 骨髓间充质干细胞是骨髓腔中一类起源于中胚层的成体干细胞,具有自我更新及多向分化潜能,在维持骨稳态和促进骨重建过程中发挥着不可或缺的作用[54]。 骨髓间充质干细胞衰老被认为是老年性骨质疏松症发生发展的重要因素之一,恢复骨髓间充质干细胞活性是一种很有前景的治疗老年性骨质疏松症的策略[55]。随着年龄的增长,老年机体内骨髓间充质干细胞表现出一系列改变:自我更新及增殖能力减退;成骨分化能力降低甚至丧失,转而趋向成脂分化;成骨相关细胞因子分泌水平降低及骨髓间充质干细胞自身代谢活动紊乱等[56],骨髓间充质干细胞衰老是引发骨稳态失衡进而导致老年性骨质疏松症的重要原因之一。有研究显示移植骨髓间充质干细胞可通过促进老年小鼠髓腔内调节性T细胞增殖并抑制凋亡,从而减轻骨丢失和促进骨重建,具有改善骨质疏松症的效果[57]。 石玉莲等[58]研究发现在骨质疏松部位注射小鼠骨髓间充质干细胞有利于骨质疏松向正常骨质转换。李杨等[59]研究表明骨髓间充质干细胞能够明显改善骨质疏松性骨折模型的骨生物力学和组织形态学指标,提高骨密度,可能与上调骨碱性磷酸酶表达、下调Ⅰ型胶原交联C-末端肽表达有关。胡涛等[60]研究显示鹿血晶(一种鹿血提取物)能够促进骨髓间充质干细胞的增殖,从而治疗骨质疏松症,但体内的效果与机制需要进一步验证。这些研究从不同角度为基于骨髓间充质干细胞的治疗提供了实验依据,为开发基于骨髓间充质干细胞的骨质疏松症治疗新方法奠定了重要基础并揭示了潜在的作用靶点。 2.4.2 中性粒细胞介导的骨髓靶向药物递送 尽管目前已经有多种用于骨质疏松症治疗的药物,但因为骨骼的低血液灌注的性质,药物在向骨骼输送方面仍存在一定问题。中性粒细胞具有归巢特性,其介导的骨髓靶向药物递送系统为骨质疏松症治疗这一难题提供了创新性解决方案。研究表明中性粒细胞可被自然输送到骨髓并能穿过骨髓-血液屏障。在诱导性骨质疏松模型中,中性粒细胞递送特立帕肽显著增加了骨矿物质密度[61],该研究利用中性粒细胞向骨髓归巢的特性开发了一个新的骨髓靶向药物递送平台,不仅克服了传统药物递送效率低的问题,还为骨质疏松症的精准治疗提供了初步实验支持。 2.4.3 巨噬细胞重编程与成骨细胞-破骨细胞耦合 目前的抗骨质疏松药物对骨折愈合效果有限且疗效不够理想,而巨噬细胞重编程与成骨细胞-破骨细胞耦合在骨质疏松症的治疗中展现了巨大潜力,代谢重编程方法是当前研究热点之一。研究表明基于沸石咪唑酯骨架8(ZIF)的骨靶向硫化氢(H?S)递送系统(ZIF-H?S-SDSSD)可以通过在沸石咪唑酯骨架8表面修饰骨靶向肽SDSSD,实现硫化氢在骨组织中的局部释放,避免了系统性硫化氢递送的潜在风险,细胞摄取后溶酶体酸性环境触发硫化氢从包裹的硫化锌中释放,同时沸石咪唑酯骨架8降解并释放Zn2?,释放的Zn2?和硫化氢协同作用,通过抑制琥珀酸积累和线粒体活性氧含量促进巨噬细胞代谢重编程,进一步调控成骨细胞-破骨细胞耦合,从而促进骨折愈合并改善骨质疏松症[62],这项研究展示了通过靶向巨噬细胞代谢重编程来调控成骨-破骨耦合并促进骨修复的可行性,为克服现有药物在骨折愈合方面的局限性提供了一种新的思路。 2.4.4 外泌体及miRNA在骨质疏松症中的潜力 外泌体及其所携带的miRNA不仅能够作为诊断和预测骨质疏松症发生发展的分子,还能通过调控靶基因表达促进骨髓间充质干细胞和成骨细胞的增殖、分化[63]。不同来源的外泌体通过调节成骨细胞增殖分化和基质钙化影响骨代谢,其中外泌体包含的miRNA是发挥此功能的重要因素[64]。Wnt信号通路是一条在生物进化中高度保守的通路,影响细胞的增殖与分化等,miRNA通过调控Wnt信号通路进一步调节整个成骨细胞谱系的定向分化,在骨质疏松症发病及治疗过程中起关键作用[65]。由上述可知,外泌体及miRNA在骨质疏松症中的研究取得了显著进展,通过调控关键信号通路和细胞功能来干预骨代谢失衡,也为开发基于外泌体/miRNA的靶向治疗新方法提供了重要的理论基础和实验依据,但临床应用转化仍需更深入的机制探索和大规模临床验证。 2.4.5 现有的治疗方法与新兴治疗进展的关系 现有的治疗方法例如抑制破骨活性的双膦酸盐;阻断破骨细胞分化的核因子受体激活因子κB配体抑制剂地舒单抗;促成骨细胞增殖的甲状旁腺激素类似物特立帕肽;补充基础物质、维持钙代谢的维生素D和钙剂;还有调节免疫炎症的部分抗炎药物等方法。 骨髓间充质干细胞可以促进调节性T细胞增殖并抑制凋亡,同时调节成骨/破骨相关因子,这种多效性作用可与双膦酸盐和核因子受体激活因子κB配体抑制剂形成双向调控。中性粒细胞靶向递送系统利用中性粒细胞的骨靶向性,有望提高药物(如特立帕肽)在骨组织的局部浓度和富集度,这种精准递送方式不仅可以增强药物的促成骨效果,还可能减少因全身暴露带来的毒副作用风险。巨噬细胞重编程疗法通过调控巨噬细胞代谢(如抑制琥珀酸积累)和调节成骨细胞-破骨细胞耦合,可能与双膦酸盐协同抑制破骨并与特立帕肽协同促进成骨细胞高效修复骨组织。外泌体携带miRNA调控Wnt信号通路,具有实现精准干预的潜力,调控Wnt通路的作用可能与抑制硬化蛋白的药物协同从而更高效促进成骨,miRNA调控属于分子层面的通路优化,理论上与现有药物的作用方向一致,并无拮抗作用。探索新兴血液细胞相关治疗方法与现有药物的协同应用是未来提升骨质疏松症治疗效果的一个极具前景的研究方向,深入理解这些潜在的协同作用机制并通过临床研究加以验证,将为开发更有效的联合治疗方案奠定基础。 2.4.6 血液细胞在骨质疏松症治疗中的研究方向与潜力 基于当前对血液细胞在骨代谢中作用机制的深入理解,有望在以下方向取得突破性进展并为骨质疏松症的治疗开辟新路径:①利用CRISPR-Cas9编辑造血干细胞的基因(如敲除核因子κB受体活化因子或增强骨保护素表达),使其后代细胞倾向于成骨或抑制破骨功能;还可以开发靶向免疫细胞的生物制剂;②可以利用单细胞技术解析骨质疏松患者血液细胞的异质性,识别关键亚群(如特定巨噬细胞或T细胞亚型)作为治疗靶点;未来还可以开发新型单克隆抗体来治疗骨质疏松症;③血液细胞可作为药物递送的载体并实现药物精准投送,从而提高治疗效果等。血液细胞作为骨代谢的核心调控者,为骨质疏松症提供了从免疫干预到干细胞再生的多层次治疗视角,这些研究方向虽展现出巨大潜力,但临床转化仍需攻克递送效率、靶向特异性和长期安全性等关键挑战。"

| [1] 杨莹.骨质疏松症的防治[J].开卷有益-求医问药,2024(12):23. [2] 郁思哲,王国威,赵东宝,等.免疫骨质疏松学:免疫系统与骨质疏松的对话[J].海军军医大学学报,2025,46(4):427-434. [3] 钟素,王漪莹,王璐瑶,等.绝经后女性继发骨质疏松发病率及危险因素分析[J].中国妇幼保健,2025,40(7):1272-1275. [4] FISCHER V, HAFFNER-LUNTZER M. Interaction between bone and immune cells: Implications for postmenopausal osteoporosis. Semin Cell Dev Biol. 2022;123:14-21. [5] 刘忠厚,向青,苏楠,等.骨质疏松的概述[C]//中国骨质疏松杂志社,北京东方亚太骨矿研究中心.第一届全国骨矿研究年会会议文集,2002:60-71. [6] TEITELBAUM SL. Bone resorption by osteoclasts. Science. 2000;289(5484):1504-1508. [7] LI X, ZHANG Y, KANG H, et al. Sclerostin binds to LRP5/6 and antagonizes canonical Wnt signaling. J Biol Chem. 2005;280(20): 19883-19887. [8] CUMMINGS SR, SAN MARTIN J, MCCLUNG MR, et al. Denosumab for prevention of fractures in postmenopausal women with osteoporosis. N Engl J Med. 2009;361(8):756-765. [9] SAAG KG, PETERSEN J, BRANDI ML, et al. Romosozumab or Alendronate for Fracture Prevention in Women with Osteoporosis. N Engl J Med. 2017;377(15):1417-1427. [10] JIN F, LI J, ZHANG YB, et al. A functional motif of long noncoding RNA Nron against osteoporosis. Nat Commun. 2021;12(1):3319. [11] LI T, YUAN J, XU P, et al. PMAIP1, a novel diagnostic and potential therapeutic biomarker in osteoporosis. Aging (Albany NY). 2024;16(4):3694-3715. [12] TANG M, TIAN L, LUO G, et al. Interferon-Gamma-Mediated Osteoimmunology. Front Immunol. 2018;9:1508. [13] DENG YJ, LI Z, WANG B, et al. Immune-related gene IL17RA as a diagnostic marker in osteoporosis. Front Genet. 2023;14:1219894. [14] GUO M, LIU H, YU Y, et al. Lactobacillus rhamnosus GG ameliorates osteoporosis in ovariectomized rats by regulating the Th17/Treg balance and gut microbiota structure. Gut Microbes. 2023;15(1):2190304. [15] 邓娟,王秀芳,孙瑞青.汉黄芩素促进自身免疫性肝炎模型大鼠Th17/Treg细胞平衡[J].基础医学与临床,2024,44(1):77-83. [16] 唐志,邵阳,李绍烁,等.单细胞测序揭示骨质疏松症患者B细胞异质性及与成骨细胞的相互作用[J].中国组织工程研究,2025, 29(26):5501-5510. [17] FRASE D, LEE C, NACHIAPPAN C, et al. The Inflammatory Contribution of B-Lymphocytes and Neutrophils in Progression to Osteoporosis. Cells. 2023;12(13):1744. [18] 郭曹培,程飘涛,杨成兵,等.骨免疫与骨代谢[J].中国组织工程研究,2024,28(14):2261-2266. [19] 何姣姣,陈以发,陈玉林,等.绝经后骨质疏松的骨免疫学机制[J].中国骨质疏松杂志, 2023,29(7):1032-1036. [20] MENG X, LIN Z, CAO S, et al. Estrogen-mediated downregulation of HIF-1α signaling in B lymphocytes influences postmenopausal bone loss. Bone Res. 2022;10(1):15. [21] DENG YX, HE WG, CAI HJ, et al. Analysis and Validation of Hub Genes in Blood Monocytes of Postmenopausal Osteoporosis Patients. Front Endocrinol (Lausanne). 2022;12:815245. [22] 吴晶云.单细胞转录组测序解析老年女性PBMC亚群中骨质疏松症相关基因[D].苏州:苏州大学,2023. [23] 党泽亮,王兴盛,王芳,等.从巨噬细胞极化角度浅析中医药治疗骨质疏松症的治疗思路[J].数理医药学杂志,2024,37(9):695-700. [24] ARDURA JA, RACKOV G, IZQUIERDO E, et al. Targeting Macrophages: Friends or Foes in Disease? Front Pharmacol. 2019;10:1255. [25] CHANEY S, VERGARA R, QIRYAQOZ Z, et al. The Involvement of Neutrophils in the Pathophysiology and Treatment of Osteoarthritis. Biomedicines. 2022;10(7):1604. [26] 冯红红,高飞.新型炎症因子与原发性骨质疏松症的研究进展[J].中国骨质疏松杂志, 2022,28(1):152-156. [27] ZHU H, LI Z, ZHOU Y, et al. Neutrophil-lymphocyte ratio as a risk factor for osteoporotic vertebrae fractures and femoral neck fractures. Medicine (Baltimore). 2022;101(48):e32125. [28] KNOWLES HJ. Distinct roles for the hypoxia-inducible transcription factors HIF-1α and HIF-2α in human osteoclast formation and function. Sci Rep. 2020;10(1):21072. [29] 姜娟,张厚莉,张许,等.红细胞分布宽度与骨质疏松症和相关骨折相关性的研究进展[J].中国研究型医院,2022,9(5):49-52. [30] OUYANG J, CUI Y, ZHU X, et al. Sex Hormones Had Mediation in the Connection Between Certain Blood Routine Parameters and Bone Loss. J Clin Densitom. 2022;25(4):544-552. [31] 王晗,王炳花,王曼利,等.苏州市老年人群红细胞参数与骨质疏松症的相关性分析[J].内蒙古医学杂志,2023,55(12):1490-1494. [32] YANG J, LI Q, FENG Y, et al. Iron Deficiency and Iron Deficiency Anemia: Potential Risk Factors in Bone Loss. Int J Mol Sci. 2023;24(8):6891. [33] LI J, WEI G, LIU G, et al. Regulating Type H Vessel Formation and Bone Metabolism via Bone-Targeting Oral Micro/Nano-Hydrogel Microspheres to Prevent Bone Loss. Adv Sci (Weinh). 2023;10(15):e2207381. [34] LI L, ZHAO C, ZHANG R, et al. Beclin 1 of megakaryocytic lineage cells is locally dispensable for platelet hemostasis but functions distally in bone homeostasis. Bone Res. 2025;13(1):32. [35] SALAMANNA F, MAGLIO M, SARTORI M, et al. Platelet Features and Derivatives in Osteoporosis: A Rational and Systematic Review on the Best Evidence. Int J Mol Sci. 2020;21(5):1762. [36] MA WC, CHENG YC, LEE WJ, et al. Circulating platelet concentration is associated with bone mineral density in women. Arch Osteoporos. 2022;17(1):44. [37] 赵籥陶,董娟,常杰,等.血小板计数水平与老年人群骨密度的相关性分析[J].河北医药,2024,46(13):1978-1981. [38] 徐定波,杨枝,王艳.老年人血小板聚集功能对骨代谢及其相关细胞因子的影响[J].中国实用医药,2022,17(20):45-48. [39] 孙蛟,丛珊,罗莉.骨质疏松免疫相关标志物的生物信息学分析及其鉴定[J].细胞与分子免疫学杂志,2023,39(12):1108-1113. [40] ZHOU Y, ZHU W, ZHANG L, et al. Transcriptomic Data Identified Key Transcription Factors for Osteoporosis in Caucasian Women. Calcif Tissue Int. 2018;103(6):581-588. [41] 史晓林,杨依然,刘钟,等.基于蛋白质组学方法分析绝经后骨质疏松症全血差异蛋白[J].中医正骨,2019,31(6):7-11. [42] APARICIO-BAUTISTA DI, BECERRA-CERVERA A, RIVERA-PAREDEZ B, et al. Label-free quantitative proteomics in serum reveals candidate biomarkers associated with low bone mineral density in Mexican postmenopausal women. Geroscience. 2024;46(2):2177-2195. [43] 霍春晖,李英华,乔智,等.血清外泌体的蛋白质组分析及其在骨质疏松中的应用[J].色谱,2019,37(8):863-871. [44] BAI B, XIE X, YUE Y, et al. Association between immune-inflammatory index and osteoporosis: a systematic review and meta-analysis. Eur J Med Res. 2025;30(1):632. [45] YE X, JIANG H, WANG Y, et al. A correlative studies between osteoporosis and blood cell composition: Implications for auxiliary diagnosis of osteoporosis. Medicine (Baltimore). 2020;99(26):e20864. [46] 邱敏丽,古洁若.骨代谢标志物在骨质疏松症诊治中的应用[J].广东医学,2024,45(1):6-11. [47] 《中国骨质疏松杂志》骨代谢专家组,张萌萌,马倩倩,等.骨代谢生化指标临床应用专家共识(2023修订版)[J].中国骨质疏松杂志,2023,29(4):469-476. [48] 陈远程,吴文,许翎,等.地舒单抗治疗的原发性骨质疏松症患者血钙及骨代谢标志物的动态变化[J].南方医科大学学报,2025, 45(4):760-764. [49] 魏懿浩,曹思旸,齐天天,等.地舒单抗治疗绝经后骨质疏松性骨折的效果及其对骨代谢标志物的影响[J].中国老年学杂志, 2024,44(11):2628-2631. [50] DU X, CHEN Z, SHUI W. Research progress of circRNA as a biomarker of osteoporosis. Front Genet. 2024;15:1378026. [51] 孙浩鹏,吴炯林,丁悦.骨转换生化标志物在骨质疏松症早期筛查中的应用进展[J].中华骨质疏松和骨矿盐疾病杂志,2024, 17(5):481-490. [52] 向奎.老年骨质疏松患者SDC4、TNC表达水平与骨代谢标志物、骨折的关系[J].临床研究,2025,33(1):79-83. [53] 罗凤.骨代谢标志物与骨密度联合诊断围绝经期骨质疏松的价值分析[J].医药前沿, 2024,14(24):129-131. [54] ARTHUR A, GRONTHOS S. Clinical Application of Bone Marrow Mesenchymal Stem/Stromal Cells to Repair Skeletal Tissue. Int J Mol Sci. 2020;21(24):9759. [55] TIAN RC, ZHANG RY, MA CF. Rejuvenation of Bone Marrow Mesenchymal Stem Cells: Mechanisms and Their Application in Senile Osteoporosis Treatment. Biomolecules. 2025; 15(2):276. [56] LI X, WANG X, ZHANG C, et al. Dysfunction of metabolic activity of bone marrow mesenchymal stem cells in aged mice. Cell Prolif. 2022;55(3):e13191. [57] 关鑫.骨髓间充质干细胞在治疗老年性骨质疏松中的作用及机制研究[D].广州:南方医科大学,2022. [58] 石玉莲,刘文清,樊庭宇,等.骨质疏松对骨髓间充质干细胞增殖、迁移与分化能力的影响[J].中国临床解剖学杂志,2025,43(2): 190-194. [59] 李杨,陈勇,白亮,等.BMSCs对骨质疏松性骨折模型大鼠的影响及作用机制[J].中国老年学杂志,2023,43(15):3819-3822. [60] 胡涛,刘娇,梁潇,等.探究中药鹿血晶对骨髓间充质干细胞的增殖作用[J].贵州中医药大学学报,2023,45(4):13-17. [61] LUO Z, LU Y, SHI Y, et al. Neutrophil hitchhiking for drug delivery to the bone marrow. Nat Nanotechnol. 2023;18(6):647-656. [62] QIN Y, ZHANG Z, GUO X, et al. A Bone-Targeting Hydrogen Sulfide Delivery System for Treatment of Osteoporotic Fracture via Macrophage Reprogramming and Osteoblast-Osteoclast Coupling. Adv Funct Mater. 2024; 36:2418822. [63] 王彬,何鹏,刘晓伟,等.外泌体微小RNA在骨质疏松症中的研究进展[J].医学研究与战创伤救治,2023,36(11):1212-1216. [64] 吴西,王中琪,宋慕格,等.外泌体对骨组织细胞的影响及应用的研究进展[J].中国比较医学杂志,2023,33(6):108-113. [65] 李玮民,李豪,杨城,等.基础到临床:miRNA调控Wnt信号通路影响骨质疏松症的现状[J].医学研究与战创伤救治,2023, 36(4):416-424. |
| [1] | Chen Huiting, Zeng Weiquan, Zhou Jianhong, Wang Jie, Zhuang Congying, Chen Peiyou, Liang Zeqian, Deng Weiming. Tail anchoring technique of vertebroplasty in treatment of osteoporotic vertebral compression fractures with intravertebral cleft: a finite element analysis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2145-2152. |
| [2] | Zeng Xuan, Weng Rui, Ye Shicheng, Tang Jiadong, Mo Ling, Li Wenchao. Two lumbar rotary manipulation techniques in treating lumbar disc herniation: a finite element analysis of biomechanical differences [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2153-2161. |
| [3] | Cheng Qisheng, Julaiti·Maitirouzi, Xiao Yang, Zhang Chenwei, Paerhati·Rexiti. Finite element analysis of novel variable-diameter screws in modified cortical bone trajectory of lumbar vertebrae [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2162-2171. |
| [4] | Liu Wenlong, Dong Lei, Xiao Zhengzheng, Nie Yu. Finite element analysis of tibial prosthesis loosening after fixed-bearing unicompartmental knee arthroplasty for osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2191-2198. |
| [5] | Chen Long, Wang Xiaozhen, Xi Jintao, Lu Qilin. Biomechanical performance of short-segment screw fixation combined with expandable polyetheretherketone vertebral body replacement in osteoporotic vertebrae [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2226-2235. |
| [6] | Hu Xiongke, Liu Shaohua, Tan Qian, Liu Kun, Zhu Guanghui. Shikonin intervention with bone marrow mesenchymal stem cells improves microstructure of femur in aged mice [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1609-1615. |
| [7] | Wen Guangwei, Zhen Yinghao, Zheng Taikeng, Zhou Shuyi, Mo Guoye, Zhou Tengpeng, Li Haishan, Lai Yiyi. Effects and mechanisms of isoginkgetin on osteoclastogenesis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(6): 1348-1358. |
| [8] | Wu Zhilin, , He Qin, Wang Pingxi, Shi Xian, Yuan Song, Zhang Jun, Wang Hao . DYRK2: a novel therapeutic target for rheumatoid arthritis combined with osteoporosis based on East Asian and European populations [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(6): 1569-1579. |
| [9] | Zhang Haiwen, Zhang Xian, Xu Taichuan, Li Chao. Bibliometric and visual analysis of the research status and trends of senescence in osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(6): 1580-1591. |
| [10] | Lai Jiaming, , Song Yuling, Chen Zixi, Wei Jinghuan, Cai Hao, , Li Guoquan, . Screening of diagnostic markers for endothelial cell Senescence in mice with radiation-induced heart disease and analysis of immune infiltration [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(6): 1450-1463. |
| [11] | Huang Jie, Zeng Hao, Wang Wenchi, Lyu Zhucheng, Cui Wei. Visualization analysis of literature on the effect of lipid metabolism on osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(6): 1558-1568. |
| [12] | Yang Zhijie, Zhao Rui, Yang Haolin, Li Xiaoyun, Li Yangbo, Huang Jiachun, Lin Yanping, Wan Lei, HuangHongxing. Postmenopausal osteoporosis: predictive values of muscle mass, grip strength, and appendicular skeletal muscle index [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(5): 1073-1080. |
| [13] | Zhou Jian, Zhang Tao, Zhou Weili, Zhao Xingcheng, Wang Jun, Shen Jie, Qian Li, Lu Ming. Effects of resistance training on quadriceps mass and knee joint function in patients with osteoporosis and sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(5): 1081-1088. |
| [14] | Cao Wenqi, Feng Xiuzhi, Zhao Yi, Wang Zhimin, Chen Yiran, Yang Xiao, Ren Yanling. Effect of macrophage polarization on osteogenesis-angiogenesis coupling in type 2 diabetic osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(4): 917-925. |
| [15] | Zeng Hao, Sun Pengcheng, Chai Yuan, Huang Yourong, Zhang Chi, Zhang Xiaoyun. Association between thyroid function and osteoporosis: genome-wide data analysis of European populations [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(4): 1019-1027. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||