Chinese Journal of Tissue Engineering Research ›› 2017, Vol. 21 ›› Issue (30): 4915-4920.doi: 10.3969/j.issn.2095-4344.2017.30.026
Research progress in the stability of miniscrews as anchorage
- 1Guangxi Medical University, Nanning 530000, Guangxi Zhuang Autonomous Region, China; 2Stomatological Hospital of Guangxi Medical University, Nanning 530000, Guangxi Zhuang Autonomous Region, China
-
Received:2017-08-23Online:2017-10-28Published:2017-11-07 -
Contact:Huang Xuan-ping, M.D., Chief physician, Professor, Stomatological Hospital of Guangxi Medical University, Nanning 530000, Guangxi Zhuang Autonomous Region, China -
About author:Chen Yan-qu, Studying for master’s degree, Guangxi Medical University, Nanning 530000, Guangxi Zhuang Autonomous Region, China -
Supported by:the Natural Science Foundation for the Youth of Guangxi Zhuang Autonomous Region, No. 2015GXNSFBA139141; the Scientific Research and Technological Development Project of Guangxi Zhuang Autonomous Region, No. 1598012-18
CLC Number:
Cite this article
Chen Yan-qu, Tang Min, Huang Xuan-ping.
share this article
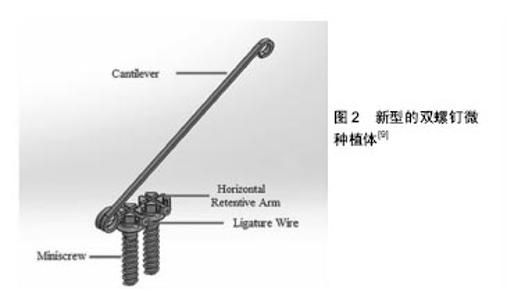
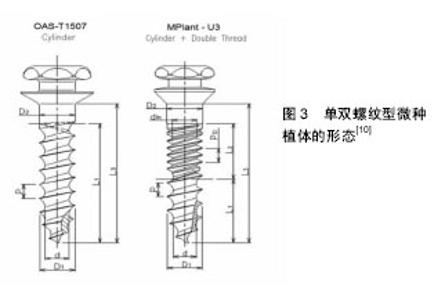
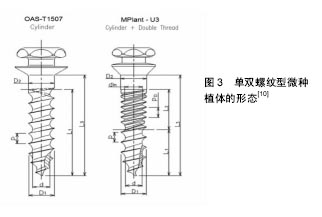
2.1 微种植体自身因素 2.1.1 微种植体的材质 纯钛和钛合金微种植体支抗目前广泛应用于正畸临床治疗,但由于其强度不够,植入以及承受较大力时易于折断[2],因而有研究尝试采用延展性及强度较好的不锈钢作为微种植体支抗,并且发现其良好的稳定性能满足正畸治疗需要[2]。但是Brown等[3]提出不锈钢微种植体存在耐腐蚀性能低,释放离子易引起微种植体周围炎症等缺点。并且雷菲菲等[4]研究发现不锈钢相较于钛合金脱落率较高,可能更有利于植入骨质相对致密且骨皮质较厚的部位。 2.1.2 微种植体的形态设计 Nienkemper等[5]研究发现其植入物稳定性随植入深度的增加而显著增大,但当植入深度为4.0-5.0 mm时,稳定性差异不大。Melo等[1]通过总结10年来患者植入微种植体的情况,发现较短(5 mm)的微种植体失败率较高。Sivamurthy等[6]研究发现直径为1 mm的微种植体可产生显著高的应力,不能安全运用于临床。Shen等[7]研究发现微种植体直径的增加有利于提高其稳定性,其螺纹高度和螺距的变化对骨应力也有影响,并且在减小骨应力和增强微种植体稳定性方面螺纹高度比螺距的影响更明显。颜丹等[8]研究认为螺距为0.5 mm时,微种植体-骨界面、微种植体本身应力和位移最小,临床稳定性最高。 Seifi等[9]设计了一种新型的双螺钉微种植体,并通过研究发现其相较于传统微种植体,增大了与骨组织的接触面积,更利于应力在各个方向的分散,从而抵消了不必要的微种植体移动,提高了微种植体的稳定性(图2)。Cha等[10]设计的双螺纹微种植体,相较于传统单螺纹微种植体具有更好的初始稳定性,但可能会导致在厚的皮质骨层的骨植入界面上的生理骨重塑限制。过多的压力发生在骨植入界面层(图3)。结合国内外学者的大量研究发现,增加微种植体的长度、直径和螺距以及双螺钉的设计都增大了微种植体-骨界面的面积,有利于骨结合,从而提高了微种植体的稳定性。但同时应考虑微种植体植入后患者的舒适度,微种植体不宜设计过大。因此对于微种植体的最优形态设计仍需进一步研究。 2.2 微种植体周围炎 微种植体被腐蚀是导致炎症发生的原因之一,而Knutson等[11]研究发现唾液中的氟会降低微种植体的抗腐蚀性能。研究发现对微种植体的表面进行处理,有利于提高其生物相容性,提高微种植体的稳定性,减少微种植体植入后的炎症反应。Tabuchi等[12]研究表明,微种植体植入后周围再生的骨组织在紫外线处理微螺钉12 min后比未处理的微螺钉周围更完整和连续,由此认为紫外线处理增加了钛合金微螺钉的生物活性,在即使没有对微螺钉表面形态改变的情况下也提高了正畸微螺钉的锚固能力。Yanaguizawa等[13]研究发现低水平的激光治疗(二极管激光660 nm,40 mW,1 min,总能量2.4 J)可以减轻种植体周围最初的炎症反应。Garcez等[14]实验显示低强度激光治疗可增加正畸微螺钉的成功率。激光能使钛等金属表面瞬间融化,从而提高种植体表面活性。国内学者采用激光加微弧氧化处理种植体表面,使纯钛表面形成一层全新的、具有弹坑状微孔和多微孔结构的二氧化钛膜,提高了种植体表面的骨沉积速率,促进骨结合。然而其内在影响机制仍有待进一步研究[15]。周宏志等[16]仅对种植体表面行微弧氧化处理,发现同样能显著提高纯钛种植体的生物相容性和骨引导性。同时,Ganzorig等[17]和Miura等[18]的研究发现低强度脉冲超声的应用增加了骨与微螺钉的接触,减少了微种植体的移动,从而促进骨愈合,刺激微螺钉周围的骨形成,增强其初始稳定性。Jang等[19]和Oh等[20]研究发现经过阳极氧化、循环预钙化和热处理使微螺钉形成覆盖有紧密磷灰石状膜的纳米管TiO2层的致密表面阵列,这增强了其骨整合能力,并提高了其稳定性。丁元圣等[21]研究发现含氟羟基磷灰石涂层钛合金与钛合金正畸微种植体相比,植入后成骨细胞更活跃,短期内骨结合更好,而炎症发生时,肿瘤坏死因子α含量升高缓慢,降低迅速,炎症持续时间短,骨重建及软组织的愈合也快。由此认为含氟羟基磷灰石涂层钛合金微种植体的骨组织相容性较好,对种植体周围炎能起到一定的抑制作用。武秀萍等[22]研究发现对微种植体表面进行酸蚀喷砂处理可以促进微螺钉植入后骨整合的形成,具有良好的初期稳定性。为避免微种植体与口腔黏膜摩擦产生损伤导致炎症的发生,Marquezan等[23]设计了一种以光固化材料覆盖于微种植体头部的临时物理屏障。综上,纯钛种植体生物活性低,无法与骨表面高效结合,且抗菌性差。因此对钛种植体进行表面改性,可提高钛种植体表面物理性能、化学性能和生物性能,而这一直是国内外学者研究的热点。 2.3 微种植体的植入方式 微种植体的植入方式可以分为助攻型和自攻型。由于自攻型微种植体直接将钉旋入牙槽骨,对骨组织产生挤压,形成较好的机械结合,而利于微种植体与骨组织之间的紧密结合。而助攻型微种植体需在手术前预钻,在植入过程中反复旋入旋出,扩大了洞口的直径,导致微种植体与骨组织不能紧密接触[24]。所以一直以来有报道自攻型微种植体稳定性高于助攻型微种植体[25]。但是亦有相反的观点出现,邹毅军[26]的研究显示助攻型的成功率高于自攻型,分析其可能的原因是由于患者骨密度过高,自攻型术式在植入中产热过多,出现骨坏死。助攻型术式可以一定角度植入,增加了与骨皮质的接触面积,而自攻型术式为避免与骨面打滑而选择了垂直植入方式。同时Iijima等[27]研究发现在没有预钻孔的高密度骨质区植入微种植体有骨折的风险。而Sharifi等[28]的动物实验研究表明微种植体的稳定性不受植入方式的影响。因此在正畸临床治疗中,由于自攻型微种植体的植入方式更为简单,手术时间相较于助攻型短,并且降低了损伤牙根的风险,更倾向于选择自攻型术式。但是也应考虑对于骨组织密度较高的区域,依旧需要使用助攻型微种植体,以避免盲目自攻而导致微种植体折断、骨折、植入道偏斜和植入过程中产热过多引起骨坏死。 2.4 微种植体的植入角度 目前关于微种植体以何种角度植入牙槽骨最有利于保证其稳定性这一问题存在不同观点。基于生物力学的应力遮挡原理,骨皮质因密度明显高于骨松质而成为应力的主要承受区,因此种植体骨界面的应力主要集中在骨皮质区。实验结果也表明与松质骨相比皮质骨显示出较高的应变值[29]。所以随着种植体植入角度的减小,种植体颈部与骨皮质接触面积的增大,应力能在更大范围内的骨皮质扩散,增强了种植体的稳定性。Sivamurthy等[6]的研究表明以30°植入可减少应力提高微种植体的稳定性,再次验证了这个观点。另一方面,董晶等[30]和于海璐等[31]的研究发现,在微种植体锥度一定时,随着植入角度由90°减小,骨皮质应力、种植体应力和位移均呈下降趋势;当植入角度在60°时出现最小值;随着角度进一步减小,应力与位移值又开始增大,30°时出现最大值。可能由于植入角度由60°到90°变化时,微种植体与骨皮质接触面积逐渐变小,导致应力集中,位移峰值呈增大趋势。植入角度由30°到60 °逐渐变大时,微种植体嵌入骨内的长度逐渐增大,集中的应力得到分散、位移相应减小。但是Lee等[32]和Perillo等[33]的研究都认为微种植体以90°植入颌骨时,骨小梁和骨皮质都受到最小应力。同时Araghbidikashani等[34]的研究表明施加的力的方向对微螺钉在各种植入角度的稳定性具有显著影响。当通过剪切力加载微螺钉时在45°植入获得最高的初始稳定性值,当施加拉力时在90°植入获得最高的主要稳定性值。 2.5 微种植体的植入部位 由于微种植体体积小,根据矫治需要,颌骨的大部分区域均可植入微种植体,理想部位应有一定的骨皮质厚度、足够的附着龈同时避开唇颊系带。骨质密度是影响微种植钉稳定性的一个重要因素[35]。Veli等[36]通过比较青少年颊皮质骨在不同垂直骨面型的研究发现由于下颌平面角大的患者磨牙区的骨密度较低和骨皮质较薄,所以下颌平面角大的高角型患者微种植体植入的成功率明显低于那些下颌平面角正常的均角型或下颌平面角较小的低角型患者。雷菲菲等[4]的研究也发现高角患者的微种植体脱落率较高。曹小青等[37]研究表明上颌骨植入的稳定性高于下颌骨。与以往所认为的由于上颌骨相对于下颌骨而言具有较薄的皮质骨厚度以及骨密度,所以下颌骨的微种植钉的稳定性高于上颌骨而不同[38]。并分析了其可能的原因有:①下颌骨的血运和营养供给不如上颌骨,随着愈合时间的延长,上颌骨取得更高的骨整合从而获得更好的后期稳定性;②下颌骨的生理结构相较于上颌更易感染;③下颌骨的骨密度高可能会造成更高的植入扭矩,同时植入过程中产热过多,也会影响微种植体周围的骨愈合从而影响其的骨整合。同时皮质骨厚度也是影响微种植体稳定性的因素[35]。邹双双等[39]的研究表明颊侧皮质骨厚度由牙槽嵴顶向根尖方向有逐渐增大的趋势,越靠近根方,植入时可以获得更好的初期稳定性。 大量研究表明微种植体植入过程中触及或者损伤邻牙牙根是导致微种植体失败的重要原因[40]。因此有必要明确微种植体植入后距牙根的安全距离。Garg等[41]的研究发现微种植体植入后在正畸加载过程中,并不是完全静止不动的,因此建议微种植体植入后距离临近牙根1.5 mm以上。Bae等[42]对需植入微种植体的正畸患者进行CT扫描和牙合扫描三维数据重建,在计算机辅助下设计微种植体植入导板。相较于仅仅依靠传统X射线片进行定位植入,三维导向植入可以使微种植体支抗准确地达到最佳植入部位,从而有效降低种植体支抗的失败率。之后Qiu等[43]也进行了基于锥形束CT影像进行正畸种植体导板的设计,并在临床上完成了微种植体的植入,初步研究显示导板引导下种植体植入安全稳定。 微种植体植入过程中损伤上颌窦也会导致失败,因此Mitsuru等[44]建议为避免上颌窦穿孔,应保证窦底厚度为6 mm或更大。李文艳等[45]建议为保证微种植体植入时颧牙槽嵴骨厚度至少6 mm且不触及上颌窦底壁,理想的植入部位为距离上颌参考平面13-16 mm,植入角度为55°-75°。 2.6 微种植体植入后的加载 微种植体加载的时机一直以来都是一个充满争议的问题。传统种植学理论认为应延时加载,因为种植体必须有一定时间的“无负载愈合期”,以期达到骨整合,从而保证微种植体的长期稳定性。基于Brunski的“微动度”理论[46],微种植体与骨组织间有100 μm内的微动度不会明显影响骨整合,因此具有良好初始稳定性的种植体在即刻负载的情况下能够形成良好的骨结合。Garg等[41]研究发现微种植体植入后的即刻加载是可行的。Bayani等[47]研究显示虽然在即刻负荷下存在去除转矩值降低的趋势,但是其在统计学上不显着。Migliorati等[48]研究发现微种植体植入后1周,稳定性相较于刚植入时有明显降低,但是即刻加载的微种植体稳定性高于延迟加载组。亦有学者提出早期加载的观点,认为微种植体的骨整合是必要的,但并不需要达到完全,缩短无负载愈合期得到部分骨整合不会影响微种植体的稳定性。Catharino等[49]发现种植钉植入15 d以后加载相较于即刻加载更利于微种植体的稳定性,并且骨结合和皮质骨的增加是与时间相关的。而范莉等[50]的研究认为微种植体植入后1 周,稳定性下降,6 周时趋于稳定。6 周后,加载正畸力对稳定性无影响。李金平等[51]的实验结果也显示延时加载微种植体的成功率明显高于早期加载,而即刻加载与延时加载成功率无明显不同。再次从临床上证实了微种植体植入后存在稳定性危险期的观点,其产生的原因可能为微种植体植入过程中产生骨损伤,破骨细胞产生,而成骨细胞建立的编织骨界面仍薄弱,生物稳定性还未建成。但对于危险期的具体时间仍有待进一步研究。吴也可等[52]研究发现,间断相比持续应力加载更有利于微种植体稳定性的获得,且12 h的加载周期比24 h更能促进骨-微种植体结合。因为早期微种植体的微动导致骨-种植体界面应力可能破坏骨与微种植体界面的形成,而间断力持续的时间更短,产生的微动和裂纹也更少。但是加载过程中的最佳间歇时间以及理想的加载/间歇循环频率仍需继续研究。 "
| [1]Melo AC, Andrighetto AR, Hirt SD, et al. Risk factors associated with the failure of miniscrews - A ten-year cross sectional study. Braz Oral Res. 2016;30(1):e124. [2]峥嵘,陈岩,包雪梅,等.不锈钢和钛合金微种植体稳定性的生物力学实验研究[J].内蒙古医科大学学报,2016,38(3):195-199.[3]Brown RN, Sexton BE, Gabriel Chu TM, et al. Comparison of stainless steel and titanium alloy orthodontic miniscrew implants: a mechanical and histologic analysis. Am J Orthod Dentofacial Orthop. 2014;145(4):496-504. [4]雷菲菲,梁芮,张晓洁,等.两种微螺钉种植体支抗在上颌后牙根间区的稳定性研究[J].口腔医学研究,2016,32(5):531-533.[5]Nienkemper M, Santel N, Hönscheid R, et al. Orthodontic mini-implant stability at different insertion depths : Sensitivity of three stability measurement methods. J Orofac Orthop. 2016;77(4):296-303.[6]Sivamurthy G, Sundari S. Stress distribution patterns at mini-implant site during retraction and intrusion--a three-dimensional finite element study. Prog Orthod. 2016;17:4.[7]Shen S, Sun Y, Zhang C, et al. Bivariate optimization of orthodontic mini-implant thread height and pitch. Int J Comput Assist Radiol Surg. 2015;10(1):109-116. [8]颜丹,张锡忠,王增全,等.螺距对支抗微种植体—骨界面影响的三维有限元分析[J].国际口腔医学杂志,2015,42(5):557-561.[9]Seifi M, Matini NS. Evaluation of primary stability of innovated orthodontic miniscrew system (STS): An ex-vivo study. J Clin Exp Dent. 2016;8(3):e255-259.[10]Cha JY, Hwang CJ, Kwon SH, et al. Strain of bone-implant interface and insertion torque regarding different miniscrew thread designs using an artificial bone model. Eur J Orthod. 2015;37(3):268-274. [11]Knutson KJ, Berzins DW. Corrosion of orthodontic temporary anchorage devices. Eur J Orthod. 2013;35(4):500-506. [12]Tabuchi M, Ikeda T, Nakagawa K, et al. Ultraviolet photofunctionalization increases removal torque values and horizontal stability of orthodontic miniscrews. Am J Orthod Dentofacial Orthop. 2015;148(2):274-282. [13]Yanaguizawa MS, Suzuki SS, Martinez EF, et al. Effects of Low-Level Laser Therapy in Orthodontic Patients on Immediate Inflammatory Response After Mini-Implants Insertion: A Preliminary Report. Photomed Laser Surg. 2017; 35(1):57-63. [14]Garcez AS, Suzuki SS, Martinez EF, et al. Effects of low-intensity laser therapy over mini-implants success rate in pigs. Lasers Med Sci. 2015;30(2):727-732.[15]郭泽鸿,周磊,容明灯,等.纯钛种植体激光-微弧氧化表面处理对早期骨结合的影响[J].口腔颌面外科杂志,2014,24(3):208-213.[16]周宏志,刘琳,陈小冬,等.荧光标记法对“脑回形”微弧氧化表面种植体早期骨结合的评价[J].口腔颌面修复学杂志, 2016,17(5): 271-276.[17]Ganzorig K, Kuroda S, Maeda Y, et al. Low-intensity pulsed ultrasound enhances bone formation around miniscrew implants. Arch Oral Biol. 2015;60(6):902-910. [18]Miura K, Motoyoshi M, Inaba M, et al. A preliminary study of the effects of low-intensity pulsed ultrasound exposure on the stability of orthodontic miniscrews in growing rats. Eur J Orthod. 2014;36(4):419-424.[19]Jang I, Shim SC, Choi DS, et al. Effect of TiO2 nanotubes arrays on osseointegration of orthodontic miniscrew. Biomed Microdevices. 2015;17(4):76. [20]Oh EJ, Nguyen TD, Lee SY, et al. Enhanced compatibility and initial stability of Ti6Al4V alloy orthodontic miniscrews subjected to anodization, cyclic precalcification, and heat treatment. Korean J Orthod. 2014;44(5):246-253.[21]丁元圣,赵玥,郭睿,等.含氟羟基磷灰石涂层对正畸微种植体骨结合及周围炎的影响[J].实用口腔医学杂志,2016,32(5): 624-626.[22]武秀萍,Hee Moonkyung,李冰,等.微种植体表面酸蚀喷砂处理对周围骨组织NGF表达的影响[J].山西医科大学学报,2015, 46(3):231-233,283.[23]Marquezan M, de Freitas AO, Nojima LI. Miniscrew covering: an alternative to prevent traumatic lesions. Am J Orthod Dentofacial Orthop. 2012;141(2):242-244. [24]沙焱,吕超贤,韩建民,等.助攻式、自攻式微种植体支抗植入法在微种植体矫治错牙合畸形中的应用[J].山东医药, 2015,55(11): 75-76.[25]Tepedino M, Masedu F, Chimenti C. Comparative evaluation of insertion torque and mechanical stability for self-tapping and self-drilling orthodontic miniscrews - an in vitro study. Head Face Med. 2017;13(1):10.[26]邹毅军.探讨用两种不同方法植入微种植体支抗的稳定性[J].当代医药论丛,2014(1):135-136.[27]Iijima M, Muguruma T, Kawaguchi M, et al. In vivo degradation of orthodontic miniscrew implants: surface analysis of as-received and retrieved specimens. J Mater Sci Mater Med. 2015;26(2):71. [28]Sharifi M, Ghassemi A, Bayani S. Effect of insertion method and postinsertion time interval prior to force application on the removal torque of orthodontic miniscrews. Int J Oral Maxillofac Implants. 2015;30(1):35-40. [29]Poorsattar Bejeh Mir A, Ravadgar M, Poorsattar Bejeh Mir M. Optimized orthodontic palatal miniscrew implant insertion angulation: a finite element analysis. Int J Oral Maxillofac Implants. 2015;30(1):e1-9.[30]董晶,张哲湛,周国良.Ⅱ类骨质中正畸微种植体锥度及植入角度对支抗稳定性影响的三维有限元分析[J].华西口腔医学杂志, 2014,32(1):13-17.[31]于海璐,蔡兴伟,马龙,等.不同植入角度及载荷方向对微种植体稳定性影响的三维有限元分析[J].解放军医学院学报, 2016,37(3): 261-265,270.[32]Lee J, Kim JY, Choi YJ, et al. Effects of placement angle and direction of orthopedic force application on the stability of orthodontic miniscrews. Angle Orthod. 2013;83(4):667-673.[33]Perillo L, Jamilian A, Shafieyoon A, et al. Finite element analysis of miniscrew placement in mandibular alveolar bone with varied angulations. Eur J Orthod. 2015;37(1):56-59. [34]Araghbidikashani M, Golshah A, Nikkerdar N, et al. In-vitro impact of insertion angle on primary stability of miniscrews. Am J Orthod Dentofacial Orthop. 2016;150(3):436-443. [35]Migliorati M, Drago S, Schiavetti I, et al. Orthodontic miniscrews: an experimental campaign on primary stability and bone properties. Eur J Orthod. 2015;37(5):531-538. [36]Veli I, Uysal T, Baysal A, et al. Buccal cortical bone thickness at miniscrew placement sites in patients with different vertical skeletal patterns. J Orofac Orthop. 2014;75(6):417-429.[37]曹小青,张莉,刘龙坤.正畸用微种植钉种植成功的多因素分析[J].口腔医学研究,2016,32(1):79-82.[38]莫嘉骥,姒蜜思,周仲豪,等.Straumann种植体早期稳定性相关因素的研究[J].中国口腔颌面外科杂志,2012,10(5):381-385.[39]邹双双,雷勇华,张亚梅,等.微种植体植入初期稳定性:错颌上颌后牙区颊侧骨皮质厚度分析[J].中国组织工程研究, 2015, 19(12):1837-1841.[40]Shan LH, Guo N, Zhou GJ, et al. Finite Element Analysis of Bone Stress for Miniscrew Implant Proximal to Root Under Occlusal Force and Implant Loading. J Craniofac Surg. 2015;26(7):2072-2076.[41]Garg KK, Gupta M. Assessment of stability of orthodontic mini-implants under orthodontic loading: A computed tomography study. Indian J Dent Res. 2015;26(3):237-243.[42]Bae MJ, Kim JY, Park JT, et al. Accuracy of miniscrew surgical guides assessed from cone-beam computed tomography and digital models. Am J Orthod Dentofacial Orthop. 2013;143(6): 893-901.[43]Qiu LL, Li S, Bai YX. Preliminary safety and stability assessment of orthodontic miniscrew implantation guided by surgical template based on cone-beam CT images. Zhonghua Kou Qiang Yi Xue Za Zhi. 2016;51(6):336-340.[44]Motoyoshi M, Sanuki-Suzuki R, Uchida Y, et al. Maxillary sinus perforation by orthodontic anchor screws. J Oral Sci. 2015;57(2):95-100. [45]李文艳,彭嘉琪,林巍,等.微种植体颌骨植入区的CBCT测量分析[J].口腔医学,2015,35(1):29-33.[46]Brunski JB. Biomechanical factors affecting the bone-dental implant interface. Clin Mater. 1992;10(3):153-201.[47]Bayani S, Masoomi F, Aghaabbasi S, et al. Evaluation of the Effect of Platelet-Released Growth Factor and Immediate Orthodontic Loading on the Removal Torque of Miniscrews. Int J Oral Maxillofac Implants. 2016;31(2):471-477.[48]Migliorati M, Drago S, Gallo F, et al. Immediate versus delayed loading: comparison of primary stability loss after miniscrew placement in orthodontic patients-a single-centre blinded randomized clinical trial. Eur J Orthod. 2016;38(6): 652-659. [49]Catharino PC, Dominguez GC, Pinto Ddos S Jr, et al. Histologic, histomorphometric, and radiographic monitoring of bone healing around in-office-sterilized orthodontic mini-implants with or without immediate load: study in rabbit tibiae. Int J Oral Maxillofac Implants. 2014;29(2):321-330.[50]范莉,缪喆,唐国华.正畸微种植体稳定性的临床共振频率分析[J].上海口腔医学,2014,23(5):614-618.[51]李金平,时超,周冠军,等.微种植体植入扭矩及载荷时机对稳定性的影响[J].河北医药,2015,37(24):3740-3742.[52]吴也可,赵立星.持续或间断应力加载下正畸微种植体稳定性的组织形态学和生物力学分析[J].口腔医学研究, 2016,32(4): 326-330. |
| [1] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [2] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [3] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [4] | He Yunying, Li Lingjie, Zhang Shuqi, Li Yuzhou, Yang Sheng, Ji Ping. Method of constructing cell spheroids based on agarose and polyacrylic molds [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 553-559. |
| [5] | He Guanyu, Xu Baoshan, Du Lilong, Zhang Tongxing, Huo Zhenxin, Shen Li. Biomimetic orientated microchannel annulus fibrosus scaffold constructed by silk fibroin [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 560-566. |
| [6] | Zhang Jianguo, Chen Chen, Hu Fengling, Huang Daoyu, Song Liang. Design and biomechanical properties of dental implant pore structure based on three-dimensional finite element analysis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 585-590. |
| [7] | Chen Xiaoxu, Luo Yaxin, Bi Haoran, Yang Kun. Preparation and application of acellular scaffold in tissue engineering and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 591-596. |
| [8] | Kang Kunlong, Wang Xintao. Research hotspot of biological scaffold materials promoting osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 597-603. |
| [9] | Shen Jiahua, Fu Yong. Application of graphene-based nanomaterials in stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 604-609. |
| [10] | Zhang Tong, Cai Jinchi, Yuan Zhifa, Zhao Haiyan, Han Xingwen, Wang Wenji. Hyaluronic acid-based composite hydrogel in cartilage injury caused by osteoarthritis: application and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 617-625. |
| [11] | Li Hui, Chen Lianglong. Application and characteristics of bone graft materials in the treatment of spinal tuberculosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 626-630. |
| [12] | Gao Cangjian, Yang Zhen, Liu Shuyun, Li Hao, Fu Liwei, Zhao Tianyuan, Chen Wei, Liao Zhiyao, Li Pinxue, Sui Xiang, Guo Quanyi. Electrospinning for rotator cuff repair [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 637-642. |
| [13] | Guan Jian, Jia Yanfei, Zhang Baoxin , Zhao Guozhong. Application of 4D bioprinting in tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 446-455. |
| [14] | Huang Bo, Chen Mingxue, Peng Liqing, Luo Xujiang, Li Huo, Wang Hao, Tian Qinyu, Lu Xiaobo, Liu Shuyun, Guo Quanyi . Fabrication and biocompatibility of injectable gelatin-methacryloyl/cartilage-derived matrix particles composite hydrogel scaffold [J]. Chinese Journal of Tissue Engineering Research, 2022, 10(16): 2600-2606. |
| [15] | Liu Jiali, Suo Hairui, Yang Han, Wang Ling, Xu Mingen. Influence of lay-down angles on mechanical properties of three-dimensional printed polycaprolactone scaffolds [J]. Chinese Journal of Tissue Engineering Research, 2022, 10(16): 2612-2617. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||