Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (2): 298-303.doi: 10.3969/j.issn.2095-4344.2956
Previous Articles Next Articles
Research strategy of gene editing technology in the gene treatment of osteoarthritis
Ma Dujun1, Peng Liping1, Chen Feng2, Jiang Shunwan1, Jiang Jinting1, Gao Kun1, Lin Zhanpeng1
- 1Department of Orthopedics, The Fourth Clinical Medical College of Guangzhou University of Traditional Chinese Medicine, Shenzhen 518033, Guangdong Province, China; 2Department of Orthopedics, Ruikang Hospital Affiliated to Guangxi University of Traditional Chinese Medicine, Nanning 530000, Guangxi Zhuang Autonomous Region, China
-
Received:2020-02-24Revised:2020-03-16Accepted:2020-05-09Online:2021-01-18Published:2020-11-21 -
Contact:Ma Dujun, Department of Orthopedics, The Fourth Clinical Medical College of Guangzhou University of Traditional Chinese Medicine, Shenzhen 518033, Guangdong Province, China -
About author:Ma Dujun, Master, Attending physician, Department of Orthopedics, The Fourth Clinical Medical College of Guangzhou University of Traditional Chinese Medicine, Shenzhen 518033, Guangdong Province, China -
Supported by:the National Natural Science Foundation of China, No. 81804124; the Natural Science Foundation of Guangdong Province, No. 2018A0303130138
CLC Number:
Cite this article
Ma Dujun, Peng Liping, Chen Feng, Jiang Shunwan, Jiang Jinting, Gao Kun, Lin Zhanpeng. Research strategy of gene editing technology in the gene treatment of osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(2): 298-303.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
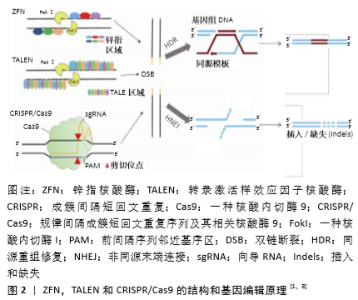
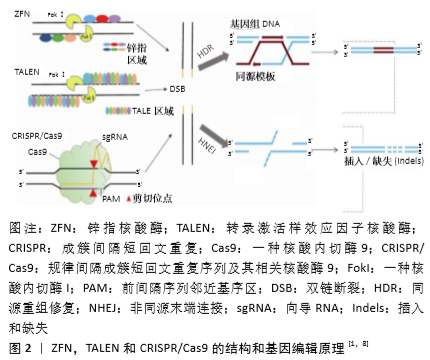
2.1 基因编辑技术概述 基因编辑技术可以实现对特定靶点基因序列进行目的基因编辑,敲入或敲除基因,这项技术是研究基因治疗疾病的最有效手段[5]。基因序列靶点基因编辑工具目前主要有:第1代基因编辑器锌指核酸酶(Zincfinger nucleases,ZFN)、第2代基因编辑器转录激活样效应因子核酸酶(Transcription activator-like effector nucleases,TALEN)和第3代基因编辑器成簇间隔短回文重复(Clustered regularly interspaced short palindromic repeats,CRISPR)[6],此3者编辑共同原理特点是核酸内切酶在靶点基因序列特定部位进行靶向酶切,触发DNA双链断裂。双链断裂时细胞内源中存在2种天然的DNA损伤应答机制,分别为同源重组修复和非同源末端连接修复。在有同源序列参加时,细胞发生双链断裂可以实现同源重组修复,进行定点基因序列外源基因的插入或靶基因修饰,反之细胞易利用非同源末端连接进行DNA的修复。相比于ZFN和TALEN,CRISPR/Cas9 基因编辑系统以其简易性、高效性及安全性被认为是当前最有潜力的基因编辑工具[7]。以上3种基因编辑技术的靶点基因识别位点、人工设计方法及作用机制等均有不同,见图2。"
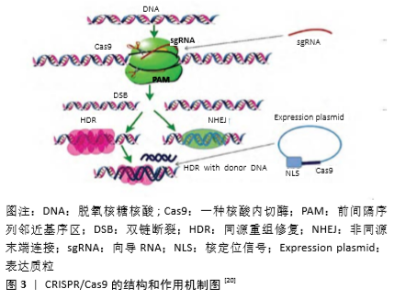
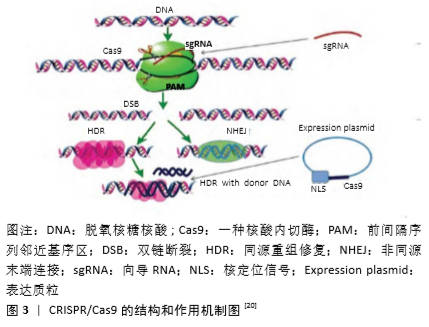
2.1.1 ZFN技术 ZFN是一种人工改造的核酸内切酶,是基因编辑技术普遍使用的开拓者,与靶点基因识别模式是蛋白质-DNA,与靶点基因结合特异性强、无免疫原性、结构小容易转染。特异性的DNA结合域和非特异性的切割域是ZFN的主要构建元件,其中结合域由一系列串联的具有Cys2-His2结构的锌指蛋白构成,不同锌指蛋白的类型和基序是ZFN识别不同DNA序列的主要原因。切割域由核酸内切酶FokI组成[9]。有2个ZFN在基因靶点序列两边识别结构域,当两个结合位点的间距为6-8 bp时,FokI单体两两自动结合形成二聚体,从而具有酶切功能,执行对靶点基因序列进行定点切割和编辑功能。 2.1.2 TALEN技术 TALEN类似ZFN具有FokI内切酶和特异性的结合域及非特异性的切割域,也是人工改造的核酸内切酶,不同点是,TALEN的结合域是人工改造的TALE蛋白,但是对靶标基因组序列进行识别、切割原理同样类似ZFN,从而实现靶点序列基因编辑。TALEN识别模式是蛋白质-DNA,结合域是重复的转录激活因子样效应物蛋白,潜在靶点很少,可操作性一般,基因编辑特异性较强、容易编辑,但结构较大,转染比较困难,这些限制了该技术的发展。由于细胞内源DNA损伤修复机制不同,导致TALEN进入核内结合DNA产生突变的能力也会存在差[10]。TALEN设计及装配太过复杂,传统分子克隆、人工合成等基因研究技术不能很好地装配多个重复序列的TALEN,目前主要是借助独立连接克隆技术、高通量固相组装技术和“Golden Gate”分子克隆等技术进行快捷的装配[11],也可通过基因编辑生物公司直接定制购买设计好的TALE阵列。近年多项研究利用TALEN技术成功的对斑马鱼、人、鼠及拟南芥等动植物基因组进行编辑,表明TALEN已经成为基因治疗研究和基因功能研究的强大工具[8]。 2.1.3 CRISPR/Cas9技术 CRISPR是一种发现于细菌和古生菌中由RNA诱导的获得性免疫系统,用来抵抗外来病毒或质粒的入侵[12]。2013年,《Science 》等杂志报道了CRISPR技术的系列研究,促使该技术快速成为基因组学研究的有力工具,并成为当前研究热点[13]。目前CRISPR技术已经在拟南芥、大肠杆菌、酵母、人、猪、鼠、猴和斑马鱼等不同生物中得到广泛的应用,成功验证了这项技术的优越性,内容涉及基因靶向修饰、基因调控表达、单基因敲除、多基因敲除、基因大片段敲除以及外源基因插入等范畴[14-15]。王昕[16]用CRISPR技术成功构建特定Cyp系列基因敲除大鼠模型,转运体P-gp和Oatp1b2基因敲除大鼠模型,并对其基因型和代谢功能进行系统验证和评价,成功构建了大鼠药物代谢模型构建大鼠药物代谢模型。2014年南京大学模式动物研究所的黄行许博士、南京医科大学的沙家豪教授,以及云南省灵长类生物医学重点实验室季维智等研究人员,在2014-12-23的《Cell Research》杂志上发表Letter文章称,继他们成功地利用CRISPR/Cas9系统对孪生食蟹猴进行精确基因组修饰后,在后续的研究中他们进一步证实了猴子生殖系细胞获得了Cas9/RNA介导的基因修饰,这是基因编辑技术首次成功运用到灵长类动物中的报道,揭示该项技术的应用将对基因治疗灵长类动物遗传性疾病的治疗具有里程碑式的意义[17]。 CRISPR/Cas9系统由CRISPR和Cas基因组成[18],具有向导RNA和Cas9核酸内切酶两部分结构,与靶基因识别模式是RNA-DNA,当有与靶基因DNA相互补的RNA序列生成时,Cas内切酶能对互补的靶点DNA双链序列进行定点切割,潜在靶点丰富,操作性简单,但是靶点特异性较低。其中Cas基因家族中的Cas9广泛地应用于该系统中,它是一种天然存在的内切酶,切割过程需要向导RNA提供帮助。向导RNA由CRISPR RNA(crRNA)和反式CRISPR RNA(tracrRNA)组成,目前有很多人工构建的向导RNA。Cas9蛋白与tracrRNA结合,通过碱基配对与crRNA结合形成双链RNA复合体,之后被前间隔序列邻近基序区的序列处理才能成功工作,再由crRNA引导朝向目标序列,介导Cas9核酸酶发现DNA靶序列,并对靶基因的DNA进行切割和编辑,具有高通量、高效率的特点[19],见图3。 2.2 骨关节炎基因治疗研究 骨关节炎是中老年人常见的疾病,患病人数均居世界首位,目前尚缺乏对骨关节炎软骨损伤修复根本有效的治疗方法[21]。软骨基质和软骨细胞是关节软骨组织两大有效构建结构,其中软骨基质是关节软骨细胞的支架部分,是软骨退变的关键。软骨细胞为软骨基质的形成提供代谢产物,两者相互影响形成正向关系。有研究报道,软骨细胞外基质降解和软骨细胞过度凋亡引起的关节软骨退变,是骨关节炎的主要病理机制,很多miRNA及编码基因参与其中[22]。外界或内环境的改变能引起软骨细胞一系列生物学的改变,如减少胶原纤维、蛋白多糖的合成,促进分泌各种炎症蛋白酶,导致多种炎性生物因子增加,加重软骨基质的损伤,这些系列生物学的改变隐藏着复杂的、相互关联的基因组事件。基因编辑应用到临床疾病研究的目的就是为了基因治疗,骨关节炎基因治疗指的是将目的基因片段引入到机体,使目的基因表达产物能够在关节结构中稳定、可控并长期表达,从而发挥修复病变损伤软骨结构和保护软骨组织避免进一步伤害的作用[23]。 2.2.1 骨关节炎基因研究策略 (1) 减轻关节炎症和抑制软骨基质降解:白细胞介素1、肿瘤坏死因子α及一氧化氮等是骨关节炎防治中热点研究炎性因子,其表达量增加时能增加关节炎症和促进软骨结构的病变。白细胞介素1可诱导关节腔结构组织分泌基质金属蛋白酶和前列腺素E2,还能促进Ⅰ型胶原、纤维结合素和滑膜黏附分子合成增多,同时能抑制软骨特异型胶原和蛋白多糖的合成;肿瘤坏死因子α可以抑制蛋白多糖合成,类似白细胞介素1具有促进基质金属蛋白酶和前列腺素E2合成的作用,同时两者还具有协同强化作用[24]。近期有研究表明一氧化氮能显著抑制实验兔软骨细胞中Ⅱ型胶原的合成,可能与一氧化氮减少Ⅱ型胶原α1链mRNA表达量、增强Ⅲ型胶原和一氧化氮合酶表达量相关。目前已经有很多炎症因子抑制剂例如基质金属蛋白酶抑制剂、纤溶酶原激活物抑制剂等开始运用于关节内炎症研究,但仍面临临床不良反应的困扰。低氧调控因子1α有利于软骨组织的改建和发育,在软骨生理活动中发挥着重要的调控作用[25],当软骨缺乏低氧调控因子1α蛋白时会出现大量软骨细胞死亡现象[26]。低氧调控因子1α和血管内皮生长因子是长骨软骨细胞生存和正常发育的必要条件[27],血管内皮生长因子是低氧调控因子1α对软骨发挥作用的靶点基因之一,有利于维持软骨细胞的活力并提高骨代谢[28]。 (2)促进软骨基质合成:多种细胞生长因子和调控因子有益于促进软骨基质的合成,如转化生长因子β1、骨形态发生蛋白2、胰岛素样生长因子1、骨形态发生蛋白7及沉默信息调节因子1等可促进软骨细胞分化和增殖,有利于关节软骨基质的合成与代谢[29-30]。许多生长因子,例如转化生长因子β1在促进软骨基质生成的同时也具有抑制软骨基质退变的双重作用。已有实验证实,在骨关节炎动物模型中将转化生长因子β1转染质粒DNA经胶原介导能够有效抑制炎症和增加蛋白多糖的表达。在犬类动物研究中,有人证实将转化生长因子β1与蛋白酶抑制剂结合,具有明显的抑制软骨退变和促进软骨基质合成的作用。 (3)改善骨关节周围淋巴回流系统:骨关节炎是一种复杂的疾病,发病与自身关节组织炎症递质释放、代谢异常、先天免疫及长期低度炎症相关[31]。近期研究证实该病发病与患病关节局部的淋巴循环改变密切相关[32-34],淋巴管主要位于关节周围、滑膜深层、脂肪垫、关节囊纤维层及韧带周围软组织间隙[35]。淋巴循环系统是二级血管循环替代系统,起到血液循环的“补偿”系统的作用。关节周围淋巴管功能障碍可导致关节肿胀,加剧炎症反应,是引起关节肿胀畸形等症状的主要原因之一[36]。LIANG等[37]采用近红外淋巴成像技术证实不同程度骨关节炎小鼠关节淋巴管数量及类型存在明显差异。ZHOU等[38]将肿瘤坏死因子-转基因小鼠作为慢性关节炎模型,对小鼠注射血管内皮生长因子-C腺相关病毒,3个月后研究表明实验鼠淋巴回流功能增强,淋巴管数量增加,炎症区域减少,软骨细胞损伤和破骨细胞数量减少。 综上可知,通过细胞分子生物学的方法研究各种调控细胞因子来有效防治骨关节炎的病理生理进展具有巨大的临床意义和社会价值,有望持久、有效的改善软骨细胞的内环境,加快软骨基质的代谢平衡。 2.2.2 骨关节炎基因编辑体系递送系统 随着CRISPR技术的新发展,改造基因组变得越来越容易。CRISPR基因组编辑系统,以及TALEN和ZFN编辑系统,正成为生物医学研究、药物发现和开发甚至基因治疗的宝贵工具。然而,对于这些系统中的每一个,有效地进入目标细胞并执行功能需要功能、高效和安全的递送技术。基因编辑载体的选择是骨关节炎基因编辑技术运用到临床的瓶颈也是目前的研究热点。由于发生骨关节炎的常见部位主要是全身负重关节,由此可知关节的局部治疗是基因研究的首选手段。对基因编辑体系的递送方法一般可以归类为病毒或非病毒[1]。病毒的方法是利用病毒载体(例如慢病毒、腺病毒与腺相关病毒)以RNA或DNA形式来包装体系,以促进有效的递送,具有良好的编辑效率和低脱靶率。非病毒递送的方法包括物理方法(例如电穿孔和基于微流控的技术)、基于纳米材料的方法(例如阳离子脂质体和细胞穿透肽)、自组装纳米粒子、质粒、RNA和蛋白质的系统[39]。 在临床试验中,一些病毒载体传递基因的过程已经证明有效,但病毒也存在着严重的安全问题。腺相关病毒是非致病性,有望成为安全的基因载体,但其表达的持久性需要进一步探查。非病毒递送载体比病毒载体具有更安全和更小的毒性及免疫原性,但也存在系列的挑战。如带负电荷的DNA和其它核酸可以被阳离子材料静电络合形成纳米颗粒,随后可被通过的细胞吞噬。迄今为止用于核酸传递的阳离子材料类中,最成功的是天然发生的和合成的脂类(例如脂质体)和聚合物(例如聚乙烯亚胺、环糊精和聚β氨基酯)。在某些情况下,基因组编辑不需要递送载体,如在体外治疗中,机械变形或电穿孔可以在细胞膜上产生短暂的孔,使核酸和蛋白质进入细胞。用于体内治疗时,高浓度及裸核酸的尾静脉水动力注射能有效地转染小鼠肝细胞,但有可能导致致命的急性不良反应,因此在人类中很少采取直接注射。核酸也可直接注入胚胎或受精卵,但人类胚胎的基因组编辑仍然备受争议[40]。鉴于这些局限性,临床上基因组编辑体内治疗可能还需要一个载体。因此,有效和安全性的提高核酸酶传送系统的效率将会有利于基因编辑技术的应用发展。近期研究表明,脂质体可能成为基因编辑传送系统中的明星载体,具有巨大的发展潜力[41]。 2.3 干细胞治疗骨关节炎的基因研究 2.3.1 干细胞的基因编辑研究 诱导多能干细胞是指具有自我更新、多向分化潜能的一类细胞重编程恢复到类似胚胎干细胞的细胞[42]。随着基因编辑脱靶率的降低和安全性的提高,诱导多能干细胞正在成为转化医学中基因编辑技术治疗细胞疾病的研究热点。诱导多能干细胞应用于临床,主要有2种方式:一种为将诱导多能干细胞直接移植到机体特定部位, 利用机体内环境的影响促进分化成特定种类的细胞;另一种是将诱导多能干细胞放在体外培育分化形成特定类型的细胞或者组织器官后再进行体内移植。诱导多能干细胞可以避免传统疾病模型的缺点来建立疾病特异性强的药物筛选模型和细胞模型[43-44],但诱导多能干细胞要真正的运用到临床实践中还需要解决系列问题:第一是安全问题,基因编辑脱靶效应会产生细胞毒性,会加速细胞凋亡[45];第二是致瘤性,未及时分化的诱导多能干细胞有可能导致肿瘤的形成[46]。因此,对诱导多能干细胞定向分化后的细胞进行筛选和建立高效的诱导定向分化的方法来降低肿瘤形成的风险尤其重要。利用基因编辑技术改造诱导多能干细胞进行细胞治疗,给难治性疾病的治疗提供了一种全新的方法。近期报道,目前基因编辑技术已经成功在大鼠胚胎干细胞、人胚胎干细胞及植物干细胞等领域展开靶点基因治疗研究[47],昆明理工大学、云南省灵长类生物医学重点实验室季维智、陈永昌和牛昱宇团队和同济大学医学院孙毅团队等合作,首次利用运用TALEN技术构建非人灵长类模型对食蟹猴瑞特综合征。 2.3.2 诱导干细胞软骨分化的基因研究 因为关节软骨损伤后较难修复,目前尚缺乏有效治疗方案,近年组织工程技术再生器官组织已经成为研究热点,因此组织工程技术再生关节软骨也存在可能。干细胞具有多向分化潜能,其中骨髓间充质干细胞是干细胞典型代表,被认为是治疗骨关节炎受损软骨和骨的最佳移植细胞[48],能够在体外定向分化并用于软骨修复[49-50],其中骨髓间充质干细胞向软骨分化是骨关节炎治疗中的关键步骤。在诱导骨髓间充质干细胞向软骨分化的过程中,多种细胞因子参与调控并发挥巨大作用。已有研究显示,多种细胞因子能使骨髓间充质干细胞表达Sox9基因,有利于促进细胞的增殖,并向软骨前期细胞分化,这是软骨形成的关键调节因素[51-52]。李大伟等[53]利用重组pIRES2-EGFP-hBMP-2质粒转染诱导人脐血间充质干细胞,RT-PCR结果表明hBMP-2 基因稳定转录,结果表明干细胞成功向软骨细胞组织分化。目前研究较多的具有促进干细胞向软骨细胞分化的细胞因子有转化生长因子β、骨形态发生蛋白、c-Jun氨基末端激酶、丝裂原活化蛋白激酶、胰岛素样生长因子、胞外信号调控激酶及成纤维细胞生长因子等,已经有专家证实中医药具有类似诱导干细胞软骨分化的作用[49],但这些细胞因子作用的具体机制尚不清楚。 "
| [1] 任云晓,肖茹丹,娄晓敏,等.基因编辑技术及其在基因治疗中的应用[J].遗传,2019,41(1):18-28. [2] MALI P, YANG L, ESVELT KM, et al. RNA-guided human genome engineering via Cas9 prashant. Science. 2013;339(6121):823-826. [3] 陈怡李,姚书忠.CRISPR/Cas9基因编辑技术的应用研究进展[J].国际生殖健康/计划生育杂志,2017,36(6):482-487. [4] 丁晓,史晨辉,孟德峰,等.骨关节炎关键基因与治疗药物的生物信息学筛选[J].中国实验方剂学杂志,2019,25(9):189-196. [5] 杨春艳,王磊,穆登彩,等.基因编辑技术在疾病治疗中的研究进展[J].中国生物工程杂志,2019,39(11):87-95. [6] CAI M, YANG Y. Targeted genome editing tools for disease modeling and gene therapy. Curr Gene Ther. 2014;14(1):2-9. [7] CONG L, RAN FA, COX D, et al. Multiplex genome engineering using CRISPR/Cas systems. Science. 2013;339(6121):819-823. [8] 牛煦然,尹树明,陈曦,等.基因编辑技术及其在疾病治疗中的研究进展[J].遗传,2019,41(7):582-598. [9] ANGUELA XM, HIGH KA. Entering the modern era of gene therapy. Annu Rev Med. 2019;70:273-288. [10] YOSHIDA K, TREEN N. TALEN-Based Knockout System. Adv Exp Med Boil. 2018;1029:131-139. [11] 何景进,王慧,付雪梅.基因编辑技术研究进展[J].发育医学电子杂志, 2019,7(3):235-240. [12] 曲道峰,沈杨,张聪聪,等.沙门氏菌CRISPR位点的结构特征比较[J].微生物学报,2018,58(2):209-2018. [13] CONG L, RAN FA, COX D, et al. Multiplex genome engineering using CRISPR/Cas systems. Science. 2013;339:819-823. [14] 吴璐,王磊,任远,等.基因组编辑技术研究进展[J].生物技术通报, 2014(11):84-90. [15] 玉婷,董金玲,冯力元,等.内源性过表达Nestin对NIH3T3细胞增殖、迁移及MAPK信号传导通路的影响[J].第三军医大学学报,2020, 42(2):125-132. [16] 王昕.基因编辑技术创新构建大鼠药物代谢模型及其应用[J].中国药理学与毒理学杂志,2019,33(10):814. [17] NIU YY, SHEN B, CUI YQ, et al. Generation of gene-modified cynomolgus monkey via Cas9/RNA-mediated gene targeting in onecell embryos. Cell. 2014;156:836-843. [18] 孙明尧,白玮,梁宏玉,等.CRISPR-Cas9技术在医药领域中的应用[J].沈阳药科大学学报,2019, 36(12):1145-1152. [19] RICHTER H, RANDAU L, PLAGENS A. Exploiting CRISPR-Cas:interference mechanisms and applications. Int J Mol Sci. 2013;14(7):14518-14531. [20] 陶洋,李金城,廖奇.CRISPR相关的生物信息学基础[J].中国生物化学与分子生物学报, 2016,32(10):1067-1076. [21] MA DJ, LI Y, XIAO W, et al. Achyranthes bidentata extract protects chondrocytes functions through suppressing glycolysis and apoptosis via MAPK/AKT signaling axis. Am J Transl Res. 2020;12(1):142-152. [22] 王继成,易智.miRNA与骨关节炎病理发展过程的相关性[J].中国组织工程研究,2019,23(24):3875-3881. [23] 顾晓东,车先达,李鹏翠,等.骨关节炎基因治疗的研究进展[J].中华骨与关节外科杂志,2019,12(5):396-398. [24] 詹子睿,邵增务.骨关节炎基因治疗进展[J].中国中医骨伤科杂志, 2004,12(3):57-59. [25] 邵进,张岩,王治,等.低氧诱导因子-1α参与骨发育及骨代谢调控的研究进展[J].中国骨质疏松杂志,2015,21(3):349-355. [26] 田大川,李海乐,肖大伟,等.联合应用软骨再生支架与突变型HIF-1α修饰BMSCs分泌的外泌体对晚期软骨缺损修复的促进作用[J].吉林大学学报,2018,44(2):216-222. [27] ALLERSTORFER D, LONGATO S, SCHWARZER C, et al. VEGF and its role in the early development of the long bone epiphysis. J Anat. 2010;216(5):611-624. [28] 马笃军,彭力平,余阗,等.牛膝总皂苷对骨关节炎模型兔软骨修复及低氧诱导因子1信号通路的影响[J].中国组织工程研究, 2019,23(27): 4332-4337. [29] BOBACZ K, GRUBER R, SOLEIMAN A, et al. Expression of bone morphogenetic protein 6 in healthy and osteoarthritic human articular chondrocytes and stimulation of matrix synthesis in vitro. Arthritis Rheum. 2003;48(9):2501-2508. [30] 于斐,曾晖,雷鸣,等.SIRT1基因敲除对骨关节炎小鼠VEGF/AKT信号通路的影响[J].中国骨质疏松杂志,2016,22(1):30-40. [31] BEENBAUM F. Osteoarthritis as an inflammatory disease (osteoarthritis is not osteoarthrosis). Osteoarthritis Cartilage. 2013;21(3):16-21. [32] 石继祥,纪斌,虞陆超,等.补肾活血方对骨关节炎小鼠局部淋巴管结构与分布的影响[J].中华中医药学刊,2018,12(12):3000-3004. [33] 张伟.张蜀茂.陈跃.淋巴系统显像的现状及研究进展[J].广东医学, 2018,39(12):3441-3447. [34] 韩海慧,王晓赟,梁倩倩,等.淋巴管系统与骨性关节炎的相关性研究进展[J].中华中医药杂志,2019,34(10):4727-4729, 4730. [35] 张武强,石继祥.骨性关节炎中淋巴管的研究进展[J].世界最新医学信息文摘,2019,19(66):106-107. [36] GUO R, ZHOU Q, PROULX ST, et al. Inhibition of lymphangiogenesis and lymphatic drainage via vascular endothelial growth factor receptor 3 blockade increases the severity of inflammation in a mouse model of chronic inflammatory arthritis. Arthritis Rheum. 2009;60(9):2666-2676. [37] LIANG QQ, SHI Q, WOODR W, et al. Peri-articular lymphatic system and“Bi” theory of Chinese medicine in the pathogenesis and treatment of arthritis. Chin J Integr Med. 2015;21(9):648-655. [38] ZHOU Q, WOOD R, SCHWA R, et al. Near-infrared lymphatic imaging demonstrates the dynamics of lymph flow and lymphangiogenesis.during the acute versus chronic phases of arthritis in mice. Arthritis Rheum. 2010;62(7):1881-1889. [39] ZISCHEWSKI J, FISCHER R, BORTESI L. Detection of on-target and off-target mutations generated by CRISPR/Cas9 and other sequence-specific nucleases. Biotechnol Adv. 2016;35(1):95-104. [40] 黄丕铂.基因编辑婴儿事件及其对科技创新管理的影响[J].科技中国, 2019,2:35-38. [41] HSU PD, LANDER ES, ZHANG F. Development and applications of CRISPR-Cas9 for genome engineering. Cell. 2014;157(6):1262-1278. [42] 杨伟,李施施,张瑄,等.基于诱导多能干细胞的基因编辑和细胞治疗[J].中国细胞生物学学报,2015,37(1):90-99. [43] ZHANG X, LI S, YANG W, et al. Patient-specificinduced pluripotent stem cell models in mitochondrial diseases. Curr Stem Cell Res Ther. 2014;9(2):134-140. [44] INOUE H, YAMANAKA S. The use of induced pluripotent stem cells in drug development. Clin Pharmacol Ther. 2011;89(5):655-661. [45] 郑武,谷峰.CRISPR/Cas9的应用及脱靶效应研究进展[J].遗传,2015, 37(10):1003-1010. [46] LOWRY WE, QUAN WL. Roadblocks en route to the clinical application of induced pluripotent stem cells. J Cell Sci. 2010;123(Pt 5):643-651. [47] 周琪.干细胞如何创造生命的奇迹[J].科学中国人,2019(12):38-42. [48] 张庆金,关若洪,张安文,等.miR-410可促进骨髓间充质干细胞定向分化为软骨细胞[J].中国组织工程研究,2019,23(1):13-17. [49] 马笃军,彭力平,王立新,等.牛膝醇提物诱导兔骨髓间充质干细胞软骨定向分化的实验研究[J].中国中医骨伤科杂志2017,25(2):6-11. [50] 陈锦富,耿倚云,王大平.定向诱导间充质干细胞成软骨分化相关活性因子研究进展[J]. 组织工程与重建外科杂志, 2018,14(4):227-230. [51] KOZHEMYAKINA E, LASSAR AB, ZELZER E. A pathway to bone: signaling molecules and transcription factors involved in chondrocyte development and maturation. Development. 2015;142(5):817-831. [52] CORREA D, SOMOZA RA, LIN P, et al. Sequential exposure to fibroblast growth factors (FGF)2,9 and 18 enhances hMSC chondrogenic differentiation. Osteoarthritis Cartilage. 2015;23(3):443-453. [53] 李大伟,孙一,姜翠萍,等.重组人骨形态发生蛋白-2质粒转染诱导人脐血间充质干细胞软骨分化研究[J].中华老年骨科与康复电子杂志, 2019,5(2):75-81. [54] YIN C, ZHANG T, QU X, et al. In vivo excision of HIV-1 provirus by saCas9 and multiplex single-guide RNAs in animal models. Mol Ther. 2017;25(5):1168-1186. [55] KC M, STEER CJ. A new era of gene editing for the treatment of human diseases. Swiss Med Wkly. 2019;149:w20021. [56] 陈曦,陈亮,李大力.基因治疗在临床应用中的研究进展[J].生物工程学报,2019,35(12):2295-2307. [57] TSAI SQ, JOUNG JK. Defining and improving the genome-wide specificities of CRISPR-Cas9 nucleases. Nat Rev Genet. 2016;17(5):300-312. |
| [1] | Tan Xinfang, Guo Yanxing, Qin Xiaofei, Zhang Binqing, Zhao Dongliang, Pan Kunkun, Li Yuzhuo, Chen Haoyu. Effect of uniaxial fatigue exercise on patellofemoral cartilage injury in a rabbit [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(在线): 1-6. |
| [2] | Xue Yadong, Zhou Xinshe, Pei Lijia, Meng Fanyu, Li Jian, Wang Jinzi . Reconstruction of Paprosky III type acetabular defect by autogenous iliac bone block combined with titanium plate: providing a strong initial fixation for the prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1424-1428. |
| [3] | Jin Tao, Liu Lin, Zhu Xiaoyan, Shi Yucong, Niu Jianxiong, Zhang Tongtong, Wu Shujin, Yang Qingshan. Osteoarthritis and mitochondrial abnormalities [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1452-1458. |
| [4] | Zhang Jichao, Dong Yuefu, Mou Zhifang, Zhang Zhen, Li Bingyan, Xu Xiangjun, Li Jiayi, Ren Meng, Dong Wanpeng. Finite element analysis of biomechanical changes in the osteoarthritis knee joint in different gait flexion angles [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1357-1361. |
| [5] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [6] | Jiang Huanchang, Zhang Zhaofei, Liang De, Jiang Xiaobing, Yang Xiaodong, Liu Zhixiang. Comparison of advantages between unilateral multidirectional curved and straight vertebroplasty in the treatment of thoracolumbar osteoporotic vertebral compression fracture [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1407-1411. |
| [7] | Wu Cong, Jia Quanzhong, Liu Lun. Relationship between transforming growth factor beta1 expression and chondrocyte migration in adult articular cartilage after fragmentation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1167-1172. |
| [8] | Li Wei, Zhu Hanmin, Wang Xin, Gao Xue, Cui Jing, Liu Yuxin, Huang Shuming. Effect of Zuogui Wan on bone morphogenetic protein 2 signaling pathway in ovariectomized osteoporosis mice [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1173-1179. |
| [9] | Wang Baojuan, Zheng Shuguang, Zhang Qi, Li Tianyang. Miao medicine fumigation can delay extracellular matrix destruction in a rabbit model of knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1180-1186. |
| [10] | Lü Yiyan, Li Hanbing, Ma Xiaoqing, Zhang Han, Zhang Yuhang, Li Genlin. Establishment and characteristic analysis of interior heat and diabetes mouse model using compound factors [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1187-1193. |
| [11] | Wang Jing, Xiong Shan, Cao Jin, Feng Linwei, Wang Xin. Role and mechanism of interleukin-3 in bone metabolism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1260-1265. |
| [12] | Xiao Hao, Liu Jing, Zhou Jun. Research progress of pulsed electromagnetic field in the treatment of postmenopausal osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1266-1271. |
| [13] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhang Qiang, Liu Jing, Shao Ming. Acupuncture for Parkinson’s disease: an insight into the action mechanism in animal experiments [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1272-1277. |
| [14] | Wu Bingshuang, Wang Zhi, Tang Yi, Tang Xiaoyu, Li Qi. Anterior cruciate ligament reconstruction: from enthesis to tendon-to-bone healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1293-1298. |
| [15] | Hui Xiaoshan, Bai Jing, Zhou Siyuan, Wang Jie, Zhang Jinsheng, He Qingyong, Meng Peipei. Theoretical mechanism of traditional Chinese medicine theory on stem cell induced differentiation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1125-1129. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||