Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (2): 304-310.doi: 10.3969/j.issn.2095-4344.2959
Previous Articles Next Articles
Self-renewal and signal regulation of myosatellite cells: application hotspots and problems
Li Lunyu, Jin Songlin, Huang Zenghao, Kang Liang, Hu Yushi, Ding Haili
- Chengdu Sport University, Chengdu 610041, Sichuan Province, China
-
Received:2020-03-30Revised:2020-03-31Accepted:2020-04-28Online:2021-01-18Published:2020-11-21 -
Contact:Ding Haili, MD, Associate professor, Doctoral supervisor, Chengdu Sport University, Chengdu 610041, Sichuan Province, China -
About author:Li Lunyu, Master candidate, Chengdu Sport University, Chengdu 610041, Sichuan Province, China -
Supported by:the National Natural Science Foundation of China, No. 81904318; National Key Research and Development Plan of China, No. 2018YFF0300604; Project supported by the Key Laboratory of Sports Medicine of General Administration of Sport of China and Sichuan Key Laboratory of Sports Medicine, No. 2017-A005
CLC Number:
Cite this article
Li Lunyu, Jin Songlin, Huang Zenghao, Kang Liang, Hu Yushi, Ding Haili. Self-renewal and signal regulation of myosatellite cells: application hotspots and problems[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(2): 304-310.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

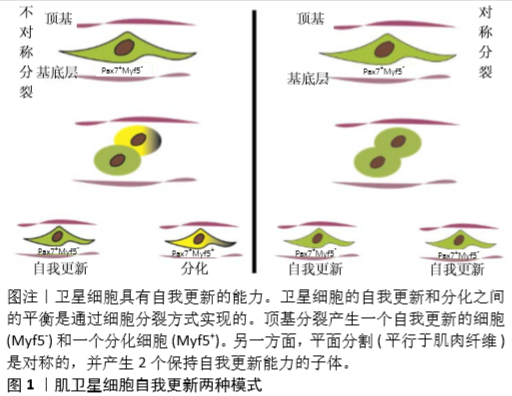
2.1 肌卫星细胞 2.1.1 肌卫星细胞形态结构 肌卫星细胞是指一类存在于肌细胞基底膜与肌膜之间的成体干细胞,呈扁平、突起状,附着于肌纤维(肌细胞)表面,参与肌纤维(肌细胞)的修复,呈现一种动态平衡状态,能被身体创伤或生长信号等刺激激活,激活后经历对称分裂和不对称分裂以扩大数量和产生子代细胞,完成增殖并最终通过彼此融合向受损纤维分化,以重建纤维的完整性和功能[2]。肌纤维受损后,肌卫星细胞通过自我更新和增殖分化,参与肌纤维适应性改变,其良好的增殖和分化能力在肌肉组织损伤、修复和再生中发挥重要作用。 2.1.2 肌卫星细胞增殖分化 在肌肉发生和肌肉再生过程中,MRFs蛋白成肌调节因子(myogenic regulatory factors,MRFs)是决定肌卫星细胞活化进程的关键因素。MRFs是肌肉特异性的碱性转录因子,包括Myf5,MyoD,myogenin和MRF4蛋白,能够充当肌源性信息的结点[3]。MRFs包含一个保守的基本DNA结合域,能够与肌肉特异性基因启动子e-box共识序列(CANNTG)结合[4]。Myf5和MyoD主要参与肌肉中非肌肉细胞(如成纤维细胞)向肌肉的转化和MRF4在肌肉发生过程中负责肌管的形成和成熟[5]。肌肉损伤发生时,肌卫星细胞沿着受损的肌纤维被激活,增殖并迁移到断裂的损伤部位形成新的肌管。肌卫星细胞被激活后表达Myf5,可以促进自身增殖;表达MyoD则诱导其退出细胞周期[6]。MyoD是肌肉再生中关键的生肌转录因子[7],肌肉再生过程中,控制肌肉特异性基因表达,如发育中肌球蛋白重链和肌生成素[8]。肌生成素的表达发生在肌管形成开始,是导致成肌细胞融合的关键因素。MRF4参与肌管的成熟,允许肌丝重组和中央细胞核迁移到细胞外围[9]。然而,MRFs家族蛋白的表达受Pax基因的调控,其中Pax3和Pax7发挥主要作用[10]。MRFs蛋白通过依次作用促进肌卫星细胞生肌分化和融合的过程,从而形成了多核肌纤维。肌生成素在此过程下游发挥作用,触发肌卫星细胞的终末分化[11]。Pax7与MyoD和Myog之间存在相互抑制,但Pax3和Pax7都不干扰Myf5的表达[12]。 2.1.3 肌卫星细胞生态位 肌卫星细胞生态位由非细胞和细胞成分组成,包括细胞外基质和生长因子、肌纤维和肌肉中非肌源性细胞(如纤维脂肪前体细胞和巨噬细胞和调节性T细胞)。肌卫星细胞生态位的各组成部分共同创造了一个复杂的微环境,在维持肌卫星细胞特性和确保对肌肉损伤的再生反应方面发挥至关重要的作用。 作为肌肉中的干细胞,肌卫星细胞的关键特征包括锚定在壁龛内维持生态位并在受伤时激活。MASHINCHIAN等[13]对健康和疾病状态下骨骼肌干细胞的研究发现,生态位处于稳态下可维持其自身静息,且表现为高度动态的再生生态位,同时产生广泛的结构重塑和不同种类细胞群的流动。反之,生态位功能障碍通过肌卫星细胞自我更新不足、干细胞池耗竭,从而损害其再生潜力,进一步决定骨骼肌重塑的最终结局,导致疾病/损伤的发生[14-15] 。GIORDANI等[16]报道认为,在急性损伤或病理状态下,原有静息状态下的肌肉干细胞被激活并产生肌原性祖细胞,大量增殖、分化和迁移融合以形成新的肌纤维并恢复组织正常生理功能;同时,活化后一定比例的细胞恢复静息状态以补充干细胞池,维持肌组织修复的能力。上述研究表明,肌卫星细胞自我更新维持生态位的稳定,是干细胞池能否持续参与肌肉再生的内生动力。 2.1.4 肌卫星细胞与骨骼肌再生 骨骼肌损伤再生包括3个连续的过程[17]:①炎症细胞浸润;②肌卫星细胞激活、分化与肌纤维融合;③肌纤维的成熟与重塑。在骨骼肌损伤部位的一段持续时间内,相应出现炎症反应,大量炎症细胞如巨噬细胞以及少量的中性粒细胞和其他的血源性细胞,它们在组织坏死部位浸润、吞噬并消融坏死组织[18-19]。在损伤部位出现组织变性和炎症反应时,肌卫星细胞也同时出现。受到损伤刺激的影响,肌卫星细胞被激活,出现细胞核增大、细胞质含量增多和细胞质密度升高、DNA合成增加的现象[20],并开始表现出分裂和增殖。在未分化的肌源性细胞中,Pax3和Pax7是支持干细胞功能的转录因子。Pax3在发育过程中首先在发育期中胚层表达,为四肢肌肉形成、细胞存活和迁移所必须。Pax7是出生后肌肉生长和维持肌卫星细胞池数量所必需的物质,研究证实它们在维持肌源性特性方面的关键作用[21]。由此,展现了肌卫星细胞3种不同分化状态:①维持干细胞库的Pax7细胞;②已进入生肌过程的MyoD1肌祖细胞;③准备与现有或新形成的肌纤维融合的Myogenin肌细胞。 骨骼肌再生、修复和重塑是不同的过程,需要一系列分子信息协调。肌纤维细胞结构的重建必须克服纤维坏死期,才能使骨骼肌完全再生,再生过程中,肌纤维须经过完全重建,而肌肉修复是一个涉及修复部分纤维或单个肌节的过程[22]。除了再生和修复,骨骼肌是一种高度可塑性的组织,能够根据适当的刺激进行重塑。例如,在进行抗阻运动训练后,骨骼肌能够增大,这与人体肌细胞核增加有关。大多数肌肉组织在面对生理压力或损伤时可进行再生和修复。这些不同的过程(即再生、修复和改造)中的每一个都是独立过程,但在某些情况下可协同发生。当骨骼肌组织需要修复或者损伤后的再生应答,肌卫星细胞从静息状态被激活,大量增殖以满足修复或者再生的需求[23], 2.2 肌卫星细胞自我更新 2.2.1 肌卫星细胞自我更新模式 肌卫星细胞的自我更新是通过不对称和对称分裂之间的平衡来实现的。肌卫星细胞可分为2个亚群:定向卫星细胞和卫星干细胞[24]。卫星干细胞可以在顶端基底方向进行不对称分裂,也可以在平面方向(相对于肌纤维)进行对称分裂。不对称分裂形成一个参与肌生成的子细胞,并维持原始的卫星干细胞。卫星干细胞的对称分裂产生2个子干细胞,并有利于卫星细胞的扩展[25],见图1。"
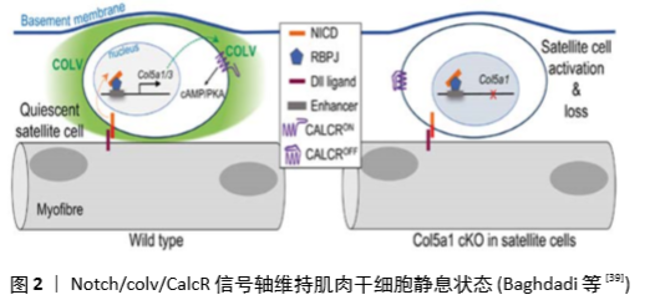
有研究从成人肌肉中分离出快周期和慢周期的卫星细胞,然后分析它们的肌源性和自我更新潜力,结果表明只有慢分裂的亚群才能在体外产生具有长期自我更新能力的后代[26]。此外,慢分裂的肌卫星细胞移植到受伤的肌肉中时有效地促进了再生。最近的一项研究表明,慢裂缓的肌卫星细胞表达较高水平的细胞周期素依赖性激酶抑制剂1B(p27Kip1和Cdkn1b),这是它们在体内长期维持所必需的[27]。肌卫星细胞进入骨骼肌谱系成为成肌细胞后会停止扩增,进一步分化与损伤的肌纤维融合或形成新的肌纤维修复骨骼肌的结构和功能;肌卫星细胞的增殖不但产生终末分化的肌肉组织,同时还获得了大量新的卫星细胞;这些新的卫星细胞以表达Pax7基因为标记,能够参与进一步的肌肉再生,被移植到新的宿主肌肉上可以修复宿主受损的细胞[28]。 2.2.2 肌卫星细胞自我更新标志 卫星细胞的激活部分是通过诱导MyoD和Myf5的表达来介导的[29]。成肌细胞的分化涉及Pax7的下调和肌生成素的重新表达,随后,已分化的成肌细胞开始彼此融合,并与其他的肌纤维融合修复受损的肌肉。未分化的肌卫星细胞可下调MyoD和Myf5的表达,并经历自我更新的增殖,从而补充肌卫星细胞池,从而确保肌肉对未来损伤的反应能力保留。 Pax7被认为是肌卫星细胞生态位及自我更新的关键标志物,Pax7在肌卫星细胞增殖、分化等不同时期的持续表达被认为是肌卫星细胞自我更新的标志。Pax基因是一个进化上高度保守的发育调控基因家族,可以编码核转录因子。其中Pax3和Pax7参与骨骼肌卫星细胞的发育过程[30]。Pax7是配对同源异型盒转录因子,可指定肌肉干细胞的肌原性身份,并可以通过刺激增殖而抑制分化而充当节点因子。ADDICKS等[31]最新研究表明肌卫星细胞中Mll1的缺失减少了肌卫星细胞的增殖和自我更新,并显着削弱了骨骼肌的再生。作为刺激肌肉干细胞增殖和分化抑制的节点因子,通过招募H3K4甲基转移酶MLL1/2以表观遗传学的方式激活靶基因[32]。研究表明,MLL1可直接调控Pax7,MLL1缺失Pax7和Myf5表达受损害而减少,成肌细胞不能增殖,但保留了其分化潜能。MLL1敲除的卫星细胞无法自我更新,干细胞池丢失。因此,激活的卫星细胞和成肌细胞中PAX7的表达绝对需要MLL1,而静止的卫星细胞则不需要。Pax7表达在静止的肌卫星细胞中不受影响,但在激活肌卫星细胞后明显下调[33]。Pax7的胱天蛋白酶3切割失活是终止自我更新过程的关键步骤。caspase 3的抑制导致Pax7蛋白的升高和肌卫星细胞的自我更新,而胱天蛋白酶激活导致Pax7裂解和成肌分化程序的启动[34]。 2.3 肌卫星细胞自我更新的信号调节 目前认为,静止的肌卫星细胞在损伤后被激活并扩增为成肌细胞,大多数成肌细胞将永久退出细胞周期并融合形成新的肌纤维,而部分成肌细胞将重新填充肌卫星细胞池[35],呈现出一种自我更新过程。在这个过程中,外在的信号级联以及内在的转录因子可指导循环肌卫星细胞下降,并适当协调新肌纤维产生和干细胞池的自我更新[36]。 2.3.1 腺苷酸活化蛋白激酶a1分子调节 细胞代谢的主要调节因子腺苷酸活化蛋白激酶调节肌卫星细胞的自我更新,这种多效性激酶具有该特性也证明了能量代谢可控制肌卫星细胞动态平衡。THERET等[37]研究结果表明,乳酸脱氢酶可以作为新的功能靶标,通过调节腺苷酸活化蛋白激酶a1依赖性途径中的代谢来调控肌卫星细胞恢复静止状态,乳酸脱氢酶反过来又可以控制氧化磷酸化/有氧糖酵解平衡。 2.3.2 eIF2α磷酸化调节 细胞应激状态下,会将mRNA储存在应激颗粒中,并在应激解除后将其释放出来进行翻译。这种转变可以在丝氨酸51位点被真核起始因子2α亚型(eukaryotic initiation factor 2α,eIF2α)磷酸化所调节。肌卫星细胞静止状态下翻译起始因子eIF2α磷酸化,积累压力维持细胞适应和生存;进入激活肌源性程序时会迅速去磷酸化。通过化合物sal003药理性抑制eIF2α磷酸酶,可以促进卫星细胞的自我更新。研究表明,在体外培养期间,对卫星细胞进行sal003处理后植入Duchenne肌营养不良小鼠模型其再生能力增加,即经过sal003处理的体外培养卫星细胞会产生更多的营养不良蛋白阳性纤维和自我更新的卫星细胞[38]。sal003存在的条件下,培养的肌卫星细胞可在体外扩增,保持再生能力,使sal003成为改进干细胞移植的潜在候选者。 2.3.3 Notch信号通路调节 Notch 信号是多种组织干细胞的调节因子,在肌肉细胞中具有更广泛的功能[39-40]。BAGHDADI等[39]新近发现Notch/ CollagenⅤ/CalcR是调控肌卫星细胞自我更新的关键信号轴,Notch释放的胞内结构域(NICD)特异性结合 重组结合蛋白-J RBP-J 后调控肌卫星细胞中的CollagenⅤ基因表达,其中具有靶向意义的是 Col5a1,Col5a3,而它们的相互作用由降钙素受体CalcR介导。Col5a1-/-会加速肌卫星细胞进入异常细胞周期,使干细胞池逐渐减少,进而导致静息态破坏和自我更新受损,见图2。 研究表明,NOTCH2调节自我更新的主要调节器。抑制Notch配体(Delta likecanonical Notch ligand 1,Dll1)活性导致pax7阳性子代缺失,影响卫星细胞的自我更新。分化过程中,分化出的DLL1表达细胞可以向卫星细胞传递自我更新的信号,从而保证相应的肌肉再生[41-42]。"
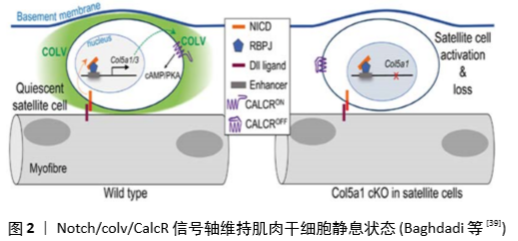
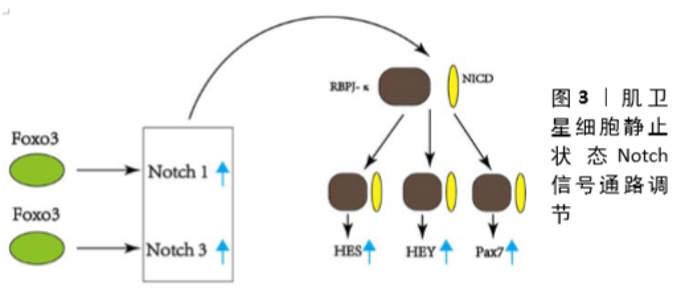
调节Notch信号的机制还包括调节配体或受体的表达。最近的研究表明,缺少Forkhead Box protein 3(FOXO3)转录因子的肌卫星细胞表现出Notch1和Notch3受体RNA水平降低[43]。FOXO3缺乏的肌卫星细胞在培养中增殖更快,更容易分化,不能保持细胞静止 [44]。FOXO3缺乏的肌卫星细胞的小鼠在连续2次肌肉损伤后表现出明显的肌肉再生障碍,可能由于卫星细胞在初次损伤后未能自我更新所致。这些研究还提出了FOXO3在瞬时扩增阶段促进卫星细胞增殖和/或存活的可能性,因为在这些小鼠损伤后1周,Pax7阳性的卫星细胞与中心有核的纤维相关的较少,进一步支持了FOXO3和静态肌卫星细胞中Notch信号之间潜在的直接联系,肌纤维中FOXO3缺乏的卫星细胞中NICD的异位表达部分恢复静态肌卫星细胞的数量[45]。这些结果表明FOXO3在卫星细胞中的一个关键功能是维持Notch受体的表达,这反过来对维持静止状态是必不可少的,见图3。"
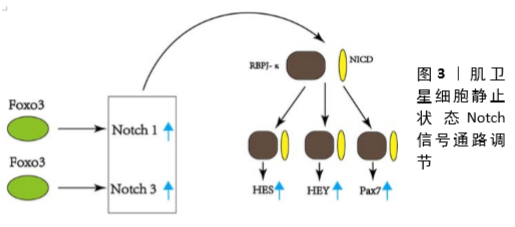
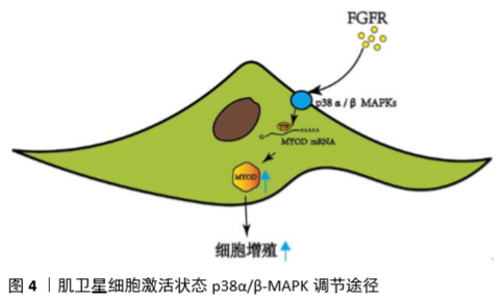
Notch信号通路在执行卫星细胞静止中起着关键作用。在配体/受体结合时,Notch胞内域(NICD,黄色)经历了几次蛋白水解性切割后,然后移位到细胞核,在那里它与重组结合蛋白J-κ效应蛋白(RBPJ-κ,棕色)相互作用。κ复合物激活靶基因的表达,包括HES和HEY家族转录因子,它们的功能是抑制MyoD。RBPJ-κ还与Pax7启动子结合并诱导其表达。Pax7诱导通过不依赖转录的机制进一步下调MyoD。 抑制Notch信号对肌卫星细胞生物学至少有3种不同的影响:①静息状态的丧失;②进入细胞周期的激活的肌卫星细胞自我更新失败;③激活的肌卫星细胞自发分化,增殖最少或没有增殖。显然,Notch激活的后果取决于特定的细胞状态,无论它是静止、激活还是增殖。这种状态依赖性可能是由于与Notch信号相互作用并影响Notch信号的其他通路的激活水平,从而导致不同的转录输出和不同的细胞后果。 2.3.4 P38 MARK信号通路调节 成纤维细胞生长因子受体酪氨酸激酶在协调细胞外信号与肌卫星细胞内部调控网络中起着重要作用。肌卫星细胞可表达成纤维细胞生长因子受体1和成纤维细胞生长因子受体4,其中,成纤维细胞生长因子受体4在胚胎肌肉发育过程中起决定细胞命运作用,成纤维细胞生长因子受体阻止终末分化。通过抑制成纤维细胞生长因子受体1信号可以减少微环境来源的成纤维细胞生长因子活性,从而阻止卫星细胞的耗竭[46]。 成纤维细胞生长因子受体1激活的细胞内信号包括调节肌卫星细胞增殖和不对称分裂的ERKMAPK和p38MAPK信号通路。当p38α/β-MAPK被证明对唤醒静态肌卫星细胞进入增殖状态至关重要时,就揭示了这种调控的显著性[47]。肌肉损伤后,被激活的肌卫星细胞会检测到来自局部环境的促肌源性刺激开始增殖。p38RNA-MAPK在增殖的肌卫星细胞中增加,在那里它们通过抑制α/β不稳定蛋白Tristetraprolin(TTP)诱导MyoD蛋白的表达[48]。静态肌卫星细胞中TTP的活性保证了MyoD mRNA的稳定,有利于肌卫星细胞的激活,见图4。 与年轻干细胞相比,新鲜分离的老年干细胞p38MAPK活性较高。伴随着p38成纤维细胞生长因子受体1MAPK信号的升高,成纤维细胞生长因子配体对αβ刺激减弱。因此,衰老的环境可能是磷酸化p38信号升高的原因,可能是由于细胞应激和炎症反应的增加,因此衰老环境导致p38,αβ,MAPK和Bernet等升高[49]。此外,高活性的p38αβMAPK阻止了不对称的p38αβMAPK信号,从而扰乱了不对称分裂和静止子细胞的产生。部分抑制p38MAPK信号可以恢复Pax7+细胞的生成和不对称磷酸化的p38MAPK。若完全抑制p38αβMAPK几乎可以消除自我更新,表明p38αβMAPK是SC自我更新所必需的[50]。综上所述,这些数据支持p38αβMAPK在肌卫星细胞自我更新中的关键作用,表明p38αβMAPK的亚细胞定位、信号持续时间和激活时间受到高度调控,以允许不对称分裂和肌卫星细胞自我更新。通过将老化的肌卫星细胞移植到年轻的宿主环境中和将年轻的肌卫星细胞移植到衰老的宿主环境中对比,年轻环境拯救老年肌卫星细胞自我更新的失败导致了老年肌卫星细胞自我更新中细胞自主缺陷的鉴定,其中成纤维细胞生长因子p38αβMAPK信号通路的改变出现在这些与年龄相关的缺陷的核心[51]。见图4。"
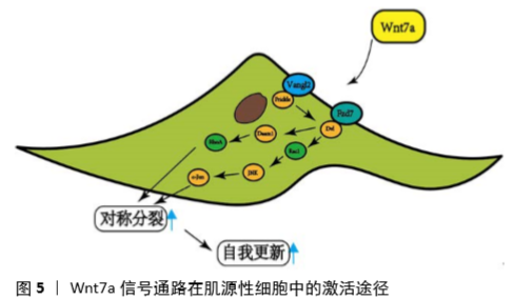
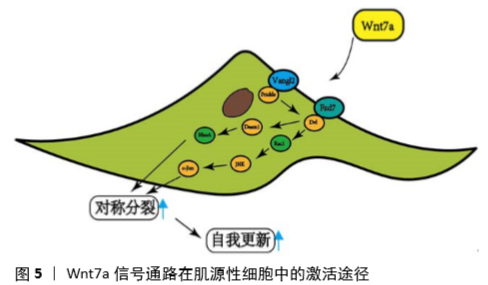
2.3.5 Wnt信号通路调节 胰岛素样生长因子1和成纤维细胞生长因子信号通路可以促进骨骼肌干细胞的增殖[52]。研究表明,经典的Wnt信号通路在调控骨骼肌干细胞增殖和分化中发挥作用[53] ,如外源Wnt1,3a,5a可以促进骨骼肌干细胞的增殖[54] ,β-catenin促进骨骼肌干细胞的自我更新并抑制其分化,而Wnt4、6则抑制骨骼肌干细胞的增殖[55]。而非经典的Wnt7a可以促进骨骼肌干细胞的对称分裂并在肌肉再生过程中诱导Wnt7a-Frizzle-7-PCP信号通路[55],Wnt7a在肌源性细胞中的激活途径。在肌源性细胞中,Wnt7a与FZD7结合,并根据肌源性细胞的不同阶段诱导不同的反应。在肌卫星干细胞中,Wnt7a与FZD7受体、Scd4辅助受体和纤维连接蛋白形成复合物,激活平面细胞极性通路。这种非规范的途径导致了对称的干细胞分裂。在肌源性祖细胞中,Wnt7a导致细胞骨架重排,促进细胞定向迁移。最后,在肌纤维中,Wnt7a以胰岛素样生长因子1不依赖的方式激活Akt/mTOR通路,促进肌纤维肥大[56],见图5。 有研究通过直接的转录控制以及与经典Wnt/β-catenin信号的相互作用,确定了肌肉干细胞中SoxF基因的关键调控功能,更重要的是,此研究数据为以前的报道提供了一个分子机制,证明Wnt/β-catenin经典信号输出的严格调控是确保骨骼肌再生所必需的。因此,SOXF因子作为肌肉干细胞静止的内在调节因子和与外在信号通路相互作用调节,活化的肌肉干细胞的扩增显示出双重活性。而且,最近的研究结果表明,在肌肉稳态条件下,衰老卫星细胞不能维持其正常的静止状态,细胞转变为不可逆的衰老前状态。随着年龄的增长,卫星细胞不能调节它们的静止,导致干细胞池的耗竭。有趣的是,卫星细胞功能损害与经典 Wnt/β-catenin的上调有关。因此,在这种情况下SOXF-β-catenin 相互作用的潜在作用[57]。 2.3.6 蛋白激酶PKCθ调节 细胞分裂中有丝分裂纺锤体的定位、生态位环境和PAR极性复合物的定位(PAR3-PAR6-aPKC)决定了分裂的类型[58]。因此,PAR复合物在细胞中的不对称定位驱动了细胞命运极化的决定因素,通过诱导MyoD在单个子细胞中的表达促进了细胞的不对称分裂。PKCθ(Protein kinase C Theta,PKCθ)是一种丝氨酸和苏氨酸激酶,属于PKCs的家族,可以调节细胞的存活、增殖和分化。 研究表明,PKCθ通过刺激对称分裂直接参与细胞的活动[59]。PKCθ缺失的情况下,肌肉急性损伤后静态肌卫星细胞池显著增加,自我更新能力增强。这些并不是炎症环境改变造成的,而是通过调节Pard3极性蛋白的定位来促进细胞对称自我更新分裂,而不影响总体增殖速率。 2.3.7 MicroRNA调节 研究发现,MicroRNAs (miRNA)可以调控着卫星细胞的增殖、分化、再进入静止状态和维持静止等多种细胞过程。在静息状态下的骨骼肌中[60],miR-31将Myf5隔离在mRNA颗粒中,保持卫星细胞进入肌源性进程的准备状态。miR-31失活通过损害成肌细胞的扩增而损害成年小鼠的肌肉再生。miR-31对于卫星细胞增殖至关重要,其缺失可促进增殖细胞的不对称细胞命运分离,从而导致成肌作用增强并重新进入静止状态。miR-31在转录后抑制白细胞介素34 mRNA,其蛋白质产物激活成肌进程所需的JAK-STAT3信号传导。因此,miR-31-白细胞介素34参与了卫星细胞的自我更新过程。"
| [1] TIERNEY MT, SACCO A. Satellite Cell Heterogeneity in Skeletal Muscle Homeostasis. Trends Cell Biol. 2016;26(6):434-444. [2] ANDES-KOBACK M, KEATING CD. Complete budding and asymmetric division of primitive model cells to produce daughter vesicles with different interior and membrane compositions. J Am Chem Soc. 2011; 133(24):9545-9555. [3] HOU GY, ZHOU HL, CAO T, et al. Expression and variation of Myf5 and MyoD1 genes in different tissues of Wuzhishan pigs. Genet Mol Res. 2015;14(2):3729-3735. [4] BOWLIN KM, EMBREE LJ, GARRY MG,et al. Kbtbd5 is regulated by MyoD and restricted to the myogenic lineage. Differentiation. 2013; 86(4-5):184-191. [5] MILEWSKA M, GRABIEC K, GRZELKOWSKA-KOWALCZYK K. Interactions of proliferation and differentiation signaling pathways in myogenesis. Postepy Hig Med Dosw (Online). 2014;68:516-526. [6] QAHAR M, TAKUMA Y, MIZUNOYA W, et al. Semaphorin 3A promotes activation of Pax7, Myf5, and MyoD through inhibition of emerin expression in activated satellite cells. FEBS Open Bio. 2016;6(6):529-539. [7] D’AGOSTINO M, TORCINARO A, MADARO L, et al. Role of mir-200c in myogenic differentiation impairment via p66shc: implication in skeletal muscle regeneration of dystrophic mdx mice. Oxid Med Cell Longev. 2018;2018:4814696. [8] ZANOU N, GAILLY P. Skeletal muscle hypertrophy and regeneration: interplay between the myogenic regulatory factors (MRFs) and insulin-like growth factors (IGFs) pathways. Cell Mol Life Sci. 2013; 70(21):4117-4130. [9] SJÖSTRÖM M, THORNELL LE, CEDERGREN E. The application of cryo microtomy in the study of the fine structure of myofilaments. J Microscopy. 2011;99(2):193-204. [10] PADILLA-BENAVIDES T, NASIPAK BT, IMBALZANO AN. Brg1 Controls the Expression of Pax7 to Promote Viability and Proliferation of Mouse Primary Myoblasts. J Cell Physiol. 2015;230(12):2990-2997. [11] JANG YJ, SON HJ, KIM JS, et al. Coffee consumption promotes skeletal muscle hypertrophy and myoblast differentiation. Food Funct. 2018; 9(2):1102-1111. [12] PANDURANGAN M, MOORTHY H, Sambandam R, et al. Effects of stress hormone cortisol on the mRNA expression of myogenenin, MyoD, Myf5, PAX3 and PAX7. Cytotechnology. 2014;66(5):839-844. [13] MASHINCHIAN O, PISCONTI A, MOAL EL, et al. The Muscle Stem Cell Niche in Health and Disease. Curr Top Dev Biol. 2018;126:23-65. [14] BENTZINGER CF, WANG YX, DUMONT NA, et al. Cellular dynamics in the muscle satellite cell niche. Embo Rep. 2013;14(12):1062-1072. [15] GIORDANI L, INCITTI T, MAGLI A, et al. Incitti T, Magli A, Darabi R, et al. Pluripotent stem cell-derived myogenic progenitors remodel their molecular signature upon in vivo engraftment. Proc Natl Acad Sci U S A. 2019;116(10):4346-4351. [16] GIORDANI L, PARISI A, LE GRAND F. Satellite Cell Self-Renewal. Curr Top Dev Biol. 2018;126:177-203. [17] FILIPPIN LI, MOREIRA AJ, MARRONI NP, et al. Nitric oxide and repair of skeletal muscle injury. Nitric Oxide. 2009;21(3-4):157-163. [18] EBNER F, SEDLYAROV V, TASCIYAN S, et al. The RNA-binding protein tristetraprolin schedules apoptosis of pathogen-engaged neutrophils during bacterial infection. J Clin Invest. 2017;127(6):2051-2065. [19] LV J, ZOU L, ZHAO L, et al. Leukotriene B₄-leukotriene B₄ receptor axis promotes oxazolone-induced contact dermatitis by directing skin homing of neutrophils and CD8⁺ T cells. Immunology. 2015;146(1):50‐58. [20] NEDERVEEN JP, JOANISSE S, SNIJDERS T, et al. The influence of capillarization on satellite cell pool expansion and activation following exercise-induced muscle damage in healthy young men. J Physiol. 2018;596(6):1063-1078. [21] YANAY N, ELBAZ M, KONIKOV-ROZENMAN J, et al. Pax7, Pax3 and Mamstr genes are involved in skeletal muscle impaired regeneration of dy2J/dy2J mouse model of Lama2-CMD. Hum Mol Genet. 2019; 28(20):3369-3390. [22] BURM JS, HWANG J, LEE YK. A New Option for the Reconstruction of Primary or Recurrent Ischial Pressure Sores: Hamstring-Adductor Magnus Muscle Advancement Flap and Direct Closure. Ann Plast Surg. 2018;80(4):400-405. [23] BOLDRIN L, MORGAN JE. Modulation of the host skeletal muscle niche for donor satellite cell grafting. Methods Mol Biol. 2013;1035:179-190. [24] ROCHETEAU P, GAYRAUD-MOREL B, SIEGL-CACHEDENIER I, et al. A Subpopulation of Adult Skeletal Muscle Stem Cells Retains All Template DNA Strands after Cell Division. Cell. 2012;148(1-2):125. [25] INSINGA A, CICALESE A, FARETTA M, et al. DNA damage in stem cells activates p21, inhibits p53, and induces symmetric self-renewing divisions. Proc Natl Acad Sci U S A. 2013;110(10):3931‐3936. [26] ONO Y, MASUDA S, NAM HS, et al. Slow-dividing satellite cells retain long-term self-renewal ability in adult muscle. J Cell Sci. 2012; 125(5): 1309-1317. [27] CHAKKALAKAL JV, CHRISTENSEN J, XIANG W, et al. Early forming labelretaining muscle stem cells require p27kip1 for maintenance of the primitive state. Development. 2014;141(8):1649-1659. [28] KOKI K, RYOSUKE D, MAKOTO H, et al. The Ror1 receptor tyrosine kinase plays a critical role in regulating satellite cell proliferation during regeneration of injured muscle. J Biol Chem. 2017;292(38): 1593915951. [29] QAHAR M, TAKUMA Y, MIZUNOYA W, et al. Semaphorin 3A promotes activation of Pax7, Myf5, and MyoD through inhibition of emerin expression in activated satellite cells. FEBS Open Bio. 2016;6(6):529-539. [30] YANAY N, ELBAZ M, KONIKOV-ROZENMAN J, et al. Pax7, Pax3 and Mamstr genes are involved in skeletal muscle impaired regeneration of dy2J/dy2J mouse model of Lama2-CMD. Hum Mol Genet. 2019; 28(20):3369‐3390. [31] ADDICKS GC, BRUN CE, SINCENNES MC, et al. MLL1 is required for PAX7 expression and satellite cell self-renewal in mice. Nat Commun. 2019;10(1):4256. [32] SOLEIMANI VD. Transcriptional dominance of Pax7 in adult myogenesis is due to high-affinity recognition of homeodomain motifs. Dev Cell. 2012;22:1208-1220. [33] LEPPER C, PARTRIDGE TA, FAN CM. An absolute requirement for Pax7-positive satellite cells in acute injury-induced skeletal muscle regeneration. Development. 2011;138(17):3639-3646. [34] DICK SA, CHANG NC, DUMONT NA, et al. Caspase 3 cleavage of Pax7 inhibits self-renewal of satellite cells. Proc Natl Acad Sci U S A. 2015;112(38):E5246-E5252. [35] LINKHART TA, CLEGG CH, HAUSCHKA SD. Control of mouse myoblast commitment to terminal differentiation by mitogens. J Supramol Struct. 1980;14(4):483-498. [36] MOHAN A, ASAKURA A. CDK inhibitors for muscle stem cell differentiation and self-renewal. J Phys Fit Sports Med. 2017;6(2):65-74. [37] THERET M, GSAIER L, SCHAFFER B, et al. AMPKα1-LDH pathway regulates muscle stem cell self-renewal by controlling metabolic homeostasis. EMBO J. 2017;36(13):1946-1962. [38] ZISMANOV, CHICHKOV, VICTOR, et al. Phosphorylation of eIF2α Is a translational control mechanism regulating muscle stem cell quiescence and self-renewal. Cell Stem Cell. 2016;18(1):79-90. [39] BAGHDADI MB, CASTEL D, MACHADO L, et al. Reciprocal signalling by Notch-Collagen V-CALCR retains muscle stem cells in their niche. Nature. 2018;557(7707):714-718. [40] VERMA M, ASAKURA Y, MURAKONDA BSR, et al. Muscle Satellite Cell Cross-Talk with a Vascular Niche Maintains Quiescence via VEGF and Notch Signaling. Cell Stem Cell. 2018;23(4):530-543. [41] YARTSEVA V, GOLDSTEIN LD, RODMAN J, et al. Heterogeneity of Satellite Cells Implicates DELTA1/NOTCH2 Signaling in Self-Renewal. Cell Rep. 2020;30(5):1491-1503.e6. [42] FUJIMAKI S, SEKO D, KITAJIMA Y, et al. Notch1 and Notch2 Coordinately Regulate Stem Cell Function in the Quiescent and Activated States of Muscle Satellite Cells. Stem Cells. 2018;36(2):278-285. [43] CASTEL D, BAGHDADI MB, MELLA S, et al. Small-RNA sequencing identifies dynamic microRNA deregulation during skeletal muscle lineage progression. Sci Rep. 2018;8(1):4208. [44] GOPINATH SD, WEBB AE, BRUNET A, et al. FOXO3 promotes quiescence in adult muscle stem cells during the process of self-renewal. Stem Cell Rep. 2014;2(4):414-426. [45] CHAKKALAKAL JV, JONES KM, BASSON MA, et al. The aged niche disrupts muscle stem cell quiescence. Nature. 2012;490(7420):355-360. [46] TROY A, CADWALLADER A, FEDOROV Y, et al. Coordination of Satellite Cell Activation and Self-Renewal by Par-Complex-Dependent Asymmetric Activation of p38α/β MAPK. Cell Stem Cell. 2012;11(4): 541-553. [47] Bernet JD, Doles JD, Hall JK, et al. P38 MAPK signaling underlies a cell autonomous loss of stem cell self-renewal in aged skeletal muscle. Nature Med. 2014;20(3):265-271. [48] MELISSA AH, JASON DD, SANDRA LC, et al. Post-transcriptional regulation of satellite cell quiescence by TTP-mediated mRNA decay. ELife. 2015;4(4):e03390. [49] BRIEN P, PUGAZHENDHI D, WOODHOUSE S, et al. p38α MAPK regulates adult muscle stem cell fate by restricting progenitor proliferation during postnatal growth and repair. Stem Cells. 2013;31(8):1597-1610. [50] PAPACONSTANTINOU J, WANG CZ, ZHANG M, et al. Attenuation of p38α MAPK stress response signaling delays the in vivo aging of skeletal muscle myofibers and progenitor cells. Aging (Albany NY). 2015;7(9):718-733. [51] BERNET JD, DOLES JD, HALL JK, et al. p38 MAPK signaling underlies a cell-autonomous loss of stem cell self-renewal in skeletal muscle of aged mice. Nat Med. 2014;20(3):265-271. [52] ZHANG J, HE L, YANG Z, et al. Lithium chloride promotes proliferation of neural stem cells in vitro, possibly by triggering the Wnt signaling pathway. Anim Cells Syst (Seoul). 2018;23(1):32-41. [53] LU X, CHEN X, XING J, et al. miR-140-5p regulates the odontoblastic differentiation of dental pulp stem cells via the Wnt1/β-catenin signaling pathway. Stem Cell Res Ther. 2019;10(1):226. [54] TAKATA H, TERADA K, OKA H, et al. Involvement of Wnt4 signaling during myogenic proliferation and differentiation of skeletal muscle. Dev Dyn. 2007;236(10):2800-2807. [55] VON MALTZAHN J, BENTZINGER CF, RUDNICKI MA. Wnt7a-Fzd7 signalling directly activates the Akt/mTOR anabolic growth pathway in skeletal muscle. Nat Cell Biol. 2011;14(2):186-191. [56] BENTZINGER C, WANG Y, VONMALTZAHN J, et al. Fibronectin Regulates Wnt7a Signaling and Satellite Cell Expansion. Cell Stem Cell. 2013; 12(1):75-87. [57] SONIA AM, Frédéric A, DESPOINA M, et al. SOXF factors regulate murine satellite cell self-renewal and function through inhibition of β-catenin activity. ELife. 2018;7:e26039. [58] KNOBLICH JA. Asymmetric cell division: recent developments and their implications for tumour biology. Nat Rev Mol Cell Biol. 2010; 11(12):849-860. [59] BENEDETTI A, FIORE PF, MADARO L, et al. Targeting PKCθ Promotes Satellite Cell Self-Renewal. Int J Mol Sci. 2020;21(7):E2419. [60] SU Y, YU Y, LIU C, et al. Fate decision of satellite cell differentiation and self-renewal by miR-31-IL34 axis. Cell Death Differ. 2020;27(3): 949-965. |
| [1] | Zhang Lichuang, Xu Hao, Ma Yinghui, Xiong Mengting, Han Haihui, Bao Jiamin, Zhai Weitao, Liang Qianqian. Mechanism and prospects of regulating lymphatic reflux function in the treatment of rheumatoid arthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1459-1466. |
| [2] | Yuan Jiabin, Zhu Zongdong, Tang Xiaoming, Wei Dan, Tan Bo, Xiao Chengwei, Zhao Ganlinwei, Liao Feng. Classification and reduction strategies for irreducible intertrochanteric femoral fracture based on anatomy [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1341-1345. |
| [3] | Pan Baoshun, Fang Zhen, Gao Mingjie, Fang Guiming, Chen Jinshui. Design for posterior atlantoaxial internal fixation system with fusion cage based on imaging data [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1372-1376. |
| [4] | Li Kun, Gao Erke, Xiong Feng, Wang Xing, Wu Danqi, Li Zhijun, Zhang Shaojie, Liu Yanan, Duo Lan, Li Ziyu. Feasibility of axial transpedicle screw internal fixation in children aged 1 to 6 years [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1383-1387. |
| [5] | Wang Shuai, Wang Liancheng, Zhang Shuhao, Li Fuli, Dong Jiaxing, Zhang Yajie. Correlation of the electromyography ratio of the paraspinal muscles on the convex and concave sides with Cobb angle, apical vertebra translation, and coronal balance distance in adolescent idiopathic scoliosis patients [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1402-1406. |
| [6] | Bao Xianguo, Gao Zengxin, Wu Zhanpo, Chen Youmin, Cheng Qinghua, Lu Haitao, Guo Changzheng, Xu Shuai. Correlation between lumbar posterior muscle and local kyphosis in patients with degenerative thoracolumbar kyphosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1418-1423. |
| [7] | Zheng Pei, Xing Xinyang, Huo Hongfeng. Exercises for activating foot valgus muscle: reciprocal inhibitory effects on antagonistic muscle elasticity, tension and hardness [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1149-1153. |
| [8] | Kong Yamin, Yan Juntao, Ma Bingxiang, Li Huawei. Massage vibration intervenes with MyoD expression and proliferation and differentiation of muscle satellite cells in rats with sciatic nerve injury [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1160-1166. |
| [9] | Li Wei, Zhu Hanmin, Wang Xin, Gao Xue, Cui Jing, Liu Yuxin, Huang Shuming. Effect of Zuogui Wan on bone morphogenetic protein 2 signaling pathway in ovariectomized osteoporosis mice [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1173-1179. |
| [10] | Wang Qin, Shen Cheng, Liao Jing, Yang Ye. Dapagliflozin improves renal injury in diabetic nephropathy rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1216-1222. |
| [11] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [12] | Wen Xiaoyu, Sun Yuhao, Xia Meng. Effects of serum containing Wuzang Wenyang Huayu Decoction on phosphorylated-tau protein expression in Alzheimer’s disease cell model [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1068-1073. |
| [13] | Liang Xuezhen, Yang Xi, Li Jiacheng, Luo Di, Xu Bo, Li Gang. Bushen Huoxue capsule regulates osteogenic and adipogenic differentiation of rat bone marrow mesenchymal stem cells via Hedgehog signaling pathway [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1020-1026. |
| [14] | Wang Jifang, Bao Zhen, Qiao Yahong. miR-206 regulates EVI1 gene expression and cell biological behavior in stem cells of small cell lung cancer [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1027-1031. |
| [15] | Zhou Hongqin, Wu Dandan, Yang Kun, Liu Qi. Exosomes that deliver specific miRNAs can regulate osteogenesis and promote angiogenesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1107-1112. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||