Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (20): 3248-3255.doi: 10.3969/j.issn.2095-4344.2529
Previous Articles Next Articles
Alternative treatment for liver failure repair: current status and development countermeasures
Guo Wei1, Lu Shan1, Fan Hong1, Li Jun2
- 1China National Center for Biotechnology Development, Beijing 100039, China; 2State Key Laboratory for Diagnosis and Treatment of Infectious Diseases, The First Affiliated Hospital, Zhejiang University School of Medicine, Hangzhou 310003, Zhejiang Province, China
-
Received:2019-07-18Revised:2019-07-27Accepted:2019-09-02Online:2020-07-18Published:2020-04-13 -
About author:Guo Wei, Master, Assistant researcher, China National Center for Biotechnology Development, Beijing 100039, China
CLC Number:
Cite this article
Guo Wei, Lu Shan, Fan Hong, Li Jun. Alternative treatment for liver failure repair: current status and development countermeasures[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(20): 3248-3255.
share this article
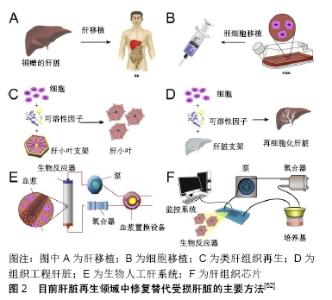
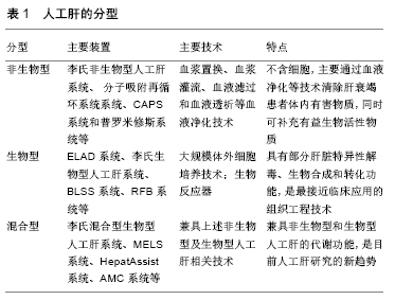
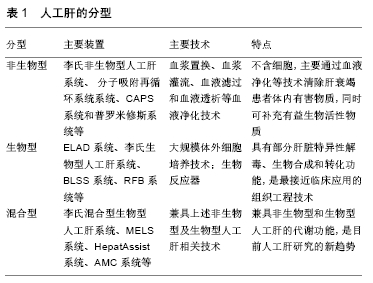
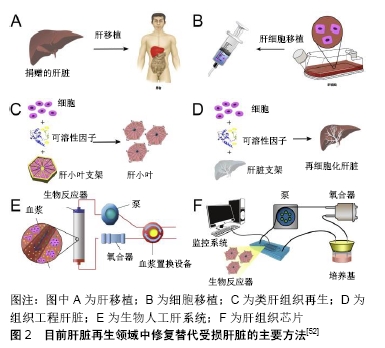
2.1.1 非生物型人工肝 是指各种不含细胞,主要通过血浆置换、血浆灌流、胆红素吸附、血液滤过和血液透析等技术清除肝衰竭患者体内的有害物质,同时补充有益生物活性物质的一种血液净化装置。目前的非生物型人工肝主要有李氏非生物型人工肝、分子吸附再循环系统、连续白蛋白净化系统和普罗米修斯系统等。目前大量临床数据显示,非生物型人工肝能够显著提高肝衰竭的临床治愈、好转率,但该系统尚不能完全替代肝脏的合成、代谢和生物转化等功能,需要进一步的研究。 2.1.2 生物型人工肝 主要由种子细胞和生物反应器构成,利用体外循环装置使肝衰竭患者血浆通过反应器内的半透膜与种子细胞进行物质交换[10],有效改善急性期肝功能,为等待肝移植患者提供足够的时间窗。另外,因生物型人工肝为体外装置,生物反应器内的肝细胞并不直接进入体内且系统设置血浆分离器,患者血细胞、免疫球蛋白不进入生物反应器内,可有效避免免疫排斥反应。目前来看,生物型人工肝是最接近临床应用的组织工程技术,同时可避免非生物型人工肝面临的新鲜血浆缺乏的问题,但如何保证反应器内种子细胞的活性是这种装置面临的最大难题。 对于生物型人工肝支持系统中的两个核心部分:种子细胞和生物反应器,目前已广泛开展了研究,并取得了阶段性进展。 首先,决定生物型人工肝安全性及有效性的重要因素为种子细胞。目前生物型人工肝种子细胞主要有几种来源:①肿瘤源性肝细胞系:如美国体外人工肝支持系统采用肿瘤源性肝细胞系HepG2、C3A等作为种子细胞,其代谢功能不佳,可能存在致瘤性,但在其Ⅲ期临床试验中,与对照(原代猪肝细胞)相比无显著性差异[11]。②原代猪肝细胞:获取方便,功能较好。如美国Arbios System公司使用猪肝细胞作为种子细胞,且已有研究团队(哈佛大学及南方医科大学等)构建了PERV基因敲除或敲减猪,以期避免其携带内源性PERV病毒的潜在生物安全风险[12-13]。③干细胞:如人胚胎干细胞、可诱导多潜能干细胞或间充质干细胞在特异条件下可诱导分化成肝样细胞,为生物型人工肝提供种子细胞。华南理工大学段玉友等已成功实现规模化人胚胎干细胞向肝样细胞分化,为人胚胎干细胞在生物型人工肝系统应用奠定了基础[14]。中科院生化和细胞研究所/微知卓生物科技有限公司将人成纤维细胞直接转分化为肝样细胞hiHep,应用于生物型人工肝系统,在小型猪动物实验中取得了成功[15]。最近国内有研究机构(鄢和新团队及惠利健团队)将原代肝细胞重编程为肝前体细胞,实现规模化的体外扩增后再分化为成熟肝细胞,为寻找生物型人工肝种子细胞提供了新思路[16-17]。④永生化肝细胞系:浙江大学李兰娟院士与李君教授利用正常人肝细胞建立的永生化肝细胞系HepLL[18],南方医科大学高毅教授开发的永生化肝细HepGL,均为生物型人工肝提供了潜在的种子细胞[13]。⑤胎肝细胞:殖能力较强,国内有研发机构也在应用胎肝细胞作为种子细胞,但受制于复杂的伦理学问题而难以应用于临床[19]。 同样,生物反应器在人工肝体系中处于关键环节,对生物人工肝的效能具有重要影响。该装置是血液(血浆)与种子细胞相互作用进行双向物质交换的主要场所,可以为细胞提供良好的生长代谢环境,保障高通量的物质交换效能。目前经典的生物反应器主要有4种:①单层平板型生物反应器:将细胞种植于平板上;②中空纤维生物反应器:将细胞培养在中空纤维的内腔或外腔;③包裹流化床式生物反应器:将肝细胞包裹于生物材料内制成多孔微囊,进行悬浮灌注培养;④灌流型生物反应器:将细胞种植在灌流床上,固定支持肝细胞培养。不同的反应器具有各自的优缺点,可根据实际情况选择不同的生物反应器。 目前国际上已具备效果评价的共4种生物型人工肝装置:①ELAD系统:由美国Baylar设计并由Vital治疗公司研制开发,由双泵透析系统和含C3A细胞的中空纤维反应器组成,是迄今为止唯一适用人肝细胞系(C3A)的人工肝装置。ELAD在临床治疗中进行了相应的试验,一项小样本单中心临床试验显示:ELAD支持治疗较对照组明显能改善患者意识状态,清除血氨和降低总胆红素水平,但未能改善患者的生存率[20]。由于临床疗效有限,ELAD于2015年8月宣布Ⅲ期临床试验失败。②李氏生物型人工肝系统:由浙大一院李兰娟团队研发,目前主要有微囊悬浮流化床式生物人工肝。该系统由微囊化人源性永生化肝细胞株HepLi4、漏斗型流化床生物反应器和双腔储液池构成。在肝衰竭猪模型中发现,与对照组(常规标准治疗组、不含细胞的生物型人工肝系统治疗组)相比,经李氏生物型人工肝系统治疗后,肝衰竭小型猪模型的血氨、乳酸浓度明显下降,生存时间显著延长[21]。③BLSS生物人工肝:由美国匹兹堡大学设计,该系统是在血液滤过的基础上增加了具有生物转化与合成的生物反应器,该系统的主要特色是中空纤维生物反应器中包含了100 g新鲜分离的猪肝细胞。2001年在4例暴发性肝衰竭患者上进行了Ⅰ期临床试验,证实了该系统的安全性[22],但需要进一步的研究来证明其有效性。④RFB系统:由意大利研制,通过将原代猪肝细胞培养于一厚约6 mm的编织-非编织层基质内。患者血液经血浆分离器后注入血浆存储器,再进一步流经生物反应器,最终回输患者体内。 2.1.3 混合型人工肝 集非生物型人工肝与生物型人工肝于一体,既包含物理、机械或化学的血液净化方法,又具备肝细胞的生物学功能,可较全面地替代肝脏解毒、生物合成和分泌代谢等功能,更好地发挥肝脏的替代作用,是目前人工肝研究的新趋势[19]。目前,该系统主要有李氏混合型人工肝系统、HepatAssist系统、MELS系统和AMC系统等。①李氏混合型人工肝系统:由李兰娟团队在非生物型人工肝基础上引入中空纤维型生物反应器,结合猪肝细胞及血浆置换构建而成。前期临床研究发现,15例肝衰竭患者中有10例经治疗后获得很好的疗效,其治疗过程中无明显不适反应[23]。②HepatAssist生物人工肝:由生物反应器与活性炭吸附器组合而成,能发挥机械解毒与生物转化的双重作用,因此HepatAssist的临床应用更具有优势。在2004年进行的前瞻性、多中心、随机对照组临床Ⅱ/Ⅲ期试验中,试验组(生物型人工肝+常规标准治疗)和对照组(常规标准治疗)患者1个月生存率无统计学差异[24],该系统未能明显提高急性肝衰竭患者的生存率。③MELS系统:由德国Charite医院研发,该装置是由多个单元组成,包括血浆置换、血液滤过、白蛋白透析、生物反应器等,主要利用新鲜分离的猪和人肝细胞进行治疗。2003年进行的Ⅰ期临床试验使8例患者成功过度到肝移植,3 年随访所有患者都存活[25]。④AMC系统:由荷兰阿姆斯特丹大学研发而成,主要由猪肝细胞和中空纤维生物反应器构成。血浆在流经AMC系统时首先进行血浆吸附,有利于生物反应器中培养的肝细胞更好地发挥作用。 国内目前已有多家医院和机构自主研发了人工肝装置,尽管生物型人工肝和混合型人工肝在肝衰竭治疗上展现出很好的发展前景,但大多仍处于动物实验阶段,尚未进行大规模临床试验,目前尚无可靠的生物人工肝产品获准上市,一旦有产品成功上市,将极大降低终末期肝病治疗成本。相信随着研究的不断深入及生物工程、生物材料、细胞生物技术等相关交叉学科的发展,必定能使细胞源及生物反应器等方面有重大突破,提高肝衰竭的治疗效果,为肝衰竭患者带来希望。 2.2 组织工程肝脏 组织工程是近年来兴起的运用生命科学与工程学原理与技术,研究、开发用于修复、维护人体组织或器官损伤后功能和形态的生物替代物的一门新兴学科[26],1987年,美国麻省理工学院化学工程师Langer和美国马萨诸塞州立大学医院临床医师Vacanti较为系统地提出了“组织工程”的概念[27],其核心是建立由细胞和生物材料构成的三维空间复合体[28],达到器官和组织的完美修复。目前组织工程发展迅速,已成为再生医学研究的核心内容和主要发展方向,在心脏、肝、肾、肺等生物化人工器官的研究方面等研究均取的了一定的成果,并有一些产品已经投放市场。全球组织工程市场份额到2020年预计将超过150亿美元,具有强大的研究价值。 随着组织工程技术的发展,利用生物材料和种子细胞构建的组织工程肝脏,可以在一定程度上模拟肝脏的合成、解毒、代谢和分泌等生理性功能,可经体内移植治疗终末期肝病,是组织功能领域的研究热点。针对器官移植供体不足的现状,功能性组织工程肝脏在器官替代及修复方向的研究具有广阔的应用前景。目前研究热点主要集中在以下几个方向。 2.2.1 生物材料的优化 目前已有大量生物材料被应用于组织工程肝脏的构建中,包括合成型高分子聚合物、天然细胞外基质和脱细胞支架。 合成型高分子聚合物:是一类具有生物相容性、可降解的合成多聚物,在组织工程应用中具有较大的应用潜能,主要包括乳酸-羟基乙酸、聚乳酸、聚己内酯、聚乙二醇等,目前已被广泛应用于种子细胞的二维培养,以及皮肤、骨、软骨、血管等组织器官的构建。有研究将聚乳酸支架联合肝细胞种植于Lewis大鼠肠系膜内,发现肝细胞均匀地分布于支架内,并呈现出良好的活性[29];LI等[30]研究发现胶原修饰的乳酸-羟基乙酸支架可提高体外培养肝细胞的黏附、增殖能力,是理想的生物材料。但合成型材料生物相容性不足,缺乏理想的解剖微结构,由此构建的组织肝脏在结构及功能上不够理想。 天然细胞外基质成分:主要包括胶原、纤连蛋白、弹性蛋白和壳聚糖等,这些材料在生物相容性、生物可降解性、解剖微结构等特性上更接近原始器官组织。研究发现,弹性蛋白样多肽可促进组织器官的结构形成及提供肝细胞的功能[31]。同时KIM等[32]将骨髓间充质干细胞培养于海藻酸盐支架内,细胞表达肝细胞特异性标记物,同时表现出肝脏特异性功能。这些研究均表明天然细胞外基质成分在组织工程领域中的优势,但由于肝脏组织结构及功能的复杂性,基于该材料构建具有一定结构和功能的肝脏工程组织仍面临着一系列挑战,如脉管结构及适宜微环境的构建问题等。 脱细胞支架:是一种通过物理、酶解或者化学法对完整肝脏进行脱细胞处理获得的生物支架。这种支架不仅保留了肝脏的主要细胞外基质成分,其内的脉管结构也得到了很好保存,其最大限度地还原了体内肝细胞生长的微环境,为种子细胞的生长、发育提供了适宜的微环境,是肝脏再生的优良材料。与以往的支架材料相比,脱细胞支架免疫原性低,且其细胞外基质及血管结构的保留使其成为组织工程领域的研究热点。目前已有研究者将人胎肝细胞、原代鼠肝细胞、干细胞等对脱细支架进行细胞再植,并成功在体外构建了具有一定功能的肝脏器官。UYGUN等[33]将再细胞化的脱细胞支架进行大鼠体内移植,虽只在体8 h,但在一定程度上证实了脱细胞-再细胞化技术构建组织工程肝进行体内移植的可行性。BAO等[34]则将再细胞化的全肝脱细胞支架移植入预先经90%肝切的大鼠体内,72 h后移植肝细胞仍保持活性,并表达了大量肝功能相关基因,但实验组(再细胞化肝脏支架治疗)与对照组(假手术组)均出现了小肝综合征。回顾这些实验发现,凝血问题是组织工程肝脏体内移植面临的关键问题。目前,支架的内皮细胞化、肝素化研究在抗凝问题上已取得了不少进展,但仍需加大研究力度以保障组织工程肝脏体内移植的顺利开展。 2.2.2 生物支架的抗凝 如何构建稳定、成熟的血管网络结构,是目前功能性类肝脏组织研究中亟待解决的关键难题。这是支架体内移植成功与否,组织工程肝脏能否充分发挥功能的关键所在。目前已有大量研究尝试进行了多种抗凝方案。 抗凝药物的应用:系统性药物干预包括抗凝剂及抗血小板药物的应用,其不良反应明显,同时抗凝效果不佳[35]。新研发的抗凝药物较传统的抗凝剂具有更小的不良反应及药物间相互作用减弱等优势。然而新型抗凝剂幷没有相应的拮抗剂[36]。目前,支架材料表面抗凝修饰在生物医学领域中具有重要应用价值[37],其中材料表面聚合电解质多层分布修饰是一项易于操作、多功能技术[38]。BAO等[34]采用层层自组装技术对移植肝脏支架进行内表面肝素抗凝修饰,其原理是:通过带电聚合物的“桥梁”作用实现肝素与细胞外基质的黏附,带电聚合物与肝素对血管内壁的反复多次铺陈,从而达到更好的肝素化效果。在生物相容性方面,该研究所采用的带正电荷聚合物-聚(二烯丙基二甲基氯化铵)幷不是理想的选择。而鱼精蛋白的生物相容性好,是理想的替代物[39]。另外,通过鱼精蛋白对支架内表面进行肝素抗凝修饰可能对提高支架再细胞化效率具有重要作用。 支架的内皮细胞化:血管腔内表面内皮细胞的完全覆盖,可有效抗血栓形成以及保证血管功能。目前,内皮细胞化已被广泛应用于心脏瓣膜[40]、骨组织工程[41]、肝脏等生物材料等研究领域[42],并取得了突破性进展。种植的内皮细胞黏附于材料管腔壁生长,形成一层较为完整的内皮层,可在一定程度上起到抗凝血的效果。但单纯内皮细胞构建的血管结构缺乏弹性和可扩张性,在血流动力学中的调节作用有限;稳定性不强,可随着体内移植时间的延长,血管结构逐渐退化;血管结构完整性不够,易发生渗漏现象,不利于后期的体内移植研究。大量研究表明,将内皮细胞、周细胞或血管平滑肌细胞、纤维母细胞等实质细胞共培养于支架内,可有效促进血管的成熟及维持血管结构的完整性,从而提高组织工程结构的血管化,经体内移植后可明显缩短与体内血管吻合的时间[43]。REN等[44]利用可诱导多潜能干细胞来源的周细胞和内皮细胞对大鼠和人的肺脱细胞支架联合再种植构建功能性肺血管,体外实验发现血管结构完整,体内移植后3 d未见血栓形成。同时研究显示胶原凝胶等生物材料构成的人工合成三维支架内,在内皮细胞与骨髓间充质干细胞共培养条件下,骨髓间充质干细胞经血小板源性生长因子的介导向内皮细胞迁移,两种细胞之间的相互接触效应可诱导骨髓间充质干细胞转分化为平滑肌细胞,其中转化生长因子1参与此诱导分化过程,从而维持血管结构的稳定[45]。鉴于现有的大量研究进展,基于全肝脱细胞支架的多细胞联合种植是目前构建功能性肝脏组织的研究热点。而如何优化多细胞之间的种植比例、不同细胞的再细胞化方案及再细胞化支架的体外培养时间都迫切需要进一步的研究来提高其抗凝效果。 2.2.3 组织工程肝脏构建的关键技术 生物材料内细胞-细胞、细胞-基质之间的相互接触作用,支架的解剖微结构及微环境,对功能性组织工程肝脏的构建至关重要。通过优化种子细胞的培养环境模拟正常组织器官的生理结构,促进功能性组织肝脏的构建。目前已有多种技术被应用于组织功能肝脏构建过程中的支架构建、再细胞化技术、灌流培养等。 脱细胞技术:由于脱细胞支架在组织工程领域的优越性,脱细胞技术已被广泛用于多种器官的脱细胞处理,如肺[46]、肾脏[47]、心脏和肝脏等[48-49]。为了优化脱细胞技术,多方面因素需要被优化,比如洗脱试剂、组织特点及相应的脱细胞技术。目前常用的脱细胞方法主要有化学处理法、物理处理法、酶处理法[50]。针对不同组织采取相应的脱细胞技术可获得较佳的脱细胞效果。对于薄层组织如皮肤、膀胱、小肠等,物理处理法即可有效洗脱细胞。对于完整的器官组织如肝脏、心脏和肾脏等,单纯地酶、渗透液或两性离子处理法脱细胞效率不高[51],而经血管灌注洗脱剂的化学或酶处理法是最佳的选择。随着脱细胞技术的优化,所获得生物支架的生物相容性更佳,解剖结构更加贴近生理结构,在组织功能肝脏的构建上具有极好的优势。 支架的再细胞化技术:早期研究显示,由成年小鼠肝脏分离获得的祖细胞具有多向分化潜能,在支架的特定环境下可定向分化为多种细胞系,从而形成类肝组织,该过程与体内肝脏发育过程类似。目前虽然尚未构建出类似的人类肝组织,但已有研究表明将人可诱导多潜能干细胞来源的肝样细胞、人间充质干细胞和人内皮细胞混合培养于基质材料内,细胞可自行组装成功能性3D肝芽样聚合物[52],见图2。由此可见多细胞联合种植在组织工程肝脏构建中的重要性。BAPTISTA等[53]发现经腔静脉移植的细胞主要定植于中央静脉的周边,而经门静脉移植的细胞主要定植于汇管区部分。同时研究表明血流剪切力可促进内皮细胞的黏附、增殖,而间质细胞易受剪切力的作用而损伤。基于上述研究结果,有研究者提出假说:两种途径的联合移植是否可有效实现全肝脱细胞支架的再细胞化,从而可有效阻止血管腔内血栓形成。 "

3D打印技术:可按照预先设计的三维模型准确定位装配细胞/材料复合物,为用人源细胞构建复杂组织器官模型,尽管目前生物3D打印技术已实现了体外手术模型和人体类器官的打印,并已在简单的组织(如皮肤、血管等)和体外药物测试模型方面取得了长足的进展[54],但还没有发展到可以替代人源器官的程度。最近有学者利用可诱导多潜能干细胞分化来源的肝细胞进行3D打印微肝组织支架,显示出较高的白蛋白分泌功能与尿素转化能力;肝细胞结合内皮细胞和成纤维细胞3D打印共培养更显示出良好的生物学功能[55-56],为今后3D 打印人工肝脏奠定了基础。 2.3 异种器官移植 异种移植是解决人类器官供体严重短缺的最佳途径。21世纪初,科学家开始利用新兴的基因编辑和体细胞克隆技术构建异种移植供体猪,并开展了大量“猪-非人灵长类异种移植”,不断刷新着异种移植物在非人灵长类体内的最长存活时间。动物器官人源化是将人源干细胞注入改造后的动物胚胎内,待其充分发育成熟,获得包含由人类细胞发育而来的器官的嵌合动物。南京医科大学戴一凡教授团队曾利用CRISPR/Cas9基因编辑技术同时敲除3个关键猪糖分子基因(GGTA1/CMAH/β4GalNT2 genes),被认为可消除异种移植的超级性排斥反应。中国科学院广州生物医药与健康研究院赖良学研究员团队曾获得了世界上第一头基因敲除半乳糖苷转移酶克隆猪。最新厦门大学夏宁绍教授团队与浙江大学李君教授团队利用人骨髓间充质干细胞移植成功创建了肝细胞与免疫细胞双嵌合的人源化小鼠[57],为未来在猪、羊等大动物体内培育“人体器官”奠定了基础。上述成果被认为向异种器官移植迈出的关键一步,但该技术距离临床应用依然还有很长的路要走。 "

| [1] 沈中阳,陆伟.中国肝移植乙型肝炎防治指南(2016版)[J].临床肝胆病杂志,2017,33(2):213-220. [2] 刘昶荣.卫健委:2017年我国器官移植手术量世界第二. https://baijiahao.baidu.com/s?id=1607589663010107836,中国青年报中青在线.2018-08-01. [3] 中华人民共和国国家卫生健康委员会.2019年最新公布:169所器官移植医疗机构名单. http://www.nhc.gov.cn/wjw/qgyzjg/ 201902/f2f2bb84e2ac4cf5993e9c7c5d30def3.shtml2019-02-25. [4] 朱继业,高鹏骥.我国公民逝世后器官捐献肝移植现状[J].中华肝脏外科手术学电子杂志,2016,5(5):273-276. [5] 范晓礼,叶啟发,王彦峰,等.比较心脏死亡器官捐赠与脑死亡器官捐赠供肝肝移植预后的荟萃分析[J].中华器官移植杂志, 2014, 35(2):86-93. [6] 谢文勇,李涛. 活体肝移植的研究进展[J].器官移植,2018,9(4): 250-254. [7] EUROPEAN ASSOCIATION FOR THE STUDY OF THE LIVER. EASL Clinical Practice Guidelines: Liver transplantation. J Hepatol.2016;64(2):433-485. [8] ZHANG J, ZHAO X, LIANG L, et al.A decade of progress in liver regenerative medicine Biomaterials. 2018;157: 161-176. [9] STRAIN AJ, NEUBERGER JM. A bioartificial liver--state of the art. Science. 2002; 295(5557): 1005-1009. [10] MEDICINE POR.Principles of Regenerative Medicine. Elsevier Inc. 2008:928-945. [11] ENOSAWA S, MIYASHITA T, TANAKA H, et al.Prolongation of survival of pigs with ischemic liver failure by treatment with a bioartificial liver using glutamine synthetase transfected recombinant HepG2. Transplant Proc. 2001;33(1-2): 1945-1947. [12] NIU D, WEI HJ, LIN L, et al.Inactivation of porcine endogenous retrovirus in pigs using CRISPR-Cas9. Science. 2017;357(6357):1303-1307. [13] LIU Q, LIU Z, DALAKAS E. Prevalence of porcine endogenous retrovirus in Chinese pig breeds and in patients treated with a porcine liver cell-based bioreactor. World J Gastroenterol. 2005;11(30):4727-4730. [14] DUAN Y, MA X, MA X, et al. Differentiation and characterization of metabolically functioning hepatocytes from human embryonic stem cells.Stem Cells. 2010;28(4): 674-686. [15] SHI XL, GAO Y, YAN Y, et al.Improved survival of porcine acute liver failure by a bioartificial liver device implanted with induced human functional hepatocytes. Cell Res. 2016;26(2): 206-216. [16] ZHANG K, ZHANG L, LIU W, et al.In Vitro Expansion of Primary Human Hepatocytes with Efficient Liver Repopulation Capacity. Cell Stem Cell.2018;23(6):806-819.e4. [17] FU GB, HUANG WJ, ZENG M, et al.Expansion and differentiation of human hepatocyte-derived liver progenitor-like cells and their use for the study of hepatotropic pathogens. Cell Res. 2019;29(1):8-22. [18] LI J, LI LJ, CAO HC, et al.Establishment of highly differentiated immortalized human hepatocyte line with simian virus 40 large tumor antigen for liver based cell therapy. ASAIO J.2005;51(3):262-268. [19] LEE SY, KIM HJ, CHOI D.Cell sources, liver support systems and liver tissue engineering: alternatives to liver transplantation. Int J Stem Cells.2015;8(1):36-47. [20] MILLIS JM, CRONIN DC, JOHNSON R, et al. Initial experience with the modified extracorporeal liver-assist device for patients with fulminant hepatic failure: system modifications and clinical impact. Transplantation.2002; 74(12):1735-1746. [21] LV G, ZHAO L, ZHANG A, et al.Bioartificial liver system based on choanoid fluidized bed bioreactor improve the survival time of fulminant hepatic failure pigs. Biotechnol Bioeng. 2011; 108(9):2229-2236. [22] MAZARIEGOS GV, PATZER JF, LOPEZ RC, et al.First clinical use of a novel bioartificial liver support system (BLSS).Am J Transplant.2002;2(3):260-266. [23] QIAN Y, LANJUAN L, JIANRONG H, et al.Study of severe hepatitis treated with a hybrid artificial liver support system.Int J Artif Organs.2003;26(6):507-513. [24] DEMETRIOU AA, BROWN RS, BUSUTTIL RW, et al. Prospective, randomized, multicenter, controlled trial of a bioartificial liver in treating acute liver failure. Ann Surg. 2004;239(5):660-667; discussion 667-670. [25] SAUER IM, KARDASSIS D, ZEILLINGER K, et al.Clinical extracorporeal hybrid liver support--phase I study with primary porcine liver cells.Xenotransplantation.2003;10(5): 460-469. [26] HOLLISTER SJ, MURPHY WL.Scafold translation:barriers between concept and clinic. Tissue Eng Part B Rev. 2011;17(6): 459-474. [27] YANNAS IV, BURKE JF, GORDON PL, et al. Design of an artificial skin. II. Control of chemical composition.J Biomed Mater Res.1980;14(2):107-132. [28] VACANTI JP, MORSE MA, SALTZMAN WM, et al. Selective cell transplantation using bioabsorbable artificial polymers as matrices.J Pediatr Surg.1988;23(1 Pt 2):3-9. [29] SOTO-GUTIERREZ A, ZHANG L, MEDBERRY C, et al.A whole-organ regenerative medicine approach for liver replacement. Tissue Eng Part C Methods. 2011;17(6): 677-686. [30] LI J, LI L, YU H, et al.Growth and metabolism of human hepatocytes on biomodified collagen poly(lactic-co-glycolic acid) three-dimensional scaffold.ASAIO J. 2006;52(3): 321-327. [31] JANORKAR AV, RAJAGOPALAN P, YARMUSH ML, et al. The use of elastin-like polypeptide-polyelectrolyte complexes to control hepatocyte morphology and function in vitro. Biomaterials.2008;29(6):625-632. [32] KIM IY, SEO SJ, MOON HS, et al.Chitosan and its derivatives for tissue engineering applications. Biotechnol Adv. 2008; 26(1):1-21. [33] UYGUN BE, SOTO-GUTIERREZ A, YAGI H, et al. Organ reengineering through development of a transplantable recellularized liver graft using decellularized liver matrix. Nat Med.2010;16(7): 814-820. [34] BAO J, SHI Y, SUN H, et al. Construction of a portal implantable functional tissue-engineered liver using perfusion-decellularized matrix and hepatocytes in rats. Cell Transplant.2011;20(5): 753-766. [35] GUTHRIE R. Review and management of side effects associated with antiplatelet therapy for prevention of recurrent cerebrovascular events. Adv Ther.2011;28(6):473-482. [36] ROJAS-HERNANDEZ CM, GARCIA DA.The novel oral anticoagulants. Semin Thromb Hemost.2013; 39(2):117-126. [37] DUQUE SL, BRACK N, POSTMA A, et al. Surface modification of electrospun fibres for biomedical applications: A focus on radical polymerization methods. Biomaterials. 2016;106:24-45. [38] ZHANG J, SENGER B, VAUTIER D, et al. Natural polyelectrolyte films based on layer-by layer deposition of collagen and hyaluronic acid. Biomaterials. 2005;26(16): 3353-3361. [39] SAMUEL RE, SHUKLA A, PAIK DH, et al. Osteoconductive protamine-based polyelectrolyte multilayer functionalized surfaces. Biomaterials.2011;32(30):7491-502. [40] SÁNCHEZ PL, FERNÁNDEZ-SANTOS ME, COSTANZA S, et al. Acellular human heart matrix: A critical step toward whole heart grafts.Biomaterials.2015;61:279-289. [41] SONG X, SHI L, CHEN L, et al. Endothelial cells modified by adenovirus vector containing nine copies hypoxia response elements and human vascular endothelial growth factor as the novel seed cells for bone tissue engineering.Acta Biochim Biophys Sin (Shanghai).2017;49(11): 973-978. [42] KO IK, PENG L, PELOSO A, et al.Bioengineered transplantable porcine livers with re-endothelialized vasculature. Biomaterials.2015;40:72-79. [43] KIM JJ, HOU L, HUANG NF. Vascularization of three-dimensional engineered tissues for regenerative medicine applications. Acta Biomater.2016;41:17-26. [44] REN X, MOSER PT, GILPIN SE, et al. Engineering pulmonary vasculature in decellularized rat and human lungs. Nat Biotechnol. 2015;33(10):1097-1102. [45] HONG M, JO H, ANKENY RF, et al.Influence of mesenchymal stem cells on the response of endothelial cells to laminar flow and shear stress.Cells Tissues Organs.2013;198(4): 289-299. [46] MAHDAVI SN, BAHARARA J, TAKBIRI M, KHAJEH AS. In vitro Decellularization of Rabbit Lung Tissue. Cell J. 2013; 15(1): 83-88. [47] SULLIVAN DC, MIRMALEK-SANI SH, DEEGAN DB, et al. Decellularization methods of porcine kidneys for whole organ engineering using a high-throughput system. Biomaterials. 2012;33(31): 7756-7764. [48] REMLINGER NT, WEARDEN PD, GILBERT TW.Procedure for decellularization of porcine heart by retrograde coronary perfusion.J Vis Exp.2012;(70):e50059. [49] ARENAS-HERRERA JE, KO IK, ATALA A, YOO JJ. Decellularization for whole organ bioengineering. Biomed Mater. 2013;8(1):014106. [50] BADYLAK SF, TAYLOR D, UYGUN K. Whole-organ tissue engineering: decellularization and recellularization of three-dimensional matrix scaffolds. Annu Rev Biomed Eng. 2011;13:27-53. [51] GUI L, CHAN SA, BREUER CK, et al. Novel utilization of serum in tissue decellularization. Tissue Eng C Methods.2010; 16(2):173-184. [52] TAKEBE T, SEKINE K, ENOMURA M, et al. Vascularized and functional human liver from an iPSC-derived organ bud transplant. Nature.2013;499(7459):481-484. [53] BAPTISTA PM, SIDDIQUI MM, LOZIER G, et al. The use of whole organ decellularization for the generation of a vascularized liver organoid. Hepatology.2011;53(2):604-617. [54] MURPHY SV, ATALA A. 3D bioprinting of tissues and organs. Nat Biotechnol. 2014;32(8):773-785. [55] MA X, QU X, ZHU W, et al. Deterministically patterned biomimetic human iPSC-derived hepatic model via rapid 3D bioprinting. Proc Natl Acad Sci U S A.2016;113(8):2206-2211. [56] LEE JW, CHOI YJ, YONG WJ, et al. Development of a 3D cell printed construct considering angiogenesis for liver tissue engineering. Biofabrication. 2016;8(1): 015007. [57] YUAN L, JIANG J, LIU X, et al. HBV infection-induced liver cirrhosis development in dual-humanised mice with human bone mesenchymal stem cell transplantation. Gut. 2019; 68(11):2044-2056. |
| [1] | Wang Menghan, Qi Han, Zhang Yuan, Chen Yanzhi. Three kinds of 3D printed models assisted in treatment of Robinson type II B2 clavicle fracture [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1403-1408. |
| [2] | Yang Yufang, Yang Zhishan, Duan Mianmian, Liu Yiheng, Tang Zhenglong, Wang Yu. Application and prospects of erythropoietin in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1443-1449. |
| [3] | Chen Kaijia, Liu Jingyun, Cao Ning, Sun Jianbo, Zhou Yan, Mei Jianguo, Ren Qiang. Application and prospect of tissue engineering in treatment of osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1450-1456. |
| [4] | Mei Jingyi, Liu Jiang, Xiao Cong, Liu Peng, Zhou Haohao, Lin Zhanyi. Proliferation and metabolic patterns of smooth muscle cells during construction of tissue-engineered blood vessels [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1043-1049. |
| [5] | Wang Shanshan, Shu Qing, Tian Jun. Physical factors promote osteogenic differentiation of stem cells [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1083-1090. |
| [6] | Ning Tianliang, Wang Kun, Wang Lingbiao, Han Pengfei. Finite element analysis on correction effect of varus foot orthosis based on the three-point force principle [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 891-899. |
| [7] | Wang Yeyuan, Du Yilang, Yu Dehao, Ning Fengting, Bai Bing. Effect of micro-arc oxidation treatment on biological activity of medical metals [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 771-776. |
| [8] | Chen Xiaofang, Zheng Guoshuang, Li Maoyuan, Yu Weiting. Preparation and application of injectable sodium alginate hydrogels [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 789-794. |
| [9] | Wang Jiani, Chen Junyu. Angiogenesis mechanism of metal ions and their application in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 804-812. |
| [10] | Zhang Ya, Mu Qiuju, Wang Zilin, Liu Hongjie, Zhu Lili. Hydrogel loaded with platelet-rich plasma promotes wound healing in diabetic rats [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 690-696. |
| [11] | Shen Ziqing, Xia Tian, Shan Yibo, Zhu Ruijun, Wan Haoxin, Ding Hao, Pan Shu, Zhao Jun. Vascularized tracheal substitutes constructed by exosome-load hydrogel-modified 3D printed scaffolds [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 697-705. |
| [12] | Zhu Liwei, Wang Jiangyue, Bai Ding. Application value of nanocomposite gelatin methacryloyl hydrogels in different bone defect environments [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 753-758. |
| [13] | Yang Yuqing, Chen Zhiyu. Role and application of early transient presence of M1 macrophages in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 594-601. |
| [14] | Gu Mingxi, Wang Changcheng, Tian Fengde, An Ning, Hao Ruihu, Guo Lin. Preparation and in vitro evaluation of a three-dimensional porous cartilage scaffold made of silk fibroin/gelatin/chitosan [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 366-372. |
| [15] | Xu Xiaodong, Zhou Jiping, Zhang Qi, Feng Chen, Zhu Mianshun, Shi Hongcan. 3D printing process of gelatin/oxidized nanocellulose skin scaffold with high elastic modulus and high porosity [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 398-403. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||