Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (20): 3256-3262.doi: 10.3969/j.issn.2095-4344.2684
Previous Articles Next Articles
Mechanism by which autophagy-mediated exercise improves bone metabolic disorder in type 2 diabetes
Lu Pengcheng, Chen Xianghe, Yang Kang, Yu Huilin, Liu Bo
- School of Physical Education, Yangzhou University, Yangzhou 225127, Jiangsu Province, China
-
Received:2019-11-01Revised:2019-11-12Accepted:2019-12-19Online:2020-07-18Published:2020-04-14 -
Contact:Chen Xianghe, Lecturer, School of Physical Education, Yangzhou University, Yangzhou 225127, Jiangsu Province, China -
About author:Lu Pengcheng, School of Physical Education, Yangzhou University, Yangzhou 225127, Jiangsu Province, China -
Supported by:the General Project of Natural Science Foundation of Jiangsu Provincial Universities, No. 17KJB180017
CLC Number:
Cite this article
Lu Pengcheng, Chen Xianghe, Yang Kang, Yu Huilin, Liu Bo. Mechanism by which autophagy-mediated exercise improves bone metabolic disorder in type 2 diabetes[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(20): 3256-3262.
share this article

2.1 自噬简述 细胞的代谢形式主要有三类:自噬、凋亡和坏死[7]。自噬是真核细胞的一种主要分解代谢方式,可通过与溶酶体结合形成自噬溶酶体降解细胞内受损的细胞器和过度累积的蛋白质。自噬可分为:①UNC-51-类似自噬激活激酶1(UNC-51-like kinase 1, ULK1)复合物和磷脂酰肌醇3-激酶(phosphatidylinositol 3-kinase,PI3K)复合物结合形成磷脂酰肌醇3-磷酸(phosphatidylinositol 3-phosphate, PI3P),自噬研究相关基因9(autophagy research related gene,ATG9)提供相关膜形成吞噬泡过程;②ATG12促进自噬体膜延伸,微管相关蛋白1轻链3 (microtubule-associated protein 1 light 3,LC3)使其关闭形成自噬体,自噬酶体和溶酶体融合形成自噬溶酶体;③通过降解内容物释放能量并在细胞内循环使用[8],见表1。自噬关键基因Beclin-1、LC3-Ⅱ等通过与白细胞介素6、沉默信息调节因子1、Cx43等关键分子或蛋白作用,从而在能量代谢、骨代谢、心肌细胞损伤、炎症反应等生物学过程中发挥重要调控作用[9]。 "

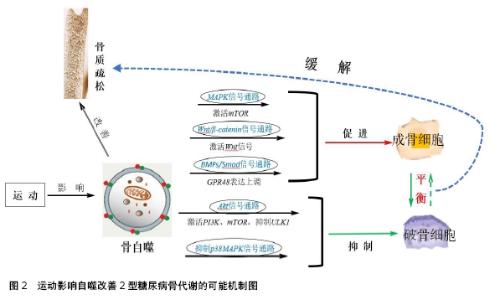
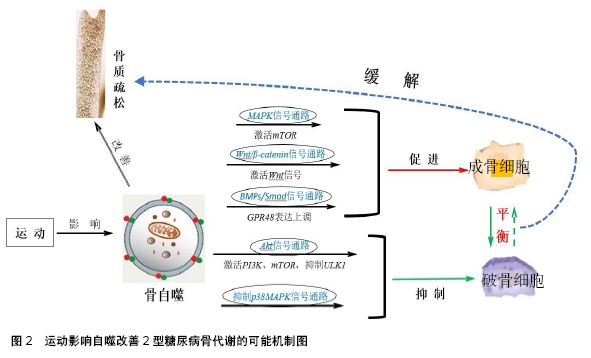
2.2 自噬对2型糖尿病骨代谢的作用影响 体内胰岛素抵抗和β细胞分泌失调会引起血糖的升高,最终导致2型糖尿病发生。在2型糖尿病前期,胰脏内胰岛β细胞过度分泌胰岛素以应对胰岛素抵抗;后期,胰岛β细胞受损,胰岛素分泌缺陷,机体出现高血糖[7]。2型糖尿病高血糖症状激增破骨细胞活性,骨量丢失增多,致使骨密度和骨强度降低[10]。现已发现,骨代谢信号通路的参与及影响类型主要有如下几个:细胞外调节蛋白激酶(extracellular regulated protein kinases,ERK)/p38MAPK通路、Wnt/ β-catenin通路、骨形态发生蛋白(bone morphogenetic proteins,BMPs)/Smad通路、RANK/RANKL信号通路、Hedgehog信号通路、小眼畸形相关转录因子(microphthalmia associated transcription factor, MITF)信号通路和过氧化物酶体增殖激活受体信号通路等,以上通路均与自噬密切相关[11-12]。而自噬在维持细胞活性、促进能量代谢和内环境稳态中发挥了重要的作用,有研究发现,在饮食肥胖小鼠模型体内观察到肝脏自噬水平下调[13],进而导致了胰岛素抵抗的出现,而恢复肥胖模型小鼠的自噬功能可以加强胰岛素作用,结果发现自噬在胰岛信号途径中发挥了重要的作用,而自噬也是影响胰岛素抵抗产生的重要原因。此外,自噬促进物质的循环不仅体现在促进能量代谢,而在维持肥胖和胰岛素抵抗患者机体的代谢平衡也扮演重要角色。对此,MAHMOUD等[14]通过研究发现高血糖和高胰岛素血症可以促使自噬小体和自噬溶酶体的积累,进而诱导自噬的发生;范梦琳等[15]也就此得出结果:自噬功能的缺失与胰岛素抵抗的发生有密切的关系,自噬也可调控胰岛素抵抗。那么,自噬如何通过相关信号通路实现对2型糖尿病骨代谢的调控呢?以下将就成骨细胞和破骨细胞对自噬在2型糖尿病骨代谢的作用机制进行综述。 2.2.1 自噬介导2型糖尿病抑制成骨细胞分化中的作用 成骨细胞源于间充质干细胞,与骨细胞的代谢密切相关。在成骨细胞向骨细胞分化的过程中会不断分泌骨胶原、骨基质,当成骨细胞进入骨基质时,自噬发挥重要作用,此过程中骨细胞的形态会发生明显变化,细胞器增多和增大[16]。在对成骨细胞自噬的研究中发现,在观察骨髓间充质干细胞向成骨细胞分化和矿化过程中发现细胞自噬功能明显加强,而运动促进成骨细胞的分化可能与自噬水平加强有关[17]。如对颅骨的成骨细胞分化研究中发现自噬流显著增加,这也表明了自噬参与了颅骨早期的成骨细胞分化[18]。另外又有研究提出,高糖高胰岛素会促进骨髓间充质干细胞衰老,提高骨髓间充质干细胞自噬程度,进而抑制成骨细胞分化及其骨形成能力[19]。NBR1(Neighbor of BRCA1 gene 1)基因作为选择性自噬的重要底物识别蛋白,WHITEHOUSE等[20]在对大鼠体内表达自噬的运送受体NBR1去除后,大鼠的骨基质、骨密度和骨含量等均显著下降,且随年龄的增长有升高的趋势。更有研究发现,敲除NBR1基因的大鼠体内p62活性却有所提高,而p62参与了调节骨组织细胞自噬的重要通路,由此可以说明NBR1基因对成骨细胞的自噬过程有着重要的影响;进一步研究发现NBR1基因对骨细胞自噬有影响的同时,NBR1基因的缺失还会对p38MAPK的调节作用有着一定影响,经ERK/p38MAPK通路对成骨细胞自噬施加影响。 在对2型糖尿病的研究中发现,胰岛素可以直接刺激成骨细胞,促进其细胞内的氨基酸积累、骨胶原及骨基质的合成与分泌[3]。此外,高糖环境能过度产生活性氧,加速成骨MC3T3-E1细胞中的自噬作用,高糖环境抑制了成骨细胞自噬,而自噬关键蛋白分子表达下调则会抑制成骨细胞分化[21],由此可以表明自噬在高血糖环境中可以维持成骨细胞的活性和功能,促进成骨细胞分化。此外,骨髓间充质干细胞在高糖环境下也会启动自噬来加强对衰老细胞的吞噬,同时提高成骨细胞分化及骨形成能力,保证骨量和骨质两者之间平衡,预防骨质疏松发生。即表现为2型糖尿病可以通过介导Wnt/β-catenin通路中的相关因子表达来实现2型糖尿病抑制骨髓间充质干细胞向成骨细胞分化以及促进成脂细胞分化的调节。因此,DAI等[22]实验得出结论,成骨细胞是促进骨形成的关键细胞,成骨细胞的自噬活性水平的降低会导致骨形成减少,骨骼质量下降和骨基质数量降低,进而影响骨组织细胞的代谢能力。 2.2.2 自噬在2型糖尿病促进破骨细胞分化中的作用 破骨细胞作为骨代谢中的重要参与细胞类型之一,是骨组织细胞中唯一具有骨吸收功能的多核细胞。2型糖尿病会导致骨吸收水平提高,促使骨吸收能力增强。而运动抑制2型糖尿病的破骨细胞分化、融核及骨吸收能力,进而改善其骨组织形态结构和骨质疏松[23]。破骨细胞具有特殊的吸收功能,在骨组织细胞代谢过程及某些局部炎症病灶的吸收中,自噬扮演重要角色。细胞内的环化酶活性的改变,会促使环磷酸腺苷指数随之升高,此时蛋白质激酶被唤醒会导致细胞内环境呈现一种磷酸化状态,致使溶酶体向细胞膜移动,随后溶酶体内的蛋白质水解酶会分泌进入细胞内环境,分解和消除陈旧的骨基质。而溶酶体是自噬体形成的必要阶段和必不可缺的重要前体,对自噬这一过程具有重要意义。这提示,自噬可参与调节破骨细胞的活性和骨的吸收功能。p62作为自噬关键调控蛋白,可作为运送受体来调节自噬,连结由RANKL诱导的自噬和破骨细胞分化及骨吸收能力。研究发现,敲除p62蛋白不仅会抑制破骨细胞中RANKL诱导自噬的产生,还会抑制破骨细胞分化,即自噬通过p62经RANKL通路影响破骨细胞的自噬水平[24]。此外,为证实p62蛋白是否参与了自噬调节营养感知信号通路,是否会影响ATG5基因对破骨细胞吸收和分解陈旧骨基质的作用过程,DESELM等[24]在敲除可表达ATG5、ATG7、ATG4b和LC3大鼠基因的实验中发现,破骨细胞缺失ATG5基因表达时并不会受到影响,但却发现破骨细胞表面的皱褶缘形成发生了变化,破骨细胞吸收能力下降,骨量丢失减少,骨体积增大。此外,当敲除ATG7、ATG4b和LC3的大鼠实验中也发现了类似结果。以上数据表明,破骨细胞在进行分化、吸收分解以及细胞表面的皱褶缘发生形变时均需要ATG5、ATG7、ATG4b和LC3等相关基因蛋白的参与,即自噬在破骨细胞分化中扮演重要角色[25]。 破骨细胞主导骨组织细胞的吸收,过量的骨降解和吸收会导致骨量的丢失及骨细胞的减少,促使2型糖尿病骨代谢紊乱,最终导致了骨质疏松的发生[26]。成骨细胞在不断分化为骨细胞的同时,细胞自身会通过吸收、降解细胞内受损的蛋白质和细胞器来改变细胞的形态结构、数量、大小及功能。这一现象与自噬发生的机制十分相似,因此HOCKING等[27]研究发现,自噬一直存在于骨细胞内部,同时也存在于成骨细胞向骨细胞的转化以及破骨细胞对陈旧骨细胞的吸收降解过程中,而骨细胞一直处于一种缺氧的矿物质环境之中,其自噬水平显著高于成骨细胞。 2型糖尿病因胰岛素抵抗和胰岛β细胞功能缺陷致使机体内分泌和代谢功能紊乱,进而引起成骨细胞分化及骨形成能力降低和破骨细胞吸收功能的增强,导致骨量减少。胰岛素因分泌不足导致机体代谢紊乱,不能充分利用葡萄糖产生能量,进而促使蛋白质和脂肪的消耗,形成负氮平衡,骨胶原分解增多、合成变少,骨基质数量减少,最终造成骨量丢失[28]。骨髓间充质干细胞作为机体骨代谢中的重要多潜能干细胞,在2型糖尿病骨重建、造血、免疫等方面有重要调控作用,而有研究发现骨髓间充质干细胞在高糖培养环境下,为了维持自身稳态会导致自噬水平显著升高,加快对细胞衰老激动剂的清除[19]。并且,研究最后得出结论:骨髓间充质干细胞在高糖培养环境下LC3-Ⅱ高表达,以及LC3-Ⅰ/LC3-Ⅱ的比值明显低于低糖培养环境,说明骨髓间充质干细胞在高糖环境下自噬水平显著升高。另有实验发现,2型糖尿病小鼠骨组织内当p38MAPK信号通路受到抑制时,p38MAPK蛋白活性下降[29],其对破骨细胞异常分化、融合等抑制减弱,骨吸收能力增强,骨密度下降,骨细胞数量减少。由此可以发现,骨组织细胞在高糖环境下,p38MAPK信号通路中的NBR1基因会诱导自噬水平升高,进而提高成骨细胞分化及骨形成能力,保持成骨细胞和破骨细胞两者之间的代谢平衡,预防骨质疏松产生。此外,有实验通过特异性敲除大鼠骨细胞中的ATG7基因来实现对自噬水平的抑制,结果发现大鼠骨组织皮质骨骨密度显著下降,进一步证实了自噬可以调控骨细胞分化及代谢[30-31]。据以上所述,自噬对2型糖尿病骨细胞的分化及功能发挥具有积极的调控作用。 2.3 自噬介导运动影响2型糖尿病骨代谢的作用机制 自噬对2型糖尿病骨代谢有着重要作用,并且运动可显著改善2型糖尿病骨代谢,但自噬是否可以介导运动改善2型糖尿病骨代谢?这也将成为接下来所要探讨的重点。2型糖尿病作为一种全身性代谢疾病,致使胰岛素抵抗和胰岛β细胞分泌功能缺陷,进而导致骨吸收大于骨形成,骨代谢紊乱,骨含量降低,造成骨质疏松。运动是一种成本低、绿色的良好干预手段,随着深入的科学研究,发现运动可作为缓解和改善2型糖尿病骨质疏松的一种有效干预方式。而自噬如何介导运动实现对2型糖尿病骨代谢紊乱的改善作用?研究发现,合理适量的运动可以促进自噬水平的增强,进而调节骨代谢,保证骨吸收和骨形成之间的代谢平衡,提高骨密度和骨含量。2型糖尿病会造成胰岛细胞分泌系统功能紊乱,抑制成骨细胞分化,使破骨细胞降解能力高于成骨细胞的分化能力,骨组织细胞降解过多,最终导致骨量丢失严重。运动作为一种非药物性干预,可直接促进机体新陈代谢,有效改善2型糖尿病骨代谢能力。在此过程中,自噬关键蛋白或分子发挥了重要调控作用,其可通过吞噬骨组织细胞内受损以及陈旧的细胞器、蛋白质和一些大分子物质来完成代谢。 2.3.1 自噬在运动促进2型糖尿病成骨细胞分化中的作用机制 2型糖尿病致使血糖浓度升高,随之产生的高糖环境促使活性氧的过度产生,此时的成骨细胞活性受到抑制,破骨细胞吸收能力强于成骨细胞骨形成能力,骨基质、骨密度下降。为了证实自噬在2型糖尿病中可以提高成骨细胞的分化能力,提高骨细胞的密度和硬度。研究发现,将哺乳动物雷帕霉素靶蛋白复合物1 (mammalian target of rapamycin complex 1,mTORC1)中的mTOR作为自噬的诱导剂作用于成骨细胞,发现成骨细胞分化显著增强。在研究MAPK通路的前期抑制mTOR的生物学作用机制时,并在后期重新激活mTOR的活性时,发现成骨细胞在此状态下的分化及骨形成能力显著升高[32]。此外,Wnt/β-catenin信号通路作为调控骨代谢的重要信号通路,可有效促进骨形成,从而调控2型糖尿病骨生长发育和代谢[33]。研究发现,运动过程中,压力过大会导致刺激异常,进而影响软骨细胞中Wnt/β-catenin途径的相关因子表达[34]。又有研究提出,运动在激活Wnt信号进行成骨作用时,其形成程度与运动强度和运动时间相关[35]。而对经典的Wnt/β-catenin信号通路的研究中发现此通路与软骨细胞肥大密切相关,这就揭示了Wnt/β-catenin信号通路在维持软骨细胞成骨稳态中的重要作用[36-37]。此外,在研究G蛋白偶联受体48(G protein coupled receptor 48, GPR48)介导运动调控骨吸收代谢的过程中发现,运动可以促进成骨细胞分化和改善骨形成代谢,同时GPR48表达上调可以激活BMPs/Smad途径,这些都在运动改善骨代谢中扮演了重要的角色[38]。 通过以上的论述都可以得到这一结论:自噬在调控骨组织细胞代谢时通过不同的信号通路对维持成骨细胞和破骨细胞的平衡发挥了重要的作用,而运动可以通过改善骨形成代谢实现提高成骨细胞的活性,预防骨类疾病的发生,促进骨骼的健康生长的作用机制还需要更多研究和数据证明。 2.3.2 自噬在运动抑制2型糖尿病破骨细胞分化中的作用机制 mTOR是一种高度保守的丝氨酸/苏氨酸激酶,作为mTORC1复合物的一部分,是营养和能量传感器,包括Raptor和mLST8蛋白,参与调节营养感知信号的重要传导通路,而该通路被认为是调控自噬的关键途径[39]。通过研究自噬的发生机制可以发现,运动可通过抑制mTORC1复合物生成来达到诱导自噬发生的目的。研究发现,运动过程中细胞能量代谢降低时,细胞会通过收缩在丝氨酸317(Ser-317)位点激活AMP依赖的蛋白激酶(AMPK)并使其磷酸化,进而激活自噬的启动激酶ULK1[40]。AMP依赖的蛋白激酶AMPK通过调节能量代谢促使结节性硬化复合物2(tuberous sclerosis complex-2,TSC2)、Raptor磷酸化达到抑制mTORC1复合物的活性,从而影响自噬机制的发生[41-42]。此外,在正常状态下,胰岛素及其相关因子也可通过激活PI3K蛋白活化Akt通路,进而激活mTOR,抑制ULK1的表达[43]。这些都表明了自噬能够影响破骨细胞的吸收功能,具体在2型糖尿病中对破骨细胞的作用机制仍需通过吸收分化受损的细胞器和蛋白质完成此过程,而运动是如何影响自噬对破骨细胞的调控还需进一步的验证。对此,有实验通过高脂饲养8周小鼠的方法进行2型糖尿病造模,结果发现小鼠体质量和肥胖指数都明显高于普通小鼠。并且,在此过程中,2型糖尿病小鼠骨细胞内的p38MAPK信号通路受到抑制,p38MAPK对破骨细胞的影响减弱,骨吸收能力明显下降,骨密度也得到了提高[29]。 越来越多数据表明,2型糖尿病的危害不仅在于血糖升高,更为严重的是其所引发的各种并发症。骨质疏松症作为2型糖尿病常见并发症,导致骨折发生概率显著升 高[44]。2型糖尿病在形成高糖环境后,成骨细胞的过度氧化促使细胞活性下降,成骨细胞分化能力减弱,同时破骨细胞的吸收能力会提高,使得骨细胞的基质和密度都呈现下降趋势。而过度氧化也会使骨细胞承受较成骨细胞、破骨细胞更多的损害,此时,胞内应激机制会启动自噬,吞噬内部受损蛋白质和细胞器,降低骨细胞的矿化能力,保证了胞内环境的稳定。在此过程中,成骨细胞中缺失p62会导致骨髓内环境失衡[45],进而抑制破骨细胞的骨吸收能力。运动作为改善骨质疏松的重要方案,运动能够提高骨密度,不同运动项目对骨密度也存在不同的影响,主要体现在诱导自噬的发生来维持破骨细胞与成骨细胞二者的动态平衡,而具体如何实现采用运动的方式来保证骨细胞自噬功能,使骨骼的重建率有所提高,需要更多的试验来进行深入研究。为证实这一理论,朱子东等[46]在其试验中发现,运动干预促进2型糖尿病的骨密度提高。此外还有一些研究提出自噬也可能是与衰老相关的骨量减少的重要因素之一,骨细胞中的p62的表达会呈现一个上升的趋势,与此同时,LC3-Ⅱ、BECN1、ULK-1的表达下调[47],而运动可以参与自噬的调控来阻止衰老所引起的骨量丢失[48]。以上论述可以表明自噬可以介导运动改善2型糖尿病骨代谢紊乱,可见图2。 "
| [1] KAYVAN Z, CASSIE JL, ALISONL MC, et al. SIRT1 is a positive regulator of in vivo bone mass and a therapeutic target for osteoporosis. PLoS One.2017;12(9): e0185236.1528. [2] 谭伟源,陈军平,宋若愚,等.2型糖尿病性骨质疏松大鼠ADSCs成骨能力的研究[J].中国骨质疏松杂志,2019, 25(9):1201-1205+1211. [3] 张玲莉,林小晶,郭健民,等.有氧运动对2型糖尿病大鼠骨代谢的影响[J].中华骨质疏松和骨矿盐疾病杂志,2019,12(3):254-260. [4] 江洪.不同运动强度干预2型糖尿病模型大鼠的骨密度变化[J].中国组织工程研究,2016,20(27):3963-3969. [5] HE Q, SHA S, SUN L, et al. GLP-1 analogue improves hepatic lipid accumulation by inducing autophagy via AMPK/mTOR pathway. Biochem Biophys Res Commun.2016; 476(4):196-203. [6] HU XK, YIN XH, ZHANG HQ, et al.Liraglutide attenuates the osteoblastic differentiation of MC3T3-E1 cells by modulating AMPK/mTOR signaling.Mol Med Rep. 2016; 14(4):3662-3668. [7] 王雨晴,李艳波.自噬与2型糖尿病关系研究进展[J].中华实用诊断与治疗杂志,2016,30(11):1041-1043. [8] WATADA H, FUJITANI Y. Autophary in pancreatic beta cells and its implication in diabetes.Mol Endocrionol. 2015;29(3): 338-348. [9] 曾祥琴,胡肇衡.糖尿病与骨质疏松的关系[J].新疆医学,2007, 37(1):119-121. [10] 应大文,刘芳.糖尿病与骨质疏松的相关性研究进展[J].实用预防医学,2015,22(10):1275-1278. [11] YAN HM, GUO J, AN Y, et al. Research progress in molecular signaling pathways on the pathogenesis of osteoporosis.Chin J Osteoporos.2016;22(10): 1336-1340. [12] WANG XF, SUN FQ, YE BL, et al. Research progress in the relationship between osteoclasts and osteoporosis.Chin J Osteoporos.2015;21(11):1420-1424. [13] YANG L, LI P, FU S, et al. Defective hepatic autophagy inobesity promotes ER stress and causes insulin resistance. Cell Metab.2010;11(6):467-478. [14] MAHMOUD AB, ELGHERIANY AA, ABDEL SHAKOR ABM. Hyperglycemia and hyperinsulinemia induced hepatocellular autophagy in male mice.Egypt Acad J Biol Sci Hisol.2015; 6(1):1. [15] 范梦琳,吴剑男,姜宏卫.自噬与胰岛素抵抗关系的研究进展[J].解放军预防医学杂志,2017,35(5):519-522. [16] SAINTPASTOU TC, GASQUE P. Bone responses in health and infectious diseases: A focus on osteoblasts. J Infect. 2017;75(4):281-292. [17] NOLLET M, SANTUCCI-DARMANIN S, BREUIL V, et al. Autophogy in osteoblasts is involved in mineralization and bone homeostasis.Autophagy.2014;10(11): 1965-1977. [18] 杨康,陈祥和,赵仁清,等.运动调控骨自噬中长链非编码RNA的作用机制[J].中国组织工程研究,2019,23(31):5065-5071. [19] 张平.Insulin-TGF-β1-SATB2通路调控BMSCs自噬影响2型糖尿病颌骨再生修复的研究[D].南京:南京医科大学,2018. [20] WHITEHOUSE CA, WATERS S, MARCHBANK K, et al. Neighbor of Brca1 gene (Nbr1) functions as a negative regulator of postnatal osteoblastic bone formation and p38 MAPK activity.Proc Natl Acad Sci USA.2010;107(29): 12913. [21] BARTOLOMÉ A, LÓPEZ-HERRADÓN A, PORTAL-NÚ, et al. Autophagy impairment aggravates the inhibitory effects of high glucose on osteoblast viability and function.Biochem J.2013;455(3):329-337. [22] DAI W, JIANG L, YUAN EL, et al. Prevention of glucocorticoid induced bone changes with beta-ecdysone.Bone.2015; 74(5): 48-57. [23] 陈祥和,李世昌,孙朋,等.游泳和下坡跑通过CN/NFAT信号途径对2型糖尿病小鼠骨吸收代谢的影响[J].中国体育科技,2018, 54(4):113-119+145. [24] DESELM CJ, MILLER BC, ZOU W, et al. Autophagy proteins regulate the secretory component of osteoclastic bone resorption.Dev Cell.2011;21(5):966-974. [25] ZHU YB, JIA GL, LU JH, et al. The relationship between autophagy activation in spinal cord and type 2 diabetic neuropathic pain in rats.Acta Physiologica Sinica.2018; 34(4):318-323. [26] 张路遥.能量代谢分子SIRT1在运动改善2型糖尿病骨代谢中的作用机制[J].中国组织工程研究,2020,24(2):276-281. [27] HOCKING LJ, WHITEHOUSE C, HELFRICH MH. Autophagy: a new player in skeletal maintenance.J Bone Miner Res.2012; 27(7):1439-1447. [28] 张娜娜.不同方式运动对2型糖尿病小鼠骨形成代谢和骨髓间充质干细胞分化的影响[D].上海:华东师范大学,2016. [29] 徐会金. 运动通过p38MAPK信号通路对2型糖尿病小鼠骨代谢的影响[D].上海:华东师范大学,2016. [30] ZHAO H, XIONG J, ONAL M, et al. Osteocyte autophagy declines with age in mice and suppression of autophagy decreases bone mass.J Bone Min Res.2012;26(5):1039. [31] 刘刚.自噬对镉致大鼠肾小管上皮细胞凋亡的影响及其调控机制[D].扬州:扬州大学,2017. [32] GÓMEZ-PUERTO MC, VERHAGEN LP, BRAAT AK, et al. Activation of autophagy by FOXO3 regulates redox homeostasis during osteogenic differentiation.Autophagy. 2016;12(10):1804-1816. [33] 赵常红,李世昌,孙朋.不同运动对生长期大鼠Wnt/β-catenin信号及软骨内成骨的影响[J].天津体育学院学报,2019,34(3): 238-242+263. [34] LIU S, ZHOU PU, ZHANG Y. Abnormal expression of key genes and proteins in the canonical Wnt/β-catenin pathway of articular cartilage in a rat model of exercise-induced osteoarthritis.Mol Med Rep. 2016;13(3):1999-2006. [35] XI C, LIHUI L, JIANMIN G, et al. Treadmill running exercise prevents senile osteoporosis and upregulates the Wnt signaling pathway in SAMP6 mice.Oncotarget. 2016;7(44): 71072-71086. [36] YASUHARA R, OHTA Y, YUASA T, et al. Roles of β-catenin signaling in phenotypic expression and proliferation of articular cartilage superficial zone cells.Lab Invest. 2011; 91(12):1739-1752. [37] PASOLD J, OSTERBERG A, PETERS K, et al. Reduced expression of Sfrp1 during chondrogenesis and in articular chondrocytes correlates with osteoarthritis in STR/ort mice. Exp Cell Res. 2013;319(5):649-659. [38] 陈祥和,彭海霞,李世昌,等.不同运动方式对II型糖尿病小鼠骨形成及BMPs/Smad途径相关分子表达的影响[J].北京体育大学学报, 2017,40(5): 51-58. [39] DIBBLE CC, MANNING BD. Signal integration by mTORC1co-ordinates nutrient input with biosynthetic output. Nat Cell Biol.2013;15(6):555. [40] KIM J, KUNDU M, VIOLLET B, et al. AMPK and mTOR regulate autophagy through direct phosphorylation of Ulk1. Nat Cell Biol.2011;13(2):132-141. [41] INOKI K, OUYANG H, ZHU T, et al. TSC2 integrates Wnt and energy signals via acoordinated phosphorylation by AMPK and GSK3 to regulate cell growth.Cell.2006;126(5):955-968. [42] GWINN DM, SHACKELFORD DB, EGAN DF, et al. AMPK phosphorylation of raptor mediates a metabolic checkpoint. Mol Cell.2008;30(2):214-226. [43] ENGIN F, NGUYEN T, YERMALOVICH A, et al. Aberrant islet unfolded protein response in type 2 diabetes.Sci Reports. 2014;11(4):4054. [44] IMPSON KA, MAVROS Y, KAY S, et al. Graded resistanceexercise and type 2 diabetes in older adults(the GRREAT2DO study):methods and baseling cohort characteristics of a randomized controlled trial.Trials.2015; 16(2):512-525. [45] CHEN KH, SENGUPTA A, NAYAK RC, et al. p62 isrequired for stem cell/progenitor retention through inhibtion of IKK/NF-kappaB/Ccl4 signaling at the bone marrow macrophage-osteoblast-niche.Cell Rep.2014;9(6):2084. [46] 朱子东,张海英,高静,等.肥胖儿童短期强化治疗前后生化及骨代谢相关指标的变化[J].中国医药指南, 2013, 11(36):143-144. [47] WOHLGEMUTH SE, SEO AY, MARZETTI E, et al. Skeletal muscle autophagy and apoptosis during aging:effects of calorie restriction and life-long exercise.Exp Gerontol.2010; 45(2):138. [48] CHEN K, YANG YH, JIANG SD, et al. Decreased activity of osteocyte autophagy with aging may contribute to the bone loss in senile population.Histochem Cell Biol.2014;14(3):285. |
| [1] | Shen Jinbo, Zhang Lin. Micro-injury of the Achilles tendon caused by acute exhaustive exercise in rats: ultrastructural changes and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1190-1195. |
| [2] | Chen Jiming, Wu Xiaojing, Liu Tianfeng, Chen Haicong, Huang Chengshuo. Effects of silymarin on liver injury and bone metabolism induced by carbon tetrachloride in mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1224-1228. |
| [3] | Wang Mengting, Gu Yanping, Ren Wenbo, Qin Qian, Bai Bingyi, Liao Yuanpeng. Research hotspots of blood flow restriction training for dyskinesia based on visualization analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1264-1269. |
| [4] | Wang Yongsheng, Wu Yang, Li Yanchun. Effect of acute high-intensity exercise on appetite hormones in adults: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1305-1312. |
| [5] | Zheng Xiaolong, He Xiaoming, Gong Shuidi, Pang Fengxiang, Yang Fan, He Wei, Liu Shaojun, Wei Qiushi. Bone turnover characteristics in patients with alcohol-induced osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 657-661. |
| [6] | Ma Zetao, Zeng Hui, Wang Deli, Weng Jian, Feng Song. MicroRNA-138-5p regulates chondrocyte proliferation and autophagy [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 674-678. |
| [7] | Xie Yang, Zhang Shujiang, Liu Menglan, Luo Ying, Yang Yang, Li Zuoxiao. Mechanism by which rapamycin protects spinal cord neurons in experimental autoimmune encephalomyelitis mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 695-700. |
| [8] | Liu Bo, Chen Xianghe, Yang Kang, Yu Huilin, Lu Pengcheng. Mechanism of DNA methylation in exercise intervention for osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 791-797. |
| [9] | Zhao Xiang, Wei Cuilan, Zhang Yeting. Neurogenesis and neuroinflammation under exercise: alteration and regulation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 813-820. |
| [10] | Chen Ziyang, Pu Rui, Deng Shuang, Yuan Lingyan. Regulatory effect of exosomes on exercise-mediated insulin resistance diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 4089-4094. |
| [11] | Jiang Xiaoyan, Zhu Haifei, Lin Haiqi, Lin Wentao. Cold therapy promotes self-limited recovery of delayed-onset muscle soreness [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3609-3613. |
| [12] | Bai Shengchao, Gao Yang, Wang Bo, Li Junping, Wang Ruiyuan. Dynamic changes of mitochondrial function of the skeletal muscle after acupuncture intervention in rats with heavy load exercise-induced injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3648-3653. |
| [13] | Lu Jie, Li Xue, Wang Lu, Fan Jia, Zhang Yeting, Lu Xiaobin, Yuan Qiongjia. Effects of different-intensity swimming exercises on spatial learning and memory ability and the expression of Orexin A in the rat cerebellum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3697-3703. |
| [14] | Wang Zhen, Lin Haiqi, He Fei, Lin Wentao. Exercise activates skeletal muscle satellite cells: exercise prevention and treatment for age-related sarcopenia and muscle injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3752-3759. |
| [15] | Wang Chaoge, Weng Xiquan, Lin Baoxuan, Chen Lina, Xu Guoqin. Exercises under cold exposure change fat type and function in obese rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3162-3167. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||