Chinese Journal of Tissue Engineering Research ›› 2017, Vol. 21 ›› Issue (18): 2927-2933.doi: 10.3969/j.issn.2095-4344.2017.18.022
Previous Articles Next Articles
3D printing of biological materials: progress and clinical application
Yang Dao-peng1, Xia Xu2
- 1 Class 2013 Medical Imaging Major, 2 Library, Southern Medical University, Guangzhou 510515, Guangdong Province, China
-
Online:2017-06-28Published:2017-07-07 -
Contact:Xia Xu, Master, Research librarian, Southern Medical University, Guangzhou 510515, Guangdong Province, China -
About author:Yang Dao-peng, Class 2013 Medical Imaging Major, Southern Medical University, Guangzhou 510515, Guangdong Province, China
CLC Number:
Cite this article
Yang Dao-peng, Xia Xu. 3D printing of biological materials: progress and clinical application[J]. Chinese Journal of Tissue Engineering Research, 2017, 21(18): 2927-2933.
share this article
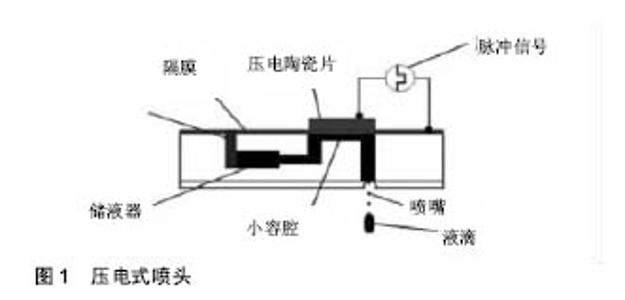
2.1 3D打印生物材料 3D打印技术发展过程中,制约其发展的主要因素有打印材料和打印工艺。3D打印生物材料除适用于3D打印机外,也要和医学应用相结合。经过多年的发展,3D打印生物材料已广泛应用于临床医疗实践。常见的3D打印生物材料主要有金属、工程塑料、光敏树脂、生物塑料、高分子凝胶等。 2.1.1 金属 用于3D打印的金属粉末材料主要有不锈钢、钛合金、钴铬合金、钼钛合金、钴铬钼合金等等。较成熟的3D金属打印技术主要有选区激光熔化(Selective Laser Melting,SLM)、电子束选区熔化(Electron Beam selective Melting,EBM)、激光近净成形(Laser Engineered Net Shaping,LENS)等[2]。金属多用于人体植入物,在满足人体安全性的前提下,还需满足抗腐蚀性、力学性能、生物功能性、生物相容性等要求。 2.1.2 工程塑料 工业上应用的工程塑料非常多。医用3D打印工程塑料主要有聚酰胺、聚醚醚酮、丙烯腈-丁二烯-苯乙烯共聚物等。由于良好的强度、耐候性和热稳定性,工程塑料在假肢假牙制作方面的应用广泛。聚醚醚酮因具有良好的生物相容性而成为理想的人工骨替换材料[3]。 2.1.3 光敏树脂 光敏树脂主要利用SLA技术合成,目前还存在很多问题。光敏树脂由光引(Photoinitiator)、预聚物(Prepolymer)、单体(Monomer)及少量添加剂(Additive)等组成[4]。目前主要用于医学模型的铸造,便于临床手术和教学等。 2.1.4 生物塑料 3D打印生物塑料主要有聚乳酸、聚(乙二醇)二丙烯酸酯、聚己内脂等。生物材料具有良好的生物可降解性、生物相容性,普遍用来打印生物工程支架,如心脏支架、骨支架等。 2.1.5 高分子凝胶 纤维素、蛋白胨、海藻酸钠、聚丙烯酸等都是高分子凝胶。比起生物塑料,高分子凝胶具有更好的生物相容性以及与人体软组织相仿的力学性能。用于生物工程支架时,能促进细胞黏附和生长,生物降解性好,可用于药物的可控释放[5]。 此外,还有一些目前应用比较少的材料,如食品材料中的糖、人造骨粉等。目前发展中的一种生物打印技术可以直接携带细胞打印,即以细胞作为打印原料。3D打印机还可以携带药物原料打印,以实现药物的可控或缓控释放。 2.2 不同打印技术对打印材料的要求 3D打印新技术层出不穷,已经出现的3D打印技术不下十余种,能够成熟运用的有3D喷印技术、选择性激光烧结技术、光固化成型技术、熔融沉积技术、数字光处理、熔丝制造、分层实体制造、电子束熔化成型、直接金属激光烧结、熔化压模式等。各种不同打印技术对打印材料要求有差别,一种材料可能只适合其中一种或几种打印技术。由于这些打印技术原理有重叠,这里不赘述,只挑选前面4种最常见的3D打印技术具体阐释。 2.2.1 3D喷印技术 3D喷印技术是根据电流体动力学原理,使用特定的喷头,喷印流态材料,直接形成模型器件的技术。工作原理见图1[6]。"
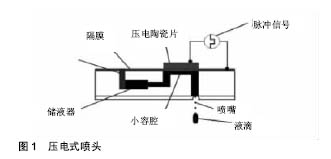
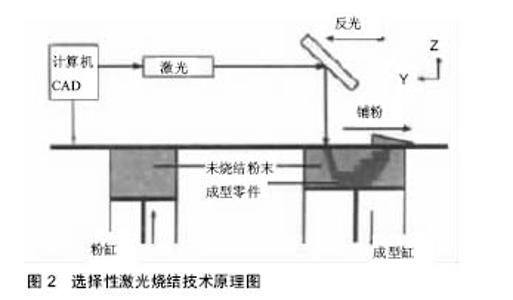
3D喷印技术要求打印材料是液态,并且通过液滴的形式从喷头喷射出来。材料可以原本就是液体,如油墨等;也可以是经过特殊工艺制成的液态材料,如陶瓷墨水[7]。陶瓷墨水就是含有陶瓷釉料成分、陶瓷色料或陶瓷着色剂的墨水。 2.2.2 光固化成型技术(SLA) 光固化成型技术原理和喷墨打印相类似,以液态光敏树脂为原料,通过紫外光扫描液态光敏树脂使其固化,层层叠加,形成所需的模型。光固化成型技术由光固化实体材料和支撑材料组成[8],两者都是光敏树脂,打印成功后支撑材料可去除。光敏树脂又叫光固化树脂,由树脂单体(monomer)及预聚体(oligomer)组成,含有活性官能团,能在紫外光照射下由光敏剂(light initiator)引发聚合反应,生成不溶的涂膜。 2.2.3 熔融沉积成型技术(FDM) 熔融沉积技术的基本原理是在计算机的控制下,将在喷头里已经加热融化的丝线状或粒状材料形成的熔体均匀喷洒出来,迅速冷切成型,塑形,做成已经设计好的模型。FDM常用的材料有可生物降解的固态聚合物线材,如PLA[9],PCL,ABS等。还有金属熔融沉积技术,如铋锡合金丝材。不过金属丝材普遍存在制造成本高,效率低等问题。 2.2.4 选择性激光烧结技术(SLS) 是通过计算机的控制,对粉末材料进行激光加热,烧结,按照预先设定好的程序逐层累积形成所需的模型。基本工艺原理见图2[10]。 适用于选择性激光烧结技术的工艺材料广泛,不需要支撑材料,包括聚合物、金属、陶瓷和诸多复合粉末[11]。由于选择性激光烧结技术自由成型,无需制模,在金属打印中具有优势。 2.3 3D打印生物材料的临床应用 3D打印在临床上的应用基本可以分为生物打印和非生物打印。生物打印是有生物活性组织或器官的打印,非生物打印是只实现外观、功能的打印。两者最大的区别就是生物打印有细胞的参与,能实现更高级的甚至贴近人体正常组织器官的生命活动,是3D打印临床应用的最终目标。 2.3.1 非生物打印 3D医学模型:由于尸体的不易获得,医学模型在基础临床教学和手术模拟中有着很广泛的应用。杜兰大学泌尿外科使用树脂材料(类似于塑料)打印肾脏模型,正常肾组织用清晰透明树脂打印,肿瘤用红色树脂打印[12]。Frolich等[13]用丙烯腈-丁二烯-苯乙烯共聚物打印脑动脉瘤,做成硅胶管的空心动脉瘤模型。医生根据CT/MRI等影像资料打印出肿瘤模型,使术者能全方位了解病变局部的解剖关系,制定详细的手术计划,进行实际手术前的手术预演和术中手术导航,从而缩短手术用时。Wanibuchi等[14]用合成树脂(聚酰胺尼龙)和无机填料(玻璃珠)组成的粉末材料打印颞骨,用于手术基础技能训练。事实上,人体的任何一个组织或器官,都可以3D打印出医学模型。使用的打印材料有树脂、石膏、工程塑料等,对材料要求低。 口腔种植体:目前口腔种植用3D打印材料品种有限,常用的有光固化树脂材料和金属钛粉等,树脂材料需要与氧化铝、氧化锆、生物陶瓷粉等骨质打印材料一起加工用于打印口腔种植体[15]。在利用光固化树脂打印牙齿的研究中,Lee等[16]发现添加4,4'- bis(N,Ndiethylamino)benzophenone(DEABP)作为引发剂能提高打印材料光固化树脂的转化效果,增强牙模型的强度。Hoang等[17]使用聚乙烯基硅氧烷硅打印牙齿。个性化定制、打印材料单一是3D打印假牙最大的特色,但美中不足的是用于支持3D打印的生物材料相对较少,且存在一定的安全隐患。 假肢假体:传统假肢,一种是廉价但仅有装饰作用,另一种是能实现基本动作却昂贵的“肌电假肢”。而3D打印技术能打印出既有功能成本又相对价钱较低的假肢。假肢材料的选择需要考虑一定的韧性和耐用性,目前用于打印假肢的原材料主要有工程塑胶、树脂粉末等。国内打印假肢的报道比较少,打印的假体较为简单粗 糙[18]。国外则起步较早,发展速度快,两位科学家用ABS塑胶打印了一个胳膊的MREX假肢,可以实现手的部分功能[19]。法国Arkema公司开发出可用于假肢及牙垫的3D打印材料[20],其商品名为“Rilsan Invent Natural”。“Rilsan Invent Natural”是原材料100%由植物制备的聚酰胺11,韧性较高,有望用于受力较大的假肢。 植入体:作为植入体的材料必须具有良好的生物相容性、强度和可塑性。目前所用材料大致可分为金属合金类(最常见的有钛合金、钴铬钼合金等)、有机高分子聚合物类(聚已内酯等)。刘亚雄等[21]系统介绍了利用光固化打印方法打印定制型钛合金植入物,这种方法定制的钛合金植入物能够准确地反映患者的个体特征,所铸造的定制型植入物的化学成分、力学性能和精度均满足相应国家标准、医药行业标准和临床植入的要求。陈大智[22]讨论了NiTi合金和Co-Cr-Mo合金作为3D打印医学植入材料的性能优点,但打印成本高,效率低,只适用于科研。有机高分子聚合物类植入材料则需要考虑材料的可降解性,足够的空隙容细胞长入,免于细胞免疫排斥等特性。密歇根大学安阿伯分校医学博士大卫•措普夫(David A. Zopf)[23]使用聚己内酯可吸收材料,通过激光烧结技术制造气管支架,移植气管支架的患儿1年后左主支气管无异常,能自主正常呼吸。为确保植入体更好的生物相容性,减少免疫排斥和磨损现象,众多科学家不断探索新的植入材料,悉尼大学生物医学工程师Philip Boughton使用一种骨水泥(类似水泥的材料与抗生素的混合物)制作出针对患者的无菌植入体[24]。目前,植入材料主要面临异体材料感染性的问题,今后的研究方向应该逐步提高植入材料的生物相容性,减少植入材料的感染性,以自体细胞形成的组织代替当前的植入材料。 生物制药:在3D打印技术的影响下,传统制药工业迎来了新的春天。生物制药科学家致力于利用3D打印技术,在保证药物疗效的前提下,优化制药过程,实现药物设计和药物个性化定制的研究,取得了一定的成果。Goyanes等[25]研发了3D熔断丝技术,以直径1.75 mm的PVA细丝为原料,以荧光素钠盐为标准装载药物,利用装载了荧光素钠盐的PVA细丝成功打印出不同填充比例的药物片剂,打印出的药物片剂符合生物医药的要求。修改药剂打印方法可实现个性定制,具有很强的实用性。Dragone等[26]利用PP(聚丙烯)打印出的反应容器进行苯甲醛和苯胺类衍生物合成N-苄叉苯胺类化合物的研究,合成转化率达94%。伍卫刚[27]利用LTY型立体打印式快速成形机,以相对分子质量为100 K/GPC的L-PLA(左旋聚乳酸颗粒为基质材料),将100 mL丙酮、20 mL乙醇、10 mL蒸馏水、0.4 mL甘油和0.2 g NaCl配比混合成粘结剂,将LVFX和TOB分别溶于粘结剂构成100 g/L含药的混合溶液,以该混合溶液为打印液打印出的多药控释型载药人工骨具有良好生物相容性、药物控释特性和缓释特性等。 与传统制药方法相比,3D药物打印优势明显,主要体现在:①原料无浪费;②可实现个性化定制;③优化制药过程;④具有控释和缓释特性等。但遗憾的是目前的药物3D打印只能进行简单的化学反应,极小部分药物原料能用于3D打印,今后还需要在3D药物打印设备开发、药物原料上进行大量的研究。 2.3.2 生物打印 生物材料支架打印:细胞的生长、繁殖、新陈代谢等生命活动需要一定的内环境,生物材料支架为细胞提供了类似体内环境的场所。支架由可降解吸收的生物材料打印而成,然后与相应的细胞混合成体外组织或器官模型,放置于培养箱或实验动物体内培养,最终得到理想的打印产物。 血管打印是生物打印的基础,有了血管里养分的供应,打印组织器官才能存活。血管3D打印目前一般采用支架材料+种子细胞的打印方式。种子细胞为血管内皮细胞或可诱导分化的干细胞。支架材料主要有人工合成多聚体,以聚乳酸为代表;天然高分子聚合物,以胶原为代表。Biglino等[28]利用市售橡胶类似物tangoplus FullCure930打印出降主动脉和主动脉弓模型。Zhao等[29]利用纤维素、胶原、聚乳酸羟基乙酸共聚物等原材料打印出支架,然后将脂肪干细胞“嫁接”到支架内,接着诱导脂肪干细胞分化生成血管内皮细胞和平滑肌细胞,成功打印出人工血管。Lee等[30]使用了生物相容性较好的材料打印人工血管用支架,如静电纺纳米纤维(ENS)和壳聚糖(CTS)等。鉴于聚(乙二醇)二丙烯酸酯具有含水量高、生物相容性好等优点,Huang等[31]用聚(乙二醇)二丙烯酸酯打印出三维血管模型,用于研究肿瘤细胞的迁移。Lee等[32]以胶原、水凝胶为支架材料,脐带静脉血内皮细胞为种子材料打印出的人工血管模型可较好模仿人体内微循环、血液渗透等生命过程。由于大动脉主要负责血液的运输,故打印模型更多考虑血管的弹性和管腔结构,较少在意生物活性材料的选取;而毛细微血管的功能较为复杂,参与机体的微循环和血氧交换反应等,对打印技术和材料要求更高,提升了打印难度。 3D打印技术近些年已在骨关节外科、颅颌面外科、脊柱外科、手足外科等领域得到应用。传统的骨组织修复包括自体骨移植、同种异体骨种植、金属支架或假体植入等,传统骨科植入材料不锈钢、钴铬钼合金、钛和钛合金等同样适用于3D打印[33]。Barnes[34]利用Ti6Al4V粉末打印了钛合金的人体脚跟,质量轻,易与人体组织整合。当然,金属等植入假体终究不具有生物活性,替代不了生物活性组织所具有的功能,还可能引起机体的免疫排斥。3D打印人工骨支架主要分为不可降解性支架和可降解性支架。不可降解骨生长支架一般为金属,李小康等[35]利用医用多孔钛合金打印出多孔钛合金椎间融合器,植入小尾寒羊的颈椎中,获得了良好的融合效果。可降解支架种类多,He等[36]用煅羊松质骨双相陶瓷复合材料/聚乙烯醇凝胶制作骨支架,在无菌骨支架上接种骨髓间充质干细胞,骨支架可使兔骨髓间充质干细胞黏附、生长、增殖,并有良好的生物力学性能和生物相容性。可见,理想的骨修复材料必须具有生物相容性、可吸收性和可降解性。 皮肤是人体最大的器官。一直以来,皮肤移植都是困扰人类的重大医学问题。皮肤内含有丰富血管和神经,皮肤细胞要靠血液的供应才能存活。因此,有人说,打印血管是打印皮肤的基础。德国弗朗霍夫激光技术研究所研究人员成功利用丙烯酸酯基的合成聚合物打印出血管,这种材料使得打印血管表面分布许多直径数百微米的微孔有利于血细胞和组织的营养交换[37]。鉴于目前3D打印技术的发展水平,打印皮肤还只能对皮肤表层(表皮和真皮)不超过200 μm进行再造(不包括血管组织)。细胞外基质是表皮细胞生长和分化的内环境,如何构建这个内环境来诱导皮肤的生成,是当前国内外研究的热点。吉林大学牛震海[38]尝试用壳聚糖和聚乙烯醇打印聚合纳米纤维支架,可模拟细胞外基质,壳聚糖具有良好的生物相容性、恰当的降解速度、优良的抑菌活性和明显的促组织生长活性,还可以促进新生血管生成。浙江大学熊思[39]应用三维打印生物活性支架的思路模拟细胞外基质以打印皮肤,使用的材料有丝素蛋白、水凝胶和碱性成纤维细胞生长因子。丝素蛋白打印的组织工程支架具有良好的生物相容性、非凡的抗拉伸强度和优越的降解性能,能促进皮肤再生。也有学者直接打印细胞外基质,如Lee等[40]用胎牛血清、胶原蛋白和水凝胶打印细胞外基质,用雾化碳酸氢钠增加水凝胶的黏性,用角化形成细胞和成纤维细胞制成细胞悬浊液打印表皮和真皮,用于疾病模型的研究。3D打印人工皮肤还只是处在实验阶段,还未真正应用于临床。寻找更优质的打印基质材料和打印微细血管材料是打印人工皮肤的关键。 目前研究最多的是如何制造出理想的细胞外基质-载体材料,即组织工程支架,然后诱导细胞形成组织器官。载体材料的选择是关键,首先得是生物材料,具有良好的生物相容性和生物可降解性,在组织形成过程中逐渐分解,且不影响新生组织的结构和功能。目前相应的材料有天然胶原、明胶、硫酸软骨素等,以及人工合成有机高分子聚合物聚乳酸、聚乙醇酸、羟基磷灰石等[41]。Reiffel等[42]用胶原蛋白水凝胶打印成生物支架,然后将干细胞和生长因子组成的液滴喷涂到凝胶支架上,用这种方法成功打印出人体肾脏、耳、鼻等器官。克里斯多夫认为糖是一种很好的3D打印生物材料[43],因为它可以在组织生成的时候溶解,研究者在打印好的糖框上裹一层细胞,一旦组织和血管成型,他们就用水把糖溶掉,再利用糖支架打印出肝脏。北卡Wake Forest 再生医学研究所Anthony Atala 博士在TED演讲中展示了他们使用3D打印机打印出来的人体肾脏[44],他们以培养出来的肾脏细胞作为打印材料,一层层将细胞打印在提前设计好的虚拟模型上。第一层是细胞,第二层是水凝胶,用来黏合固定细胞,然后一层层重复,直到整个肾脏打印出来。等到细胞存活了,水凝胶被降解,留下来的细胞形成了一个完整的器官架构。这个初期的肾脏再被移到培养器中,提供养分,促进生长。Atala博士已经观察到这个初期肾脏模型产生了尿样物质,表示已经有了部分肾脏功能。 由于人体复杂器官结构和功能的多样性,目前各种器官打印都还是处在研究阶段,还面临着打印器官自身生存性和生物活性等问题,需要挖掘更合适的生物材料来实现与细胞组装成为一个功能体,实现有功能、有活性人体器官的打印。 细胞直接打印:3D打印不光打印生物活性支架,真正使用细胞来打印也已经实现。相比于利用支架种植细胞,细胞直接打印可以获得更高的细胞浓度。一般情况下,细胞直接打印需携带一定的基质材料,最常用的有水凝胶、纤维蛋白原液等。苏格兰研究人员首次利用3D打印技术,对人类胚胎干细胞进行打印[45]。宋杨等[46]以第4代人体脂肪来源干细胞作为种子细胞,进行成骨化诱导,采用碱性磷酸酶染色和茜素红矿化染色检测其成骨分化能力,将种子细胞加入2%海藻酸钠-8%明胶混合物(细胞浓度约为1×109 L-1),经过打印获得细胞-海藻酸钠-明胶共混物打印体,植入裸鼠背部皮下,最后获得的样本具有一定的成骨能力。Cui等[47]以PEG-DMA/软骨细胞混合溶液为生物墨水,在紫外光照射下进行软骨缺损部位原位打印,细胞成活率比较高。肿瘤细胞也可用于3D打印,杭州电子科技大学以明胶、海藻酸钠、卵巢癌细胞制成细胞悬浊液置于3D打印机打印,得到卵巢癌三维结构模型[48],用于研究癌细胞转移。细胞直接3D打印难题在于提高打印后细胞的成活率,以及促进打印细胞的生长、分化。 "
| [1]刘许,宋阳. 用于3D打印的生物相容性高分子材料[J]. 合成树脂及塑料,2015,32(4): 96-99.[2]赵冰净,胡敏.金属3D打印技术在口腔医学应用前景[J]. 口腔颌面外科杂志,2015,25(4): 311-314.[3]陈庆,曾军堂,陈韦坤. 3D打印塑料材料技术现状和发展趋势[J]. 新材料产业,2015(6): 27-32.[4]孙聚杰. 3D打印材料及研究热点[J]. 丝网印刷,2013(12): 34-39.[5]贺超良,汤朝晖,田华雨,等. 3D打印技术制备生物医用高分子材料的研究进展[J]. 高分子学报,2013,52(6): 722-732.[6]孙云. 三维喷印成形质量优化研究[J]. 无线互联科技, 2016,(4): 129-131.[7]王志华. 3D喷墨打印带来陶瓷行业新革命[J].中国印刷,2015(8): 79-83.[8]谢彪,王小腾,邱俊峰,等. 光固化3D打印高分子材料[J]. 山东化工,2014,43(11): 70-72.[9]Plymill A,Minneci R,Greeley DA, et al. Graphene and Carbon Nanotube PLA Composite Feedstock Development for Fused Deposition Modeling. University of Tennessee Honors Thesis Projects, 2016.[10]马旭东. 选择性激光烧结在3D打印中的应用[J]. 工程技术研究, 2016(7): 71.[11]王小萍,程炳坤,贾德民. 选择性激光烧结用聚合物粉末材料的研究进展[J]. 合成材料老化与应用, 2016,45(3): 108-113.[12]3D打印肾肿瘤[J]. 中国医学计算机成像杂志, 2014,20(5): 411.[13]Frölich AM, Spallek J, Brehmer L, et al. 3D Printing of Intracranial Aneurysms Using Fused Deposition Modeling Offers Highly Accurate Replications. AJNR Am J Neuroradiol. 2016;37(1):120-124.[14]Wanibuchi M, Noshiro S, Sugino T, et al. Training for Skull Base Surgery with a Colored Temporal Bone Model Created by Three-Dimensional Printing Technology. World Neurosurg. 2016;91:66-72.[15]徐步光,李丹荣,宁锐剑. 3D打印技术在口腔种植领域的应用及对牙科工业发展的革命性影响[J].中国医疗器械信息, 2015(8): 13-18.[16]Lee DH, Mai HN, Yang JC, et al. The effect of 4,4'-bis(N,N-diethylamino) benzophenone on the degree of conversion in liquid photopolymer for dental 3D printing. J Adv Prosthodont. 2015;7(5):386-391.[17]Hoang LN, Thompson GA, Cho SH, et al. Die spacer thickness reproduction for central incisor crown fabrication with combined computer-aided design and 3D printing technology: an in vitro study.J Prosthet Dent. 2015;113(5): 398-404.[18]牛思远,汤恁妤. 3D打印已实现假肢“私人定制”[N]. 南方日报, 2015-06-01(3).[19]3D技术使假肢定制更上一层楼[J]. 工业设计, 2012(8):54.[20]法国Arkema公司开发出可用于假肢及牙垫的3D打印材料[J]. 石油化工, 2015(4): 505.[21]刘亚雄,贺健康,秦勉,等. 定制型钛合金植入物的光固化3D打印及精密铸造[J]. 稀有金属材料与工程, 2014(S1): 339-342.[22]陈大智. 基于3D打印模具设计制备钼钛合金及钴铬钼合金医学植入材料的工艺和材料学研究[D]. 长沙:中南大学,2014.[23]3D打印气管支架植入成功[J]. 中国器械医疗杂志, 2014(4): 300.[24]悉尼大学开发出3D打印骨骼植入物技术[J]. 化工新型材料, 2015(3): 241.[25]Goyanes A, Buanz AB, Basit AW, et al. Fused-filament 3D printing (3DP) for fabrication of tablets. Int J Pharm. 2014; 476(1-2):88-92.[26]Dragone V, Sans V, Rosnes MH, et al. 3D-printed devices for continuous-flow organic chemistry. Beilstein J Org Chem. 2013;9:951-959.[27]伍卫刚. 三维打印技术制备多药控释型载药人工骨及其治疗慢性骨髓炎的实验研究[D]. 武汉:华中科技大学, 2010.[28]Biglino G, Verschueren P, Zegels R, et al. Rapid prototyping compliant arterial phantoms for in-vitro studies and device testing. J Cardiovasc Magn Reson. 2013;15:2.[29]Zhao X, Liu L, Wang J, et al. In vitro vascularization of a combined system based on a 3D printing technique. J Tissue Eng Regen Med. 2016;10(10):833-842.[30]Lee SJ, Heo DN, Park JS, et al. Characterization and preparation of bio-tubular scaffolds for fabricating artificial vascular grafts by combining electrospinning and a 3D printing system. Phys Chem Chem Phys. 2015;17(5): 2996-2999.[31]Huang TQ, Qu X, Liu J, et al. 3D printing of biomimetic microstructures for cancer cell migration. Biomed Microdevices. 2014;16(1):127-132.[32]Lee VK, Kim DY, Ngo H, et al. Creating perfused functional vascular channels using 3D bio-printing technology. Biomaterials. 2014;35(28):8092-8102.[33]易超然,罗婕姝,王文军,等. 3D打印技术在骨组织修复个体化治疗中的应用进展[J]. 中南医学科学杂志, 2015,43(3): 330-333.[34]Barnes JE.Manufacturing a human heel in titanium via 3D printing. Med J Aust. 2015;202(3):118.[35]李小康,伍苏华,李轶,等.3D打印多孔钛合金与聚醚醚酮椎间融合器对羊颈椎融合效果的对比研究[J]. 中华创伤骨科杂志, 2015, 17(1):34-39.[36]He HY, Zhang JY, Mi X, et al. Rapid prototyping for tissue-engineered bone scaffold by 3D printing and biocompatibility study. Int J Clin Exp Med. 2015;8(7): 11777-11785.[37]3D打印人造血管获重大突破[J]. 中国光学,2015(5): 889-890.[38]牛震海. 电纺PVA/壳聚糖复合纳米纤维支架在组织工程皮肤中的实验研究[D]. 吉林:吉林大学, 2011.[39]熊思. 丝素蛋白的降解性能及其三维打印生物活性支架在皮肤修复中的应用研究[D]. 杭州:浙江大学, 2015.[40]Lee V, Singh G, Trasatti JP, et al. Design and fabrication of human skin by three-dimensional bioprinting. Tissue Eng Part C Methods. 2014;20(6):473-484.[41]何创龙,王远亮,杨立华,等. 人工器官的快速成形制造[J]. 山东生物医学工程, 2003, 22(2): 46-50.[42]Reiffel AJ, Kafka C, Hernandez KA, et al. High-fidelity tissue engineering of patient-specific auricles for reconstruction of pediatric microtia and other auricular deformities. PLoS One. 2013;8(2):e56506.[43]用3D打印的糖支架制造人工肝脏[J]. 工业设计,2013(11): 43-44.[44]吕洛衿. 打印一个骨盆,打印一个肾脏——3D打印引领医学革命[J]. 作文, 2014(4): 62-63.[45]Villar G, Graham AD, Bayley H. A tissue-like printed material. Science. 2013;340(6128):48-52.[46]宋杨,王晓飞,王宇光. 人脂肪间充质干细胞与生物材料共混物三维打印体的体内成骨[J]. 北京大学学报:医学版, 2016, 48(1): 45-50.[47]Cui X, Breitenkamp K, Finn MG, et al. Direct human cartilage repair using three-dimensional bioprinting technology. Tissue Eng Part A. 2012;18(11-12):1304-1312.[48]石然,徐铭恩,周青青,等. 基于细胞3D打印技术的体外肿瘤模型构建研究[J]. 中国生物医学工程学报, 2015, 34(5): 618-622. |
| [1] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [2] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [3] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [4] | Song Yuxin, Zhang Tongtong, Niu Jianxiong, Wang Zengping, Wen Jie, Zhang Qunli, Xue Wen, Liu Lin. Precise screw placement of 3D printing model and orthopedic robot in spinal deformity [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 904-907. |
| [5] | Tan Guozhong, Tu Xinran, Guo Liyang, Zhong Jialin, Zhang Yang, Jiang Qianzhou. Biosafety evaluation of three-dimensional printed gelatin/sodium alginate/58S bioactive glass scaffolds for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 521-527. |
| [6] | He Yunying, Li Lingjie, Zhang Shuqi, Li Yuzhou, Yang Sheng, Ji Ping. Method of constructing cell spheroids based on agarose and polyacrylic molds [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 553-559. |
| [7] | He Guanyu, Xu Baoshan, Du Lilong, Zhang Tongxing, Huo Zhenxin, Shen Li. Biomimetic orientated microchannel annulus fibrosus scaffold constructed by silk fibroin [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 560-566. |
| [8] | Chen Xiaoxu, Luo Yaxin, Bi Haoran, Yang Kun. Preparation and application of acellular scaffold in tissue engineering and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 591-596. |
| [9] | Kang Kunlong, Wang Xintao. Research hotspot of biological scaffold materials promoting osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 597-603. |
| [10] | Shen Jiahua, Fu Yong. Application of graphene-based nanomaterials in stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 604-609. |
| [11] | Wang Ruanbin, Cheng Liqian, Chen Kai. Application and value of polymer materials in three-dimensional printing biological bones and scaffolds [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 610-616. |
| [12] | Zhang Tong, Cai Jinchi, Yuan Zhifa, Zhao Haiyan, Han Xingwen, Wang Wenji. Hyaluronic acid-based composite hydrogel in cartilage injury caused by osteoarthritis: application and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 617-625. |
| [13] | Li Hui, Chen Lianglong. Application and characteristics of bone graft materials in the treatment of spinal tuberculosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 626-630. |
| [14] | Gao Cangjian, Yang Zhen, Liu Shuyun, Li Hao, Fu Liwei, Zhao Tianyuan, Chen Wei, Liao Zhiyao, Li Pinxue, Sui Xiang, Guo Quanyi. Electrospinning for rotator cuff repair [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 637-642. |
| [15] | Song Yan, Zheng Kun, Wei Haoxin, Lu Dezhi, Xu Yuanjing, Wang Xiaowen, Wang Jinwu. reliability of flat feet evaluated by foot posture index and its application in three-dimensional printing insoles [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 344-349. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||