Chinese Journal of Tissue Engineering Research ›› 2015, Vol. 19 ›› Issue (27): 4423-4428.doi: 10.3969/j.issn.2095-4344.2015.27.029
Establishing animal models of atherosclerosis
Huang Ai-liang, Huang Rong-zhi, Huang Xiao-qian, Huang Jian-hua, Zhou Yan
- School of Pharmaceutical Sciences, Guangxi Medical University, Nanning 530021, Guangxi Zhuang Autonomous Region, China
-
Online:2015-06-30Published:2015-06-30 -
Contact:Zhou Yan, M.D., Associate professor, School of Pharmaceutical Sciences, Guangxi Medical University, Nanning 530021, Guangxi Zhuang Autonomous Region, China -
About author:Huang Ai-liang, Studying for master’s degree, School of Preclinical Medicine, Guangxi Medical University, Nanning 530021, Guangxi Zhuang Autonomous Region, China -
Supported by:grants from the National Natural Science Foundation of China, No. 81360192; the Natural Science Foundation of Guangxi Zhuang Autonomous Region, No. 2012GXNSFCA053004; grants from the Higher Education Foundation of Guangxi Zhuang Autonomous Region, No. 201203YB041
CLC Number:
Cite this article
Huang Ai-liang, Huang Rong-zhi, Huang Xiao-qian, Huang Jian-hua, Zhou Yan. Establishing animal models of atherosclerosis[J]. Chinese Journal of Tissue Engineering Research, 2015, 19(27): 4423-4428.
share this article
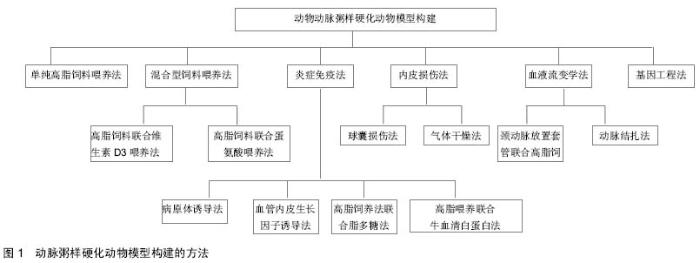
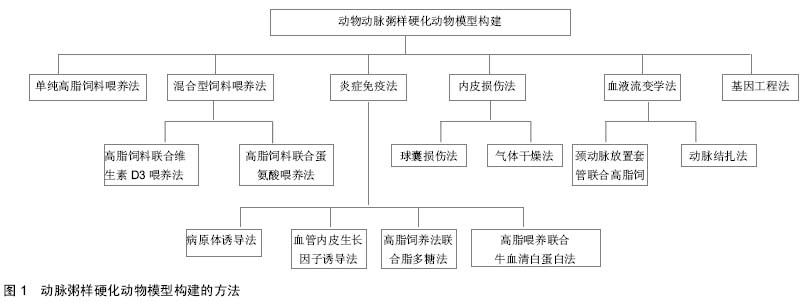
2.1 纳入资料基本概况 纳入的文献包括动脉粥样硬化的发病机制类文章4篇[1-4],单纯高脂饲料喂养法5篇[5-9],混合喂养法6篇[10-15],炎症免疫法12篇[16-27],内皮损伤法10篇[28-37]。血液流变学法3篇[38-40],基因工程法4篇[41-44]。以此为依据对动脉粥样硬化动物模型的方法进行归纳、分类及总结。 2.2 纳入资料的研究结果特征 见图1。 2.2.1 单纯高脂饲料喂养法造模 动脉粥样硬化病变的突出特点之一是脂质的积累,脂质沉积是动脉粥样硬化发生发展的关键因素[5],高脂状态的建立是复制动脉 粥样硬化模型的基础。夏机良等[6]采用高脂膳食喂养中老年雄性食蟹猴12个月后,在食蟹猴外周血白细胞内检测到39个动脉粥样硬化相关基因随血脂升高表达显著改变,此时形成动脉粥样硬化早期模型。有研究予新西兰白兔高脂饲料持续喂养5周后即可形成动脉粥样硬化的早期病变模型[7]。孙玉梅等[8]采用高脂高胆固醇饲料喂养雄性日本大耳白兔,于12周后血管内超声发现病变大血管的斑块负荷大于50%,并成功构建了动脉粥样硬化模型。杨润梅等[9]在建模动物的选择上进行了改进,认为豚鼠具有许多与人相似的特征,如以低密度脂蛋白为载体携带血液中大部分胆固醇,肝脏游离胆固醇较酯化胆固醇浓度高,合成和分解胆固醇比率适当等,予高脂饲料诱导豚鼠6周后即可发现主动脉管壁明显增厚,内膜单核细胞、巨噬细胞浸润与聚集增多,有部分动物动脉内膜表层可发展形成脂纹脂斑病变,而予大鼠同样方法却未见类似病变,因此提出高脂饲料诱导豚鼠是较为理想的研究早期动脉粥样硬化模型。 单纯高脂饲料喂养法操作简单,成本较低,该方法建立模型较符合人类饮食的特点,病理改变与人早期相似, 但其造模时间较长,不易形成类似人体的后期粥样斑块病变,期间易导致继发感染从而影响实验的稳定性,因此大多数研究人员开始研究在高脂饲养的基础上联合其他方法以加速动脉粥样硬化建立。 2.2.2 混合型饲料喂养法造模 高脂饲料联合维生素D3喂养法造模:动脉壁钙化是动脉粥样硬化的临床特征,维生素D3导致血钙升高,损坏动脉壁,使平滑肌细胞发生变性或钙化,从而形成动脉粥样硬化。赵娟等[10]对Wistar大鼠饲以高脂饲料基础上给予腹腔注射维生素D3,4周后,其血清Ca2+、三酰甘油及低密度脂蛋白C明显升高,动脉内膜下可见明显的钙化,出现典型动脉粥样硬化病理变化。黄晓婷等[11]采用类似的方法,6周后大鼠主动脉内膜明显增厚,可见斑块环管腔大部甚至全周,有的粥样斑块突出管腔,斑块内可见大量泡沫细胞及多层排列,内皮细胞缺失或不连续,中膜平滑肌增生。有研究予大白兔高脂喂养8周并于第一天腹腔注射维生素D3建模,可在颈动脉观察到管壁明显增厚,管壁有大量脂质沉积,可见大量的泡沫细胞和动脉粥样硬化斑块[12]。 高脂饲料联合蛋氨酸喂养法造模:近几年国内外有研究表明高同型半胱氨酸能损伤内皮细胞,饮食诱导的高同型半胱氨酸血症可促进动脉粥样硬化的进展[13]。有研究予低密度脂蛋白受体基因敲除的小鼠高脂饲料联合蛋氨酸喂养后,发现模型组小鼠血清中同型半胱氨酸、胆固醇、三酰甘油和低密度脂蛋白胆固醇较单纯高脂喂养组明显升高,且其动脉粥样病变更为严重[14]。 以上两种混合型饲料喂养法复制动脉粥样硬化模型经济、省时省力且病变过程较稳定,而且高脂饲料联合维生素D3喂养法弥补了单纯高脂喂养的动物大动脉只有胆固醇沉积而无明显钙沉积的不足,且其易形成后期粥样斑块病变,是比较好的建模方法,动脉粥样硬化模型形成的质量与维生素D3剂量有密切关系,过高过低均不利于模型的建立,甚至剂量过高还会导致动物的死亡,选择合适的剂量成为建模成功的关键[15]。 2.2.3 炎症免疫法造模 病原体诱导法造模:近年研究表明病原体感染与动脉粥样硬化的发生密切相关。目前常用于动脉粥样硬化模型研究的病原体主要有肺炎衣原体、肺炎支原体、幽门螺杆菌和牙周病原菌等。有报道肺炎衣原体、肺炎支原体感染能通过上调炎症反应因子的表达而促进动脉粥样硬化的发生[16-17]。李永强等[18]通过肺炎衣原体菌株TWAR感染SPF级C57BL/6J小鼠并以高脂饲料喂养进行建模,每只小鼠注射3×107包涵体单位%,以后每8周注射1次,喂养40周,结果发现小鼠主动脉根部出现动脉粥样硬化性损害并且形成明显斑块。Hp感染后的动物可以改变脂类代谢从而促进动脉粥样硬化的发生[19]。陶珍等[20]以高脂饲料喂养新西兰兔6周再经耳缘静脉注射幽门螺杆菌,每间隔24 h注射1次,连续3次,第8周可复制出明显的动脉粥样硬化模型。有研究通过有活性牙周病原菌组、灭活的牙周病原菌组和牙周病原菌+脂多糖组在载脂蛋白E基因(Apo E-/-)敲除小鼠上复制出动脉粥样硬化模型[21],通过分析各组血脂浓度及组织病理学指标证实感染牙周病原菌的感染能通过加强机体固有免疫力及过氧化反应加速动脉粥样硬化的发展,能加速动脉粥样硬化模型的建立。 通过该方法建立动脉粥样硬化动物模型,从免疫学角度考虑病因和发病机制,了解疾病的发生发展过程,是一种比较新的思路,可以通过检测血清相应免疫分子,为疾病的临床分析和治疗提供可靠依据。 血管内皮生长因子诱导法造模:研究表明血管内皮生长因子可诱导血管新生、内皮细胞增殖及通透性增加,促进炎症的反应,促进动脉粥样硬化的发生[22-23]。肖敏等[24]以高脂饲料喂养白兔21 d后肌注血管内皮生长因子65,21 d后可见胸主动脉内膜厚度增厚,斑块形成明显。 高脂饲养法联合脂多糖法造模:脂多糖能上调内皮细胞表达VCAM-1(vascular cell adhesion molecular-1),VCAM-1能促进核转录因子κB和Sp1的向细胞核内转运,上调炎症因子基因的表达,促使免疫反应的发生。 Lee等[25]在高脂饲养的基础上腹腔注射脂多糖于C57BL/6小鼠,每周注射3次,共12周,完成了动脉粥样硬化模型的建立。结果显示胸主动脉内膜增厚的厚度比单纯高脂饮食组或单纯注射脂多糖组明显。 高脂喂养联合牛血清白蛋白法造模:李琳等[26]高脂饲料喂养日本大耳白兔1周后,静脉注射小牛血清白蛋白,在10周后血管内膜增厚,形成了稳定的动脉粥样硬化斑块;由于注射小牛血清蛋白造成全身性免疫炎症反应,加上高脂饮食直接导致脂质代谢紊乱,两者结合后产生复杂的生物效应,由此形成的斑块比同等时间内的高脂饮食加脂肪乳灌胃更稳定。 由于诱导炎症反应的物质颇多,除上述物质外,研究人员联合使用牛血清白蛋白和卵清白蛋白诱导炎症反应也完成建模。葛金文等[27]经兔耳缘静脉注射牛血清白蛋白,同时皮下卵清白蛋白联合高脂饮食喂养,结果表明血管内膜增厚,脂质斑块形成。. 2.2.4 内皮损伤法造模 脂质浸润和内皮损伤是产生粥样硬化病变最基本条件,粥样硬化形成的起始阶段是血管内皮细胞的功能障碍,而血管内膜受损可以加快其的形成。目前的损伤法常见有神经损伤、内皮干燥、球囊损伤等,其主要原理是造成血管内膜损伤,进而引发一系列的炎症反应和内膜反应,最终形成动脉粥样硬化,在这种方法中,脂喂养造成的动物高脂血症是引起动脉粥样硬化的基础;而各种方法导致内膜损伤,加快了动脉粥样硬化的形成,从而节省了造模所需要的时间,由此建立的模型病变过程与人类动脉粥样硬化的演变过程相似,已被广泛应用。 球囊损伤法造模:梅卫义等[28]单用球囊损伤法造模,将球囊导管插入猪冠状动脉后再拉动以损伤血管内膜,在建模后28 d切片发现损伤的管壁处脂质沉着及平滑肌细胞明显增生,大量的泡沫细胞及淋巴细胞等聚集,形成典型的动脉粥样硬化模型。目前冯斌等[29]发现血管内皮损伤和高血脂在动脉粥样硬化进展中是相互促进的,故当机体处于高脂状态时再进行机械损伤可明显缩短粥样斑块出现的时间;与单纯的饲喂高脂饲料相比,此方法形成的内膜明显增厚,斑块与纤维帽结构也更明显,所诱导建立形成斑块的过程和成分与人类的具有较高的相似性,该模型模拟了临床经皮腔内血管成形术过程,且死亡率低,成功率高,是经皮腔内血管成形术的动脉阶段局部用药或转基因治疗实验的首选模型。陈素欣等[30]用新西兰大白兔为动物建模,高脂饲料喂养1周后实行腹主动脉球囊扩张术,术后2周,在损伤部位发现管壁增厚、管腔狭窄,粥样斑块隆起明显,内含泡沫细胞。何艳等[31]用类似的方法损伤颈总动脉,在术后4周,在损伤部位内膜增厚显著,并有泡沫细胞及坏死组织形成的脂质斑块。国外也有报道[32]称联合用高脂和球囊损伤术明显缩短动脉粥样硬化建模时间。 此法建模优点是时间短,定位明确,易于评价,并可根据不同的研究目的和动物,选用不同的动脉造模,常用的是大鼠和兔,常用的有颈动脉、腹主动脉、主动脉弓和冠状动脉,都获得成功模型,该法定位在腹主动脉相对困难,但此法形成的斑块较易脱落而形成血栓,若球囊大小控制不佳会导致动脉破裂或建模失败。 气体干燥法造模:武晓玲等[33]在高脂饲料喂养日本大耳白兔1周后,在颈动脉行空气干燥术,术后2周这段血管僵硬、增厚,8周时趋于成熟的斑块中有大脂核和纤维帽,12周时成熟的斑块中可见明显的钙化。而王茁伉等[34]改用脂肪乳剂灌胃和医用氮气干燥法,术后8周部分斑块内可见坏死钙化的成熟斑块,大大缩短了造模时间,该模型用乳剂灌胃取代高脂喂养,克服了动物食性因素的影响。国外也有类似报道,有研究用高脂饲养联合冷液氮注射入兔颈动脉刺激血管内膜,第8周建成动脉粥样硬化模型[35]。这种方法不同的研究者用不同的时间和气流量都能成功地形成动脉粥样硬化病变,故其建模最合适的时间及气流量仍需进一步探讨。该模型利用气流损伤血管,其可控性较强,使之结果更易评价,便于进行各型研究。 2.2.5 血液流变学法造模 血流速度和切应力的改变是动脉粥样硬化形成的危险因素之一[36],利用手术的办法对正常血流速度和切应力进行人为的改变使机体发生一系列相应的应答,从而促进动脉粥样硬化的形成。此法造成的模型能够人为控制动脉粥样硬化的形成部位,特别有利于对动脉粥样硬化的并发症脑卒中研究,但对操作者技术要求高,同时与自发型的动脉粥样硬化存在一定的差别。 颈动脉放置套管联合高脂饲养法造模:硅胶圈通过缩小血管的直径而改变血液流动状态达到造模的目的。危当恒等[37]在兔的左颈动脉外放置硅胶管后缝合并联合高脂饲养,4周后形成明显的动脉粥样硬化斑块, 斑块内含有大量炎性细胞和泡沫细胞,病变区有大量脂质沉着,成功复制了动脉粥样硬化模型。 动脉结扎法造模:此法对血管结扎缝合使血管内血流速度和切应力发生改变而造模。有研究结扎C57B1/6J小鼠左侧颈外动脉、甲状腺下动脉和颈内动脉进行造模[38],研究结扎后血管的血流动力学改变及血流改变后该部分血管的变化,发现1周后血管内外膜细胞明显增生伴有大量的巨噬细胞浸润。中国众多学者利用类似的方法并联合多种方法进行造模。王庆林等[39]利用雌性SD大鼠颈动脉结扎联合高脂饲养法建立模型发现,单纯高脂喂养对照组在喂养10周内没有引起动脉内膜的变化,而血管钳夹组大鼠在喂养2周时发现血管内皮细胞变性、增生且少量泡沫细胞形成,喂养10周时多其动脉内膜可见白色条纹或大小不等黄白色斑块隆起,表面有纤维组织覆盖,形成典型的“纤维帽”。徐翔等[40]利用动脉结扎术联合高脂饲养及腹腔注射维生素D3的方法,在Wistar雄性大鼠钳夹侧血管12周后发现含脂质空泡的泡沫细胞沉积、粥样斑块或纤维斑块及坏死组织,中膜平滑肌细胞排列紊乱,弹性纤维不明显,血管壁明显增厚,腔内可见血栓形成,完成了模型的建立。 2.2.6 基因工程法造模 随着转基因技术的成熟,有研究者[41]用基因改良的小鼠分别对炎症、高血压、蛋白酶、细胞外基质、糖代谢及免疫系统等相关的基因进行敲除或者过度表达,如Apo E-/-小鼠、LDLR-/-小鼠、MCPI-1-/-小鼠作为动物对象采取上述各种方法建模,除具备各自优点外,还具备速度更快、质量更高、更加接近自然发生的动脉粥样硬化进程的优点,但此动物的来源费用也较高[42-44]。"
| [1] Chen Z, Xu H. Anti-Inflammatory and Immunomodulatory Mechanism of Tanshinone IIA for Atherosclerosis. Evid Based Complement Alternat Med. 2014;2014:267976. [2] Xu Y, Ashline D, Liu L, et al. The glycosylation-dependent interaction of perlecan core protein with LDL: implications for atherosclerosis. J Lipid Res. 2014:M053017. [3] Calvayrac O, Rodríguez-Calvo R, Martí-Pamies I, et al. NOR-1 modulates the inflammatory response of vascular smooth muscle cells by preventing NFκB activation. 2014;(12). doi: 10.1016/j.yjmcc.2014.12.015. [4] Lin Y, Liu P, Adhikari N, et al. RIP140 contributes to foam cell formation and atherosclerosis by regulating cholesterol homeostasis in macrophages. J Mol Cell Cardiol. 2014;(12): 287-294 [5] Salisbury D, Bronas U. Inflammation and immune system contribution to the etiology of atherosclerosis: mechanisms and methods of assessment. Nurs Res. 2014;63(5):375-385. [6] 夏机良,郝香芬,曾小明,等.动脉粥样硬化相关基因在高血脂食蟹猴中的差异表达[J].中国动脉硬化杂志,2011,19(5): 390-394. [7] Niimi M, Keyamura Y, Nozako M, et al. Probucol inhibits the initiation of atherosclerosis in cholesterol-fed rabbits. Lip Health Dis. 2013;12:166. [8] 孙玉梅,张金盈,闫继锋,等.转导骨桥蛋白短发夹状RNA预防动粥样硬化模型兔血管成形后的再狭窄[J].中国组织工程研究, 2014, 18(18):2801-2805. [9] 杨润梅,李金莲,高南南,等.豚鼠早期动脉粥样硬化模型的建立、机制研究及与大鼠模型的比较[J].中国药理学通报,2011,27(2): 285-289. [10] 赵娟,李相军,孙波,等.维生素D3联合高脂饲料建立大鼠动脉粥样硬化模型[J].实用医学杂志,2009,25(21):3569-3571. [11] 黄晓婷,杨冬业,郑楚,等.八角莽草酸的抗动脉粥样硬化作用机制研究[J].中国实验方剂学杂志,2014,20(11):126-130. [12] Chen M. Effects of chinese herbal compound “Xuemai Ning”on rabbit atherosclerosis model and expression of ABCA1. Int J Biomed Sci. 2013;9(3):153-161. [13] Julve J, Escolà-Gil JC, Rodríguez-Millán E, et al. Methionine-induced hyperhomocysteinemia impairs the antioxidant ability of high-density lipoproteins without reducing in vivo macrophage-specific reverse cholesterol transport. Mol Nutr Food Res. 2013;57(10):1814-1824. [14] Guo HY, Xu FK, Lv HT, et al. Hyperhomocysteinemia independently causes and promotes atherosclerosis in LDL receptor-deficient mice. J Geriatr Cardiol. 2014;11(1):74-78. [15] 周红,吴晓燕,袁艺标,等.三种剂量维生素D3结合高脂饲料建立大鼠动脉粥样硬化模型的比较[J].中国动脉硬化杂志,2012, 20(11):995-998. [16] 朱翠明,汪世平,游晓星,等.肺炎支原体脂质相关膜蛋白在动脉粥样硬化发生发展中的作用机制[J].中国动脉硬化杂志,2012, 20(9): 773-776. [17] Justin FD, Grant NP. Possibilities for therapeutic interventions in disrupting Chlamydophila pneumonia involvement in atherosclerosis. Clin Pharmacol. 2010;24: 607-617. [18] 李永强,董吁钢,马虹,等.肺炎衣原体感染对小鼠内皮功能及动脉粥样硬化发展的影响[J].中国临床研究,2013,26(12):1292- 1296. [19] 刘玲梅,罗雁,刘会领,等.幽门螺杆菌感染对动脉粥样硬化的影响[J].中华医院感染学杂志,2013,23(9):2072-2076. [20] 陶珍,曲乐丰,丁素菊,等.幽门螺杆菌感染致兔颈动脉粥样硬化模型的建立[J].第二军医大学学报,2010,31(1):37-41. [21] Jia R, Kurita-Ochiai T. Periodontal pathogen accelerates lipid peroxidation and atherosclerosis. J Dent Res. 2013;92(3): 247-252. [22] Pieter WH, Atherosclerotic plaque development and instability: a dual role for VEGF. Ann Med. 2009;41:257-264. [23] 李婷,刘访遥.血清单核细胞趋化蛋白-1、血管内皮生长因子与冠状动脉粥样硬化的关系[J].社区医学杂志,2010,8(19):10-12. [24] 肖敏,王玮,党书毅,等.血管内皮生长因子165对实验性兔动脉粥样硬化斑块形成的影响[J].中国动脉硬化杂志,2005,13(4): 421-424. [25] LeeWR, Kim KH, An HJ, et al. Effects of chimeric decoy oligodeoxynucleotide in the regulation of transcription factors NF-kB and Sp1 in an animal model of atherosclerosis. Basic Clin Pharmacol Toxicol. 2013;112:236-243.[26] 李琳,窦健霖,楚天舒,等.高脂饲料喂养加静脉注射小牛血清白蛋白建立兔动脉粥样硬化模型[J].中国组织工程研究,2012,16(20): 3690-3693. [27] 葛金文,刘吉勇,朱惠斌,等.阿托伐他汀对动脉粥样硬化兔氧化应激/炎症反应的影响[J].中国动脉硬化杂志,2011,19(12): 979-983. [28] 梅卫义,杜志民,胡承恒,等.球囊损伤和早期动脉粥样硬化猪冠状动脉妊娠相关血浆蛋白A和诱导型一氧化氮合酶的表达[J].中国病理生理杂志,2009,25(9):1848-1852. [29] 冯斌,杨庭树,张华巍.高脂饲料喂养与动脉内膜球囊损伤结合建立兔腹主动脉粥样硬化模型[J].中国组织工程研究与临床康复, 2009,13(15):2911-2914. [30] 陈素欣,齐晓勇,孟存良,等.腹主动脉球囊扩张过程中白细胞介素8水平表达对血管内皮功能的影响[J].中国组织工程研究与临床康复,2009,13(30):5813-5818. [31] 何艳,谢清平,吴立荣,等.银杏黄酮苷元干预兔颈总动脉损伤后内膜增生及血凝素样氧化低密度脂蛋白受体1的表达[J].中国组织工程研究与临床康复,2010,14(28):5228-5232. [32] Koniari I, Apostolakis E. Transauricular balloon angioplasty in rabbit thoracic aorta: a novel model of experimental restenosis. Lipids Health Dis. 2014;13(1):33. [33] 武晓玲,罗春霞,迟路湘.采用高脂饲料加空气干燥术建立颈动脉粥样硬化动物模型[J].微循环学杂志,2006,16(3):62-63. [34] 王茁伉,彭成,王忠等.脂肪乳剂灌胃加氮气损伤建立兔颈动脉粥样硬化动物模型[J].中国实验方剂学杂志,2013;19(11):176-179. [35] Mehrad H, Mokhtari-Dizaji M, Ghanaati H, et al. Developing a rabbit model of neointimal stenosis and atherosclerotic fibrous plaque rupture. J Teh Univ Heart Ctr. 2011;6(3):117-125. [36] Nam D, Ni CW, Rezvan A, et al. Partial carotid ligation is a model of acutely induced disturbed flow, leadingto rapid endothelial dysfunction and atherosclerosis. Am J Physiol Heart Circ Physiol. 2009;297:H1535-H1543. [37] 危当恒,夏敏,贾小英,等.组织蛋白酶L在动脉粥样硬化病变中的表达以及对巨噬细胞脂质蓄积的影响[J].中国动脉硬化杂志, 2011,19(12):963-968. [38] Vyacheslav AK, Bradford CB. Flow-induced vascular remodeling in the mouse: a model for carotid intima-media thickening. Arterioscler Thromb Vasc Biol. 2003;23:2185- 2191. [39] 王庆林,陈文捷,万佳,等.颈总动脉钳夹术加高脂饮食建立大鼠颈动脉粥样硬化模型[J].实用医学杂志,2010,26(4):562-564. [40] 徐翔,吴梅,李斌,等.动脉钳夹联合高胆固醇饮食、维生素D3建立大鼠颈总动脉粥样硬化模型[J].国际脑血管病杂志,2013,21(4): 288-292. [41] Godfrey SG, Catherine AR. Animal models of atherosclerosis. Arterioscler Thromb Vasc Boil. 2012;32:1104-1115. [42] 徐冰,聂波,徐颖,等.基于ApoE-/-小鼠动脉粥样硬化模型的四妙勇安汤活性部位配伍规律研究.辽宁中医杂志,2013,40(6): 1250-1251. [43] Merino H, Parthasarthy S. Partial ligation-induced carotid artery occlusion induces leukocyte recruitment and lipid accumulation-A shear stress model of atherosclerosis. Mol Cell Biochem. 2013;372:267-273. [44] 余飞,黄东雅,堵翠,等.ApoE-/-小鼠颈总动脉粥样硬化动物模型的建立[J].中华实验外科杂志,2013,30(2):401-402. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Kong Desheng, He Jingjing, Feng Baofeng, Guo Ruiyun, Asiamah Ernest Amponsah, Lü Fei, Zhang Shuhan, Zhang Xiaolin, Ma Jun, Cui Huixian. Efficacy of mesenchymal stem cells in the spinal cord injury of large animal models: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1142-1148. |
| [4] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [5] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [6] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [7] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [8] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [9] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [10] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [11] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [12] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [13] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [14] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [15] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||